第二节:富集在海水中的元素——氯(课件)
文档属性
| 名称 | 第二节:富集在海水中的元素——氯(课件) |

|
|
| 格式 | pptx | ||
| 文件大小 | 392.5KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-07-06 00:00:00 | ||
图片预览





文档简介
(共15张PPT)
富集在海水中的元素——氯
一、 氯元素的原子结构与自然界的存在
1、氯的原子结构和性质
结构:Cl +17 2 8 7
性质:主要化合价:-1,+1,+3, +5,+7
得电子能力强,非金属性强
1、氯气的分子结构
Cl2 : Cl—Cl
氯气属于双原子分子结构
2、氯气的物理性质
(色、状、味、水溶性、密度、毒性)
(1)氯气是黄绿色有刺激性气味的有毒气体
(2)氯气可溶于水,氯水呈浅黄绿色
(常温常压下,1体积水可溶解2体积氯气)
(3)密度比空气大
二、 活泼的黄绿色气体——氯气
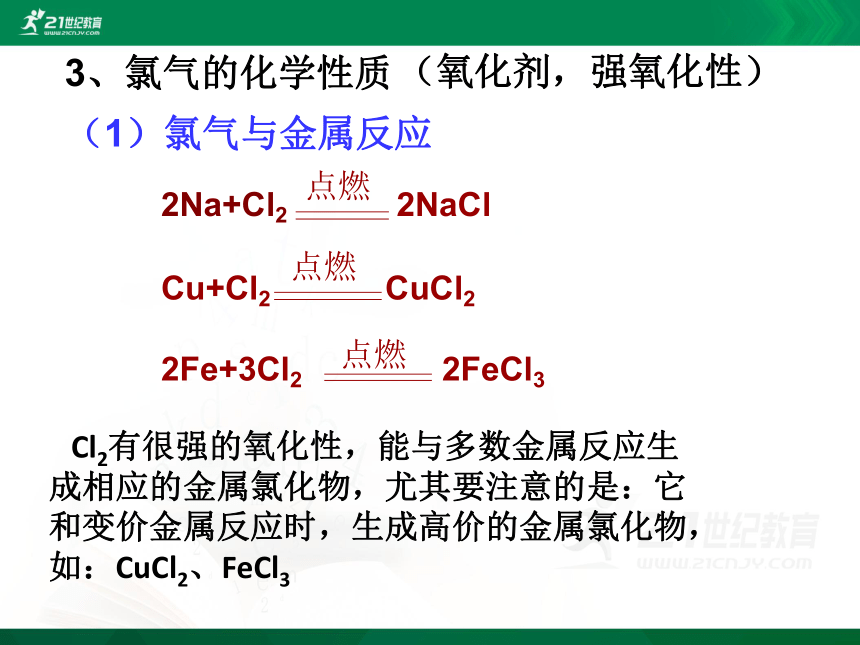
3、氯气的化学性质
(氧化剂,强氧化性)
(1)氯气与金属反应
2Na+Cl2 2NaCl
点燃
Cu+Cl2 CuCl2
点燃
点燃
2Fe+3Cl2 2FeCl3
Cl2有很强的氧化性,能与多数金属反应生
成相应的金属氯化物,尤其要注意的是:它
和变价金属反应时,生成高价的金属氯化物,
如:CuCl2、FeCl3
(2)氯气与某些非金属反应
H2+Cl2 2HCl
点燃
H2+Cl2 2HCl
光照
2P + 3Cl2(少量) 2PCl3
点燃
(液态)
2P + 5Cl2(过量) 2PCl5
点燃
(固态)
氯气与金属反应时,是实实在在的得电子,
而在与非金属(如H2)反应时,氯原子和氢原
子都想得电子,最后双方为了达到稳定,形成
共用电子对。 即使这样,形成的共用电子对还
是偏向氯,偏离氢,从而使氯显-1价。
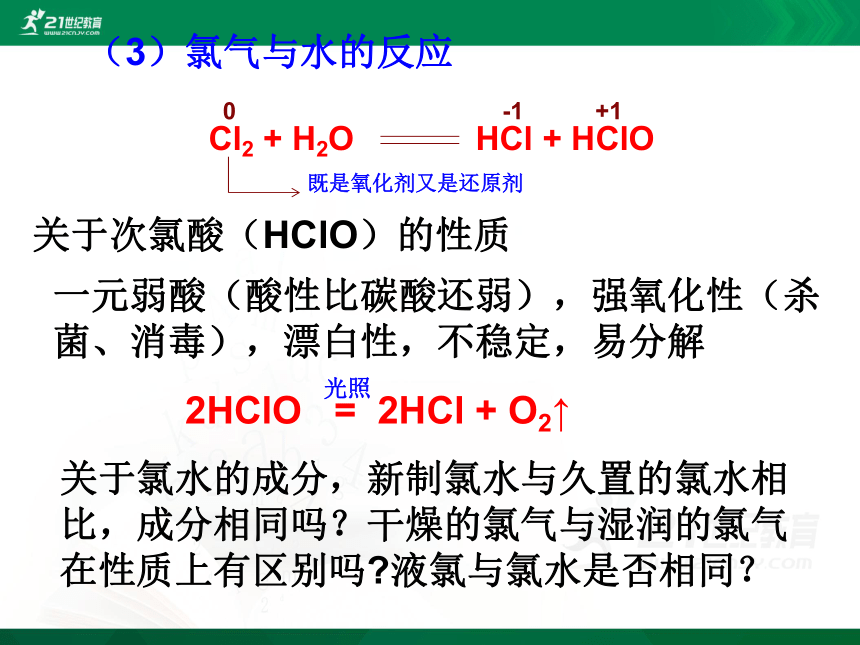
(3)氯气与水的反应
Cl2 + H2O HCl + HClO
0
-1
+1
既是氧化剂又是还原剂
关于次氯酸(HClO)的性质
一元弱酸(酸性比碳酸还弱),强氧化性(杀菌、消毒),漂白性,不稳定,易分解
2HClO = 2HCl + O2↑
光照
关于氯水的成分,新制氯水与久置的氯水相比,成分相同吗?干燥的氯气与湿润的氯气在性质上有区别吗 液氯与氯水是否相同?
(4)与碱溶液的反应
氯气与水反应生成了盐酸和次氯酸,如果把氯气通如NaOH溶液中,能否发生反应?为什么?
思考
Cl2 + 2OH- = Cl- + ClO- + H2O
实验室制氯气时,多余的氯气用NaOH溶液吸收
关于漂白粉的制取、成分、漂白原理:
2Ca(OH)2 + 2Cl2 = CaCl2 + Ca(ClO)2 + 2H2O
漂白粉的成分
漂白粉的有效成分
CaCl2 和 Ca(ClO)2的混合物
Ca(ClO)2
(5)与盐溶液的反应
漂白粉的漂白原理:它的水溶液与空气中的CO2接触反应生成次氯酸的过程。
Ca(ClO)2 + CO2 + H2O = CaCO3 ↓+ 2HClO
与FeCl2 、NaBr、KI等盐溶液反应(表现氯气的强氧化性)
2Fe2+ + Cl2 = 2Fe3+ + 2Cl-
Cl2 + 2Br- = 2Cl- + Br2
Cl2 + 2 I- = 2Cl- + I2
探究:
新制的氯水有什么性质?能与那些物质发生反应?
4、氯气的实验室制备
(原理、试剂、仪器、装置、验满、尾气处理)
氯气的制法:
1、反应物的要求和代替品?
2、气体发生装置的特点
3、各仪器的名称和作用
4、排空收集气体时导气管的位置
5、尾气的处理?
6、整个实验过程的操作?
7、工业制法的化学反应方程式
三、 氯离子的检验
原理:利用Cl-和Ag+ 反应生成生成不溶于
稀硝酸的白色沉淀 Ag++Cl- = AgCl↓
检验试剂:硝酸银和稀硝酸
待测物质
加入足量
的稀硝酸
白色沉淀
加入
硝酸银
1.有关氯的叙述正确的是( )
A.液氯和氯水是同一物质
B.红磷在氯气中燃烧产生白色烟雾
C.氯气与水的反应中氯是氧化剂,水是还原剂
D.用氯制漂白粉是为了得到易贮存的漂白剂
四、巩固练习
B、D
2.可以用于除去氯气中水蒸气的干燥剂是 ( )
A. 碱石灰 B.浓硫酸
C.无水氯化钙 D.固体烧碱
3.制取漂白液的化学方程式是:Cl2+2NaOH=NaCl+NaClO+H2O,该反应的氧化剂与还原剂之比为 ( )
A.1:1 B.1:2
C. 2:1 D. 3:2
B、C
A
4.(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是_______ ________________。
潮湿有色布条褪色而干燥有色布条不褪色
(2)为防止氯气尾气污染空气,根据氯水显酸性的性质,可用 溶液吸收多余的氯气,原理是(用化学方程式表示)____________________根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是__________(填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是_______ _(用字母代号填)。
A.O2 B.Cl2 C.CO2 D.HClO
氢氧化钠(NaOH)
2NaOH+Cl2=NaClO+NaCl+H2O
Ca(ClO)2
C
富集在海水中的元素——氯
一、 氯元素的原子结构与自然界的存在
1、氯的原子结构和性质
结构:Cl +17 2 8 7
性质:主要化合价:-1,+1,+3, +5,+7
得电子能力强,非金属性强
1、氯气的分子结构
Cl2 : Cl—Cl
氯气属于双原子分子结构
2、氯气的物理性质
(色、状、味、水溶性、密度、毒性)
(1)氯气是黄绿色有刺激性气味的有毒气体
(2)氯气可溶于水,氯水呈浅黄绿色
(常温常压下,1体积水可溶解2体积氯气)
(3)密度比空气大
二、 活泼的黄绿色气体——氯气
3、氯气的化学性质
(氧化剂,强氧化性)
(1)氯气与金属反应
2Na+Cl2 2NaCl
点燃
Cu+Cl2 CuCl2
点燃
点燃
2Fe+3Cl2 2FeCl3
Cl2有很强的氧化性,能与多数金属反应生
成相应的金属氯化物,尤其要注意的是:它
和变价金属反应时,生成高价的金属氯化物,
如:CuCl2、FeCl3
(2)氯气与某些非金属反应
H2+Cl2 2HCl
点燃
H2+Cl2 2HCl
光照
2P + 3Cl2(少量) 2PCl3
点燃
(液态)
2P + 5Cl2(过量) 2PCl5
点燃
(固态)
氯气与金属反应时,是实实在在的得电子,
而在与非金属(如H2)反应时,氯原子和氢原
子都想得电子,最后双方为了达到稳定,形成
共用电子对。 即使这样,形成的共用电子对还
是偏向氯,偏离氢,从而使氯显-1价。
(3)氯气与水的反应
Cl2 + H2O HCl + HClO
0
-1
+1
既是氧化剂又是还原剂
关于次氯酸(HClO)的性质
一元弱酸(酸性比碳酸还弱),强氧化性(杀菌、消毒),漂白性,不稳定,易分解
2HClO = 2HCl + O2↑
光照
关于氯水的成分,新制氯水与久置的氯水相比,成分相同吗?干燥的氯气与湿润的氯气在性质上有区别吗 液氯与氯水是否相同?
(4)与碱溶液的反应
氯气与水反应生成了盐酸和次氯酸,如果把氯气通如NaOH溶液中,能否发生反应?为什么?
思考
Cl2 + 2OH- = Cl- + ClO- + H2O
实验室制氯气时,多余的氯气用NaOH溶液吸收
关于漂白粉的制取、成分、漂白原理:
2Ca(OH)2 + 2Cl2 = CaCl2 + Ca(ClO)2 + 2H2O
漂白粉的成分
漂白粉的有效成分
CaCl2 和 Ca(ClO)2的混合物
Ca(ClO)2
(5)与盐溶液的反应
漂白粉的漂白原理:它的水溶液与空气中的CO2接触反应生成次氯酸的过程。
Ca(ClO)2 + CO2 + H2O = CaCO3 ↓+ 2HClO
与FeCl2 、NaBr、KI等盐溶液反应(表现氯气的强氧化性)
2Fe2+ + Cl2 = 2Fe3+ + 2Cl-
Cl2 + 2Br- = 2Cl- + Br2
Cl2 + 2 I- = 2Cl- + I2
探究:
新制的氯水有什么性质?能与那些物质发生反应?
4、氯气的实验室制备
(原理、试剂、仪器、装置、验满、尾气处理)
氯气的制法:
1、反应物的要求和代替品?
2、气体发生装置的特点
3、各仪器的名称和作用
4、排空收集气体时导气管的位置
5、尾气的处理?
6、整个实验过程的操作?
7、工业制法的化学反应方程式
三、 氯离子的检验
原理:利用Cl-和Ag+ 反应生成生成不溶于
稀硝酸的白色沉淀 Ag++Cl- = AgCl↓
检验试剂:硝酸银和稀硝酸
待测物质
加入足量
的稀硝酸
白色沉淀
加入
硝酸银
1.有关氯的叙述正确的是( )
A.液氯和氯水是同一物质
B.红磷在氯气中燃烧产生白色烟雾
C.氯气与水的反应中氯是氧化剂,水是还原剂
D.用氯制漂白粉是为了得到易贮存的漂白剂
四、巩固练习
B、D
2.可以用于除去氯气中水蒸气的干燥剂是 ( )
A. 碱石灰 B.浓硫酸
C.无水氯化钙 D.固体烧碱
3.制取漂白液的化学方程式是:Cl2+2NaOH=NaCl+NaClO+H2O,该反应的氧化剂与还原剂之比为 ( )
A.1:1 B.1:2
C. 2:1 D. 3:2
B、C
A
4.(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是_______ ________________。
潮湿有色布条褪色而干燥有色布条不褪色
(2)为防止氯气尾气污染空气,根据氯水显酸性的性质,可用 溶液吸收多余的氯气,原理是(用化学方程式表示)____________________根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是__________(填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是_______ _(用字母代号填)。
A.O2 B.Cl2 C.CO2 D.HClO
氢氧化钠(NaOH)
2NaOH+Cl2=NaClO+NaCl+H2O
Ca(ClO)2
C
