新人教版九年级下册同步测试:8.2 金属的化学性质(解析版)
文档属性
| 名称 | 新人教版九年级下册同步测试:8.2 金属的化学性质(解析版) |

|
|
| 格式 | zip | ||
| 文件大小 | 37.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-07-07 00:00:00 | ||
图片预览



文档简介
新人教版九年级下册《8.2
金属的化学性质》同步练习卷
一、选择题
1.早在2000多年前的西汉时期就有“曾青得铁则化为铜”的记载,从现代化学的观点理解,这句话的含义是( )
A.木炭还原氧化铜生成单质铜
B.氧化铜在单质铁的催化作用下,分解生成铜
C.氢氧化铜沉淀和铁反应生成单质铜
D.单质铁从含铜的化合物的溶液中置换出铜
2.用熟石灰(化学式为Ca(OH)2)和硫酸铜来配制农药波尔多液时,不能使用的容器是( )
A.铝制容器
B.铁制容器
C.塑料容器
D.玻璃容器
3.把过量的铁粉加人到硫酸铜溶液中,充分反应后过滤,留在滤纸上的物质是( )
A.铁
B.铜
C.硫酸铜
D.铁和铜
4.可以用金属与相应的酸直接反应制取的盐是( )
A.FeCl3B.CuCl2C.HgCl2D.MgCl2
5.为验证铁、铜、铝三种金属的活动性顺序,可选用的一组物质是( )
A.AlCl3溶液、Cu、FeSO4溶液
B.CuSO4溶液、Fe、AlCl3溶液
C.AlCl3溶液、Fe、Cu
D.Al、Cu和AgNO3溶液
6.向AgNO3、Cu(NO3)2、Mg(NO3)2的混合溶液中加入一些锌粉,完全反应后过滤,不可能存在的情况是( )
A.滤纸上有Ag、Cu,滤液中有Zn2+、Mg2+、Ag+
B.滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Mg2+
C.滤纸上有Ag、Cu,滤液中有Zn2+、Mg2+
D.滤纸上有Ag、Cu、Zn,滤液中有Zn2+、Mg2+
二、非选择题
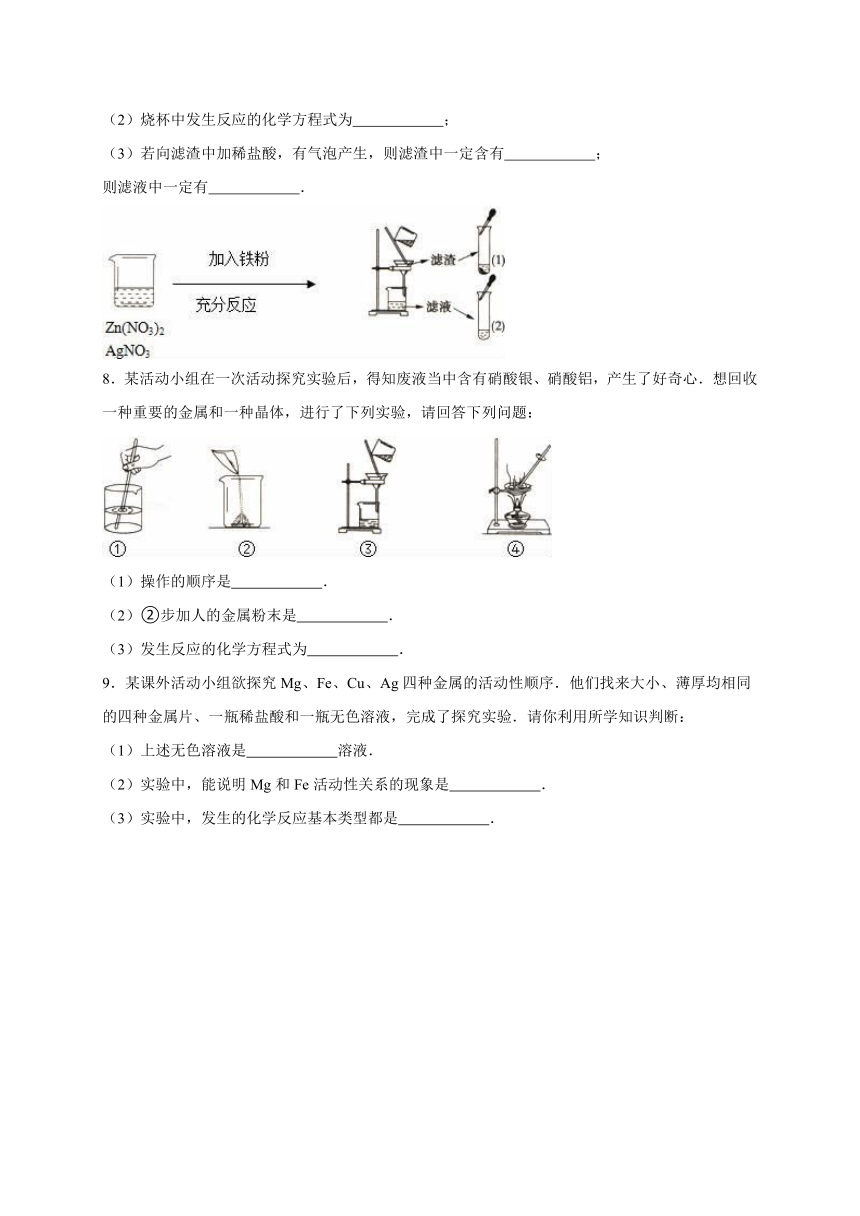
7.根据下列操作回答问题:
(1)图中的操作错误是 ;
(2)烧杯中发生反应的化学方程式为 ;
(3)若向滤渣中加稀盐酸,有气泡产生,则滤渣中一定含有 ;
则滤液中一定有 .
8.某活动小组在一次活动探究实验后,得知
( http: / / www.21cnjy.com )废液当中含有硝酸银、硝酸铝,产生了好奇心.想回收一种重要的金属和一种晶体,进行了下列实验,请回答下列问题:
(1)操作的顺序是 .
(2)②步加人的金属粉末是 .
(3)发生反应的化学方程式为 .
9.某课外活动小组欲探究Mg、Fe、Cu、
( http: / / www.21cnjy.com )Ag四种金属的活动性顺序.他们找来大小、薄厚均相同的四种金属片、一瓶稀盐酸和一瓶无色溶液,完成了探究实验.请你利用所学知识判断:
(1)上述无色溶液是 溶液.
(2)实验中,能说明Mg和Fe活动性关系的现象是 .
(3)实验中,发生的化学反应基本类型都是 .
新人教版九年级下册《8.2
金属的化学性质》同步练习卷
参考答案与试题解析
一、选择题
1.早在2000多年前的西汉时期就有“曾青得铁则化为铜”的记载,从现代化学的观点理解,这句话的含义是( )
A.木炭还原氧化铜生成单质铜
B.氧化铜在单质铁的催化作用下,分解生成铜
C.氢氧化铜沉淀和铁反应生成单质铜
D.单质铁从含铜的化合物的溶液中置换出铜
【考点】金属的化学性质.
【专题】结合课本知识的信息;金属与金属材料.
【分析】铁比铜活泼,能够把铜从它的可溶性盐中置换出来.
【解答】解:“曾青得铁则化为铜”,从现代化学的观点理解,这句话的含义是单质铁从含铜的化合物的溶液中置换出铜.
故选:D.
【点评】要会利用金属活动顺序表分析实验,氢
( http: / / www.21cnjy.com )前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.
2.用熟石灰(化学式为Ca(OH)2)和硫酸铜来配制农药波尔多液时,不能使用的容器是( )
A.铝制容器
B.铁制容器
C.塑料容器
D.玻璃容器
【考点】金属的化学性质.
【专题】金属与金属材料.
【分析】根据若配制农药波尔
( http: / / www.21cnjy.com )多液的原料能与容器的主要成分发生化学反应,则不能使用这种容器配制;结合在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,进行分析判断.
【解答】解:A、在金属活动性顺序中,铝在铜的前面,能与硫酸铜反应生成硫酸铝和铜,使药效降低,不能使用铝制容器,故选项正确.
B、在金属活动性顺序中,铁在铜的前面,能与硫酸铜反应生成硫酸亚铁和铜,使药效降低,不能使用铁制容器,故选项正确.
C、塑料容器与熟石灰和硫酸都不反应,可以使用塑料容器,故选项错误.
D、玻璃容器与熟石灰和硫酸都不反应,可以使用玻璃容器,故选项错误.
故选:AB.
【点评】本题难度不大,掌握能用于盛放农药波尔多液的容器不能与原料发生化学反应、金属的化学性质是正确解答本题的关键.
3.把过量的铁粉加人到硫酸铜溶液中,充分反应后过滤,留在滤纸上的物质是( )
A.铁
B.铜
C.硫酸铜
D.铁和铜
【考点】金属的化学性质.
【专题】金属与金属材料.
【分析】铁比铜活泼,能和硫酸铜反应生成硫酸亚铁和铜.
【解答】解:铁比铜活泼,能和硫酸铜反应
( http: / / www.21cnjy.com )生成硫酸亚铁和铜,把过量的铁粉加人到硫酸铜溶液中,充分反应后过滤,留在滤纸上的物质是反应生成的铜和过量的铁.
故选:D.
【点评】要会利用金属活动顺序表分析
( http: / / www.21cnjy.com )实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.
4.可以用金属与相应的酸直接反应制取的盐是( )
A.FeCl3B.CuCl2C.HgCl2D.MgCl2
【考点】金属的化学性质.
【专题】结合课本知识的信息;金属与金属材料.
【分析】铁和稀盐酸反应生成氯化亚铁和氢气;
铜不能和稀盐酸反应;
汞不能和稀盐酸反应;
镁和稀盐酸反应生成氯化镁和氢气.
【解答】解:A、铁和稀盐酸反应生成氯化亚铁和氢气,因此氯化铁不能由金属与相应的酸直接反应制取;
B、铜不能和稀盐酸反应,因此氯化铜不能由金属与相应的酸直接反应制取;
C、汞不能和稀盐酸反应,因此氯化汞不能由金属与相应的酸直接反应制取;
D、镁和稀盐酸反应生成氯化镁和氢气,因此氯化镁可以用金属与相应的酸直接反应制取.
故选:D.
【点评】要会利用金属活动顺序表分析
( http: / / www.21cnjy.com )实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.
5.为验证铁、铜、铝三种金属的活动性顺序,可选用的一组物质是( )
A.AlCl3溶液、Cu、FeSO4溶液
B.CuSO4溶液、Fe、AlCl3溶液
C.AlCl3溶液、Fe、Cu
D.Al、Cu和AgNO3溶液
【考点】金属活动性顺序及其应用.
【专题】金属与金属材料.
【分析】验证铜、铁、铝三种金属的活动性强弱,
( http: / / www.21cnjy.com )一般是利用金属与酸反应或金属与盐溶液的反应,通过金属和酸是否反应或剧烈程度判断金属的活动性,或通过金属是否能和盐溶液发生置换反应判断金属活动性.
【解答】解:A、铜和FeSO4溶液、AlCl3溶液都不反应,无法判断铁和铝的活泼性,故错;
B、铁与CuSO4溶液反应,与AlCl3溶液不反应,能判断三种金属的活动性顺序,故对;
C、Cu、Fe均不能置换出AlCl3溶液中的铝,无法判断铁、铜的金属活动性,故错;
D、AgNO3溶液和铝、铜都反应,没有铁.无法判断铁、铜、铝的活泼性,故错.
故选:B.
【点评】化学实验方案的设计
( http: / / www.21cnjy.com )与评价是素质教育的基本要求,是考查学生能力的主要题目类型,同时也是实验教与学难点所在,在具体设计时,要充分利用教材资源,对其原理透彻理解,学会信息迁移,既要模仿,又要注重创新,在评价时要注重比较的方法.
6.向AgNO3、Cu(NO3)2、Mg(NO3)2的混合溶液中加入一些锌粉,完全反应后过滤,不可能存在的情况是( )
A.滤纸上有Ag、Cu,滤液中有Zn2+、Mg2+、Ag+
B.滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Mg2+
C.滤纸上有Ag、Cu,滤液中有Zn2+、Mg2+
D.滤纸上有Ag、Cu、Zn,滤液中有Zn2+、Mg2+
【考点】金属的化学性质.
【专题】结合课本知识的信息;金属与金属材料.
【分析】镁比锌活泼,锌比铜活泼,铜比银活泼,因此锌能和硝酸铜反应生成硝酸锌和铜,能和硝酸银反应生成硝酸锌和银.
【解答】解:A、加入一些
( http: / / www.21cnjy.com )锌粉时,锌先和硝酸银反应,当硝酸银完全反应后,锌再和硝酸铜反应,因此当滤纸上有Ag、Cu时,滤液中一定不含有Ag+,该选项说法不正确;
B、加入一些锌粉时,锌先和硝酸银反应,
( http: / / www.21cnjy.com )当锌不足以和硝酸银完全反应,即锌不足时,滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Mg2+,该选项说法正确;
C、加入一些锌粉时,锌先和硝酸银反应,
( http: / / www.21cnjy.com )当硝酸银完全反应后,锌再和硝酸铜反应,因此当滤纸上有Ag、Cu时,滤液中有Zn2+、Mg2+,该选项说法正确;
D、加入一些锌粉时,锌先和硝酸银反
( http: / / www.21cnjy.com )应,当硝酸银完全反应后,锌再和硝酸铜反应,因此当滤纸上有Ag、Cu、Zn时,滤液中有Zn2+、Mg2+,该选项说法正确.
故选:A.
【点评】要会利用金属活动顺序表分析实验,
( http: / / www.21cnjy.com )氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.
二、非选择题
7.根据下列操作回答问题:
(1)图中的操作错误是 胶头滴管伸入试管中 ;
(2)烧杯中发生反应的化学方程式为 Fe+2AgNO3═Fe(NO3)2+2Ag ;
(3)若向滤渣中加稀盐酸,有气泡产生,则滤渣中一定含有 Ag、Fe ;
则滤液中一定有 Zn(NO3)2、Fe(NO3)2 .
【考点】金属的化学性质;书写化学方程式、文字表达式、电离方程式.
【专题】金属与金属材料.
【分析】锌比铁活泼,铁比银活泼,铁和硝酸银反应生成硝酸亚铁和银,铁不能和硝酸锌反应;
铁能和稀盐酸反应生成氯化亚铁和氢气,银不能和稀盐酸反应.
【解答】解:(1)图中的操作错误是胶头滴管伸入试管中;
(2)烧杯中,铁和硝酸银反应生成硝酸亚铁和银,发生反应的化学方程式为:Fe+2AgNO3═Fe(NO3)2+2Ag;
(3)若向滤渣中加稀盐酸,有气泡产生,说明铁过量,则滤渣中一定含有Ag、Fe;
铁过量,则滤液中一定有Zn(NO3)2、Fe(NO3)2,一定不含有AgNO3.
故填:胶头滴管伸入试管中;Fe+2AgNO3═Fe(NO3)2+2Ag;Ag、Fe;Zn(NO3)2、Fe(NO3)2.
【点评】要会利用金属活动顺序表分析实
( http: / / www.21cnjy.com )验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.
8.某活动小组在一次活动探究实验后,得
( http: / / www.21cnjy.com )知废液当中含有硝酸银、硝酸铝,产生了好奇心.想回收一种重要的金属和一种晶体,进行了下列实验,请回答下列问题:
(1)操作的顺序是 ②①③④ .
(2)②步加人的金属粉末是 铝粉 .
(3)发生反应的化学方程式为 Al+3AgNO3═Al(NO3)3+3Ag .
【考点】金属的化学性质;书写化学方程式、文字表达式、电离方程式.
【专题】结合课本知识的信息;金属与金属材料.
【分析】铝比银活泼,能和硝酸银反应生成硝酸铝和银.
【解答】解:(1)想回收银并且得到硝酸铝晶体,应该进行的操作顺序是②①③④;
(2)②步加人的金属粉末是铝粉;
(3)加入铝粉后,铝能和硝酸银反应生成硝酸铝和银,反应的化学方程式为:Al+3AgNO3═Al(NO3)3+3Ag.
故填:②①③④;铝粉;Al+3AgNO3═Al(NO3)3+3Ag.
【点评】要会利用金属活动顺序表
( http: / / www.21cnjy.com )分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.
9.某课外活动小组欲探究Mg、Fe、C
( http: / / www.21cnjy.com )u、Ag四种金属的活动性顺序.他们找来大小、薄厚均相同的四种金属片、一瓶稀盐酸和一瓶无色溶液,完成了探究实验.请你利用所学知识判断:
(1)上述无色溶液是 硝酸银 溶液.
(2)实验中,能说明Mg和Fe活动性关系的现象是 镁与稀盐酸反应速率比铁与稀盐酸反应速率快 .
(3)实验中,发生的化学反应基本类型都是 置换反应 .
【考点】金属活动性顺序及其应用;反应类型的判定.
【专题】金属与金属材料.
【分析】根据金属活动性顺序表及其应用分析,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
【解答】解:由金属活动性顺序表及其应用可知
( http: / / www.21cnjy.com ),运用稀盐酸首先可验证镁比铁活泼,镁、铁比铜、银活泼.因为稀盐酸和铁镁能反应生成氢气而铜银与稀盐酸不反应不产生氢气,且镁比铁产生氢气的速度快.但不能验证铜和银的金属活动性.利用在金属活动顺序表中前面的金属能把后面的金属从它的化合物的溶液中置换出来,可用硝酸银的无色溶液来比较铜银的活动性.所以:
(1)上述无色溶液是硝酸银溶液.
(2)实验中,能说明Mg和Fe活动性关系的现象是:镁与稀盐酸反应速率比铁与稀盐酸反应速率快.
(3)实验中,发生的化学反应是金属与酸、盐的反应,都属于置换反应.
故答案:(1)硝酸银溶液;②镁与稀盐酸反应速率比铁与稀盐酸反应速率快;③置换反应.
【点评】主要考查了对金属活动性顺序的实验探究,掌握住金属和酸、盐反应,培养学生对知识的灵活应用,考查学生分析问题和计算能力.
金属的化学性质》同步练习卷
一、选择题
1.早在2000多年前的西汉时期就有“曾青得铁则化为铜”的记载,从现代化学的观点理解,这句话的含义是( )
A.木炭还原氧化铜生成单质铜
B.氧化铜在单质铁的催化作用下,分解生成铜
C.氢氧化铜沉淀和铁反应生成单质铜
D.单质铁从含铜的化合物的溶液中置换出铜
2.用熟石灰(化学式为Ca(OH)2)和硫酸铜来配制农药波尔多液时,不能使用的容器是( )
A.铝制容器
B.铁制容器
C.塑料容器
D.玻璃容器
3.把过量的铁粉加人到硫酸铜溶液中,充分反应后过滤,留在滤纸上的物质是( )
A.铁
B.铜
C.硫酸铜
D.铁和铜
4.可以用金属与相应的酸直接反应制取的盐是( )
A.FeCl3B.CuCl2C.HgCl2D.MgCl2
5.为验证铁、铜、铝三种金属的活动性顺序,可选用的一组物质是( )
A.AlCl3溶液、Cu、FeSO4溶液
B.CuSO4溶液、Fe、AlCl3溶液
C.AlCl3溶液、Fe、Cu
D.Al、Cu和AgNO3溶液
6.向AgNO3、Cu(NO3)2、Mg(NO3)2的混合溶液中加入一些锌粉,完全反应后过滤,不可能存在的情况是( )
A.滤纸上有Ag、Cu,滤液中有Zn2+、Mg2+、Ag+
B.滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Mg2+
C.滤纸上有Ag、Cu,滤液中有Zn2+、Mg2+
D.滤纸上有Ag、Cu、Zn,滤液中有Zn2+、Mg2+
二、非选择题
7.根据下列操作回答问题:
(1)图中的操作错误是 ;
(2)烧杯中发生反应的化学方程式为 ;
(3)若向滤渣中加稀盐酸,有气泡产生,则滤渣中一定含有 ;
则滤液中一定有 .
8.某活动小组在一次活动探究实验后,得知
( http: / / www.21cnjy.com )废液当中含有硝酸银、硝酸铝,产生了好奇心.想回收一种重要的金属和一种晶体,进行了下列实验,请回答下列问题:
(1)操作的顺序是 .
(2)②步加人的金属粉末是 .
(3)发生反应的化学方程式为 .
9.某课外活动小组欲探究Mg、Fe、Cu、
( http: / / www.21cnjy.com )Ag四种金属的活动性顺序.他们找来大小、薄厚均相同的四种金属片、一瓶稀盐酸和一瓶无色溶液,完成了探究实验.请你利用所学知识判断:
(1)上述无色溶液是 溶液.
(2)实验中,能说明Mg和Fe活动性关系的现象是 .
(3)实验中,发生的化学反应基本类型都是 .
新人教版九年级下册《8.2
金属的化学性质》同步练习卷
参考答案与试题解析
一、选择题
1.早在2000多年前的西汉时期就有“曾青得铁则化为铜”的记载,从现代化学的观点理解,这句话的含义是( )
A.木炭还原氧化铜生成单质铜
B.氧化铜在单质铁的催化作用下,分解生成铜
C.氢氧化铜沉淀和铁反应生成单质铜
D.单质铁从含铜的化合物的溶液中置换出铜
【考点】金属的化学性质.
【专题】结合课本知识的信息;金属与金属材料.
【分析】铁比铜活泼,能够把铜从它的可溶性盐中置换出来.
【解答】解:“曾青得铁则化为铜”,从现代化学的观点理解,这句话的含义是单质铁从含铜的化合物的溶液中置换出铜.
故选:D.
【点评】要会利用金属活动顺序表分析实验,氢
( http: / / www.21cnjy.com )前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.
2.用熟石灰(化学式为Ca(OH)2)和硫酸铜来配制农药波尔多液时,不能使用的容器是( )
A.铝制容器
B.铁制容器
C.塑料容器
D.玻璃容器
【考点】金属的化学性质.
【专题】金属与金属材料.
【分析】根据若配制农药波尔
( http: / / www.21cnjy.com )多液的原料能与容器的主要成分发生化学反应,则不能使用这种容器配制;结合在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,进行分析判断.
【解答】解:A、在金属活动性顺序中,铝在铜的前面,能与硫酸铜反应生成硫酸铝和铜,使药效降低,不能使用铝制容器,故选项正确.
B、在金属活动性顺序中,铁在铜的前面,能与硫酸铜反应生成硫酸亚铁和铜,使药效降低,不能使用铁制容器,故选项正确.
C、塑料容器与熟石灰和硫酸都不反应,可以使用塑料容器,故选项错误.
D、玻璃容器与熟石灰和硫酸都不反应,可以使用玻璃容器,故选项错误.
故选:AB.
【点评】本题难度不大,掌握能用于盛放农药波尔多液的容器不能与原料发生化学反应、金属的化学性质是正确解答本题的关键.
3.把过量的铁粉加人到硫酸铜溶液中,充分反应后过滤,留在滤纸上的物质是( )
A.铁
B.铜
C.硫酸铜
D.铁和铜
【考点】金属的化学性质.
【专题】金属与金属材料.
【分析】铁比铜活泼,能和硫酸铜反应生成硫酸亚铁和铜.
【解答】解:铁比铜活泼,能和硫酸铜反应
( http: / / www.21cnjy.com )生成硫酸亚铁和铜,把过量的铁粉加人到硫酸铜溶液中,充分反应后过滤,留在滤纸上的物质是反应生成的铜和过量的铁.
故选:D.
【点评】要会利用金属活动顺序表分析
( http: / / www.21cnjy.com )实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.
4.可以用金属与相应的酸直接反应制取的盐是( )
A.FeCl3B.CuCl2C.HgCl2D.MgCl2
【考点】金属的化学性质.
【专题】结合课本知识的信息;金属与金属材料.
【分析】铁和稀盐酸反应生成氯化亚铁和氢气;
铜不能和稀盐酸反应;
汞不能和稀盐酸反应;
镁和稀盐酸反应生成氯化镁和氢气.
【解答】解:A、铁和稀盐酸反应生成氯化亚铁和氢气,因此氯化铁不能由金属与相应的酸直接反应制取;
B、铜不能和稀盐酸反应,因此氯化铜不能由金属与相应的酸直接反应制取;
C、汞不能和稀盐酸反应,因此氯化汞不能由金属与相应的酸直接反应制取;
D、镁和稀盐酸反应生成氯化镁和氢气,因此氯化镁可以用金属与相应的酸直接反应制取.
故选:D.
【点评】要会利用金属活动顺序表分析
( http: / / www.21cnjy.com )实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.
5.为验证铁、铜、铝三种金属的活动性顺序,可选用的一组物质是( )
A.AlCl3溶液、Cu、FeSO4溶液
B.CuSO4溶液、Fe、AlCl3溶液
C.AlCl3溶液、Fe、Cu
D.Al、Cu和AgNO3溶液
【考点】金属活动性顺序及其应用.
【专题】金属与金属材料.
【分析】验证铜、铁、铝三种金属的活动性强弱,
( http: / / www.21cnjy.com )一般是利用金属与酸反应或金属与盐溶液的反应,通过金属和酸是否反应或剧烈程度判断金属的活动性,或通过金属是否能和盐溶液发生置换反应判断金属活动性.
【解答】解:A、铜和FeSO4溶液、AlCl3溶液都不反应,无法判断铁和铝的活泼性,故错;
B、铁与CuSO4溶液反应,与AlCl3溶液不反应,能判断三种金属的活动性顺序,故对;
C、Cu、Fe均不能置换出AlCl3溶液中的铝,无法判断铁、铜的金属活动性,故错;
D、AgNO3溶液和铝、铜都反应,没有铁.无法判断铁、铜、铝的活泼性,故错.
故选:B.
【点评】化学实验方案的设计
( http: / / www.21cnjy.com )与评价是素质教育的基本要求,是考查学生能力的主要题目类型,同时也是实验教与学难点所在,在具体设计时,要充分利用教材资源,对其原理透彻理解,学会信息迁移,既要模仿,又要注重创新,在评价时要注重比较的方法.
6.向AgNO3、Cu(NO3)2、Mg(NO3)2的混合溶液中加入一些锌粉,完全反应后过滤,不可能存在的情况是( )
A.滤纸上有Ag、Cu,滤液中有Zn2+、Mg2+、Ag+
B.滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Mg2+
C.滤纸上有Ag、Cu,滤液中有Zn2+、Mg2+
D.滤纸上有Ag、Cu、Zn,滤液中有Zn2+、Mg2+
【考点】金属的化学性质.
【专题】结合课本知识的信息;金属与金属材料.
【分析】镁比锌活泼,锌比铜活泼,铜比银活泼,因此锌能和硝酸铜反应生成硝酸锌和铜,能和硝酸银反应生成硝酸锌和银.
【解答】解:A、加入一些
( http: / / www.21cnjy.com )锌粉时,锌先和硝酸银反应,当硝酸银完全反应后,锌再和硝酸铜反应,因此当滤纸上有Ag、Cu时,滤液中一定不含有Ag+,该选项说法不正确;
B、加入一些锌粉时,锌先和硝酸银反应,
( http: / / www.21cnjy.com )当锌不足以和硝酸银完全反应,即锌不足时,滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Mg2+,该选项说法正确;
C、加入一些锌粉时,锌先和硝酸银反应,
( http: / / www.21cnjy.com )当硝酸银完全反应后,锌再和硝酸铜反应,因此当滤纸上有Ag、Cu时,滤液中有Zn2+、Mg2+,该选项说法正确;
D、加入一些锌粉时,锌先和硝酸银反
( http: / / www.21cnjy.com )应,当硝酸银完全反应后,锌再和硝酸铜反应,因此当滤纸上有Ag、Cu、Zn时,滤液中有Zn2+、Mg2+,该选项说法正确.
故选:A.
【点评】要会利用金属活动顺序表分析实验,
( http: / / www.21cnjy.com )氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.
二、非选择题
7.根据下列操作回答问题:
(1)图中的操作错误是 胶头滴管伸入试管中 ;
(2)烧杯中发生反应的化学方程式为 Fe+2AgNO3═Fe(NO3)2+2Ag ;
(3)若向滤渣中加稀盐酸,有气泡产生,则滤渣中一定含有 Ag、Fe ;
则滤液中一定有 Zn(NO3)2、Fe(NO3)2 .
【考点】金属的化学性质;书写化学方程式、文字表达式、电离方程式.
【专题】金属与金属材料.
【分析】锌比铁活泼,铁比银活泼,铁和硝酸银反应生成硝酸亚铁和银,铁不能和硝酸锌反应;
铁能和稀盐酸反应生成氯化亚铁和氢气,银不能和稀盐酸反应.
【解答】解:(1)图中的操作错误是胶头滴管伸入试管中;
(2)烧杯中,铁和硝酸银反应生成硝酸亚铁和银,发生反应的化学方程式为:Fe+2AgNO3═Fe(NO3)2+2Ag;
(3)若向滤渣中加稀盐酸,有气泡产生,说明铁过量,则滤渣中一定含有Ag、Fe;
铁过量,则滤液中一定有Zn(NO3)2、Fe(NO3)2,一定不含有AgNO3.
故填:胶头滴管伸入试管中;Fe+2AgNO3═Fe(NO3)2+2Ag;Ag、Fe;Zn(NO3)2、Fe(NO3)2.
【点评】要会利用金属活动顺序表分析实
( http: / / www.21cnjy.com )验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.
8.某活动小组在一次活动探究实验后,得
( http: / / www.21cnjy.com )知废液当中含有硝酸银、硝酸铝,产生了好奇心.想回收一种重要的金属和一种晶体,进行了下列实验,请回答下列问题:
(1)操作的顺序是 ②①③④ .
(2)②步加人的金属粉末是 铝粉 .
(3)发生反应的化学方程式为 Al+3AgNO3═Al(NO3)3+3Ag .
【考点】金属的化学性质;书写化学方程式、文字表达式、电离方程式.
【专题】结合课本知识的信息;金属与金属材料.
【分析】铝比银活泼,能和硝酸银反应生成硝酸铝和银.
【解答】解:(1)想回收银并且得到硝酸铝晶体,应该进行的操作顺序是②①③④;
(2)②步加人的金属粉末是铝粉;
(3)加入铝粉后,铝能和硝酸银反应生成硝酸铝和银,反应的化学方程式为:Al+3AgNO3═Al(NO3)3+3Ag.
故填:②①③④;铝粉;Al+3AgNO3═Al(NO3)3+3Ag.
【点评】要会利用金属活动顺序表
( http: / / www.21cnjy.com )分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.
9.某课外活动小组欲探究Mg、Fe、C
( http: / / www.21cnjy.com )u、Ag四种金属的活动性顺序.他们找来大小、薄厚均相同的四种金属片、一瓶稀盐酸和一瓶无色溶液,完成了探究实验.请你利用所学知识判断:
(1)上述无色溶液是 硝酸银 溶液.
(2)实验中,能说明Mg和Fe活动性关系的现象是 镁与稀盐酸反应速率比铁与稀盐酸反应速率快 .
(3)实验中,发生的化学反应基本类型都是 置换反应 .
【考点】金属活动性顺序及其应用;反应类型的判定.
【专题】金属与金属材料.
【分析】根据金属活动性顺序表及其应用分析,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
【解答】解:由金属活动性顺序表及其应用可知
( http: / / www.21cnjy.com ),运用稀盐酸首先可验证镁比铁活泼,镁、铁比铜、银活泼.因为稀盐酸和铁镁能反应生成氢气而铜银与稀盐酸不反应不产生氢气,且镁比铁产生氢气的速度快.但不能验证铜和银的金属活动性.利用在金属活动顺序表中前面的金属能把后面的金属从它的化合物的溶液中置换出来,可用硝酸银的无色溶液来比较铜银的活动性.所以:
(1)上述无色溶液是硝酸银溶液.
(2)实验中,能说明Mg和Fe活动性关系的现象是:镁与稀盐酸反应速率比铁与稀盐酸反应速率快.
(3)实验中,发生的化学反应是金属与酸、盐的反应,都属于置换反应.
故答案:(1)硝酸银溶液;②镁与稀盐酸反应速率比铁与稀盐酸反应速率快;③置换反应.
【点评】主要考查了对金属活动性顺序的实验探究,掌握住金属和酸、盐反应,培养学生对知识的灵活应用,考查学生分析问题和计算能力.
同课章节目录
