4.1化学式 教学设计 化学科粤版2024九年级上册
文档属性
| 名称 | 4.1化学式 教学设计 化学科粤版2024九年级上册 |

|
|
| 格式 | docx | ||
| 文件大小 | 459.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-07-14 00:00:00 | ||
图片预览

文档简介
第四单元 化学式与化学方程式
4.1 化学式
1.知识与技能
(1)能说出化学式的含义。
(2)能依据物质组成、利元素化合价书写常见物质的化学式。
(3)能根据化学式进行物质组成的简单计算。
2.过程与方法
逐步形成对事物进行抽象概括和定量处理的能力。
3.情感态度与价值观
养成尊重客观实际,认真、严谨的科学态度。
【重点】1.通常用化学式表示物质的组成。
2.可以利用元素化合价书写化学式。
3.写化学式时,正价元素通常写在左边,负价元素通常写在右边。原子的数目用阿拉伯数字写在元素符号的右下角。在金属化合物中,金属元素一般呈正价,非金属元素一般呈负价;在非金属氧化物中,非金属元素一般呈正价。根据化合物中各种元素化合价的代数和等于零的原则,确定化合物中各种元素原子的数目。
4.简单化合物的中文命名原则。
5.两种元素组成的化合物,在两种元素中间用“化”字连接,如氧化铜(CuO)
6.化学式中元素的名称从右向左读,与化学式的写法刚好相反,如氯化钠(NaC1)。
7.元素的原子个数在该元素之前先读出,如五氧化二磷(P2O5)。
8.含有复杂原子团的化合物,要根据其特征来称呼,不需读出原子或原子团的个数,如氢氧化钠(NaOH) 、碳酸钙(CaCO3)、硫酸钠(Na2SO4) 等。
【难点】1.元素的化合价。
2.元素的化合价在化学式中的体现。
3.化学式的读写。
[新课导入]
知识回顾
1.什么是元素具有相同核电荷数(即质子数)的一类原子的总称。
2.物质、元素、分子、原子之间的关系
3.元素符号
为方便区分和交流,国际上规定每种元素都采用统一的符号来表示,这种符号叫做元素符号。
如:H——氢元素
O——氧元素
Cl——氯元素
4.元素符号的含义
宏观意义:表示一种元素;有的元素还表示一种物质,如Fe
微观意义:表示一个原子;如元素符号H宏观上表示氢元素;微观上表示一个氢原子。
若在元素符号的前面加一个数字,则只表示原子的个数,此时无宏观意义。
如:“3H”“5C”“7Na”
[课程讲授]
一、怎样表示物质的组成与构成
构成物质时,各元素的原子或离子之间存在一定的数量关系,如二氧化碳是由碳元素和氧元素组成,每个二氧化碳分子又是由1个碳原子和2个氧原子构成。所以我们可以用CO2来表示二氧化碳的组成。
1.化学式:国际上用元素符号和数字的组合表示物质组成的式子。
思考:
①任何物质都有化学式吗?
只有纯净物才能用化学式表示其组成
②同种物质可以有不同的化学式吗?
一种物质只有一个化学式。
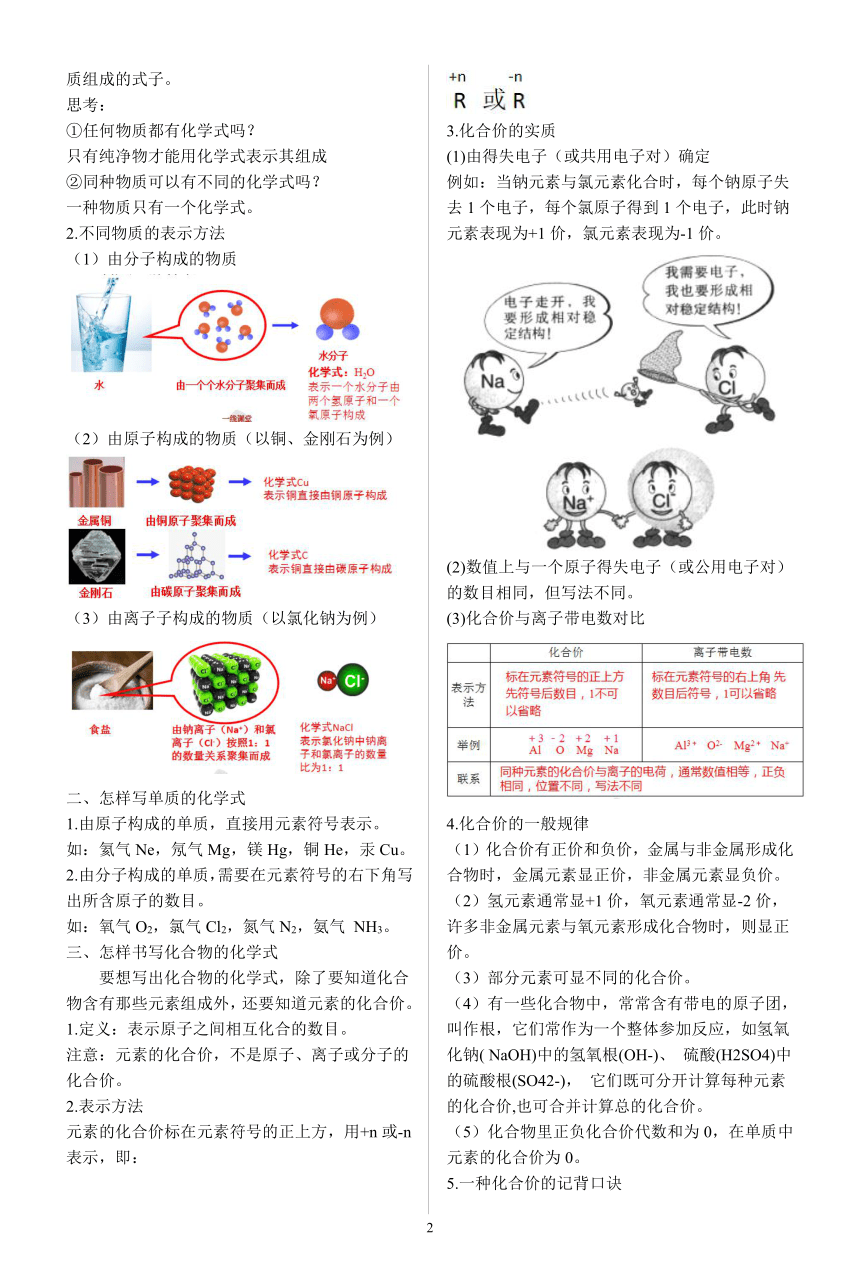
2.不同物质的表示方法
(1)由分子构成的物质
(2)由原子构成的物质(以铜、金刚石为例)
(3)由离子子构成的物质(以氯化钠为例)
二、怎样写单质的化学式
1.由原子构成的单质,直接用元素符号表示。
如:氦气Ne,氖气Mg,镁Hg,铜He,汞Cu。
2.由分子构成的单质,需要在元素符号的右下角写出所含原子的数目。
如:氧气O2,氯气Cl2,氮气N2,氨气 NH3。
三、怎样书写化合物的化学式
要想写出化合物的化学式,除了要知道化合物含有那些元素组成外,还要知道元素的化合价。
1.定义:表示原子之间相互化合的数目。
注意:元素的化合价,不是原子、离子或分子的化合价。
2.表示方法
元素的化合价标在元素符号的正上方,用+n或-n表示,即:
3.化合价的实质
(1)由得失电子(或共用电子对)确定
例如:当钠元素与氯元素化合时,每个钠原子失去1个电子,每个氯原子得到1个电子,此时钠元素表现为+1价,氯元素表现为-1价。
(2)数值上与一个原子得失电子(或公用电子对)的数目相同,但写法不同。
(3)化合价与离子带电数对比
4.化合价的一般规律
(1)化合价有正价和负价,金属与非金属形成化合物时,金属元素显正价,非金属元素显负价。
(2)氢元素通常显+1价,氧元素通常显-2价,许多非金属元素与氧元素形成化合物时,则显正价。
(3)部分元素可显不同的化合价。
(4)有一些化合物中,常常含有带电的原子团,叫作根,它们常作为一个整体参加反应,如氢氧化钠( NaOH)中的氢氧根(OH-)、 硫酸(H2SO4)中的硫酸根(SO42-), 它们既可分开计算每种元素的化合价,也可合并计算总的化合价。
(5)化合物里正负化合价代数和为0,在单质中元素的化合价为0。
5.一种化合价的记背口诀
一价氢氯(负)钾钠银 二价氧(负)钙钡镁锌
三铝四硅五氮磷二 三三铁、二四碳
二四六硫价可变 铜汞二价最常见
负一硝酸氢氧根 负二硫酸碳酸根
负三记住磷酸根 正一价的是铵根
注:可对照教材上的“部分常用元素或原子团的化合价”表格进行记背。
化合价和化学式
1.标注元素的化合价
(1)既要标注正负,又要标注数值
(2)求下列物质中带下划线元素的化合价
(3)求下列物质中根的化合价
2.根据化合价写化学式
根据化合价写化学式还可以使用十字交叉法(以CO2的书写为例)
(1)写出元素,正价在左,负价在右
(2)标出各元素的化合价
(3)化合价的绝对值标在另一元素下
(4)角标化简
3.含有“根”化合物的化学式书写
写法基本与前面相同,当“根”的个数≧1时,需要加括号。
随堂小练
写出下列物质的化学式
硫酸铜CuSO4,碳酸钠Na2CO3, 氢氧化铝Al(OH)3,硝酸银AgNO3,硫酸铝NH4Cl, 氯化铵Al2(SO4)3。
四、怎样读化合物的化学式
从右向左读作:某化某或某酸某
(1)由两种元素组成的化合物:“某化某”
如:KCl CaO CuO Na2S NaCl HCl
氯化钾 氧化钙 氧化铜 硫化钠 氯化钠 氯化氢
(2)氧化物有时要读出各原子的个数:“几氧化几某”
如:Fe3O4 Fe2O3 CO2 CO P2O5
四氧化三铁 氧化铁 二氧化碳 一氧化碳 五氧化二磷
MnO2 SO2 SO3 NO NO2 Al2O3
二氧化锰 二氧化硫 三氧化硫 一氧化氮 二氧化氮 氧化铝
(3)含有原子团的化合物:“某酸某” “氢氧化某”
如:Na2CO3 AgNO3 K2SO4 (NH4)2SO4
碳酸钠 硝酸银 硫酸钾 硫酸铵
NaOH Ca(OH)2 Fe(OH)3 Ba(OH)2
氢氧化钠 氢氧化钙 氢氧化铁 氢氧化钡
(4)如果酸根与H组合,直接读“某酸”
如:HCl H2CO3 H2SO4 HNO3 H3PO4
盐酸 碳酸 硫酸 硝酸 磷酸
化学式的含义
1.由分子构成的物质化学式的意义
2.由原子构成的物质化学式的意义
3.由离子构成的物质化学式的意义(以NaCl为例)
若化学式前加上数字,表示微粒的个数,不再有宏观意义。
五、怎样根据化学式进行计算
1.计算相对分子质量
相对分子质量:化学式中各原子的相对原子质量总和。
例1.计算水的相对分子质量
=2×1+16=18
例2.计算 NH4NO3 的相对分子质量
= 14×2+1×4+16×3=80
例3.计算 Al2(SO4)3 的相对分子质量
= 27×2+(32×1+16×4)×3
=342
随堂小测
1.计算CaCO3的相对分子质量
=40×1+12×1+16×3=100
2.计算CuSO4·5H2O的相对分子质量
=64×1+32×1+16×4+5×(1×2+16)=250
3.计算(NH4)2SO4的相对分子质量
=(14×1+1×4)×2+32×1+16×4=132
2.计算组成化合物各元素的质量比
化合物各元素的质量比等于它们的相对原子质量之和的比。
例.计算水中氢元素与氧元素的质量比
=(2×1):16=1:8
随堂小测
1.计算CO2中碳、氢元素的质量比
=12:16×2=3:8
2.计算NH4NO3中氮、氢、氧元素的质量比
=(14×2):(1×5):(16×3)=7:1:12
3.计算Ca(OH)2中钙、氧、氢元素的质量比
=40:(16×2):(1×2)=20:16:1
3.计算化合物种某元素的质量分数
例1.求水(H2O)中氢元素的质量分数
例2.计算硝酸铵NH4NO3中氮元素质量分数
随堂小测
相对原子质量:H-1 C-12 N-14 O-16 Ca-40
1.求CaCO3中氧元素的质量分数
2.求CO(NH2)2中氮元素的质量分数
4.求化合物中元素的质量或已知元素的质量求化合物的质量
某元素的质量=化合物的质量×某元素的质量分数
化合物的质量=某元素的质量÷某元素的质量分数
例1.18g水中含g氢元素。
例2. g二氧化硫中含硫元素32g。
[随堂小结]
1.化学式:用元素符号和数字的组合来表示物质组成的式子。
2.化学式的含义:宏观、微观。
3.化学式的写法:单质、化合物。
4.化合价:与单个离子所带电荷数(或公用电子对数)有关,标注在元素符号的上方。
5.化合物中元素的化合价代数和为0,单质中元素的化合价为0。
6.根据化合价书写化学式。
7.有关化学式的计算。
[典型例题]
第1课时
考点一:化学式的意义
【例1】下列化学用语中,既能表示一种物质,还能表示一种元素的是( C )
A.H B.Cl2 C.Cu D.2N
【例2】下列关于CH4(甲烷)的意义中,不正确的是( D )
A.表示甲烷这种物质
B.表示一个甲烷分子
C.表示甲烷是由碳元素和氢元素组成的
D.表示甲烷气体由一个碳原子和4个氢原子组成
考点二:化学式的书写
【例3】用下列物质的化学式填空:a.铜丝 b.干冰 c.氢气 d.氧气 e.过氧化氢。
(1)可用作清洁能源的是H2;
(2)可用于人工降雨的是CO2;
(3)可用作导线的是Cu;
(4)能供给生物呼吸的是O2。
【例4】用元素符号或化学式填空。
氮气N2;2个氮原子2N;氦气He;2个氧分子2O2;铁Fe。
利用原子最外层电子数来讲解元素的化合价有一定的说服力,学生也易于记忆元素的化合价,效果比较好。书写化学式,对学生来说有一定的难度,需要让学生多练习、掌握。在教学过程中,可以把教材中的书写化学式的方法让学生自学,还重点讲解十字交叉法,这种方法更利于学生接受。关于化学方程式的计算,主要是“求总”“求分”“求比例”,对于数学功底较好的学生,难度不大,但是对于一般的学生,需要先做出示例,让学生先模仿,再练习,最终熟能生巧。
4.1 化学式
1.知识与技能
(1)能说出化学式的含义。
(2)能依据物质组成、利元素化合价书写常见物质的化学式。
(3)能根据化学式进行物质组成的简单计算。
2.过程与方法
逐步形成对事物进行抽象概括和定量处理的能力。
3.情感态度与价值观
养成尊重客观实际,认真、严谨的科学态度。
【重点】1.通常用化学式表示物质的组成。
2.可以利用元素化合价书写化学式。
3.写化学式时,正价元素通常写在左边,负价元素通常写在右边。原子的数目用阿拉伯数字写在元素符号的右下角。在金属化合物中,金属元素一般呈正价,非金属元素一般呈负价;在非金属氧化物中,非金属元素一般呈正价。根据化合物中各种元素化合价的代数和等于零的原则,确定化合物中各种元素原子的数目。
4.简单化合物的中文命名原则。
5.两种元素组成的化合物,在两种元素中间用“化”字连接,如氧化铜(CuO)
6.化学式中元素的名称从右向左读,与化学式的写法刚好相反,如氯化钠(NaC1)。
7.元素的原子个数在该元素之前先读出,如五氧化二磷(P2O5)。
8.含有复杂原子团的化合物,要根据其特征来称呼,不需读出原子或原子团的个数,如氢氧化钠(NaOH) 、碳酸钙(CaCO3)、硫酸钠(Na2SO4) 等。
【难点】1.元素的化合价。
2.元素的化合价在化学式中的体现。
3.化学式的读写。
[新课导入]
知识回顾
1.什么是元素具有相同核电荷数(即质子数)的一类原子的总称。
2.物质、元素、分子、原子之间的关系
3.元素符号
为方便区分和交流,国际上规定每种元素都采用统一的符号来表示,这种符号叫做元素符号。
如:H——氢元素
O——氧元素
Cl——氯元素
4.元素符号的含义
宏观意义:表示一种元素;有的元素还表示一种物质,如Fe
微观意义:表示一个原子;如元素符号H宏观上表示氢元素;微观上表示一个氢原子。
若在元素符号的前面加一个数字,则只表示原子的个数,此时无宏观意义。
如:“3H”“5C”“7Na”
[课程讲授]
一、怎样表示物质的组成与构成
构成物质时,各元素的原子或离子之间存在一定的数量关系,如二氧化碳是由碳元素和氧元素组成,每个二氧化碳分子又是由1个碳原子和2个氧原子构成。所以我们可以用CO2来表示二氧化碳的组成。
1.化学式:国际上用元素符号和数字的组合表示物质组成的式子。
思考:
①任何物质都有化学式吗?
只有纯净物才能用化学式表示其组成
②同种物质可以有不同的化学式吗?
一种物质只有一个化学式。
2.不同物质的表示方法
(1)由分子构成的物质
(2)由原子构成的物质(以铜、金刚石为例)
(3)由离子子构成的物质(以氯化钠为例)
二、怎样写单质的化学式
1.由原子构成的单质,直接用元素符号表示。
如:氦气Ne,氖气Mg,镁Hg,铜He,汞Cu。
2.由分子构成的单质,需要在元素符号的右下角写出所含原子的数目。
如:氧气O2,氯气Cl2,氮气N2,氨气 NH3。
三、怎样书写化合物的化学式
要想写出化合物的化学式,除了要知道化合物含有那些元素组成外,还要知道元素的化合价。
1.定义:表示原子之间相互化合的数目。
注意:元素的化合价,不是原子、离子或分子的化合价。
2.表示方法
元素的化合价标在元素符号的正上方,用+n或-n表示,即:
3.化合价的实质
(1)由得失电子(或共用电子对)确定
例如:当钠元素与氯元素化合时,每个钠原子失去1个电子,每个氯原子得到1个电子,此时钠元素表现为+1价,氯元素表现为-1价。
(2)数值上与一个原子得失电子(或公用电子对)的数目相同,但写法不同。
(3)化合价与离子带电数对比
4.化合价的一般规律
(1)化合价有正价和负价,金属与非金属形成化合物时,金属元素显正价,非金属元素显负价。
(2)氢元素通常显+1价,氧元素通常显-2价,许多非金属元素与氧元素形成化合物时,则显正价。
(3)部分元素可显不同的化合价。
(4)有一些化合物中,常常含有带电的原子团,叫作根,它们常作为一个整体参加反应,如氢氧化钠( NaOH)中的氢氧根(OH-)、 硫酸(H2SO4)中的硫酸根(SO42-), 它们既可分开计算每种元素的化合价,也可合并计算总的化合价。
(5)化合物里正负化合价代数和为0,在单质中元素的化合价为0。
5.一种化合价的记背口诀
一价氢氯(负)钾钠银 二价氧(负)钙钡镁锌
三铝四硅五氮磷二 三三铁、二四碳
二四六硫价可变 铜汞二价最常见
负一硝酸氢氧根 负二硫酸碳酸根
负三记住磷酸根 正一价的是铵根
注:可对照教材上的“部分常用元素或原子团的化合价”表格进行记背。
化合价和化学式
1.标注元素的化合价
(1)既要标注正负,又要标注数值
(2)求下列物质中带下划线元素的化合价
(3)求下列物质中根的化合价
2.根据化合价写化学式
根据化合价写化学式还可以使用十字交叉法(以CO2的书写为例)
(1)写出元素,正价在左,负价在右
(2)标出各元素的化合价
(3)化合价的绝对值标在另一元素下
(4)角标化简
3.含有“根”化合物的化学式书写
写法基本与前面相同,当“根”的个数≧1时,需要加括号。
随堂小练
写出下列物质的化学式
硫酸铜CuSO4,碳酸钠Na2CO3, 氢氧化铝Al(OH)3,硝酸银AgNO3,硫酸铝NH4Cl, 氯化铵Al2(SO4)3。
四、怎样读化合物的化学式
从右向左读作:某化某或某酸某
(1)由两种元素组成的化合物:“某化某”
如:KCl CaO CuO Na2S NaCl HCl
氯化钾 氧化钙 氧化铜 硫化钠 氯化钠 氯化氢
(2)氧化物有时要读出各原子的个数:“几氧化几某”
如:Fe3O4 Fe2O3 CO2 CO P2O5
四氧化三铁 氧化铁 二氧化碳 一氧化碳 五氧化二磷
MnO2 SO2 SO3 NO NO2 Al2O3
二氧化锰 二氧化硫 三氧化硫 一氧化氮 二氧化氮 氧化铝
(3)含有原子团的化合物:“某酸某” “氢氧化某”
如:Na2CO3 AgNO3 K2SO4 (NH4)2SO4
碳酸钠 硝酸银 硫酸钾 硫酸铵
NaOH Ca(OH)2 Fe(OH)3 Ba(OH)2
氢氧化钠 氢氧化钙 氢氧化铁 氢氧化钡
(4)如果酸根与H组合,直接读“某酸”
如:HCl H2CO3 H2SO4 HNO3 H3PO4
盐酸 碳酸 硫酸 硝酸 磷酸
化学式的含义
1.由分子构成的物质化学式的意义
2.由原子构成的物质化学式的意义
3.由离子构成的物质化学式的意义(以NaCl为例)
若化学式前加上数字,表示微粒的个数,不再有宏观意义。
五、怎样根据化学式进行计算
1.计算相对分子质量
相对分子质量:化学式中各原子的相对原子质量总和。
例1.计算水的相对分子质量
=2×1+16=18
例2.计算 NH4NO3 的相对分子质量
= 14×2+1×4+16×3=80
例3.计算 Al2(SO4)3 的相对分子质量
= 27×2+(32×1+16×4)×3
=342
随堂小测
1.计算CaCO3的相对分子质量
=40×1+12×1+16×3=100
2.计算CuSO4·5H2O的相对分子质量
=64×1+32×1+16×4+5×(1×2+16)=250
3.计算(NH4)2SO4的相对分子质量
=(14×1+1×4)×2+32×1+16×4=132
2.计算组成化合物各元素的质量比
化合物各元素的质量比等于它们的相对原子质量之和的比。
例.计算水中氢元素与氧元素的质量比
=(2×1):16=1:8
随堂小测
1.计算CO2中碳、氢元素的质量比
=12:16×2=3:8
2.计算NH4NO3中氮、氢、氧元素的质量比
=(14×2):(1×5):(16×3)=7:1:12
3.计算Ca(OH)2中钙、氧、氢元素的质量比
=40:(16×2):(1×2)=20:16:1
3.计算化合物种某元素的质量分数
例1.求水(H2O)中氢元素的质量分数
例2.计算硝酸铵NH4NO3中氮元素质量分数
随堂小测
相对原子质量:H-1 C-12 N-14 O-16 Ca-40
1.求CaCO3中氧元素的质量分数
2.求CO(NH2)2中氮元素的质量分数
4.求化合物中元素的质量或已知元素的质量求化合物的质量
某元素的质量=化合物的质量×某元素的质量分数
化合物的质量=某元素的质量÷某元素的质量分数
例1.18g水中含g氢元素。
例2. g二氧化硫中含硫元素32g。
[随堂小结]
1.化学式:用元素符号和数字的组合来表示物质组成的式子。
2.化学式的含义:宏观、微观。
3.化学式的写法:单质、化合物。
4.化合价:与单个离子所带电荷数(或公用电子对数)有关,标注在元素符号的上方。
5.化合物中元素的化合价代数和为0,单质中元素的化合价为0。
6.根据化合价书写化学式。
7.有关化学式的计算。
[典型例题]
第1课时
考点一:化学式的意义
【例1】下列化学用语中,既能表示一种物质,还能表示一种元素的是( C )
A.H B.Cl2 C.Cu D.2N
【例2】下列关于CH4(甲烷)的意义中,不正确的是( D )
A.表示甲烷这种物质
B.表示一个甲烷分子
C.表示甲烷是由碳元素和氢元素组成的
D.表示甲烷气体由一个碳原子和4个氢原子组成
考点二:化学式的书写
【例3】用下列物质的化学式填空:a.铜丝 b.干冰 c.氢气 d.氧气 e.过氧化氢。
(1)可用作清洁能源的是H2;
(2)可用于人工降雨的是CO2;
(3)可用作导线的是Cu;
(4)能供给生物呼吸的是O2。
【例4】用元素符号或化学式填空。
氮气N2;2个氮原子2N;氦气He;2个氧分子2O2;铁Fe。
利用原子最外层电子数来讲解元素的化合价有一定的说服力,学生也易于记忆元素的化合价,效果比较好。书写化学式,对学生来说有一定的难度,需要让学生多练习、掌握。在教学过程中,可以把教材中的书写化学式的方法让学生自学,还重点讲解十字交叉法,这种方法更利于学生接受。关于化学方程式的计算,主要是“求总”“求分”“求比例”,对于数学功底较好的学生,难度不大,但是对于一般的学生,需要先做出示例,让学生先模仿,再练习,最终熟能生巧。
同课章节目录
