3.2 金属的腐蚀和防护 课件 (5)
文档属性
| 名称 | 3.2 金属的腐蚀和防护 课件 (5) |

|
|
| 格式 | zip | ||
| 文件大小 | 6.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-07-09 00:00:00 | ||
图片预览







文档简介
课件23张PPT。金属的腐蚀和防护教学目标:??
1?理解金属腐蚀的原因?
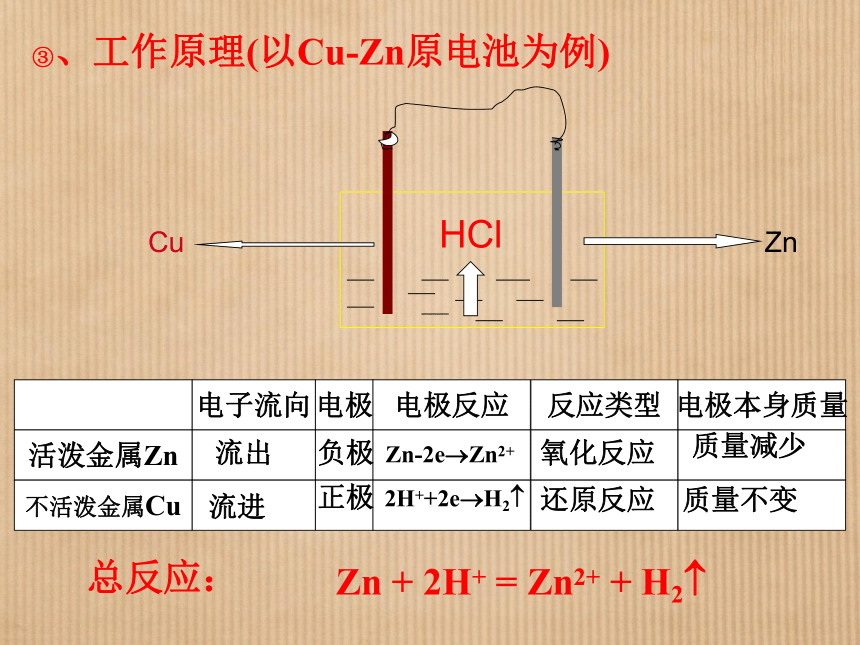
2?了解保护金属的一些方法?一、金属的腐蚀1、金属腐蚀1)定义(P49):金属的腐蚀是指金属或合金与周围接触到的气体或液体进行化学反应而腐蚀损耗的过程2)本质金属失去电子被氧化的过程2、原电池复习①、定义:②、构成条件把化学能转变为电能的装置③、工作原理(以Cu-Zn原电池为例)流出流进负极正极Zn-2e?Zn2+2H++2e?H2?氧化反应还原反应质量减少质量不变小结:①、原电池反应与普通氧化—还原反应在原理上是一样只是把氧化还原反应分别在两极进行,所以有电流产生。②、较活泼的金属通常为负极,被氧化而溶解;较不活泼的金属为正极,附近阳离子被还原而析出物质(如:H2)。 A、B、C三种金属两两接触后跟稀硫酸作用,判断
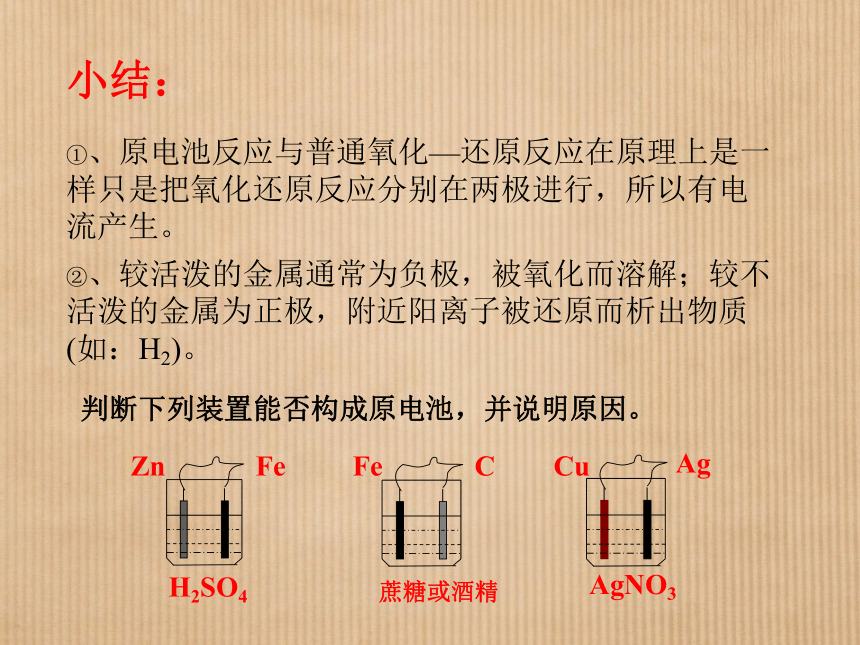
这三种金属的活动性:(1)在原电池中,作负极的金属、发生溶解的金属、发生氧化反应的金属等是相对活泼金属;
(2)在原电池中,作正极的金属、在酸中有氢气析出的金属、质量增加的金属为相对不活泼金属。练习1.C>B>A★判断金属活动性的规律:
①金属与水或酸反应越剧烈,该金属越活泼。
②金属所对应的氢氧化物的碱性越强,该金属越 活泼。
③一种金属能从另一种金属盐的溶液中将其置换 出 来,则该金属活泼性比另一金属强。
④两金属能够构成原电池时,做负极的金属比做正 极金属活泼。
⑤在电解过程中,一般地先得电子的金属阳离子对 应的金属单质的活泼性比后得电子的金属阳离子对应 的金属单质的活泼性差。1、为什么实验室制H2用粗锌比纯锌反应速率快? 2、实验室制氢气时常加入少量硫酸铜溶液,以加快反应速率,原因是什么?思考题:形成原电池可加快化学反应速率① 、析氢腐蚀正极条件:酸性环境负极Fe2++2OH–==Fe(OH) 2?4Fe(OH)2 + O2 + 2H2O==4Fe(OH)3Fe(OH)3?铁锈(Fe2O3 ·nH2O)② 、吸氧腐蚀 正极: 条件: 中性或碱性环境 负极: Fe-2e- == Fe2+2H2O+O2+4e-==4OH–思考题:马口铁和白口铁一旦有划痕后,在潮湿的空气中,谁被腐蚀的速度快?
作业:P53 1、2
“新学案”第二课时以下物品采用哪种方法防锈?? 海边码头上的钢轨、铁的徽章、放电熨斗的支架、钢刀片、铁制水闸、儿童游戏场中秋千架的钢架。 1.改变金属的内部组织结构
例如制造各种耐腐蚀的合金,如在普通钢铁中加入铬、镍等制成不锈钢。
二、金属的防护2.保护层法:在金属表面覆盖保护层,使金属制品与周围腐蚀介质隔离,从而防止腐蚀。 1).在钢铁制件表面涂上机油、凡士林、油漆或覆盖搪瓷、塑料等耐腐蚀的非金属材料。2).用电镀、热镀、喷镀等方法,在钢铁表面镀上一层不易被腐蚀的金属,如锌、锡、铬、镍等。这些金属常因氧化而形成一层致密的氧化物薄膜,从而阻止水和空气等对钢铁的腐蚀。3.【电化学保护】: ①将被保护的金属作为腐蚀电池的阴极,使其不受到腐蚀,所以也叫阴极保护法。这种方法主要有以下两种:
[牺牲阳极保护法] 此法是将活泼金属(如锌或锌的合金)连接在被保护的金属上,当发生电化腐蚀时,这种活泼金属作为负极发生氧化反应,因而减小或防止被保护金属的腐蚀。这种方法常用于保护水中的钢桩和海轮外壳等例如水中钢铁闸门的保护,通常在轮船的外壳水线以下处或在靠近螺旋浆的舵上焊上若干块锌块,来防止船壳等的腐蚀。[外加电流的保护法] 将被保护的金属和电源的负极连接,另选一块能导电的惰性材料接电源正极。通电后,使金属表面产生负电荷(电子)的聚积,因而抑制了金属失电子而达到保护目的。此法主要用于防止在土壤、海水及河水中的金属设备受到腐蚀。
②电化学保护的的另一种方法叫阳极保护法,即通过外加电压,使阳极在一定的电位范围内发生钝化的过程。可有效地阻滞或防止金属设备在酸、碱、盐类中腐蚀。1)、改变金属的内部结构2)、在金属表面覆盖保护层3)、电化学保护法金属防护方法总结练习1.下列现象与电化学腐蚀无关的是:( )
A.黄铜(铜锌合金)制作的铜锣不易产生铜绿
B.生铁比纯铁更易生锈
C.铁质器件附有铜质配件,在接触处易生锈
D银质奖牌久置表面变暗D2.铁钉和碳棒用导线连接后,浸入到食盐溶液中,可能发生的反应是: ( )
A.碳棒上放出Cl2 B.碳棒附近产生OH-
C.碳棒上放出H2 D.铁钉被氧化BD
1?理解金属腐蚀的原因?
2?了解保护金属的一些方法?一、金属的腐蚀1、金属腐蚀1)定义(P49):金属的腐蚀是指金属或合金与周围接触到的气体或液体进行化学反应而腐蚀损耗的过程2)本质金属失去电子被氧化的过程2、原电池复习①、定义:②、构成条件把化学能转变为电能的装置③、工作原理(以Cu-Zn原电池为例)流出流进负极正极Zn-2e?Zn2+2H++2e?H2?氧化反应还原反应质量减少质量不变小结:①、原电池反应与普通氧化—还原反应在原理上是一样只是把氧化还原反应分别在两极进行,所以有电流产生。②、较活泼的金属通常为负极,被氧化而溶解;较不活泼的金属为正极,附近阳离子被还原而析出物质(如:H2)。 A、B、C三种金属两两接触后跟稀硫酸作用,判断
这三种金属的活动性:(1)在原电池中,作负极的金属、发生溶解的金属、发生氧化反应的金属等是相对活泼金属;
(2)在原电池中,作正极的金属、在酸中有氢气析出的金属、质量增加的金属为相对不活泼金属。练习1.C>B>A★判断金属活动性的规律:
①金属与水或酸反应越剧烈,该金属越活泼。
②金属所对应的氢氧化物的碱性越强,该金属越 活泼。
③一种金属能从另一种金属盐的溶液中将其置换 出 来,则该金属活泼性比另一金属强。
④两金属能够构成原电池时,做负极的金属比做正 极金属活泼。
⑤在电解过程中,一般地先得电子的金属阳离子对 应的金属单质的活泼性比后得电子的金属阳离子对应 的金属单质的活泼性差。1、为什么实验室制H2用粗锌比纯锌反应速率快? 2、实验室制氢气时常加入少量硫酸铜溶液,以加快反应速率,原因是什么?思考题:形成原电池可加快化学反应速率① 、析氢腐蚀正极条件:酸性环境负极Fe2++2OH–==Fe(OH) 2?4Fe(OH)2 + O2 + 2H2O==4Fe(OH)3Fe(OH)3?铁锈(Fe2O3 ·nH2O)② 、吸氧腐蚀 正极: 条件: 中性或碱性环境 负极: Fe-2e- == Fe2+2H2O+O2+4e-==4OH–思考题:马口铁和白口铁一旦有划痕后,在潮湿的空气中,谁被腐蚀的速度快?
作业:P53 1、2
“新学案”第二课时以下物品采用哪种方法防锈?? 海边码头上的钢轨、铁的徽章、放电熨斗的支架、钢刀片、铁制水闸、儿童游戏场中秋千架的钢架。 1.改变金属的内部组织结构
例如制造各种耐腐蚀的合金,如在普通钢铁中加入铬、镍等制成不锈钢。
二、金属的防护2.保护层法:在金属表面覆盖保护层,使金属制品与周围腐蚀介质隔离,从而防止腐蚀。 1).在钢铁制件表面涂上机油、凡士林、油漆或覆盖搪瓷、塑料等耐腐蚀的非金属材料。2).用电镀、热镀、喷镀等方法,在钢铁表面镀上一层不易被腐蚀的金属,如锌、锡、铬、镍等。这些金属常因氧化而形成一层致密的氧化物薄膜,从而阻止水和空气等对钢铁的腐蚀。3.【电化学保护】: ①将被保护的金属作为腐蚀电池的阴极,使其不受到腐蚀,所以也叫阴极保护法。这种方法主要有以下两种:
[牺牲阳极保护法] 此法是将活泼金属(如锌或锌的合金)连接在被保护的金属上,当发生电化腐蚀时,这种活泼金属作为负极发生氧化反应,因而减小或防止被保护金属的腐蚀。这种方法常用于保护水中的钢桩和海轮外壳等例如水中钢铁闸门的保护,通常在轮船的外壳水线以下处或在靠近螺旋浆的舵上焊上若干块锌块,来防止船壳等的腐蚀。[外加电流的保护法] 将被保护的金属和电源的负极连接,另选一块能导电的惰性材料接电源正极。通电后,使金属表面产生负电荷(电子)的聚积,因而抑制了金属失电子而达到保护目的。此法主要用于防止在土壤、海水及河水中的金属设备受到腐蚀。
②电化学保护的的另一种方法叫阳极保护法,即通过外加电压,使阳极在一定的电位范围内发生钝化的过程。可有效地阻滞或防止金属设备在酸、碱、盐类中腐蚀。1)、改变金属的内部结构2)、在金属表面覆盖保护层3)、电化学保护法金属防护方法总结练习1.下列现象与电化学腐蚀无关的是:( )
A.黄铜(铜锌合金)制作的铜锣不易产生铜绿
B.生铁比纯铁更易生锈
C.铁质器件附有铜质配件,在接触处易生锈
D银质奖牌久置表面变暗D2.铁钉和碳棒用导线连接后,浸入到食盐溶液中,可能发生的反应是: ( )
A.碳棒上放出Cl2 B.碳棒附近产生OH-
C.碳棒上放出H2 D.铁钉被氧化BD
