8.1第一课时酸性溶液和碱性溶液 教学设计(表格式)
文档属性
| 名称 | 8.1第一课时酸性溶液和碱性溶液 教学设计(表格式) |

|
|
| 格式 | docx | ||
| 文件大小 | 17.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-07-17 00:00:00 | ||
图片预览

文档简介
第一课时 酸性溶液和碱性溶液
课标分析 内容要求 1.知道常见的酸碱指示剂及其变色规律。 2.认识使用酸碱指示剂和pH试纸检验溶液的酸碱性。 学业要求 1.了解检验溶液酸碱性的基本方法。 2.学会用酸碱指示剂、pH试纸检验溶液的酸碱性。
教材分析 这节内容是初中化学教材中的重点内容,不仅对前面所学的知识内容总结归纳,还与学生在高中阶段的化学学习有很大关系,起到承上启下的作用。在第七章学生已学习了溶液的相关知识,溶液的酸碱性是溶液的一个特性,溶液酸碱性的强弱对其化学反应及应用有重大的影响,因此,了解并检验溶液的酸碱性有重要的意义。教材在编写上注重学生的生活体验,从学生熟悉的环境入手设计问题,便于学生认知的深化,有利于激发学生的学习兴趣。
学情分析 本课时的内容是在学生学习溶液的相关知识,知道溶液的某些性质的基础上展开的。而溶液的酸碱性也是溶液的特性之一,对于这些学生并不陌生,在之前的教学中都有涉及过。如二氧化碳的水溶液能使石蕊溶液变红、氨水能使酚酞溶液变红。学生具有相应的知识片断,但没有深入系统学习,很好地利用这些知识片断是本节课成功的关键。
素养目标 1.能识别生活中常见溶液的酸碱性。 2.能列举常见的酸碱指示剂,通过实验检验溶液的酸碱性。 3.学生能够理解溶液的酸碱性的概念,培养学生的实验操作能力和观察能力。
教学重点 溶液酸碱性及其检验。
教学难点 1.培养学生发现问题、分析实验的能力。 2.培养学生概括、归纳、总结知识的能力。
续表
教学过程
教师活动 学生活动 设计意图
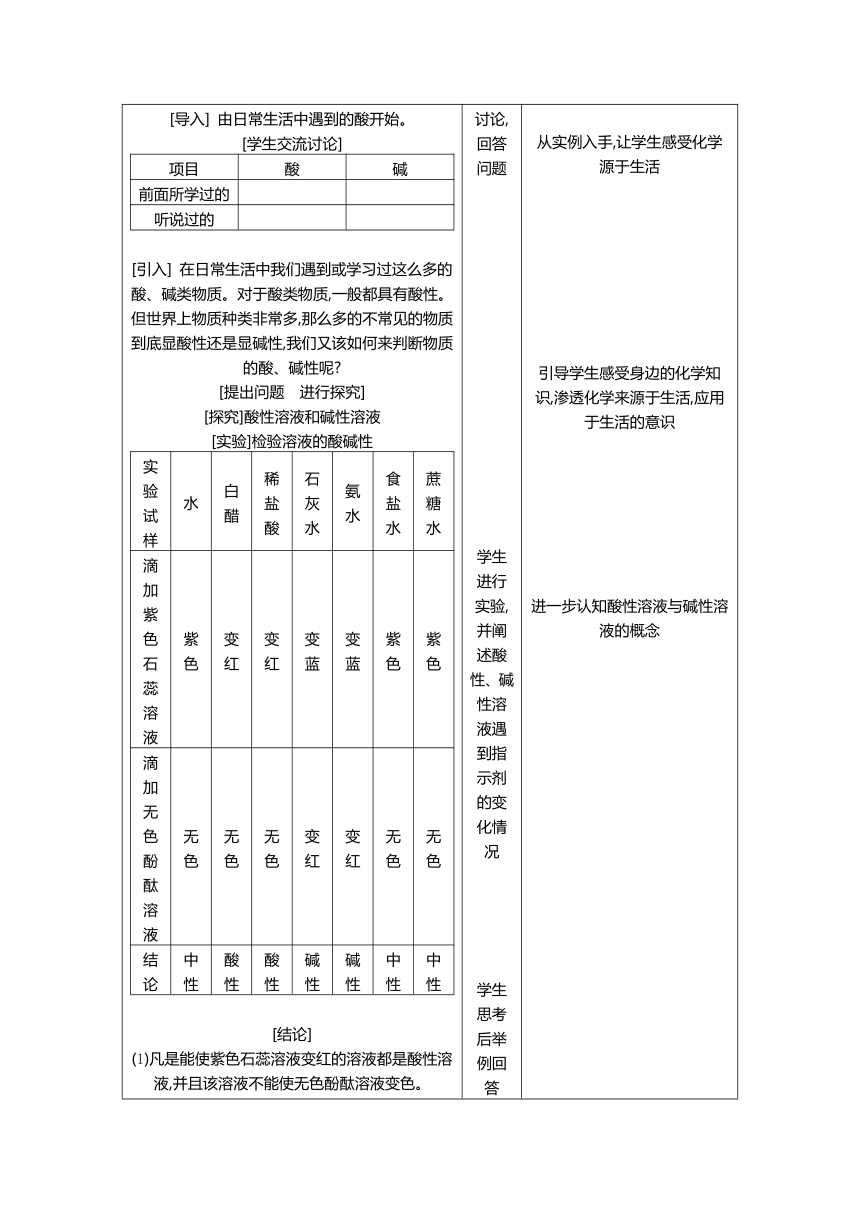
[创设情境 导入新课] [导入] 由日常生活中遇到的酸开始。 [学生交流讨论] 项目酸碱前面所学过的听说过的
[引入] 在日常生活中我们遇到或学习过这么多的酸、碱类物质。对于酸类物质,一般都具有酸性。但世界上物质种类非常多,那么多的不常见的物质到底显酸性还是显碱性,我们又该如何来判断物质的酸、碱性呢 [提出问题 进行探究] [探究]酸性溶液和碱性溶液 [实验]检验溶液的酸碱性 实验试样水白醋稀盐酸石灰水氨水食盐水蔗糖水滴加紫色石蕊溶液紫色变红变红变蓝变蓝紫色紫色滴加无色酚酞溶液无色无色无色变红变红无色无色结论中性酸性酸性碱性碱性中性中性
[结论] (1)凡是能使紫色石蕊溶液变红的溶液都是酸性溶液,并且该溶液不能使无色酚酞溶液变色。 (2)凡是能使紫色石蕊溶液变蓝的溶液都是碱性溶液,并且该溶液能使无色酚酞溶液变红。 (3)不能使紫色石蕊溶液变色,也不能使无色酚酞溶液变色的溶液,我们称为中性溶液。 (4)如紫色石蕊溶液及无色酚酞溶液等能检验水溶液酸碱性的试剂,称为酸碱指示剂。 [注意]我们有时候还用蓝色或红色石蕊试纸来检验溶液的酸碱性。 酸性溶液使蓝色石蕊试纸变红,碱性溶液使红色石蕊试纸变蓝。 [思考]酸性溶液一定是酸溶液吗 碱性溶液一定是碱溶液吗 答案:酸性溶液不一定是酸溶液,但酸溶液一定是酸性溶液;碱性溶液不一定是碱溶液,但碱溶液一定是碱性溶液。 [例题]下列哪种试剂能鉴别出硫酸、氢氧化钾和氯化钠三种无色稀溶液(A) A.紫色石蕊溶液 B.稀盐酸 C.氢氧化钠溶液 D.氯化钾溶液 讨论,回答问题 学生进行实验,并阐述酸性、碱性溶液遇到指示剂的变化情况 学生思考后举例回答 学生依据所学知识,按照老师的要求完成题目评价任务 从实例入手,让学生感受化学源于生活 引导学生感受身边的化学知识,渗透化学来源于生活,应用于生活的意识 进一步认知酸性溶液与碱性溶液的概念
续表
课堂小结
酸碱指示剂能用来测定溶液的酸碱性,紫色石蕊溶液遇酸性溶液变成红色,遇碱性溶液变成蓝色;无色酚酞溶液遇酸性溶液不变色,遇碱性溶液变成红色,因此可以用来鉴别酸性或碱性物质。
板书设计 第1节 溶液的酸碱性 第一课时 酸性溶液和碱性溶液 1.紫色石蕊溶液 2.无色酚酞溶液 3.溶液的酸碱性 (1)酸性溶液——呈酸性(用紫色石蕊溶液、蓝色石蕊试纸检验) (2)碱性溶液——呈碱性(用紫色石蕊溶液、无色酚酞溶液、红色石蕊试纸检验) (3)中性溶液——呈中性(用紫色石蕊溶液检验)
教学反思 在知识储备方面,学生已了解了用酸碱指示剂能鉴别溶液的酸碱性等片断,同时也具备了一些学习化学的方法,但没有深入系统学习,利用这些知识片段进行学习是本节课成功的一个关键。在基本实验知识和操作技能方面,学生初步具备并能够在教师指导下完成实验,得到较直观的结论,但是归纳实验方法、独立设计实验的能力尚显薄弱。通过创设特定的教学情境,引导学生动手实验,能激发学生的学习和探究兴趣,灵活掌握和应用知识。
课标分析 内容要求 1.知道常见的酸碱指示剂及其变色规律。 2.认识使用酸碱指示剂和pH试纸检验溶液的酸碱性。 学业要求 1.了解检验溶液酸碱性的基本方法。 2.学会用酸碱指示剂、pH试纸检验溶液的酸碱性。
教材分析 这节内容是初中化学教材中的重点内容,不仅对前面所学的知识内容总结归纳,还与学生在高中阶段的化学学习有很大关系,起到承上启下的作用。在第七章学生已学习了溶液的相关知识,溶液的酸碱性是溶液的一个特性,溶液酸碱性的强弱对其化学反应及应用有重大的影响,因此,了解并检验溶液的酸碱性有重要的意义。教材在编写上注重学生的生活体验,从学生熟悉的环境入手设计问题,便于学生认知的深化,有利于激发学生的学习兴趣。
学情分析 本课时的内容是在学生学习溶液的相关知识,知道溶液的某些性质的基础上展开的。而溶液的酸碱性也是溶液的特性之一,对于这些学生并不陌生,在之前的教学中都有涉及过。如二氧化碳的水溶液能使石蕊溶液变红、氨水能使酚酞溶液变红。学生具有相应的知识片断,但没有深入系统学习,很好地利用这些知识片断是本节课成功的关键。
素养目标 1.能识别生活中常见溶液的酸碱性。 2.能列举常见的酸碱指示剂,通过实验检验溶液的酸碱性。 3.学生能够理解溶液的酸碱性的概念,培养学生的实验操作能力和观察能力。
教学重点 溶液酸碱性及其检验。
教学难点 1.培养学生发现问题、分析实验的能力。 2.培养学生概括、归纳、总结知识的能力。
续表
教学过程
教师活动 学生活动 设计意图
[创设情境 导入新课] [导入] 由日常生活中遇到的酸开始。 [学生交流讨论] 项目酸碱前面所学过的听说过的
[引入] 在日常生活中我们遇到或学习过这么多的酸、碱类物质。对于酸类物质,一般都具有酸性。但世界上物质种类非常多,那么多的不常见的物质到底显酸性还是显碱性,我们又该如何来判断物质的酸、碱性呢 [提出问题 进行探究] [探究]酸性溶液和碱性溶液 [实验]检验溶液的酸碱性 实验试样水白醋稀盐酸石灰水氨水食盐水蔗糖水滴加紫色石蕊溶液紫色变红变红变蓝变蓝紫色紫色滴加无色酚酞溶液无色无色无色变红变红无色无色结论中性酸性酸性碱性碱性中性中性
[结论] (1)凡是能使紫色石蕊溶液变红的溶液都是酸性溶液,并且该溶液不能使无色酚酞溶液变色。 (2)凡是能使紫色石蕊溶液变蓝的溶液都是碱性溶液,并且该溶液能使无色酚酞溶液变红。 (3)不能使紫色石蕊溶液变色,也不能使无色酚酞溶液变色的溶液,我们称为中性溶液。 (4)如紫色石蕊溶液及无色酚酞溶液等能检验水溶液酸碱性的试剂,称为酸碱指示剂。 [注意]我们有时候还用蓝色或红色石蕊试纸来检验溶液的酸碱性。 酸性溶液使蓝色石蕊试纸变红,碱性溶液使红色石蕊试纸变蓝。 [思考]酸性溶液一定是酸溶液吗 碱性溶液一定是碱溶液吗 答案:酸性溶液不一定是酸溶液,但酸溶液一定是酸性溶液;碱性溶液不一定是碱溶液,但碱溶液一定是碱性溶液。 [例题]下列哪种试剂能鉴别出硫酸、氢氧化钾和氯化钠三种无色稀溶液(A) A.紫色石蕊溶液 B.稀盐酸 C.氢氧化钠溶液 D.氯化钾溶液 讨论,回答问题 学生进行实验,并阐述酸性、碱性溶液遇到指示剂的变化情况 学生思考后举例回答 学生依据所学知识,按照老师的要求完成题目评价任务 从实例入手,让学生感受化学源于生活 引导学生感受身边的化学知识,渗透化学来源于生活,应用于生活的意识 进一步认知酸性溶液与碱性溶液的概念
续表
课堂小结
酸碱指示剂能用来测定溶液的酸碱性,紫色石蕊溶液遇酸性溶液变成红色,遇碱性溶液变成蓝色;无色酚酞溶液遇酸性溶液不变色,遇碱性溶液变成红色,因此可以用来鉴别酸性或碱性物质。
板书设计 第1节 溶液的酸碱性 第一课时 酸性溶液和碱性溶液 1.紫色石蕊溶液 2.无色酚酞溶液 3.溶液的酸碱性 (1)酸性溶液——呈酸性(用紫色石蕊溶液、蓝色石蕊试纸检验) (2)碱性溶液——呈碱性(用紫色石蕊溶液、无色酚酞溶液、红色石蕊试纸检验) (3)中性溶液——呈中性(用紫色石蕊溶液检验)
教学反思 在知识储备方面,学生已了解了用酸碱指示剂能鉴别溶液的酸碱性等片断,同时也具备了一些学习化学的方法,但没有深入系统学习,利用这些知识片段进行学习是本节课成功的一个关键。在基本实验知识和操作技能方面,学生初步具备并能够在教师指导下完成实验,得到较直观的结论,但是归纳实验方法、独立设计实验的能力尚显薄弱。通过创设特定的教学情境,引导学生动手实验,能激发学生的学习和探究兴趣,灵活掌握和应用知识。
同课章节目录
