2.1共价键 课件 (3)
图片预览





文档简介
课件24张PPT。第一节
共价键学与问 你能用电子式表示H2、HCl、Cl2
分子的形成过程吗? 为什么不可能有H3、H2Cl、Cl3
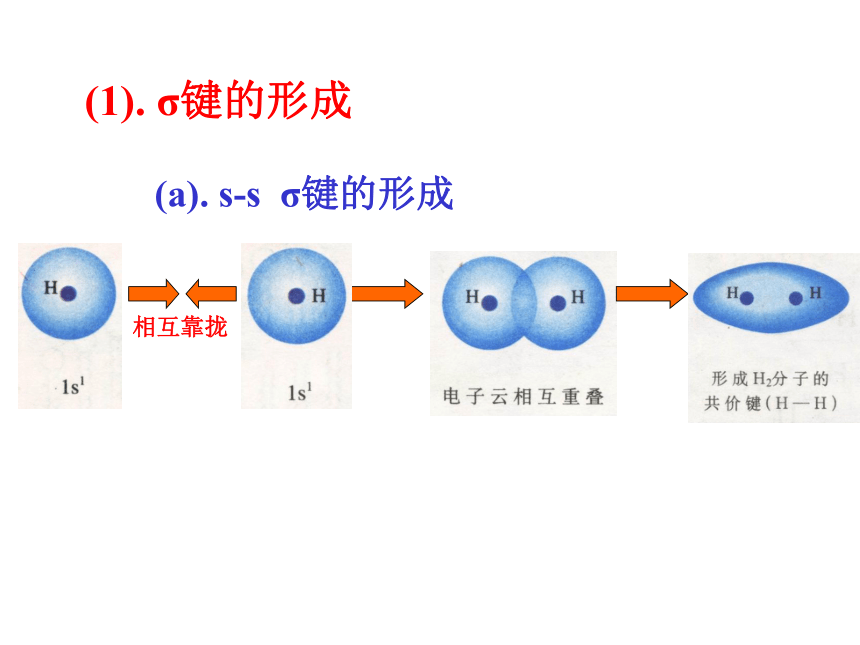
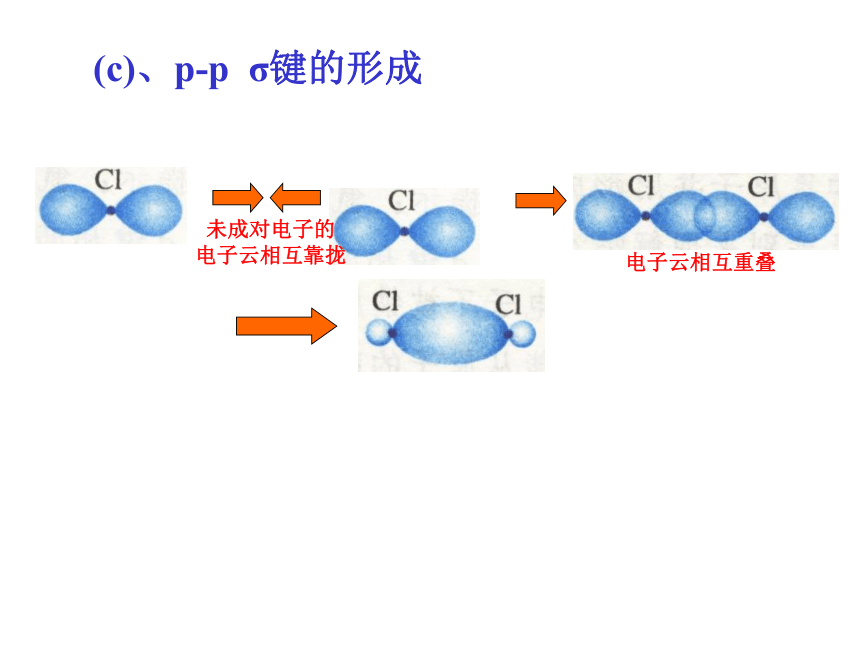
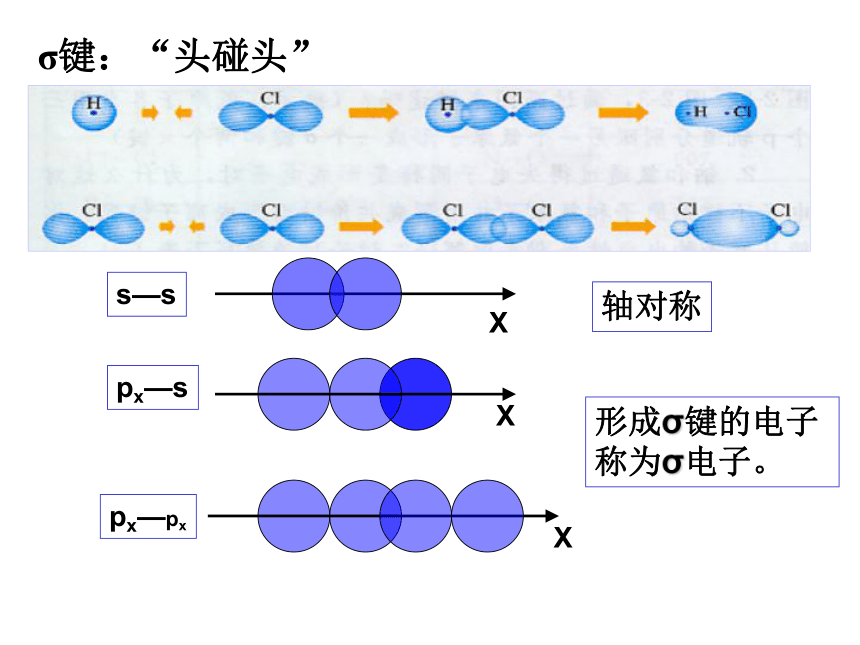
分子的形成?1、共价键特点 按照共价键的共用电子对理论,一个原子有几个未成对电子,便可和几个自旋相反的电子配对成键,这就是共价键的“饱和性”。H 原子、Cl原子都只有一个未成对电子,因而只能形成H2、HCl、Cl2分子,不能形成H3、H2Cl、Cl3分子2、共价键的形成(a). s-s σ键的形成(1). σ键的形成(b). s-p σ键的形成电子云相互重叠电子云相互重叠(c)、p-p σ键的形成σ键:“头碰头”Xs—sXpx—sXpx—px轴对称形成σ键的电子
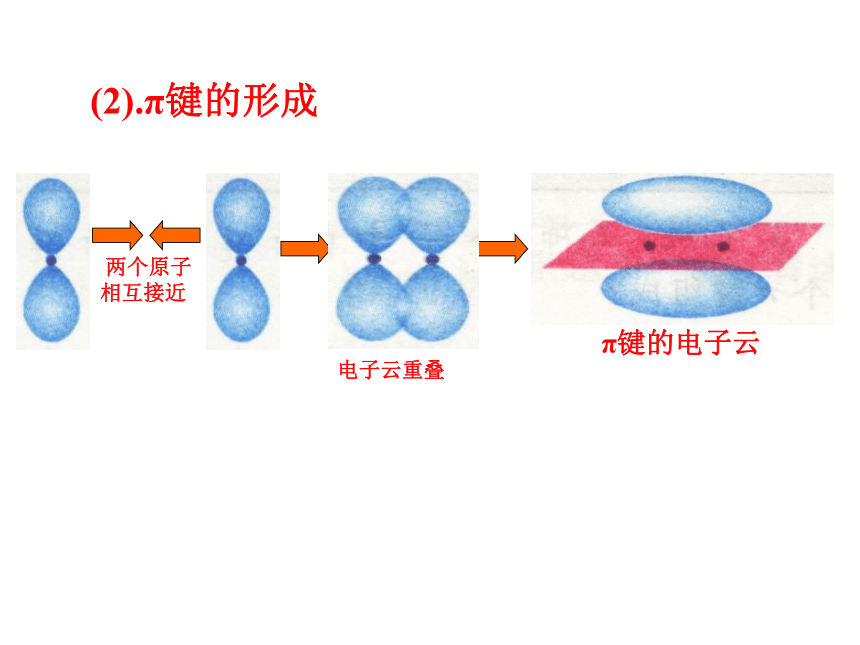
称为σ电子。(2).π键的形成电子云重叠π键的电子云 π键:“肩并肩”XZZpZ—pZ形成π键的电子称为π电子。镜像对称小结沿轴方向
“头碰头”平行方向
“肩并肩”轴对称镜像对称强度大,
不易断裂强度较小,易断裂共价单键是σ键,共价双键中一个是 σ键,另一个是π键,共价三键中一个是σ键,另两个为π键。因而含有π键的化合物与只有σ键的化合物的化学性质不同,如我们熟悉的乙烷和乙烯的性质不同。 以上由原子轨道相互重叠形成的σ键和π键是共价键的两种基本类型,是分子结构的价键理论中最基本的组成部分。价键理论:价键理论的要点1.电子配对原理2.最大重叠原理两原子各自提供1个自旋方向相反的电子彼此配对。两个原子轨道重叠部分越大,两核间电子的概率密度越大,形成的共价键越牢固,分子越稳定。科学探究1.已知氮分子的共价键是三键,你能模仿图2-1、图2-2、图2-3,通过画图来描述吗?(提示:氮原子各自 用三个p轨道分别跟另一个氮原子形成一个σ键和两个π键。Pz-Pzπ键科学探究1.N2分子形成2.钠和氯通过得失电子同样也是形成电子对,为什么这对电子不被钠原子和氯原子共用形成共价键而形成离子键呢?你能从原子的电负性差别来理解吗?讨论后请填写表2-2:0.9 3.02.1 3.02.5 3.52.10.91.0离子共价1.73.乙烷、乙烯和乙炔分子中的共价键分别有几个σ键和几个π键组成?乙烷分子中由7个σ键组成;乙烯分子中由5个σ键和1个π键组成;乙炔分子中由3个σ键和2个π键组成。小结沿轴方向
“头碰头”平行方向
“肩并肩”轴对称镜像对称强度大,
不易断裂强度较小,易断裂共价单键是σ键,共价双键中一个是 σ键,另一个是π键,共价三键中一个是σ键,另两个为π键。1、下列说法正确的是
A、含有共价键的化合物一定是共价化合物
B、分子中只有共价键的化合物一定是共价化合物
C、由共价键形成的分子一定是共价化合物
D、只有非金属原子间才能形成共价键
2、氮分子中的化学键是 A、3个σ键 B、1个σ键,2个π键 C、个π键 D、个σ键,1个π键 B B3、下列说法中正确的是 A、p轨道之间以“肩并肩”重叠可形成σ键
B、p轨道之间以“头对头”重叠可形成π键
C、s和p轨道以“头对头”重叠可形成σ键
D、共价键是两个原子轨道以“头对头”重叠形成的C4、在氯化氢分子中,形成共价键的原子轨道是 A、 氯原子的2p轨道和氢原子的1s轨道
B、 氯原子的2p轨道和氢原子的2p轨道
C、氯原子的3p轨道和氢原子的1s轨道
D、氯原子的3p轨道和氢原子的3p轨道C 73小结沿轴方向
“头碰头”平行方向
“肩并肩”轴对称镜像对称强度大,
不易断裂强度较小,易断裂共价单键是σ键,共价双键中一个是 σ键,另一个是π键,共价三键中一个是σ键,另两个为π键。
共价键学与问 你能用电子式表示H2、HCl、Cl2
分子的形成过程吗? 为什么不可能有H3、H2Cl、Cl3
分子的形成?1、共价键特点 按照共价键的共用电子对理论,一个原子有几个未成对电子,便可和几个自旋相反的电子配对成键,这就是共价键的“饱和性”。H 原子、Cl原子都只有一个未成对电子,因而只能形成H2、HCl、Cl2分子,不能形成H3、H2Cl、Cl3分子2、共价键的形成(a). s-s σ键的形成(1). σ键的形成(b). s-p σ键的形成电子云相互重叠电子云相互重叠(c)、p-p σ键的形成σ键:“头碰头”Xs—sXpx—sXpx—px轴对称形成σ键的电子
称为σ电子。(2).π键的形成电子云重叠π键的电子云 π键:“肩并肩”XZZpZ—pZ形成π键的电子称为π电子。镜像对称小结沿轴方向
“头碰头”平行方向
“肩并肩”轴对称镜像对称强度大,
不易断裂强度较小,易断裂共价单键是σ键,共价双键中一个是 σ键,另一个是π键,共价三键中一个是σ键,另两个为π键。因而含有π键的化合物与只有σ键的化合物的化学性质不同,如我们熟悉的乙烷和乙烯的性质不同。 以上由原子轨道相互重叠形成的σ键和π键是共价键的两种基本类型,是分子结构的价键理论中最基本的组成部分。价键理论:价键理论的要点1.电子配对原理2.最大重叠原理两原子各自提供1个自旋方向相反的电子彼此配对。两个原子轨道重叠部分越大,两核间电子的概率密度越大,形成的共价键越牢固,分子越稳定。科学探究1.已知氮分子的共价键是三键,你能模仿图2-1、图2-2、图2-3,通过画图来描述吗?(提示:氮原子各自 用三个p轨道分别跟另一个氮原子形成一个σ键和两个π键。Pz-Pzπ键科学探究1.N2分子形成2.钠和氯通过得失电子同样也是形成电子对,为什么这对电子不被钠原子和氯原子共用形成共价键而形成离子键呢?你能从原子的电负性差别来理解吗?讨论后请填写表2-2:0.9 3.02.1 3.02.5 3.52.10.91.0离子共价1.73.乙烷、乙烯和乙炔分子中的共价键分别有几个σ键和几个π键组成?乙烷分子中由7个σ键组成;乙烯分子中由5个σ键和1个π键组成;乙炔分子中由3个σ键和2个π键组成。小结沿轴方向
“头碰头”平行方向
“肩并肩”轴对称镜像对称强度大,
不易断裂强度较小,易断裂共价单键是σ键,共价双键中一个是 σ键,另一个是π键,共价三键中一个是σ键,另两个为π键。1、下列说法正确的是
A、含有共价键的化合物一定是共价化合物
B、分子中只有共价键的化合物一定是共价化合物
C、由共价键形成的分子一定是共价化合物
D、只有非金属原子间才能形成共价键
2、氮分子中的化学键是 A、3个σ键 B、1个σ键,2个π键 C、个π键 D、个σ键,1个π键 B B3、下列说法中正确的是 A、p轨道之间以“肩并肩”重叠可形成σ键
B、p轨道之间以“头对头”重叠可形成π键
C、s和p轨道以“头对头”重叠可形成σ键
D、共价键是两个原子轨道以“头对头”重叠形成的C4、在氯化氢分子中,形成共价键的原子轨道是 A、 氯原子的2p轨道和氢原子的1s轨道
B、 氯原子的2p轨道和氢原子的2p轨道
C、氯原子的3p轨道和氢原子的1s轨道
D、氯原子的3p轨道和氢原子的3p轨道C 73小结沿轴方向
“头碰头”平行方向
“肩并肩”轴对称镜像对称强度大,
不易断裂强度较小,易断裂共价单键是σ键,共价双键中一个是 σ键,另一个是π键,共价三键中一个是σ键,另两个为π键。
