3.3 金属晶体 课件 (6)
文档属性
| 名称 | 3.3 金属晶体 课件 (6) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-07-12 00:00:00 | ||
图片预览










文档简介
课件42张PPT。 金 属 晶 体 一、金属共同的物理性质容易导电、导热、有延展性、有金属光泽等。金属为什么具有这些共同性质呢?二、金属的结构问题:构成金属的粒子有哪些?金属的结构是怎样的?通过射线进行研究发现,在金属中,金属原子好像许多硬球一层一层紧密地堆积着,每一个金属原子周围有许多相同的金属原子围绕着。金属单质的晶体中原子之间以金属键相互结合组成粒子:
作用力:金属阳离子和自由电子金属离子和自由电子之间的较强作用——金属键(电子气理论)金属键“电子气理论”(自由电子理论)——金属原子脱落下来的价电子形成遍布整个晶体的“电子气”,被所有原子所共用,从而把所有的原子维系在一起。 金属键的成键微粒:金属阳离子和自由电子。存在于金属单质和合金中。
金属键的特征:自由电子可以在整块金属中自由 移动,因此金属键没有方向性和饱和性。
金属键
金属键的本质:“电子气理论”(自由电子理论)
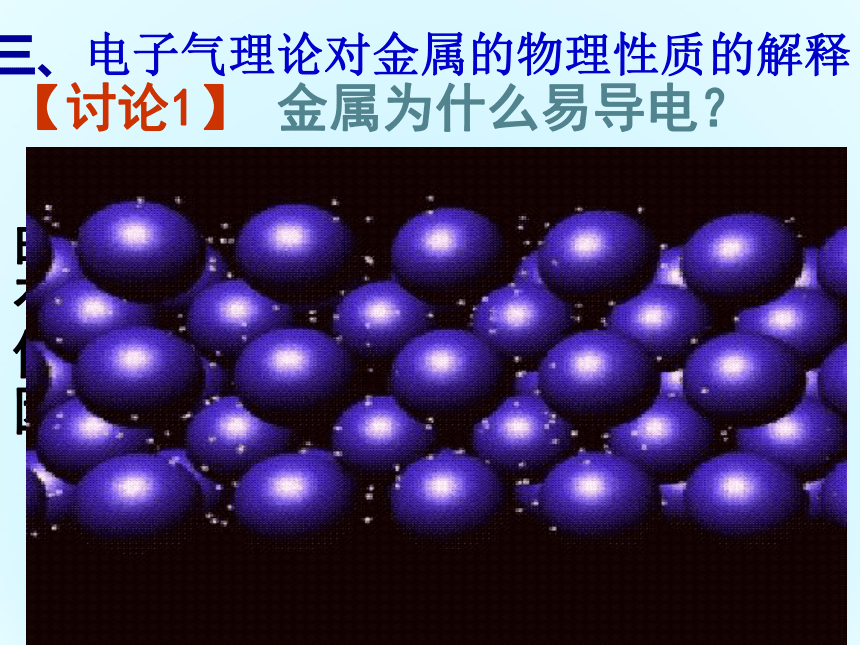
金属原子脱落来的价电子形成遍布整个晶体的“电子气”,被所有原子所共用,从而把所有的原子维系在一起。【讨论1】 金属为什么易导电?
在金属晶体中,存在着许多自由电子,这些自由电子的运动是没有一定方向的,但在外加电场的条件下自由电子就会发生定向运动,因而形成电流,所以金属容易导电。三、电子气理论对金属的物理性质的解释【讨论2】金属为什么易导热? 当金属某部分受热时,那个区域里的自由电子能量增加,运动速度加快,通过碰撞,把能量传给金属离子。
金属容易导热,是由于自由电子运动时与金属离子碰撞把能量从温度高的部分传到温度低的部分。【讨论3】金属为什么具有较好的延展性?
?? 金属晶体中由于金属离子与自由电子间的相互作用没有方向性,各原子层之间发生相对滑动以后,仍可保持这种相互作用,因而即使在外力作用下,发生形变也不易断裂。
4、金属晶体结构具有金属光泽和颜色由于自由电子可吸收所有频率的光,然后很快释放出各种频率的光,因此绝大多数金属具有银白色或钢灰色光泽。而某些金属(如铜、金、铯、铅等)由于较易吸收某些频率的光而呈现较为特殊的颜色。
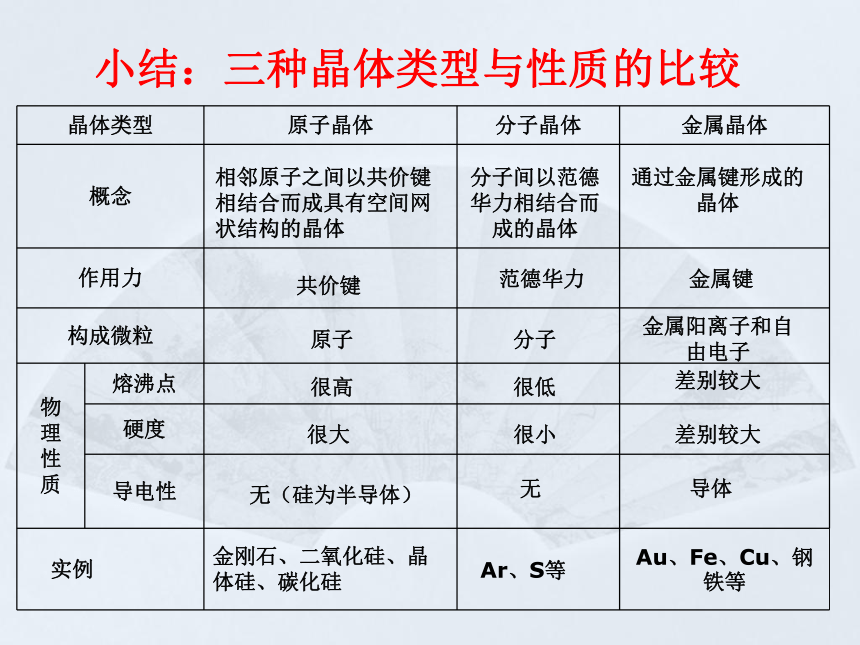
当金属成粉末状时,金属晶体的晶面取向杂乱、晶格排列不规则,吸收可见光后辐射不出去,所以成黑色。5、影响金属键强弱的因素:金属阳离子半径越小,所带电荷越多,自由电子越多,金属键越强,熔点就相应越高,硬度也越大小结:三种晶体类型与性质的比较相邻原子之间以共价键相结合而成具有空间网状结构的晶体共价键
原子
很大
很高
无(硅为半导体)分子分子间以范德华力相结合而成的晶体
范德华力
很低很小
无通过金属键形成的晶体
金属键
金属阳离子和自由电子
差别较大
差别较大
导体四、金属晶体的原子堆积模型
由于金属键没有方向性,每个金属原子中的电子分布基本是球对称的,所以可以把金属晶体看成是由直径相等的圆球的三维空间堆积而成的。1.理论基础:紧密堆积:微粒之间的作用力,使微粒间尽可能的相互接近,使它们占有最小的空间。
空间利用率:空间被晶格质点占据的百分数。用来表示紧密堆积的程度。
配位数:在密堆积中,一个原子或离子周围距离最近且相等的原子或离子的数目。I 型II 型配位数为4配位数为6密置层非密置层12341234562.金属晶体的原子在二维平面的堆积模型哪种排列方式圆球周围剩余空隙最小?剩余的空隙较大——非密置层
剩余空隙最小 ——密置层; 3.空间堆积模型a.简单立方堆积(Po)晶胞含几个原子?金属原子半径r与正方体边长a的关系:a = 2 r配位数:6空间利用率:52%b.钾型----体心立方堆积:
这种堆积晶胞是一个体心立方,每个晶胞含 个原子,空间
利用率也不高(68%),属于非
密置层堆积,配位数为 ,
如碱金属、Fe等采取这种堆积方式。28金属原子半径r与正方体边长a的关系:b = 4 rb 第二层对第一层来讲最紧密的堆积方式是将球对准 1,3,5 位 ( 或对准 2,4,6 位,其情形是一样的 )思考:第三层如何才能作到密置层的堆积呢?金属晶体的两种最密堆积方式──镁型和铜型镁型和铜型镁型铜型a.镁型 第三层的一种排列方式,是将球对准第一层每一个球,于是每两层形成一个周期,即 AB AB 堆积方式。(2)密置层在三维空间堆积----六方最密堆积
六方最密堆积 下图是镁型紧密堆积的前视图A123456789101112 这种堆积晶胞空间利用率高(74%),属于最密置层堆积,配位数为 ,许多金属(如Mg、Zn、Ti等)采取这种堆积方式。12金属原子的半径r与六棱柱的边长a、高h
的关系: a = 2 rh =a32b.铜型 第三层的另一种排列方式,是将球对准第一层的 2,4,6 位,不同于 AB 两层的位置,这是 C 层。4----面心立方最密堆积
铜型铜型边长为 a
面对角线边长为 a=4r金属原子半径 r与正方体边长a 的关系:此种立方紧密堆积的前视图A空间利用率也为74%,配位数 12 ( 同层 6, 上下层各 3 ) 下图是铜型型紧密堆积的前视图A
C
B
A
C
B
A面心立方最密堆积堆积方式及性质小结简单立方堆积体心立方密堆积六方最密堆积面心立方六方体心立方简单立方74%74%68%52%121286Cu、Ag、AuMg、Zn、TiNa、K、FePo【课堂小结】 金属晶体中原子的堆积方式 非密置层 简单立方堆积 --Po 体心立方堆积--K Na Fe 密置层六方密堆积--Mg Zn Ti 面心立方堆积--Cu Au Ag Al三种最常见堆积方式 详见书76—资料卡片练习:课后书77练习1.金属能导电的原因是( ) A.金属晶体中金属阳离子与自由电子间的 相互作用较弱 B.金属晶体中的自由电子在外加电场作用下可发生定向移动 C.金属晶体中的金属阳离子在外加电场作用下可发生定向移动 D.金属晶体在外加电场作用下可失去电子 B2.金属键的强弱与金属价电子数的多少有关,价电子数越多金属键越强;与金属阳离子的半径大小也有关,金属阳离子的半径越大,金属键越弱。据此判断下列金属熔点逐渐升高的是 ( )
A、Li Na K B、Na Mg Al
C、Li Be Mg D、Li Na MgB3.下列有关金属晶体叙述正确的是( )
A、常温下金属单质都以金属晶体形式存在
B、金属离子与自由电子之间的强烈作用,在一定外力作用下,不因形变而消失
C、钙的熔、沸点低于钾
D、温度越高,金属的导电性越好B 5.已知金属铜为面心立方晶体,如图所示,铜的相对原子质量为63.54,密度为8.936g/cm3,试求:
(1)图中正方形边长a,
(2)铜的金属半径raarrorr提示:
数出面心立方中的铜的个数:
作用力:金属阳离子和自由电子金属离子和自由电子之间的较强作用——金属键(电子气理论)金属键“电子气理论”(自由电子理论)——金属原子脱落下来的价电子形成遍布整个晶体的“电子气”,被所有原子所共用,从而把所有的原子维系在一起。 金属键的成键微粒:金属阳离子和自由电子。存在于金属单质和合金中。
金属键的特征:自由电子可以在整块金属中自由 移动,因此金属键没有方向性和饱和性。
金属键
金属键的本质:“电子气理论”(自由电子理论)
金属原子脱落来的价电子形成遍布整个晶体的“电子气”,被所有原子所共用,从而把所有的原子维系在一起。【讨论1】 金属为什么易导电?
在金属晶体中,存在着许多自由电子,这些自由电子的运动是没有一定方向的,但在外加电场的条件下自由电子就会发生定向运动,因而形成电流,所以金属容易导电。三、电子气理论对金属的物理性质的解释【讨论2】金属为什么易导热? 当金属某部分受热时,那个区域里的自由电子能量增加,运动速度加快,通过碰撞,把能量传给金属离子。
金属容易导热,是由于自由电子运动时与金属离子碰撞把能量从温度高的部分传到温度低的部分。【讨论3】金属为什么具有较好的延展性?
?? 金属晶体中由于金属离子与自由电子间的相互作用没有方向性,各原子层之间发生相对滑动以后,仍可保持这种相互作用,因而即使在外力作用下,发生形变也不易断裂。
4、金属晶体结构具有金属光泽和颜色由于自由电子可吸收所有频率的光,然后很快释放出各种频率的光,因此绝大多数金属具有银白色或钢灰色光泽。而某些金属(如铜、金、铯、铅等)由于较易吸收某些频率的光而呈现较为特殊的颜色。
当金属成粉末状时,金属晶体的晶面取向杂乱、晶格排列不规则,吸收可见光后辐射不出去,所以成黑色。5、影响金属键强弱的因素:金属阳离子半径越小,所带电荷越多,自由电子越多,金属键越强,熔点就相应越高,硬度也越大小结:三种晶体类型与性质的比较相邻原子之间以共价键相结合而成具有空间网状结构的晶体共价键
原子
很大
很高
无(硅为半导体)分子分子间以范德华力相结合而成的晶体
范德华力
很低很小
无通过金属键形成的晶体
金属键
金属阳离子和自由电子
差别较大
差别较大
导体四、金属晶体的原子堆积模型
由于金属键没有方向性,每个金属原子中的电子分布基本是球对称的,所以可以把金属晶体看成是由直径相等的圆球的三维空间堆积而成的。1.理论基础:紧密堆积:微粒之间的作用力,使微粒间尽可能的相互接近,使它们占有最小的空间。
空间利用率:空间被晶格质点占据的百分数。用来表示紧密堆积的程度。
配位数:在密堆积中,一个原子或离子周围距离最近且相等的原子或离子的数目。I 型II 型配位数为4配位数为6密置层非密置层12341234562.金属晶体的原子在二维平面的堆积模型哪种排列方式圆球周围剩余空隙最小?剩余的空隙较大——非密置层
剩余空隙最小 ——密置层; 3.空间堆积模型a.简单立方堆积(Po)晶胞含几个原子?金属原子半径r与正方体边长a的关系:a = 2 r配位数:6空间利用率:52%b.钾型----体心立方堆积:
这种堆积晶胞是一个体心立方,每个晶胞含 个原子,空间
利用率也不高(68%),属于非
密置层堆积,配位数为 ,
如碱金属、Fe等采取这种堆积方式。28金属原子半径r与正方体边长a的关系:b = 4 rb 第二层对第一层来讲最紧密的堆积方式是将球对准 1,3,5 位 ( 或对准 2,4,6 位,其情形是一样的 )思考:第三层如何才能作到密置层的堆积呢?金属晶体的两种最密堆积方式──镁型和铜型镁型和铜型镁型铜型a.镁型 第三层的一种排列方式,是将球对准第一层每一个球,于是每两层形成一个周期,即 AB AB 堆积方式。(2)密置层在三维空间堆积----六方最密堆积
六方最密堆积 下图是镁型紧密堆积的前视图A123456789101112 这种堆积晶胞空间利用率高(74%),属于最密置层堆积,配位数为 ,许多金属(如Mg、Zn、Ti等)采取这种堆积方式。12金属原子的半径r与六棱柱的边长a、高h
的关系: a = 2 rh =a32b.铜型 第三层的另一种排列方式,是将球对准第一层的 2,4,6 位,不同于 AB 两层的位置,这是 C 层。4----面心立方最密堆积
铜型铜型边长为 a
面对角线边长为 a=4r金属原子半径 r与正方体边长a 的关系:此种立方紧密堆积的前视图A空间利用率也为74%,配位数 12 ( 同层 6, 上下层各 3 ) 下图是铜型型紧密堆积的前视图A
C
B
A
C
B
A面心立方最密堆积堆积方式及性质小结简单立方堆积体心立方密堆积六方最密堆积面心立方六方体心立方简单立方74%74%68%52%121286Cu、Ag、AuMg、Zn、TiNa、K、FePo【课堂小结】 金属晶体中原子的堆积方式 非密置层 简单立方堆积 --Po 体心立方堆积--K Na Fe 密置层六方密堆积--Mg Zn Ti 面心立方堆积--Cu Au Ag Al三种最常见堆积方式 详见书76—资料卡片练习:课后书77练习1.金属能导电的原因是( ) A.金属晶体中金属阳离子与自由电子间的 相互作用较弱 B.金属晶体中的自由电子在外加电场作用下可发生定向移动 C.金属晶体中的金属阳离子在外加电场作用下可发生定向移动 D.金属晶体在外加电场作用下可失去电子 B2.金属键的强弱与金属价电子数的多少有关,价电子数越多金属键越强;与金属阳离子的半径大小也有关,金属阳离子的半径越大,金属键越弱。据此判断下列金属熔点逐渐升高的是 ( )
A、Li Na K B、Na Mg Al
C、Li Be Mg D、Li Na MgB3.下列有关金属晶体叙述正确的是( )
A、常温下金属单质都以金属晶体形式存在
B、金属离子与自由电子之间的强烈作用,在一定外力作用下,不因形变而消失
C、钙的熔、沸点低于钾
D、温度越高,金属的导电性越好B 5.已知金属铜为面心立方晶体,如图所示,铜的相对原子质量为63.54,密度为8.936g/cm3,试求:
(1)图中正方形边长a,
(2)铜的金属半径raarrorr提示:
数出面心立方中的铜的个数:
