3.4 离子晶体 课件 (4)
文档属性
| 名称 | 3.4 离子晶体 课件 (4) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-07-12 00:00:00 | ||
图片预览





文档简介
课件17张PPT。第四节 离子晶体2、晶体中存在的微粒:阴、阳离子3、微粒间的作用力:离子键4、哪些类物质属于离子晶体?大多数盐、强碱、活泼金属氧化物一、离子晶体1、定义:离子键:由阴、阳离子通过离子键结合而成的晶体。判断正误:
1、离子晶体一定是离子化合物。
2、含有离子的晶体一定是离子晶体。
3、离子晶体中只含离子键。
4、离子晶体中一定含金属阳离子。
5、由金属元素与非金属元素组成的晶体一定是离子晶体。×√×××配位数:离子晶体中,一个离子周围最邻近的异电性离子的 数目。缩写为C. N.。(1)钠离子和氯离子的位置:①钠离子和氯离子位于立方体的顶角上,并交错排列。
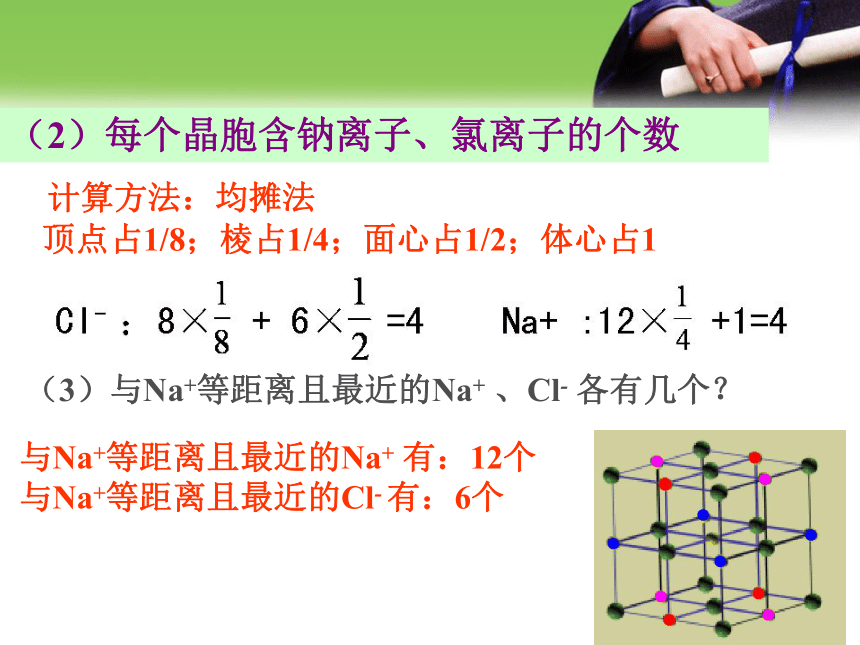
②钠离子:体心和棱中点;氯离子:面心和顶点,或者反之。5、晶胞类型:(1)氯化钠型晶胞(3)与Na+等距离且最近的Na+ 、Cl- 各有几个? 计算方法:均摊法
顶点占1/8;棱占1/4;面心占1/2;体心占1 (2)每个晶胞含钠离子、氯离子的个数与Na+等距离且最近的Na+ 有:12个
与Na+等距离且最近的Cl- 有:6个
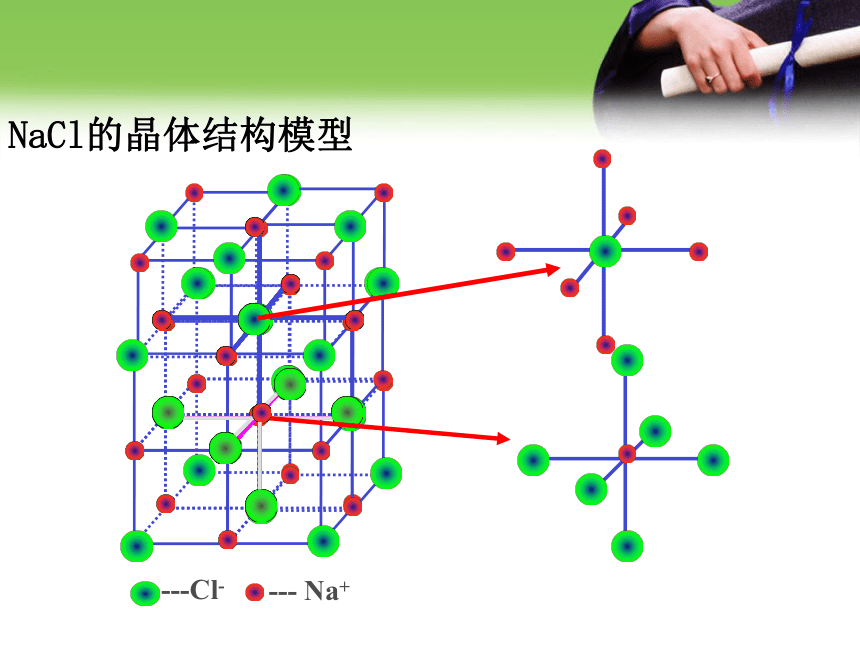
NaCl的晶体结构模型 返回原处NaCl晶体中阴、阳离子配位数5、几种离子晶体
(1)NaCl晶体
每个Na+周围最近且等距离的Cl-有 个,
每个Cl-周围最近且等距离的Na+有 个;
在每个Na+周围最近且等距离的Na+有 个,
在每个Cl-周围最近等距离的Cl-有 个。
Na+和Cl-的配位数分别为 、 。
一个NaCl晶胞中含 个Na+和 个Cl-。
NaCl晶体中 NaCl分子,
化学式NaCl表示 。6612446无126Na+和Cl-的最简个数比(2)氯化铯型晶胞CsCl的晶体结构及晶胞构示意图CsCl晶胞(1)铯离子和氯离子的位置:铯离子:体心
氯离子:顶点;或者反之。(2)每个晶胞含铯离子、氯离子的个数铯离子:1个 ;氯离子:1个(3)与铯离子等距离且最近的铯离子、氯离子各有几个?铯离子:6个 ;氯离子:8个(2)CsCl晶体
每个Cs+周围最近且等距离的Cl-有 个,每个Cl-周围最近且等距离的Cs+有 个;在每个Cs+周围最近且等距离的Cs+有 个,在每个Cl-周围最近等距离的Cl-有 个。一个CsCl晶胞中含 个Cs+和 个Cl-。 Cs+和Cl-的配位数分别为 、 。88661188(3)CaF2晶体
每个Ca2+周围最近且等距离的F-有 个,每个F-周围最近且等距离的Ca2+有 个;
在每个Ca2+周围最近且等距离的Ca2+有 个,在每个F-周围最近等距离的F-有 个。一个CaF2晶胞中
含 个Ca2+和 个F-; Ca2+和F-的配位数分别为 、 。841264884Ca2+F-找出CsCl、NaCl两种离子晶体中阳离子和阴离子的配位数,它们是否相等?6688决定离子晶体结构的因素几何因素
晶体中正负离子的半径比
电荷因素
晶体中正负离子的电荷比
键性因素
离子键的纯粹因素二、晶格能1、晶格能的定义:气态离子形成1mol离子晶体释放的能量。3、晶格能的作用:晶格能越大,形成的离子晶体越稳定,而且熔点越高,硬度越大。2、影响晶格能大小的因素:阴、阳离子的半径越小,晶格能越大。
阴、阳离子所带电荷越多,晶格能越大。练习:比较下列晶体熔沸点高低:
(1)NaF KCl NaCl (2)MgO Al2O3(1)NaF>NaCl>KCl(2) Al2O3 >MgOThank you
1、离子晶体一定是离子化合物。
2、含有离子的晶体一定是离子晶体。
3、离子晶体中只含离子键。
4、离子晶体中一定含金属阳离子。
5、由金属元素与非金属元素组成的晶体一定是离子晶体。×√×××配位数:离子晶体中,一个离子周围最邻近的异电性离子的 数目。缩写为C. N.。(1)钠离子和氯离子的位置:①钠离子和氯离子位于立方体的顶角上,并交错排列。
②钠离子:体心和棱中点;氯离子:面心和顶点,或者反之。5、晶胞类型:(1)氯化钠型晶胞(3)与Na+等距离且最近的Na+ 、Cl- 各有几个? 计算方法:均摊法
顶点占1/8;棱占1/4;面心占1/2;体心占1 (2)每个晶胞含钠离子、氯离子的个数与Na+等距离且最近的Na+ 有:12个
与Na+等距离且最近的Cl- 有:6个
NaCl的晶体结构模型 返回原处NaCl晶体中阴、阳离子配位数5、几种离子晶体
(1)NaCl晶体
每个Na+周围最近且等距离的Cl-有 个,
每个Cl-周围最近且等距离的Na+有 个;
在每个Na+周围最近且等距离的Na+有 个,
在每个Cl-周围最近等距离的Cl-有 个。
Na+和Cl-的配位数分别为 、 。
一个NaCl晶胞中含 个Na+和 个Cl-。
NaCl晶体中 NaCl分子,
化学式NaCl表示 。6612446无126Na+和Cl-的最简个数比(2)氯化铯型晶胞CsCl的晶体结构及晶胞构示意图CsCl晶胞(1)铯离子和氯离子的位置:铯离子:体心
氯离子:顶点;或者反之。(2)每个晶胞含铯离子、氯离子的个数铯离子:1个 ;氯离子:1个(3)与铯离子等距离且最近的铯离子、氯离子各有几个?铯离子:6个 ;氯离子:8个(2)CsCl晶体
每个Cs+周围最近且等距离的Cl-有 个,每个Cl-周围最近且等距离的Cs+有 个;在每个Cs+周围最近且等距离的Cs+有 个,在每个Cl-周围最近等距离的Cl-有 个。一个CsCl晶胞中含 个Cs+和 个Cl-。 Cs+和Cl-的配位数分别为 、 。88661188(3)CaF2晶体
每个Ca2+周围最近且等距离的F-有 个,每个F-周围最近且等距离的Ca2+有 个;
在每个Ca2+周围最近且等距离的Ca2+有 个,在每个F-周围最近等距离的F-有 个。一个CaF2晶胞中
含 个Ca2+和 个F-; Ca2+和F-的配位数分别为 、 。841264884Ca2+F-找出CsCl、NaCl两种离子晶体中阳离子和阴离子的配位数,它们是否相等?6688决定离子晶体结构的因素几何因素
晶体中正负离子的半径比
电荷因素
晶体中正负离子的电荷比
键性因素
离子键的纯粹因素二、晶格能1、晶格能的定义:气态离子形成1mol离子晶体释放的能量。3、晶格能的作用:晶格能越大,形成的离子晶体越稳定,而且熔点越高,硬度越大。2、影响晶格能大小的因素:阴、阳离子的半径越小,晶格能越大。
阴、阳离子所带电荷越多,晶格能越大。练习:比较下列晶体熔沸点高低:
(1)NaF KCl NaCl (2)MgO Al2O3(1)NaF>NaCl>KCl(2) Al2O3 >MgOThank you
