2.2 影响化学反应速率的因素 课件 (5)
文档属性
| 名称 | 2.2 影响化学反应速率的因素 课件 (5) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-07-12 00:00:00 | ||
图片预览







文档简介
课件41张PPT。1.理解外界条件(浓度、温度、压强、催化剂等)对化学反应速率的影响,认识其一般规律。
2.了解催化剂在生产、生活和科学研究领域中的重大作用。
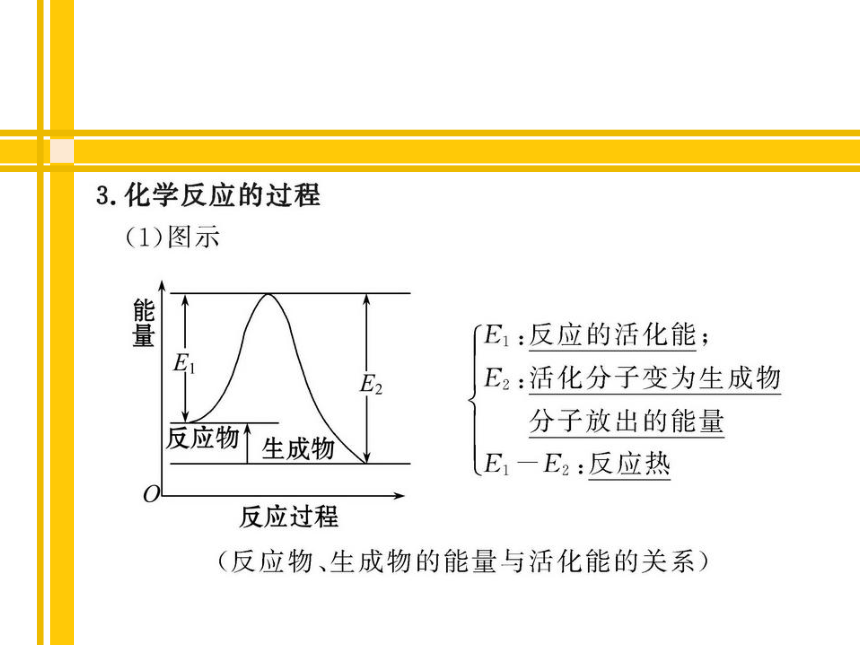
3.知道活化能的含义及其对化学反应速率的影响。脱水性学习目标一、有关化学反应速率的影响因素的注意事项1.浓度
固态或纯液体物质的浓度是常数,则有:
(1)增加其用量时,化学反应速率不变;
(2)增大其表面积或将其溶于溶剂中时,化学反应速率增大。2.温度
温度对吸热反应影响显著,则有:
(1)升高温度,吸热反应、放热反应的化学反应速率都增大,但吸热反应增大得多;
(2)降低温度,吸热反应、放热反应的化学反应速率都减小,但吸热反应减小得多。
3.催化剂
催化剂同等程度地增大正、逆反应的化学反应速率。4.压强
对于有气体参加的反应而言,改变压强,对化学反应速率产生影响的根本原因是引起浓度的改变。所以,在讨论压强对反应速率的影响时,应区分引起压强改变的原因。
(1)恒温时
增加压强 体积缩小 浓度增大 反应速率加快。(2)恒容时
①充入气体反应物 浓度增大 总压增大 反应速率加快;
②充入“惰气” 总压增大,但各气体的分压不变,即各气体的浓度不变,反应速率不变。
(3)恒压时
充入“惰气” 体积增大 各反应物浓度减小 反应速率减慢。(1)分析压强改变对化学反应速率的影响时,关键是看气体浓度是否有变化:若气体浓度有变化,化学反应速率一定改变;若气体浓度无变化,化学反应速率不改变。
(2)能够增大活化分子百分数的条件是:升高温度和加入催化剂。
(3)一定能够增大化学反应速率的条件是升高温度。【典例1】(2011·中山高二检测)对于可逆反应2A+3B
2C ΔH<0,下列条件的改变一定可以加快正反应速率的是
A.增加压强
B.升高温度
C.增加A的量
D.加入二氧化锰作催化剂解答该题要注意以下三点:【变式训练】
(2011·北京朝阳区高二检测)现
有可逆反应:X(g)+Y(g)
2Z(g)+W(s) ΔH<0,右图表示该
反应的反应过程。若使a曲线变为
b曲线,可采用的措施是( )A.加入催化剂
B.增大W的用量
C.降低温度
D.增大体积
【解析】选A。据图可知,使a曲线变为b曲线,应增大反应速率,只有A符合;B项W为固体,增大用量,反应速率不变;C、D两项使反应速率减小。二、有关化学反应速率的图像分析1.解答图像题的方法【典例2】(2011·扬州高二检测)一
定条件下进行反应2X(g)+Y(g)
Z(s)+3W(g) ΔH<0。达到平衡后,
t1时刻改变某一条件所得v-t图像如
图,则改变的条件为
A.增大压强 B.升高温度
C.加催化剂 D.增大生成物浓度解答该题要注意以下三点:选B。图像特点:t1时刻正、逆反应速率都增大,但逆反应速率增大的多,因为该反应正反应是放热反应,故升高温度时,正、逆反应速率都增大,但逆反应速率增大的多,B项正确;该反应是气体体积不变的反应,故增大压强时,正、逆反应速率都增大,且增大的程度相同,A错误;加入催化剂,正、逆反应速率都增大,且增大的程度相同,C错误;增大生成物浓度,逆反应速率瞬间增大,但正反应速率在这一瞬间不变,故D错误。【互动探究】请结合例题分析,画出A、C、D三项的图像。
提示:①该反应前后气体总物质的量不变,增大压强,正、逆反应速率同等程度的增大,使用催化剂也是同等程度的增大正逆反应速率,故A、C项的图像相似。A、C的图像为:②增大生成物浓度的瞬间,逆反应速率增大,正反应速率不变,D项的图像为:【变式训练】(2011·扬州高二检测)某可逆反应的正反应是吸热反应,温度对此反应的正、逆反应速率影响的曲线如图所示,其中正确的是( )【解析】选B。因为该反应正反应是吸热反应,故升高温度时,正、逆反应速率都增大,但正反应速率增大得多,B项正确。Thank you!
2.了解催化剂在生产、生活和科学研究领域中的重大作用。
3.知道活化能的含义及其对化学反应速率的影响。脱水性学习目标一、有关化学反应速率的影响因素的注意事项1.浓度
固态或纯液体物质的浓度是常数,则有:
(1)增加其用量时,化学反应速率不变;
(2)增大其表面积或将其溶于溶剂中时,化学反应速率增大。2.温度
温度对吸热反应影响显著,则有:
(1)升高温度,吸热反应、放热反应的化学反应速率都增大,但吸热反应增大得多;
(2)降低温度,吸热反应、放热反应的化学反应速率都减小,但吸热反应减小得多。
3.催化剂
催化剂同等程度地增大正、逆反应的化学反应速率。4.压强
对于有气体参加的反应而言,改变压强,对化学反应速率产生影响的根本原因是引起浓度的改变。所以,在讨论压强对反应速率的影响时,应区分引起压强改变的原因。
(1)恒温时
增加压强 体积缩小 浓度增大 反应速率加快。(2)恒容时
①充入气体反应物 浓度增大 总压增大 反应速率加快;
②充入“惰气” 总压增大,但各气体的分压不变,即各气体的浓度不变,反应速率不变。
(3)恒压时
充入“惰气” 体积增大 各反应物浓度减小 反应速率减慢。(1)分析压强改变对化学反应速率的影响时,关键是看气体浓度是否有变化:若气体浓度有变化,化学反应速率一定改变;若气体浓度无变化,化学反应速率不改变。
(2)能够增大活化分子百分数的条件是:升高温度和加入催化剂。
(3)一定能够增大化学反应速率的条件是升高温度。【典例1】(2011·中山高二检测)对于可逆反应2A+3B
2C ΔH<0,下列条件的改变一定可以加快正反应速率的是
A.增加压强
B.升高温度
C.增加A的量
D.加入二氧化锰作催化剂解答该题要注意以下三点:【变式训练】
(2011·北京朝阳区高二检测)现
有可逆反应:X(g)+Y(g)
2Z(g)+W(s) ΔH<0,右图表示该
反应的反应过程。若使a曲线变为
b曲线,可采用的措施是( )A.加入催化剂
B.增大W的用量
C.降低温度
D.增大体积
【解析】选A。据图可知,使a曲线变为b曲线,应增大反应速率,只有A符合;B项W为固体,增大用量,反应速率不变;C、D两项使反应速率减小。二、有关化学反应速率的图像分析1.解答图像题的方法【典例2】(2011·扬州高二检测)一
定条件下进行反应2X(g)+Y(g)
Z(s)+3W(g) ΔH<0。达到平衡后,
t1时刻改变某一条件所得v-t图像如
图,则改变的条件为
A.增大压强 B.升高温度
C.加催化剂 D.增大生成物浓度解答该题要注意以下三点:选B。图像特点:t1时刻正、逆反应速率都增大,但逆反应速率增大的多,因为该反应正反应是放热反应,故升高温度时,正、逆反应速率都增大,但逆反应速率增大的多,B项正确;该反应是气体体积不变的反应,故增大压强时,正、逆反应速率都增大,且增大的程度相同,A错误;加入催化剂,正、逆反应速率都增大,且增大的程度相同,C错误;增大生成物浓度,逆反应速率瞬间增大,但正反应速率在这一瞬间不变,故D错误。【互动探究】请结合例题分析,画出A、C、D三项的图像。
提示:①该反应前后气体总物质的量不变,增大压强,正、逆反应速率同等程度的增大,使用催化剂也是同等程度的增大正逆反应速率,故A、C项的图像相似。A、C的图像为:②增大生成物浓度的瞬间,逆反应速率增大,正反应速率不变,D项的图像为:【变式训练】(2011·扬州高二检测)某可逆反应的正反应是吸热反应,温度对此反应的正、逆反应速率影响的曲线如图所示,其中正确的是( )【解析】选B。因为该反应正反应是吸热反应,故升高温度时,正、逆反应速率都增大,但正反应速率增大得多,B项正确。Thank you!
