3.4 难溶电解质的溶解平衡 课件 (1)
文档属性
| 名称 | 3.4 难溶电解质的溶解平衡 课件 (1) |

|
|
| 格式 | zip | ||
| 文件大小 | 415.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-07-12 00:00:00 | ||
图片预览








文档简介
课件21张PPT。高考化学一轮复习水溶液中的离子平衡第4讲
难溶电解质的溶解平衡1.了解难溶电解质的溶解平衡。
2.知道沉淀转化的本质。
3.能应用溶度积常数进行简单计算。
4.认识沉淀反应在生产、科研、环保等领域的应用。【考纲要求】0.1mol/L的NaCl溶液与0.1mol/L的AgNO3溶液等体积混合后,溶液中是否还有Ag+?【思考与交流】【归纳小结】
1.溶解平衡的概念
2.溶解平衡的特征
【讨论】
要使溶液中的 Ag+浓度增大有哪些方法?【归纳小结】
3.影响因素
4.溶度积常数1.把CaSO4(足量)放入水中,一段时间后达到如下平衡CaSO4(s) Ca2+(aq)+SO42-(aq)下列措施,能够使CaSO4(s)减少的是:A.降低温度 B.加少量的水
C加少量的Na2SO4固体 D.加少量的CaCl2固体B【巩固练习】2.某课外小组为了探究BaSO4的 溶解度,分别将BaSO4放入: ① 5ml水 ?②40ml 0.2mol/L氢氧化钡溶液 ?③20ml 0.5mol/L的硫酸溶液 ? ④40ml0.1mol/L的硫酸钠溶液中,溶解至饱和。以上四个溶液中,Ba2+ 的浓度由大到小的顺序为 ( )
A、 ② > ①> ③ > ④
B、 ② > ① > ④ > ③?
C、① > ④ > ③ > ②
D、① > ② > ④ > ③? B50ml 浓度为2×10-5mol/L的AgNO3溶液中加入50ml浓度为2×10-5mol/L的NaCl溶液50ml能否生成沉淀?为什么?已知Ksp(AgCl)=1.56×10-10【思考与交流】【归纳小结】沉淀的生成已知 :难溶电解质Cu(OH)2在常温下的Ksp=2×10-20,则常温下:
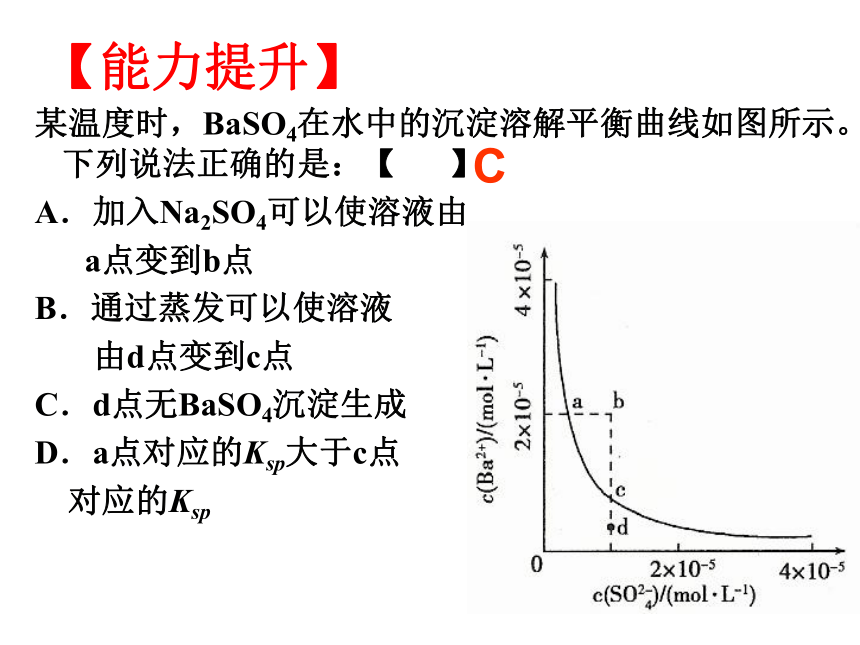
(1)某CuSO4溶液里c(Cu2+)=0.02 mol·L-1,如要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于________。(设调整溶液的pH时,忽略溶液体积不变)5【巩固练习】某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是:【 】
A.加入Na2SO4可以使溶液由
a点变到b点
B.通过蒸发可以使溶液
由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点
对应的Ksp
C【能力提升】在25℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式)Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20已知25℃时。沉淀的先后【思考与交流】【归纳小结】(2013·新课标全国卷Ⅰ·11)已知
Ksp(AgCl)=1.56×10-10,
Ksp(AgBr)=7.7×10-13,
Ksp(Ag2CrO4)=9.0×10-12。
某溶液中含有Cl-、Br-和CrO42-,浓度均为0.010
mol·L-1,向该溶液中逐滴加入0.010 mol·L-1的
AgNO3溶液时,三种阴离子产生沉淀的先后顺序
为 ( )
A.Cl-、Br-、CrO42- B.CrO42-、Br-、Cl-
C.Br-、Cl-、CrO42- D.Br-、CrO42-、Cl-C【能力提升】0.1mol/L的NaCl溶液与0.1mol/L的AgNO3溶液等体积混合后,所得溶液中加入浓度较大的NaI溶液会有什么现象?【思考与交流】沉淀的转化【归纳小结】【能力提升】B2判断正误,正确的划“√”,错误的划“×”
(1)不可能使要除去的离子全部通过沉淀除去。一般认为残留在溶液中的离子浓度小于1.0×10-5mol·L-1时,沉淀已经完全 ( )
(2)在一定条件下,溶解度较小的沉淀也可以转化成溶解度较大的沉淀 ( )
(3)常温下,向BaCO3饱和溶液中加入Na2CO3固体,BaCO3的Ksp减小 ( )
(4)溶度积常数Ksp只受温度影响,温度升高Ksp增大 ( )
(5)常温下,向Mg(OH)2饱和溶液中加入NaOH固体,Mg(OH)2的Ksp不变 ( )
2.一定温度下,在氢氧化钙的悬浊液中,存在氢氧化钙固体与其电离的离子间的溶解平衡关系:Ca(OH)2(s) Ca2+(aq)+2OH-(aq)。向此种悬浊液中加入少量的氧化钙粉末,下列叙述正确的是 :【 】
A.溶液中钙离子数目减小
B.溶液中钙离子浓度减少
C.溶液中氢氧根离子浓度增大
D.pH减小A若在绝热的体系中进行,溶液的体积变化可忽略不计【讨论】【2014年高考上海卷第11题】向饱和澄清石灰水中加入少量CaC2,充分反应后恢复到原来的温度,所得溶液中
A.c(Ca2+)、c(OH-)均增大
B.c(Ca2+)、c(OH-)均保持不变
C.c(Ca2+)、c(OH-)均减小
D.c(OH-)增大、c(H+)减小
B【体验高考】B【综合运用】B【综合运用】(2013·北京高考·10)实验:①0.1 mol·L-1AgNO3
溶液和0.1 mol·L-1NaCl溶液等体积混合得到浊液
a,过滤得到滤液b和白色沉淀c;
②向滤液b中滴加0.1 mol·L-1KI溶液,出现浑浊;
③向沉淀c中滴加0.1 mol·L-1KI溶液,沉淀变为
黄色。下列分析不正确的是 ( )
A.浊液a中存在沉淀溶解平衡:
AgCl(s) Ag+(aq)+Cl-(aq)
B.滤液b中不含有Ag+
C.③中颜色变化说明AgCl转化为AgI
D.实验可以证明AgI比AgCl更难溶B 21
已知:25°C时,Ksp[R(OH)2]=5.61×10-12,Ksp(RF2)=7.42×10-11。下列说法正确的是( )
A.25°C时,饱和R(OH)2溶液与饱和RF2溶液相比,前者的c(R2+)大
B.25°C时,在R(OH)2的悬浊液中加入少量的NH4Cl固体,c(R2+)增大(不考虑Cl-的影响)
C.25°C,R(OH)2固体在20 mL 0.01mol·L-1氨水中的Ksp比在20 mL 0.01 mol·L-1 NH4Cl溶液中的Ksp小
D.25°C时,在RF2在盐酸中的溶解度小于在蒸馏水中的溶解度。B【练习】
难溶电解质的溶解平衡1.了解难溶电解质的溶解平衡。
2.知道沉淀转化的本质。
3.能应用溶度积常数进行简单计算。
4.认识沉淀反应在生产、科研、环保等领域的应用。【考纲要求】0.1mol/L的NaCl溶液与0.1mol/L的AgNO3溶液等体积混合后,溶液中是否还有Ag+?【思考与交流】【归纳小结】
1.溶解平衡的概念
2.溶解平衡的特征
【讨论】
要使溶液中的 Ag+浓度增大有哪些方法?【归纳小结】
3.影响因素
4.溶度积常数1.把CaSO4(足量)放入水中,一段时间后达到如下平衡CaSO4(s) Ca2+(aq)+SO42-(aq)下列措施,能够使CaSO4(s)减少的是:A.降低温度 B.加少量的水
C加少量的Na2SO4固体 D.加少量的CaCl2固体B【巩固练习】2.某课外小组为了探究BaSO4的 溶解度,分别将BaSO4放入: ① 5ml水 ?②40ml 0.2mol/L氢氧化钡溶液 ?③20ml 0.5mol/L的硫酸溶液 ? ④40ml0.1mol/L的硫酸钠溶液中,溶解至饱和。以上四个溶液中,Ba2+ 的浓度由大到小的顺序为 ( )
A、 ② > ①> ③ > ④
B、 ② > ① > ④ > ③?
C、① > ④ > ③ > ②
D、① > ② > ④ > ③? B50ml 浓度为2×10-5mol/L的AgNO3溶液中加入50ml浓度为2×10-5mol/L的NaCl溶液50ml能否生成沉淀?为什么?已知Ksp(AgCl)=1.56×10-10【思考与交流】【归纳小结】沉淀的生成已知 :难溶电解质Cu(OH)2在常温下的Ksp=2×10-20,则常温下:
(1)某CuSO4溶液里c(Cu2+)=0.02 mol·L-1,如要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于________。(设调整溶液的pH时,忽略溶液体积不变)5【巩固练习】某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是:【 】
A.加入Na2SO4可以使溶液由
a点变到b点
B.通过蒸发可以使溶液
由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点
对应的Ksp
C【能力提升】在25℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式)Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20已知25℃时。沉淀的先后【思考与交流】【归纳小结】(2013·新课标全国卷Ⅰ·11)已知
Ksp(AgCl)=1.56×10-10,
Ksp(AgBr)=7.7×10-13,
Ksp(Ag2CrO4)=9.0×10-12。
某溶液中含有Cl-、Br-和CrO42-,浓度均为0.010
mol·L-1,向该溶液中逐滴加入0.010 mol·L-1的
AgNO3溶液时,三种阴离子产生沉淀的先后顺序
为 ( )
A.Cl-、Br-、CrO42- B.CrO42-、Br-、Cl-
C.Br-、Cl-、CrO42- D.Br-、CrO42-、Cl-C【能力提升】0.1mol/L的NaCl溶液与0.1mol/L的AgNO3溶液等体积混合后,所得溶液中加入浓度较大的NaI溶液会有什么现象?【思考与交流】沉淀的转化【归纳小结】【能力提升】B2判断正误,正确的划“√”,错误的划“×”
(1)不可能使要除去的离子全部通过沉淀除去。一般认为残留在溶液中的离子浓度小于1.0×10-5mol·L-1时,沉淀已经完全 ( )
(2)在一定条件下,溶解度较小的沉淀也可以转化成溶解度较大的沉淀 ( )
(3)常温下,向BaCO3饱和溶液中加入Na2CO3固体,BaCO3的Ksp减小 ( )
(4)溶度积常数Ksp只受温度影响,温度升高Ksp增大 ( )
(5)常温下,向Mg(OH)2饱和溶液中加入NaOH固体,Mg(OH)2的Ksp不变 ( )
2.一定温度下,在氢氧化钙的悬浊液中,存在氢氧化钙固体与其电离的离子间的溶解平衡关系:Ca(OH)2(s) Ca2+(aq)+2OH-(aq)。向此种悬浊液中加入少量的氧化钙粉末,下列叙述正确的是 :【 】
A.溶液中钙离子数目减小
B.溶液中钙离子浓度减少
C.溶液中氢氧根离子浓度增大
D.pH减小A若在绝热的体系中进行,溶液的体积变化可忽略不计【讨论】【2014年高考上海卷第11题】向饱和澄清石灰水中加入少量CaC2,充分反应后恢复到原来的温度,所得溶液中
A.c(Ca2+)、c(OH-)均增大
B.c(Ca2+)、c(OH-)均保持不变
C.c(Ca2+)、c(OH-)均减小
D.c(OH-)增大、c(H+)减小
B【体验高考】B【综合运用】B【综合运用】(2013·北京高考·10)实验:①0.1 mol·L-1AgNO3
溶液和0.1 mol·L-1NaCl溶液等体积混合得到浊液
a,过滤得到滤液b和白色沉淀c;
②向滤液b中滴加0.1 mol·L-1KI溶液,出现浑浊;
③向沉淀c中滴加0.1 mol·L-1KI溶液,沉淀变为
黄色。下列分析不正确的是 ( )
A.浊液a中存在沉淀溶解平衡:
AgCl(s) Ag+(aq)+Cl-(aq)
B.滤液b中不含有Ag+
C.③中颜色变化说明AgCl转化为AgI
D.实验可以证明AgI比AgCl更难溶B 21
已知:25°C时,Ksp[R(OH)2]=5.61×10-12,Ksp(RF2)=7.42×10-11。下列说法正确的是( )
A.25°C时,饱和R(OH)2溶液与饱和RF2溶液相比,前者的c(R2+)大
B.25°C时,在R(OH)2的悬浊液中加入少量的NH4Cl固体,c(R2+)增大(不考虑Cl-的影响)
C.25°C,R(OH)2固体在20 mL 0.01mol·L-1氨水中的Ksp比在20 mL 0.01 mol·L-1 NH4Cl溶液中的Ksp小
D.25°C时,在RF2在盐酸中的溶解度小于在蒸馏水中的溶解度。B【练习】
