3.4 难溶电解质的溶解平衡 课件 (3)
文档属性
| 名称 | 3.4 难溶电解质的溶解平衡 课件 (3) |

|
|
| 格式 | zip | ||
| 文件大小 | 785.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-07-12 00:00:00 | ||
图片预览





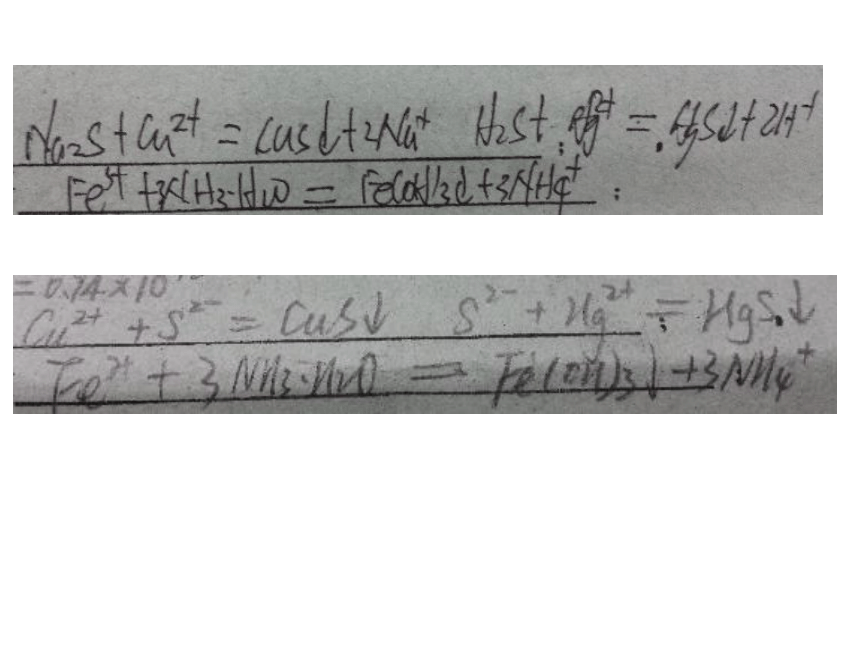
文档简介
课件14张PPT。难溶电解质的溶解平衡
沉淀溶解平衡(2)
沉淀溶解平衡的应用【学习目标】
1、能从溶度积和沉淀溶解平衡的角度理解沉淀的生成;
2、能从沉淀溶解平衡移动的角度解释沉淀的溶解。【复习巩固1】【复习巩固2】3、假设溶液中Fe3+的浓度为0.10mol/L,计算刚开始形成Fe(OH)3沉淀时,溶液中的的c(OH—)、c(H+)和pH值。
(已知Ksp(Fe(OH)3)= 4.0×10—38,
=0.74,lg1.35=0.13)
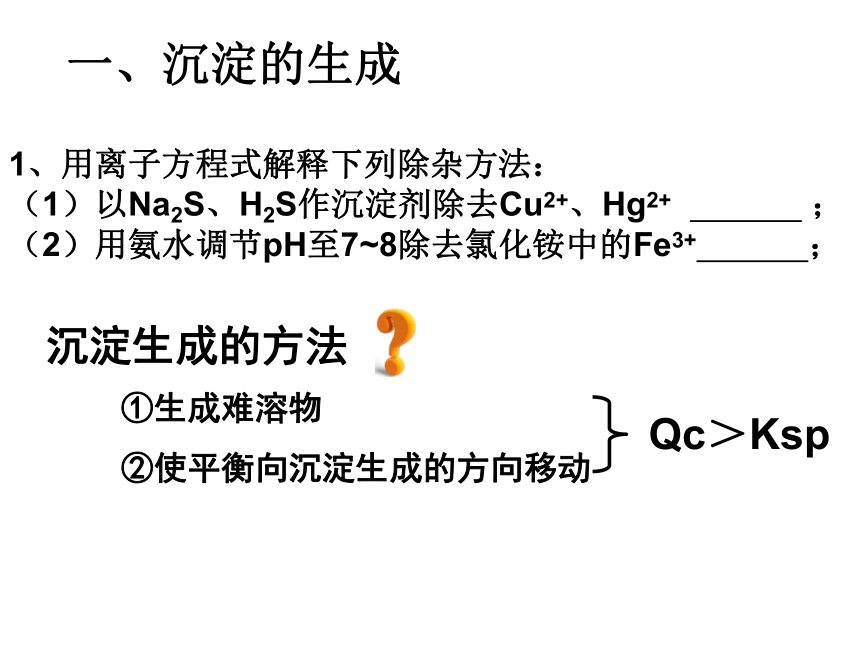
一、沉淀的生成1、用离子方程式解释下列除杂方法:
(1)以Na2S、H2S作沉淀剂除去Cu2+、Hg2+ ;
(2)用氨水调节pH至7~8除去氯化铵中的Fe3+ ; ①生成难溶物
②使平衡向沉淀生成的方向移动Qc>Ksp2、工业上制取纯净的CuCl2·2H2O的主要过程是:
①将粗氧化铜(含少量Fe)溶解于稀盐酸中,过滤,得到含Cu2+、Fe2+、Fe3+、Cl—的滤液A
②对上述滤液进行如下操作,二、沉淀的溶解难溶于水的CaCO3沉淀可以溶于盐酸CaCO3 + 2HCl == CaCl2 + CO2↑ + H2O能否从沉淀溶解平衡移动角度解释?HCl与CO32-反应,令c( CO32- )减小,
使平衡向溶解的方向移动。二、沉淀的溶解1、从沉淀溶解平衡移动角度解释难溶于水的Cu(OH)2沉淀可以溶于盐酸 .设法不断移去溶解平衡体系中的相应离子,使平衡向沉淀溶解的方向移动Qc<Ksp二、沉淀的溶解2、实验:
向盛有少量Mg(OH)2沉淀的试管中滴加NH4Cl溶液。现象:白色沉淀溶解【小组讨论完成(2)(3)】甲同学的解释是: Mg(OH)2(s) Mg2+(aq)+2OH-(aq) ①
NH4+ + H2O NH3·H2O+H+ ②
H+ + OH- H2O ③
由于NH4+水解显酸性,导致平衡①右移,沉淀溶解。
乙同学的解释是: Mg(OH)2(s) Mg2+(aq)+2OH-(aq) ①
NH4+ + OH- NH3·H2O ④
由于NH4Cl电离出的NH4+与Mg(OH)2电离出的OH—离子结合,
生成了弱的电解质NH3·H2O,导致平衡①右移,沉淀溶解。
丙同学不能肯定哪位同学的解释合理,于是选用CH3COONH4(水溶液显中性)来证明甲、乙两位同学的解释。得到结论如下:
若 ,则甲同学正确;
若 ,则乙同学正确。沉淀不溶解沉淀溶解【反馈练习】(1)KSCN溶液
(2)与溶液中的H+反应,使Al3+ 水解完全生成Al(OH)3 沉淀
(3)2NH3?H2O + Fe2+ = Fe(OH)2↓+2NH4+
(4) Fe(OH)2 +H2C2O4=FeC2O4 +2H2O
(5)化肥
沉淀溶解平衡的应用【学习目标】
1、能从溶度积和沉淀溶解平衡的角度理解沉淀的生成;
2、能从沉淀溶解平衡移动的角度解释沉淀的溶解。【复习巩固1】【复习巩固2】3、假设溶液中Fe3+的浓度为0.10mol/L,计算刚开始形成Fe(OH)3沉淀时,溶液中的的c(OH—)、c(H+)和pH值。
(已知Ksp(Fe(OH)3)= 4.0×10—38,
=0.74,lg1.35=0.13)
一、沉淀的生成1、用离子方程式解释下列除杂方法:
(1)以Na2S、H2S作沉淀剂除去Cu2+、Hg2+ ;
(2)用氨水调节pH至7~8除去氯化铵中的Fe3+ ; ①生成难溶物
②使平衡向沉淀生成的方向移动Qc>Ksp2、工业上制取纯净的CuCl2·2H2O的主要过程是:
①将粗氧化铜(含少量Fe)溶解于稀盐酸中,过滤,得到含Cu2+、Fe2+、Fe3+、Cl—的滤液A
②对上述滤液进行如下操作,二、沉淀的溶解难溶于水的CaCO3沉淀可以溶于盐酸CaCO3 + 2HCl == CaCl2 + CO2↑ + H2O能否从沉淀溶解平衡移动角度解释?HCl与CO32-反应,令c( CO32- )减小,
使平衡向溶解的方向移动。二、沉淀的溶解1、从沉淀溶解平衡移动角度解释难溶于水的Cu(OH)2沉淀可以溶于盐酸 .设法不断移去溶解平衡体系中的相应离子,使平衡向沉淀溶解的方向移动Qc<Ksp二、沉淀的溶解2、实验:
向盛有少量Mg(OH)2沉淀的试管中滴加NH4Cl溶液。现象:白色沉淀溶解【小组讨论完成(2)(3)】甲同学的解释是: Mg(OH)2(s) Mg2+(aq)+2OH-(aq) ①
NH4+ + H2O NH3·H2O+H+ ②
H+ + OH- H2O ③
由于NH4+水解显酸性,导致平衡①右移,沉淀溶解。
乙同学的解释是: Mg(OH)2(s) Mg2+(aq)+2OH-(aq) ①
NH4+ + OH- NH3·H2O ④
由于NH4Cl电离出的NH4+与Mg(OH)2电离出的OH—离子结合,
生成了弱的电解质NH3·H2O,导致平衡①右移,沉淀溶解。
丙同学不能肯定哪位同学的解释合理,于是选用CH3COONH4(水溶液显中性)来证明甲、乙两位同学的解释。得到结论如下:
若 ,则甲同学正确;
若 ,则乙同学正确。沉淀不溶解沉淀溶解【反馈练习】(1)KSCN溶液
(2)与溶液中的H+反应,使Al3+ 水解完全生成Al(OH)3 沉淀
(3)2NH3?H2O + Fe2+ = Fe(OH)2↓+2NH4+
(4) Fe(OH)2 +H2C2O4=FeC2O4 +2H2O
(5)化肥
