2.1 脂肪烃 课件 (1)
文档属性
| 名称 | 2.1 脂肪烃 课件 (1) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-07-12 00:00:00 | ||
图片预览

文档简介
课件25张PPT。第二章 烃和卤代烃第一节 脂肪烃第二课时
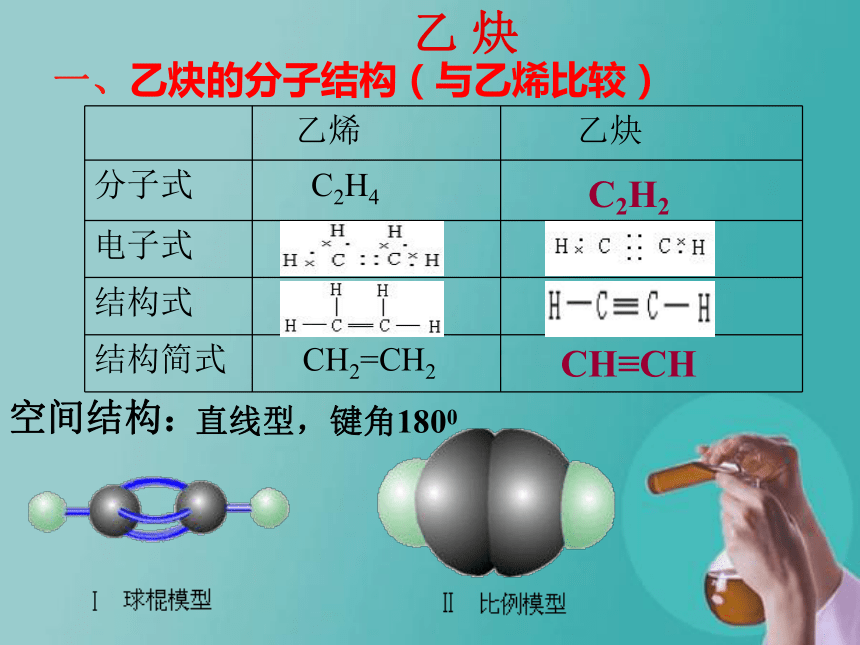
乙炔的实验室制法及性质乙 炔一、乙炔的分子结构(与乙烯比较)
直线型,键角1800空间结构:CH≡CH C2H2 思考 根据乙烯、乙炔的分子结构特点,你能否预测乙炔可能具有什么化学性质?
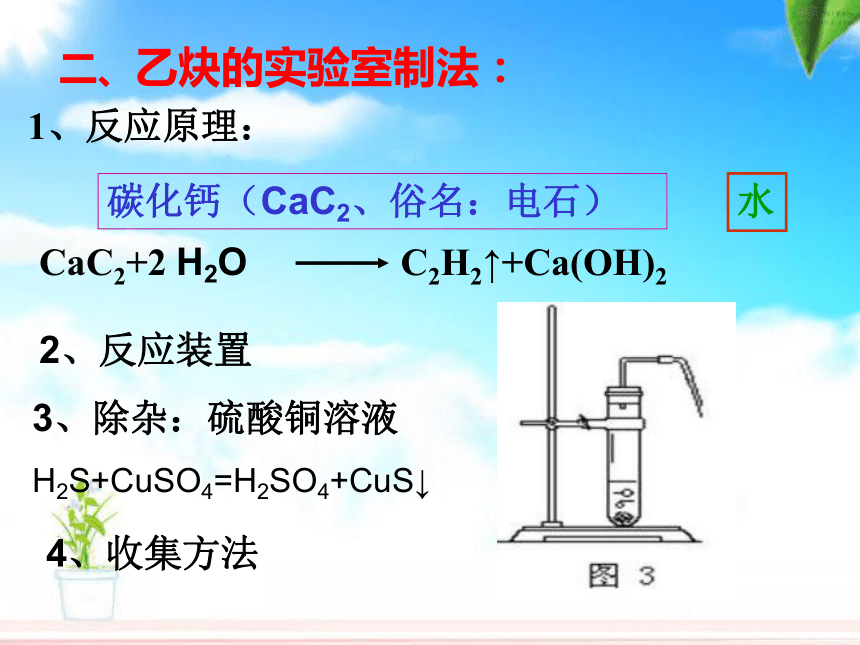
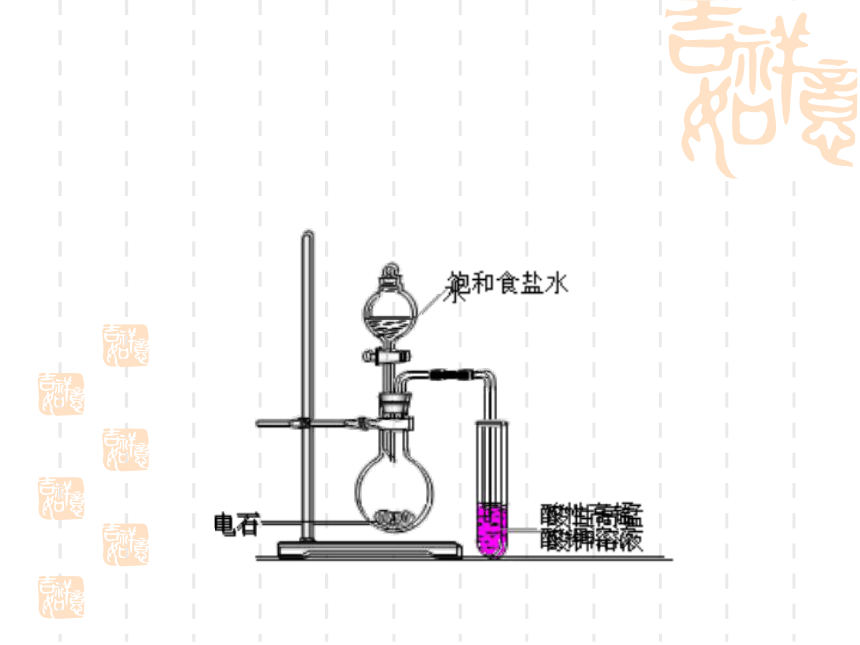
-C≡C- 二、乙炔的实验室制法: 1、反应原理:碳化钙(CaC2、俗名:电石)水2、反应装置
3、除杂:硫酸铜溶液
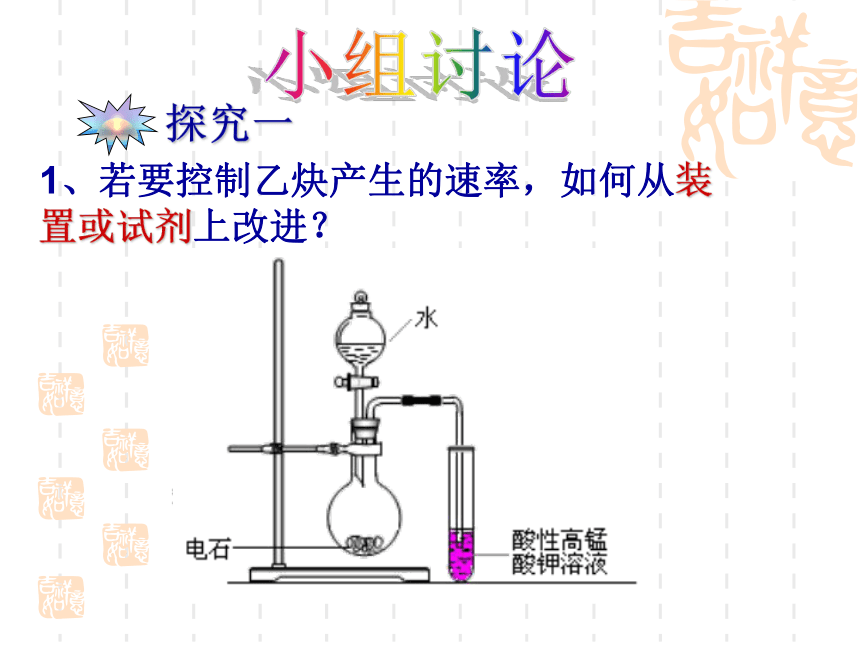
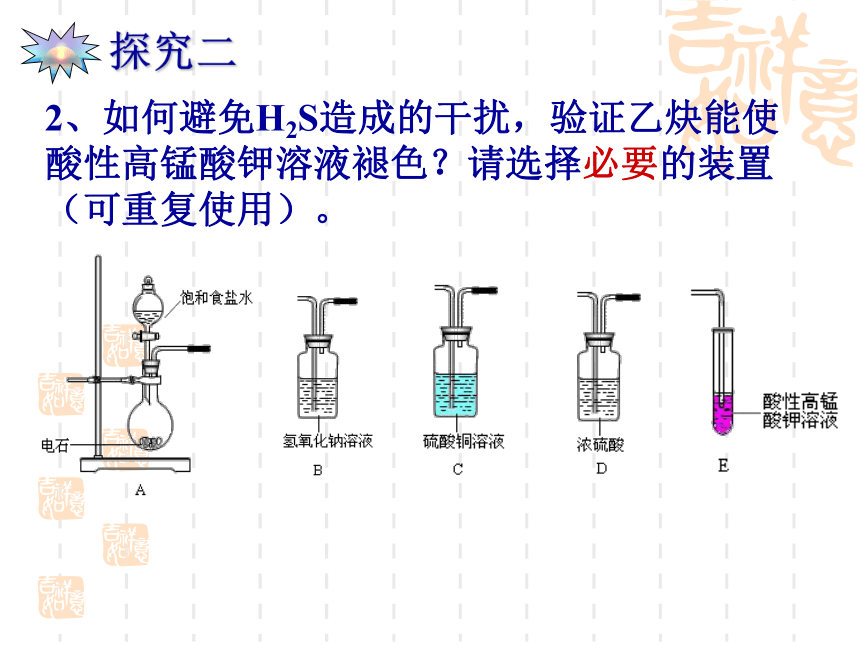
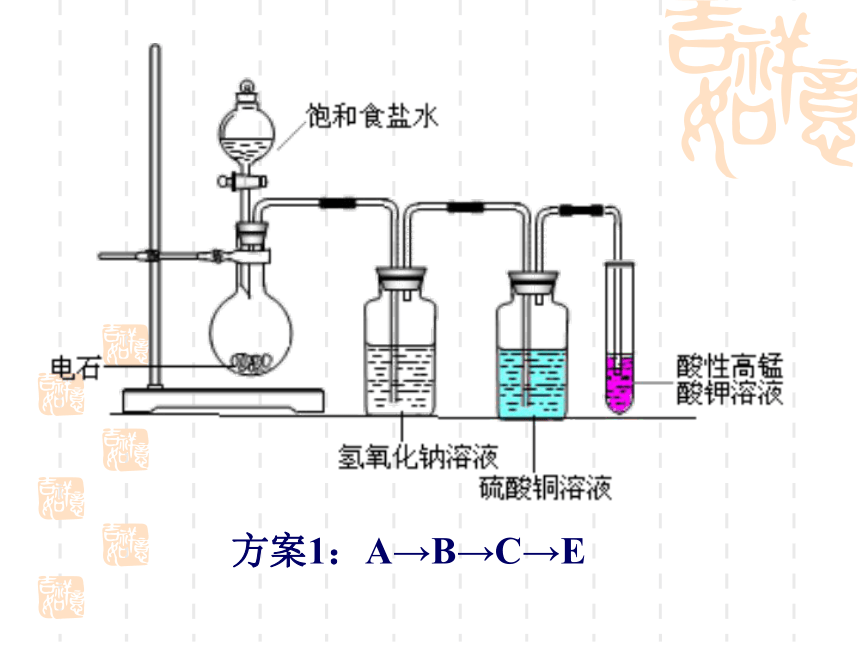
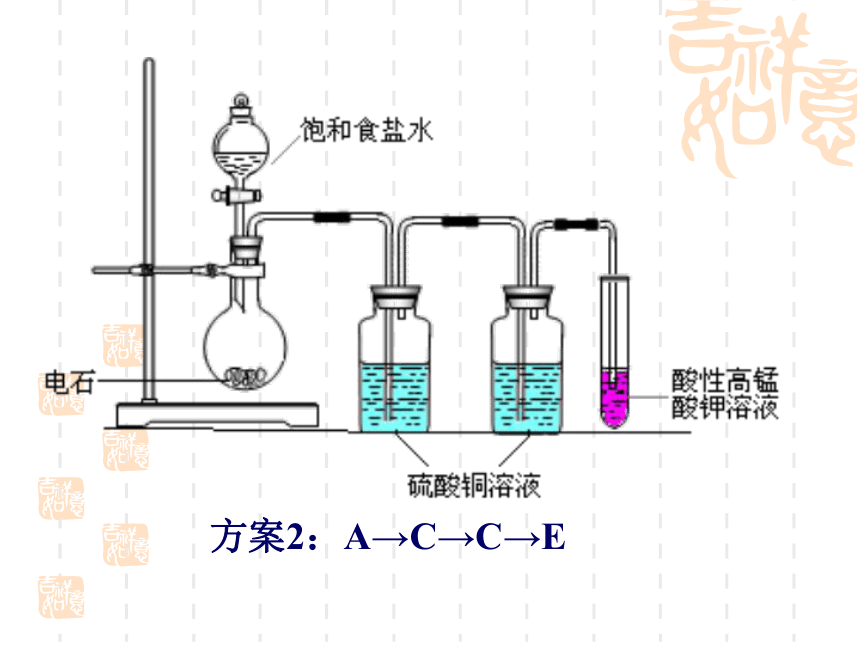
H2S+CuSO4=H2SO4+CuS↓ 4、收集方法1、若要控制乙炔产生的速率,如何从装置或试剂上改进?小组讨论2、如何避免H2S造成的干扰,验证乙炔能使酸性高锰酸钾溶液褪色?请选择必要的装置(可重复使用)。方案1:A→B→C→E方案2:A→C→C→E3、下列哪种装置可以收集到较为纯净的乙炔 ?图1图2图3如果将图3装置中的水倒掉,分别充入氮气、氢气和二氧化碳的话又哪种方案可行?如果可行,进、出口方向如何选择?步骤: (2)向锥形瓶中加入电石,再
向分液漏斗中加入硫酸铜溶液。
(3)用分液漏斗逐滴加入硫酸
铜溶液。(4) 观察实验现象。(1) 组装好装置后先检查气密性。三、乙炔的性质(一)物理性质: 实验探究溶液紫色逐渐褪去。 溶液橙色逐渐褪去。 火焰明亮,并伴有浓烟。(二)化学性质:1、氧化反应:(1)可燃性:火焰明亮,并伴有浓烟。氧炔焰:乙炔燃烧放出大量的热,在O2中燃烧,产生的氧炔焰温度高达3000℃以上,可用于切割、焊接金属。氧炔焰切割金属焊 枪溶液紫色逐渐褪去2KMnO4+ 3H2SO4+ C2H2→2MnSO4+ K2SO4+2CO2↑+ 4H2O(2)乙炔能使酸性KMnO4溶液褪色。1, 2—二溴乙烯1, 1, 2, 2—四溴乙烷乙炔也能使溴的四氯化碳溶液褪色。2、加成反应①②与H2加成 ③与HCl加成乙炔的用途1、乙炔燃烧时产生的氧炔焰可用来切割或焊接金属。2、 乙炔是一种重要的基本有机原料,可以用来制备氯乙烯、 聚氯乙烯和乙醛等。聚氯乙烯薄膜3、导电塑料——聚乙炔小结
性质用途结构 制法CH≡CH练一练:
1、用哪些方法可以区别甲烷和乙炔?① 分别点燃甲烷和乙炔,若火焰明亮有大量黑烟生成的是乙炔;火焰呈蓝色的是甲烷。② 将甲烷和乙炔分别通入两支盛有溴水的试管中,能使溴水褪色的是乙炔;不使溴水褪色的是甲烷。③ 将甲烷和乙炔分别通入两支盛有酸性高锰酸钾溶液的试管中,能使酸性高锰酸钾溶液褪色的是乙炔;不使酸性高锰酸钾溶液褪色的是甲烷。聚氯乙烯在使用的过程中,易发生老化,会变硬、发脆、开裂等,并释放出对人体有害的氯化氢,故不宜使用聚氯乙烯制品直接盛装食物。2、聚氯乙烯是一种合成树脂,可用于制备塑料和合成纤维等。聚氯乙烯可由H2、Cl2、电石和水为原料制取。请写出有关的反应方程式。恳请批评指正谢谢
乙炔的实验室制法及性质乙 炔一、乙炔的分子结构(与乙烯比较)
直线型,键角1800空间结构:CH≡CH C2H2 思考 根据乙烯、乙炔的分子结构特点,你能否预测乙炔可能具有什么化学性质?
-C≡C- 二、乙炔的实验室制法: 1、反应原理:碳化钙(CaC2、俗名:电石)水2、反应装置
3、除杂:硫酸铜溶液
H2S+CuSO4=H2SO4+CuS↓ 4、收集方法1、若要控制乙炔产生的速率,如何从装置或试剂上改进?小组讨论2、如何避免H2S造成的干扰,验证乙炔能使酸性高锰酸钾溶液褪色?请选择必要的装置(可重复使用)。方案1:A→B→C→E方案2:A→C→C→E3、下列哪种装置可以收集到较为纯净的乙炔 ?图1图2图3如果将图3装置中的水倒掉,分别充入氮气、氢气和二氧化碳的话又哪种方案可行?如果可行,进、出口方向如何选择?步骤: (2)向锥形瓶中加入电石,再
向分液漏斗中加入硫酸铜溶液。
(3)用分液漏斗逐滴加入硫酸
铜溶液。(4) 观察实验现象。(1) 组装好装置后先检查气密性。三、乙炔的性质(一)物理性质: 实验探究溶液紫色逐渐褪去。 溶液橙色逐渐褪去。 火焰明亮,并伴有浓烟。(二)化学性质:1、氧化反应:(1)可燃性:火焰明亮,并伴有浓烟。氧炔焰:乙炔燃烧放出大量的热,在O2中燃烧,产生的氧炔焰温度高达3000℃以上,可用于切割、焊接金属。氧炔焰切割金属焊 枪溶液紫色逐渐褪去2KMnO4+ 3H2SO4+ C2H2→2MnSO4+ K2SO4+2CO2↑+ 4H2O(2)乙炔能使酸性KMnO4溶液褪色。1, 2—二溴乙烯1, 1, 2, 2—四溴乙烷乙炔也能使溴的四氯化碳溶液褪色。2、加成反应①②与H2加成 ③与HCl加成乙炔的用途1、乙炔燃烧时产生的氧炔焰可用来切割或焊接金属。2、 乙炔是一种重要的基本有机原料,可以用来制备氯乙烯、 聚氯乙烯和乙醛等。聚氯乙烯薄膜3、导电塑料——聚乙炔小结
性质用途结构 制法CH≡CH练一练:
1、用哪些方法可以区别甲烷和乙炔?① 分别点燃甲烷和乙炔,若火焰明亮有大量黑烟生成的是乙炔;火焰呈蓝色的是甲烷。② 将甲烷和乙炔分别通入两支盛有溴水的试管中,能使溴水褪色的是乙炔;不使溴水褪色的是甲烷。③ 将甲烷和乙炔分别通入两支盛有酸性高锰酸钾溶液的试管中,能使酸性高锰酸钾溶液褪色的是乙炔;不使酸性高锰酸钾溶液褪色的是甲烷。聚氯乙烯在使用的过程中,易发生老化,会变硬、发脆、开裂等,并释放出对人体有害的氯化氢,故不宜使用聚氯乙烯制品直接盛装食物。2、聚氯乙烯是一种合成树脂,可用于制备塑料和合成纤维等。聚氯乙烯可由H2、Cl2、电石和水为原料制取。请写出有关的反应方程式。恳请批评指正谢谢
