2.1 脂肪烃 课件 (2)
文档属性
| 名称 | 2.1 脂肪烃 课件 (2) |

|
|
| 格式 | zip | ||
| 文件大小 | 4.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-07-12 00:00:00 | ||
图片预览








文档简介
课件25张PPT。乙炔 炔烃 小魔术 电石气实际上就是乙炔,我国古时对此曾有“器中放石几块,滴水则产气,点之则燃”的记载。
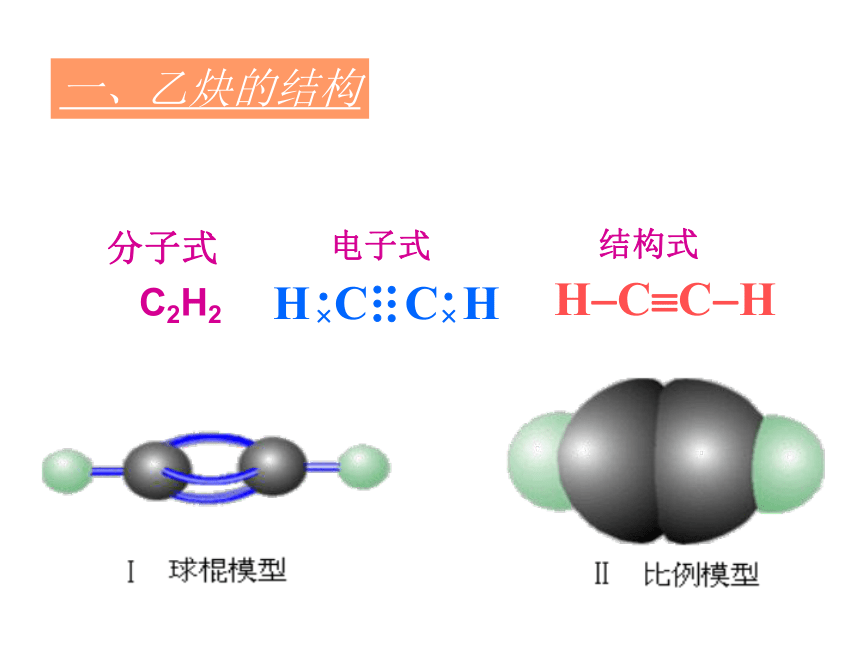
可以燃烧的冰一、乙炔的结构分子式 C2H2电子式结构式H?C?C?H二、乙炔的物理性质1.乙炔是 色 味的气体2.密度比空气的密度 . 3. 溶于水,易溶于无稍小微有机溶剂无全部单键,
饱和有碳碳双键,不饱和有碳碳三键,不饱和取代
燃烧加成、加聚、
燃烧
被酸性KMnO4氧化?温故而知新:2、反应原理:三、乙炔的实验室制法1、药品:水碳化钙(CaC2、俗名:电石)①取用电石时,不能用手拿而要用镊子取,原因是什么?②为使反应缓和进行以获得平稳的乙炔气流,可用什么代替水;③应选用什么样的配套装置来控制水量?饱和食盐水 分液漏斗 (1)因电石中含有 CaS、Ca3P2等,也会与水反应,产生H2S、PH3等气体,所以所制乙炔气体会有难闻的臭味; (2)如何去除乙炔的臭味呢?请选择合适的装置和试剂。思考:实验室制的乙炔为什么会有臭味呢? 1. 氧化反应 (1)与氧气四、乙炔化学性质现象:为什么?火焰明亮,冒浓烟四)炔烃氧炔焰:乙炔燃烧放出大量的热,在O2中燃烧,产生的氧炔焰温度高达3000℃以上,可用于切割、焊接金属。氧炔焰切割金属焊 枪乙炔的化学性质:
(2)与酸性KMnO4
乙炔能使酸性KMnO4溶液褪色。
KMnO4 + H2SO4+ C2H2→ MnSO4+ K2SO4+ CO2↑+ H2O 1,1,2,2-四溴乙烷CH≡CH + 2Br2 → CHBr2CHBr22.? 加成反应:试一试: 一定条件下,乙炔还能与H2、其它卤素单质、HX、H2O等发生加成反应,你能写出乙炔与H2 反应的方程式吗?聚氯乙烯在使用的过程中,易发生老化,会变硬、发脆、开裂等,并释放出对人体有害的氯化氢,故不宜使用聚氯乙烯制品直接盛装食物。学贵有用聚氯乙烯是一种合成树脂,可用于制备塑料和合成纤维等。聚氯乙烯可由H2、Cl2和乙炔为原料制取。你能写出有关的反应方程式吗?氯乙烯:提示:吹塑定型的塑料薄膜(2)氧炔焰可用来切割或焊接金属。五、乙炔的用途(1)基本化工原料,可以用来制备氯
乙烯、聚氯乙烯等。1.不能使酸性KMnO4溶液褪色的是 ( )
A.乙烯 B.聚乙烯
C.丙烯 D.乙炔
2.关于炔烃的下列描述正确的是 ( )
A.分子里含有碳碳三键的不饱和链烃叫炔烃
B.炔烃分子里的所有碳原子都在同一直线上
C.炔烃易发生加成反应,也易发生取代反应
D.不能使溴水褪色,但可使酸性高锰酸钾溶液褪色
3.既可以鉴别乙烷和乙炔,又可以除去乙烷中含有的乙炔 的方法是 ( )
A.通人足量的溴水中
B.与足量酸性高锰酸钾溶液反应
C.点燃
D. 在一定条件下与氢气加成BAA自我检测4、所有原子都在同一直线上的是…………( )
A、C2H4 B、C2H2
C、C2H6 D、CO2
5、区别乙烯和乙炔的最简单可行的方法…( )
A、用溴水 B、用酸性KMnO4溶液
C、点燃 D、与H2加成
BC
6、由乙炔为原料制取CHClBr—CH2Br ,下列方法中最可行是
A、先与HBr加成再与HCl加成 B、先与HCl加成再与Br2加成
C、先与Br2加成再与Cl2加成 D、先与Cl2加成再与HBr加成
7、在有催化剂的条件下,将a L乙炔和乙烯的混合气体与足量的
H2 加成,消耗1.25a L H2 ,则乙烯和乙炔的体积比为 ( )
A、1∶1 B、2∶1 C、3∶1 D、4∶18、科学家于1995年合成了一种化学式为C200H200含有多个C≡C (碳碳叁键)的链状烃,其分子中含有C≡C最多是
A.49个 B.50个
C.51个 D.无法确定C10、含一叁键的炔烃,氢化后的产物结构简式为
此炔烃可能有的结构有( )
A、1种 B、2 C、3种 D、4种B11、在标准状况下将11.2升乙烯和乙炔的混合气通入到溴水中充分反应,测得有128克溴参加了反应,测乙烯、乙炔的物质的量之比为( )
A.1∶2 B.2∶3 C.3∶4 D.4∶5 B12、描述CH3—CH = CH—C≡C—CF3分子结构的下列叙述中正确的是( )
A.6个碳原子有可能都在一条直线上
B.6个碳原子不可能都在一条直线上
C.6个碳原子有可能都在同一平面上
D.6个碳原子不可能都在同一平面上 B、C作业:课后习题恳请批评指正谢谢
可以燃烧的冰一、乙炔的结构分子式 C2H2电子式结构式H?C?C?H二、乙炔的物理性质1.乙炔是 色 味的气体2.密度比空气的密度 . 3. 溶于水,易溶于无稍小微有机溶剂无全部单键,
饱和有碳碳双键,不饱和有碳碳三键,不饱和取代
燃烧加成、加聚、
燃烧
被酸性KMnO4氧化?温故而知新:2、反应原理:三、乙炔的实验室制法1、药品:水碳化钙(CaC2、俗名:电石)①取用电石时,不能用手拿而要用镊子取,原因是什么?②为使反应缓和进行以获得平稳的乙炔气流,可用什么代替水;③应选用什么样的配套装置来控制水量?饱和食盐水 分液漏斗 (1)因电石中含有 CaS、Ca3P2等,也会与水反应,产生H2S、PH3等气体,所以所制乙炔气体会有难闻的臭味; (2)如何去除乙炔的臭味呢?请选择合适的装置和试剂。思考:实验室制的乙炔为什么会有臭味呢? 1. 氧化反应 (1)与氧气四、乙炔化学性质现象:为什么?火焰明亮,冒浓烟四)炔烃氧炔焰:乙炔燃烧放出大量的热,在O2中燃烧,产生的氧炔焰温度高达3000℃以上,可用于切割、焊接金属。氧炔焰切割金属焊 枪乙炔的化学性质:
(2)与酸性KMnO4
乙炔能使酸性KMnO4溶液褪色。
KMnO4 + H2SO4+ C2H2→ MnSO4+ K2SO4+ CO2↑+ H2O 1,1,2,2-四溴乙烷CH≡CH + 2Br2 → CHBr2CHBr22.? 加成反应:试一试: 一定条件下,乙炔还能与H2、其它卤素单质、HX、H2O等发生加成反应,你能写出乙炔与H2 反应的方程式吗?聚氯乙烯在使用的过程中,易发生老化,会变硬、发脆、开裂等,并释放出对人体有害的氯化氢,故不宜使用聚氯乙烯制品直接盛装食物。学贵有用聚氯乙烯是一种合成树脂,可用于制备塑料和合成纤维等。聚氯乙烯可由H2、Cl2和乙炔为原料制取。你能写出有关的反应方程式吗?氯乙烯:提示:吹塑定型的塑料薄膜(2)氧炔焰可用来切割或焊接金属。五、乙炔的用途(1)基本化工原料,可以用来制备氯
乙烯、聚氯乙烯等。1.不能使酸性KMnO4溶液褪色的是 ( )
A.乙烯 B.聚乙烯
C.丙烯 D.乙炔
2.关于炔烃的下列描述正确的是 ( )
A.分子里含有碳碳三键的不饱和链烃叫炔烃
B.炔烃分子里的所有碳原子都在同一直线上
C.炔烃易发生加成反应,也易发生取代反应
D.不能使溴水褪色,但可使酸性高锰酸钾溶液褪色
3.既可以鉴别乙烷和乙炔,又可以除去乙烷中含有的乙炔 的方法是 ( )
A.通人足量的溴水中
B.与足量酸性高锰酸钾溶液反应
C.点燃
D. 在一定条件下与氢气加成BAA自我检测4、所有原子都在同一直线上的是…………( )
A、C2H4 B、C2H2
C、C2H6 D、CO2
5、区别乙烯和乙炔的最简单可行的方法…( )
A、用溴水 B、用酸性KMnO4溶液
C、点燃 D、与H2加成
BC
6、由乙炔为原料制取CHClBr—CH2Br ,下列方法中最可行是
A、先与HBr加成再与HCl加成 B、先与HCl加成再与Br2加成
C、先与Br2加成再与Cl2加成 D、先与Cl2加成再与HBr加成
7、在有催化剂的条件下,将a L乙炔和乙烯的混合气体与足量的
H2 加成,消耗1.25a L H2 ,则乙烯和乙炔的体积比为 ( )
A、1∶1 B、2∶1 C、3∶1 D、4∶18、科学家于1995年合成了一种化学式为C200H200含有多个C≡C (碳碳叁键)的链状烃,其分子中含有C≡C最多是
A.49个 B.50个
C.51个 D.无法确定C10、含一叁键的炔烃,氢化后的产物结构简式为
此炔烃可能有的结构有( )
A、1种 B、2 C、3种 D、4种B11、在标准状况下将11.2升乙烯和乙炔的混合气通入到溴水中充分反应,测得有128克溴参加了反应,测乙烯、乙炔的物质的量之比为( )
A.1∶2 B.2∶3 C.3∶4 D.4∶5 B12、描述CH3—CH = CH—C≡C—CF3分子结构的下列叙述中正确的是( )
A.6个碳原子有可能都在一条直线上
B.6个碳原子不可能都在一条直线上
C.6个碳原子有可能都在同一平面上
D.6个碳原子不可能都在同一平面上 B、C作业:课后习题恳请批评指正谢谢
