实验4-5综合实验设计实践 课件 (2)
文档属性
| 名称 | 实验4-5综合实验设计实践 课件 (2) |  | |
| 格式 | zip | ||
| 文件大小 | 3.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-07-12 22:47:56 | ||
图片预览





文档简介
课件15张PPT。热烈欢迎各位专家、老师
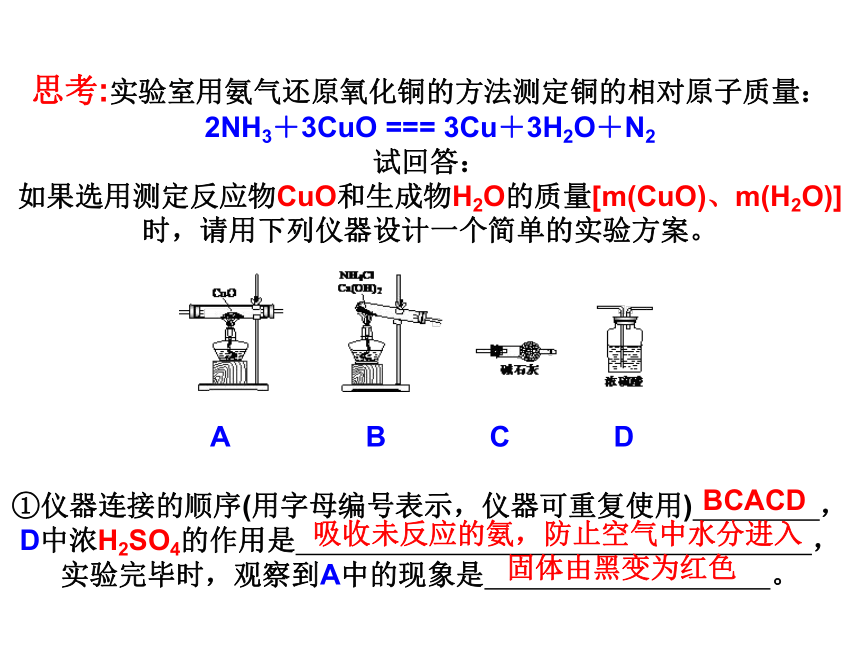
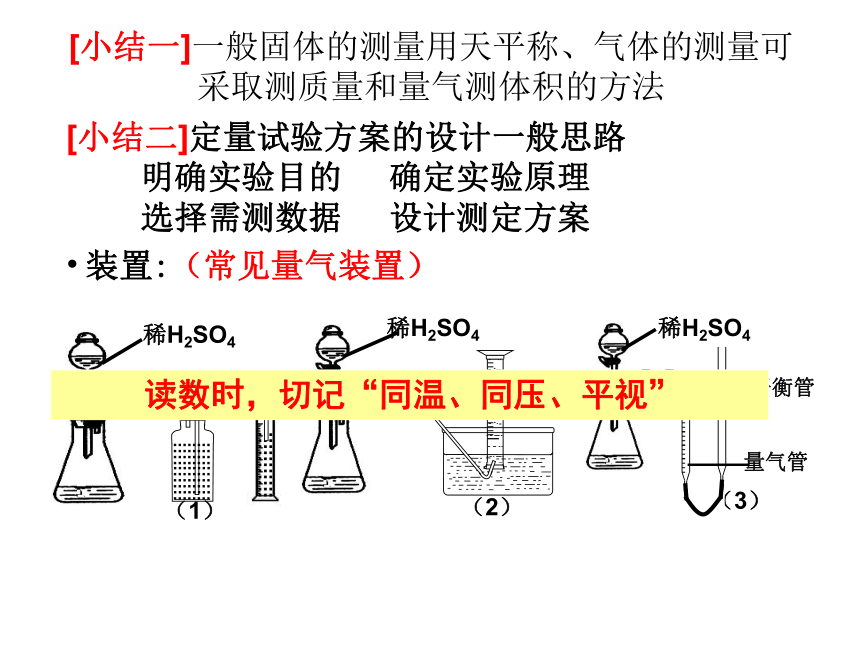
光临指导 化学定量实验既是中学实验复习的重点,也是高考化学命题的热点。认真分析近几年高考试题,定量实验考查方式主要有:4、考查定量实验的基本操作和误差分析 2、考查定量实验方案的设计与评价 1、考查计量仪器的特点和正确使用 3、考查实验数据和实验结果的分析 思考:实验室用氨气还原氧化铜的方法测定铜的相对原子质量: 2NH3+3CuO === 3Cu+3H2O+N2 试回答: 如果选用测定反应物CuO和生成物H2O的质量[m(CuO)、m(H2O)]时,请用下列仪器设计一个简单的实验方案。 ? ? ? ? ? A B C D ? ①仪器连接的顺序(用字母编号表示,仪器可重复使用) ,D中浓H2SO4的作用是 ,实验完毕时,观察到A中的现象是 。 BCACD吸收未反应的氨,防止空气中水分进入固体由黑变为红色 ⑵如果仍采用上述仪器装置,其它方案可选用测定的物理量有 。 A.m(Cu)和m(CuO) B.m(N2)和m(H2O) C.m(Cu)和m(H2O) D.m(NH3)和m(H2O) AC[小结一]一般固体的测量用天平称、气体的测量可采取测质量和量气测体积的方法 装置:(常见量气装置) 读数时,切记“同温、同压、平视”[小结二]定量试验方案的设计一般思路
明确实验目的 确定实验原理
选择需测数据 设计测定方案
如何测定已部分氧化的Na2SO3的纯度?沉淀法气体法滴定法讨论:方案:测定Na2SO3的纯度,你能想出几种方案?方案一:沉淀法 (沉淀SO42-) 原理:结论:Na2SO3样品的质量分数为步骤:2H+ + SO32- = H2O+SO2?
Ba2+ + SO42- = BaSO4?1、为何加入过量的沉淀剂?问题与思考:2、如何判断沉淀是否完全?3、如何洗涤沉淀?4、如何判断沉淀已洗涤干净?
若未洗涤干净,测定结果将 。
(填偏大、偏小、无影响)方案二:气体法( ①测定SO2的质量) 原理: 2H++SO32-=H2O+SO2?步骤:装置:Na2SO3样品的质量分数为结论:1、为了测量结果准确,B中溶液
应采用_______________
饱和NaHSO3溶液2、加入硫酸还是盐酸制取SO2?4、如何改进实验,减
小A中滴加硫酸而引
起的误差?3、若读数时,装置⑶中液面如图所示,所测结果 。
(填偏大、偏小、无影响)
量气法问题与思考:Na2SO3样品的质量分数为方案三:氧化还原滴定法原理:步骤:5SO32-+2MnO4-+6H+ = 5SO42-+2Mn2++3H2O结论:温馨提醒:陷阱:体积的倍数关系?称m1g 样品溶于水配成250mL溶液问题与思考:1、盛KMnO4溶液的滴定管应选 式(酸、碱)滴定管.
理由是 。2、为确定滴定终点,选择何种指示剂,说明理由?3、判断到达滴定终点的实验现象是 。 4、若滴定前俯视刻度,滴定终点时仰视刻度
所测结果将 (填偏大、偏小、无影响)5、如何保证数据的精确度? 实验方案设计的基本要求
科学性
安全性
可行性
简约性 明确实验目的 确定实验原理
(根据物质特性与题设条件) 推敲实验细节
(优化方案减小偶然误差 ) 设计实验方案
(获得实验数据的途径) 定量实验方案的设计与评价常见思路:分析实验数据得出结论 (2011福建) Ⅱ.牙膏样品中碳酸钙的定量测定
利用下图装置进行实验,充分反应后测定C中生成的BaCO3
沉淀质量,以确定碳酸钙的质量分数, 回答下列问题:
(3)实验过程中需持续缓缓通入空气。其作用除了可搅拌
B、C中的反应物外,还有:___________________。
(4)C中反应生成BaCO3的化学方程式是____________ 。
(5)下列措施中,不能提高测定准确度的是 。
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A—B之间增添盛有浓硫酸的洗气装置
d.在B—C之间增添盛有饱和碳酸氢钠溶液的洗气装置谢谢!欢迎批评指正!
光临指导 化学定量实验既是中学实验复习的重点,也是高考化学命题的热点。认真分析近几年高考试题,定量实验考查方式主要有:4、考查定量实验的基本操作和误差分析 2、考查定量实验方案的设计与评价 1、考查计量仪器的特点和正确使用 3、考查实验数据和实验结果的分析 思考:实验室用氨气还原氧化铜的方法测定铜的相对原子质量: 2NH3+3CuO === 3Cu+3H2O+N2 试回答: 如果选用测定反应物CuO和生成物H2O的质量[m(CuO)、m(H2O)]时,请用下列仪器设计一个简单的实验方案。 ? ? ? ? ? A B C D ? ①仪器连接的顺序(用字母编号表示,仪器可重复使用) ,D中浓H2SO4的作用是 ,实验完毕时,观察到A中的现象是 。 BCACD吸收未反应的氨,防止空气中水分进入固体由黑变为红色 ⑵如果仍采用上述仪器装置,其它方案可选用测定的物理量有 。 A.m(Cu)和m(CuO) B.m(N2)和m(H2O) C.m(Cu)和m(H2O) D.m(NH3)和m(H2O) AC[小结一]一般固体的测量用天平称、气体的测量可采取测质量和量气测体积的方法 装置:(常见量气装置) 读数时,切记“同温、同压、平视”[小结二]定量试验方案的设计一般思路
明确实验目的 确定实验原理
选择需测数据 设计测定方案
如何测定已部分氧化的Na2SO3的纯度?沉淀法气体法滴定法讨论:方案:测定Na2SO3的纯度,你能想出几种方案?方案一:沉淀法 (沉淀SO42-) 原理:结论:Na2SO3样品的质量分数为步骤:2H+ + SO32- = H2O+SO2?
Ba2+ + SO42- = BaSO4?1、为何加入过量的沉淀剂?问题与思考:2、如何判断沉淀是否完全?3、如何洗涤沉淀?4、如何判断沉淀已洗涤干净?
若未洗涤干净,测定结果将 。
(填偏大、偏小、无影响)方案二:气体法( ①测定SO2的质量) 原理: 2H++SO32-=H2O+SO2?步骤:装置:Na2SO3样品的质量分数为结论:1、为了测量结果准确,B中溶液
应采用_______________
饱和NaHSO3溶液2、加入硫酸还是盐酸制取SO2?4、如何改进实验,减
小A中滴加硫酸而引
起的误差?3、若读数时,装置⑶中液面如图所示,所测结果 。
(填偏大、偏小、无影响)
量气法问题与思考:Na2SO3样品的质量分数为方案三:氧化还原滴定法原理:步骤:5SO32-+2MnO4-+6H+ = 5SO42-+2Mn2++3H2O结论:温馨提醒:陷阱:体积的倍数关系?称m1g 样品溶于水配成250mL溶液问题与思考:1、盛KMnO4溶液的滴定管应选 式(酸、碱)滴定管.
理由是 。2、为确定滴定终点,选择何种指示剂,说明理由?3、判断到达滴定终点的实验现象是 。 4、若滴定前俯视刻度,滴定终点时仰视刻度
所测结果将 (填偏大、偏小、无影响)5、如何保证数据的精确度? 实验方案设计的基本要求
科学性
安全性
可行性
简约性 明确实验目的 确定实验原理
(根据物质特性与题设条件) 推敲实验细节
(优化方案减小偶然误差 ) 设计实验方案
(获得实验数据的途径) 定量实验方案的设计与评价常见思路:分析实验数据得出结论 (2011福建) Ⅱ.牙膏样品中碳酸钙的定量测定
利用下图装置进行实验,充分反应后测定C中生成的BaCO3
沉淀质量,以确定碳酸钙的质量分数, 回答下列问题:
(3)实验过程中需持续缓缓通入空气。其作用除了可搅拌
B、C中的反应物外,还有:___________________。
(4)C中反应生成BaCO3的化学方程式是____________ 。
(5)下列措施中,不能提高测定准确度的是 。
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A—B之间增添盛有浓硫酸的洗气装置
d.在B—C之间增添盛有饱和碳酸氢钠溶液的洗气装置谢谢!欢迎批评指正!
同课章节目录
- 第一单元 从实验走进化学
- 课题一 实验化学起步
- 实验1-1 蓝瓶子实验
- 课题二 化学实验的绿色追求
- 实验1-2 氯气的生成及其性质的微型实验
- 实验1-3 污水处理--电浮选凝聚法
- 第二单元 物质的获取
- 课题一 物质的分离和提纯
- 实验2-1 纸上层析分离甲基橙和酚酞
- 实验2-2 海水的蒸馏
- 实验2-3 从海带中提取碘
- 课题二 物质的制备
- 实验2-4 硫酸亚铁铵的制备
- 实验2-5 乙酸乙酯的制备及反应条件探究
- 实验2-6 氢氧化铝的制备
- 第三单元 物质的检测
- 课题一 物质的检验
- 实验3-1 几种无机离子的检验
- 实验3-2 几种有机物的检验
- 实验3-3 植物体中某些元素的检验
- 课题二 物质含量的测定
- 实验3-4 酸碱滴定曲线的测绘
- 实验3-5 比色法测定抗贫血药物中铁的含量
- 实验3-6 食醋中总酸量的测定
- 第四单元 研究型实验
- 课题一 物质性质的研究
- 实验4-1 纯净物与混合物性质的比较
- 实验4-2 金属镁、铝、锌化学性质的探究
- 课题二 身边化学问题的探究
- 实验4-3 含氯消毒液性质、作用的探究
- 实验4-4 饮料的研究
