实验3-6 食醋中总酸量的测定 课件(18张)
文档属性
| 名称 | 实验3-6 食醋中总酸量的测定 课件(18张) |

|
|
| 格式 | zip | ||
| 文件大小 | 340.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-07-12 00:00:00 | ||
图片预览






文档简介
课件18张PPT。第三章 物质的检测第二节 物质含量的测定第5课时新课标人教版高中化学课件系列选修6 实验化学食醋中总酸量的测定实验3-6 食醋中总酸量的测定 教学目标:1、掌握中和滴定的实验原理、操作步骤、实验结果和误差分析。
2、学习食醋中总酸量测定的原理、方法和操作技术。
3、进一步规范滴定管、容量瓶的使用,练习中和的基本操作,熟悉液体试样中组分含量的测定方法。
4、体验用化学定量分析方法解决实际问题的过程,培养实事求是的科学态度。 食醋中总酸量的测定回顾:食醋中总酸量的测定1、中和滴定的原理是什么?一般步骤是什么?
用一种已知物质的量浓度的酸(或碱)跟未知浓度的碱(或酸)完全中和,测出二者所用的体积,根据化学方程式中酸和碱完全中和时物质的量的比值,而得出未知浓度的碱(或酸)的物质的量浓度。
一般步骤是:制备标准溶液—滴定管检漏、洗涤、润洗、装液、读数—取一定体积的待测溶液于锥形瓶并加两滴指示剂—用标准液滴定至终点并读数—重复操作两次—用平均值进行计算。2、中和滴定的两个关键问题是什么?①用精确度较高的仪器测定参加反应的酸、碱溶液的体积,正确使用滴定管;
②准确判断反应终点。3、滴定终点如何判断? 当加入最后一滴半滴标准液时,锥形瓶内溶液颜色发生突变,而且在30秒内不退色即达滴定终点。食醋中总酸量的测定实验目标1.认识用NaOH溶液滴定醋酸的反应原理。
2.练习移液管、滴定管的使用方法,初步掌握中和滴
定的基本技能。
3.能通过实验收集有关数据,并正确地加以处理。
4.应用中和滴定法测定食醋的含酸量,体验用化学定
量分析方法解决实际问题的过程。
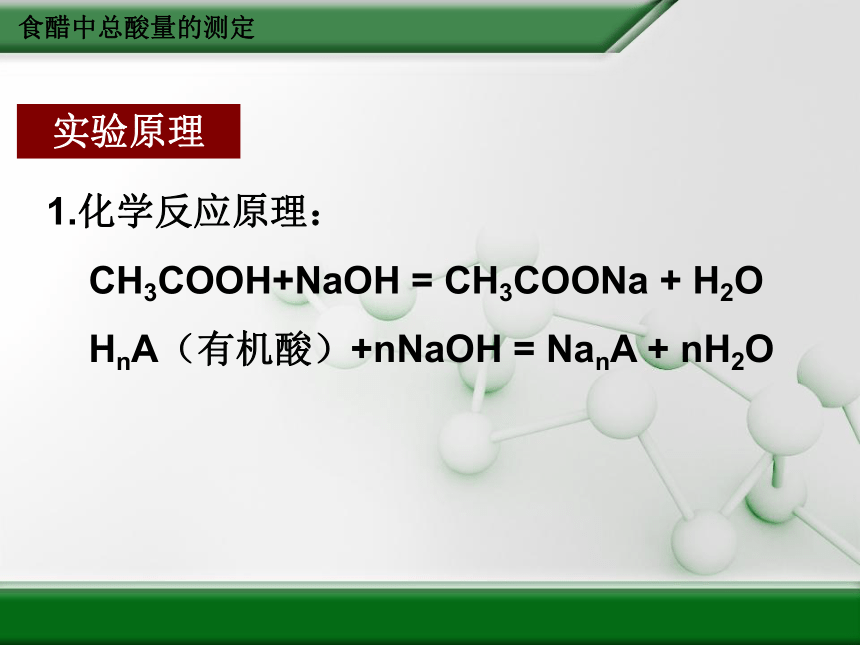
5.养成实事求是的科学态度。食醋中总酸量的测定实验原理 1.化学反应原理:
CH3COOH+NaOH = CH3COONa + H2O
HnA(有机酸)+nNaOH = NanA + nH2O食醋中总酸量的测定*2.NaOH溶液浓度的标定
(1)配制NaOH饱和溶液,放置一段时间后,吸取上 层清液,稀释到约0.1mol/L,即可得NaOH标准溶液。
(2)用邻苯二甲酸氢钾(HOOCC6H4COOK)作为基准物质,以酚酞作为指示剂,标定上述NaOH标准溶液。 m/M = c(NaOH)×V(NaOH) 食醋中总酸量的测定3.实验数据的处理:
m(CH3COOH) = c(NaOH)·V(NaOH)·M(CH3COOH)
100mL食醋中所含醋酸的质量为:
m′(CH3COOH) = c(NaOH)·V(NaOH)·
M(CH3COOH)× ×
根据3次接近的平行测定值,可计算食醋中总酸含量的平均值。食醋中总酸量的测定实验准备实验方案实验方案 仪器的洗涤溶液的装配★NaOH标准溶液配制食醋中总酸量的测定食醋中总酸量测定步骤:食醋中总酸量的测定(1)制备式样和0.10mol/LNaOH标准溶液
(2)滴定管检漏、洗涤、润洗、装液、读数
(3)取20.00毫升式样于250毫升锥形瓶并加两滴酚酞溶液
(4)用标准液滴定至终点并读数
(5)重复操作两次
(6)取平均值计算醋中的总酸量。3.数据处理与结论食醋中总酸量的测定讨论:1、实验中为什么用白醋?若用陈醋要做什么处理? 用白醋便于观察滴定终点颜色的变化。若用陈醋需要用活性炭进行脱色处理,或用PH计判断滴定终点。食醋中总酸量的测定2、为什么要把醋稀释10倍?3、配制NaOH标准溶液和稀释醋的蒸馏水为什么要煮沸2到3分钟?除去溶解的CO2,消去其对实验的影响。食醋中总酸量的测定把待测的醋稀释是防止NaOH标准溶液的用量超过滴定管的总量,稀释10倍则是方便计算。误差分析: 偏大 偏小 偏大 偏大 偏小 偏大 偏大 偏小 偏小食醋中总酸量的测定1.白醋:效果较好
2.香醋:稀释10倍
3.陈醋: 颜色很深注意事项 食醋中总酸量的测定(1)移液管尖嘴残留液体的处理
(2)滴定前后碱式滴定管中不能有气泡
(3)滴定管使用前要用待盛放的溶液润洗
锥形瓶不能用待测液润洗
(4)滴定终点的判断
(5)读数时是否平视几个关健
实验操作
食醋中总酸量的测定Thanks
谢谢您的观看!
2、学习食醋中总酸量测定的原理、方法和操作技术。
3、进一步规范滴定管、容量瓶的使用,练习中和的基本操作,熟悉液体试样中组分含量的测定方法。
4、体验用化学定量分析方法解决实际问题的过程,培养实事求是的科学态度。 食醋中总酸量的测定回顾:食醋中总酸量的测定1、中和滴定的原理是什么?一般步骤是什么?
用一种已知物质的量浓度的酸(或碱)跟未知浓度的碱(或酸)完全中和,测出二者所用的体积,根据化学方程式中酸和碱完全中和时物质的量的比值,而得出未知浓度的碱(或酸)的物质的量浓度。
一般步骤是:制备标准溶液—滴定管检漏、洗涤、润洗、装液、读数—取一定体积的待测溶液于锥形瓶并加两滴指示剂—用标准液滴定至终点并读数—重复操作两次—用平均值进行计算。2、中和滴定的两个关键问题是什么?①用精确度较高的仪器测定参加反应的酸、碱溶液的体积,正确使用滴定管;
②准确判断反应终点。3、滴定终点如何判断? 当加入最后一滴半滴标准液时,锥形瓶内溶液颜色发生突变,而且在30秒内不退色即达滴定终点。食醋中总酸量的测定实验目标1.认识用NaOH溶液滴定醋酸的反应原理。
2.练习移液管、滴定管的使用方法,初步掌握中和滴
定的基本技能。
3.能通过实验收集有关数据,并正确地加以处理。
4.应用中和滴定法测定食醋的含酸量,体验用化学定
量分析方法解决实际问题的过程。
5.养成实事求是的科学态度。食醋中总酸量的测定实验原理 1.化学反应原理:
CH3COOH+NaOH = CH3COONa + H2O
HnA(有机酸)+nNaOH = NanA + nH2O食醋中总酸量的测定*2.NaOH溶液浓度的标定
(1)配制NaOH饱和溶液,放置一段时间后,吸取上 层清液,稀释到约0.1mol/L,即可得NaOH标准溶液。
(2)用邻苯二甲酸氢钾(HOOCC6H4COOK)作为基准物质,以酚酞作为指示剂,标定上述NaOH标准溶液。 m/M = c(NaOH)×V(NaOH) 食醋中总酸量的测定3.实验数据的处理:
m(CH3COOH) = c(NaOH)·V(NaOH)·M(CH3COOH)
100mL食醋中所含醋酸的质量为:
m′(CH3COOH) = c(NaOH)·V(NaOH)·
M(CH3COOH)× ×
根据3次接近的平行测定值,可计算食醋中总酸含量的平均值。食醋中总酸量的测定实验准备实验方案实验方案 仪器的洗涤溶液的装配★NaOH标准溶液配制食醋中总酸量的测定食醋中总酸量测定步骤:食醋中总酸量的测定(1)制备式样和0.10mol/LNaOH标准溶液
(2)滴定管检漏、洗涤、润洗、装液、读数
(3)取20.00毫升式样于250毫升锥形瓶并加两滴酚酞溶液
(4)用标准液滴定至终点并读数
(5)重复操作两次
(6)取平均值计算醋中的总酸量。3.数据处理与结论食醋中总酸量的测定讨论:1、实验中为什么用白醋?若用陈醋要做什么处理? 用白醋便于观察滴定终点颜色的变化。若用陈醋需要用活性炭进行脱色处理,或用PH计判断滴定终点。食醋中总酸量的测定2、为什么要把醋稀释10倍?3、配制NaOH标准溶液和稀释醋的蒸馏水为什么要煮沸2到3分钟?除去溶解的CO2,消去其对实验的影响。食醋中总酸量的测定把待测的醋稀释是防止NaOH标准溶液的用量超过滴定管的总量,稀释10倍则是方便计算。误差分析: 偏大 偏小 偏大 偏大 偏小 偏大 偏大 偏小 偏小食醋中总酸量的测定1.白醋:效果较好
2.香醋:稀释10倍
3.陈醋: 颜色很深注意事项 食醋中总酸量的测定(1)移液管尖嘴残留液体的处理
(2)滴定前后碱式滴定管中不能有气泡
(3)滴定管使用前要用待盛放的溶液润洗
锥形瓶不能用待测液润洗
(4)滴定终点的判断
(5)读数时是否平视几个关健
实验操作
食醋中总酸量的测定Thanks
谢谢您的观看!
同课章节目录
- 第一单元 从实验走进化学
- 课题一 实验化学起步
- 实验1-1 蓝瓶子实验
- 课题二 化学实验的绿色追求
- 实验1-2 氯气的生成及其性质的微型实验
- 实验1-3 污水处理--电浮选凝聚法
- 第二单元 物质的获取
- 课题一 物质的分离和提纯
- 实验2-1 纸上层析分离甲基橙和酚酞
- 实验2-2 海水的蒸馏
- 实验2-3 从海带中提取碘
- 课题二 物质的制备
- 实验2-4 硫酸亚铁铵的制备
- 实验2-5 乙酸乙酯的制备及反应条件探究
- 实验2-6 氢氧化铝的制备
- 第三单元 物质的检测
- 课题一 物质的检验
- 实验3-1 几种无机离子的检验
- 实验3-2 几种有机物的检验
- 实验3-3 植物体中某些元素的检验
- 课题二 物质含量的测定
- 实验3-4 酸碱滴定曲线的测绘
- 实验3-5 比色法测定抗贫血药物中铁的含量
- 实验3-6 食醋中总酸量的测定
- 第四单元 研究型实验
- 课题一 物质性质的研究
- 实验4-1 纯净物与混合物性质的比较
- 实验4-2 金属镁、铝、锌化学性质的探究
- 课题二 身边化学问题的探究
- 实验4-3 含氯消毒液性质、作用的探究
- 实验4-4 饮料的研究
