人教版化学八年级全册课件 3.2 原子的构成 (共47张PPT)
文档属性
| 名称 | 人教版化学八年级全册课件 3.2 原子的构成 (共47张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-07-12 00:00:00 | ||
图片预览




文档简介
课件47张PPT。课题2:原子的构成
近代科学原子论(1803年)一切物质都是由最小的不能再分的粒子——原子构成。
原子模型:原子是坚实的、不可再分的实心球。英国化学家道尔顿
(J.Dalton , 1766~1844)原子并不是构成物质的最小微粒 ——汤姆生发现了电子(1897年)英国物理学家汤姆生
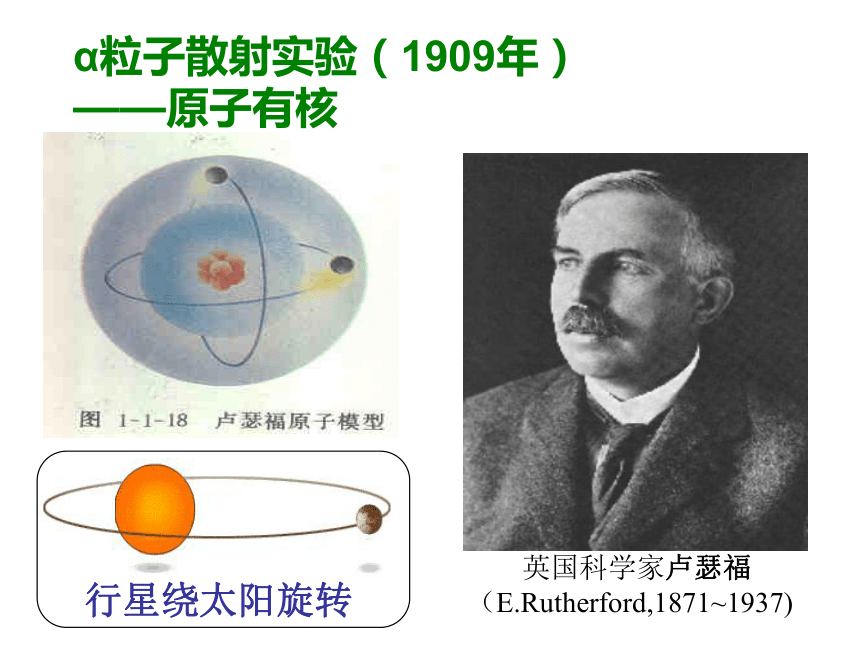
(J.J.Thomson ,1856~1940)α粒子散射实验(1909年) ——原子有核英国科学家卢瑟福
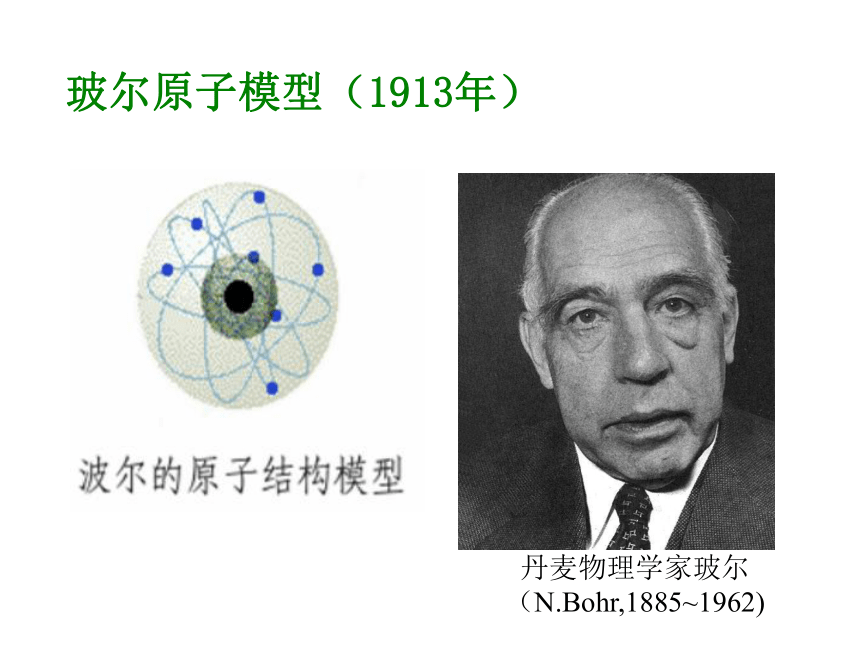
(E.Rutherford,1871~1937) 行星绕太阳旋转玻尔原子模型(1913年)丹麦物理学家玻尔
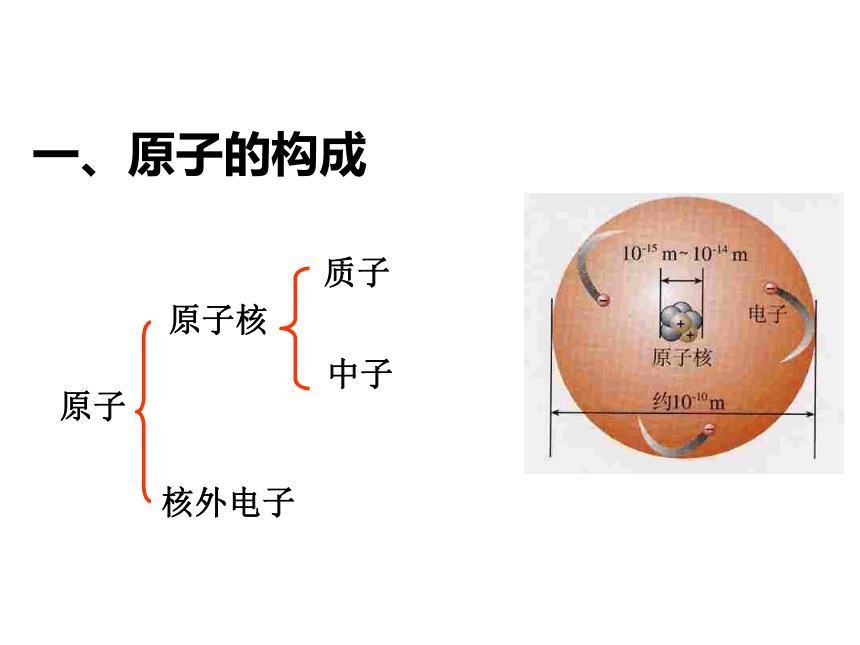
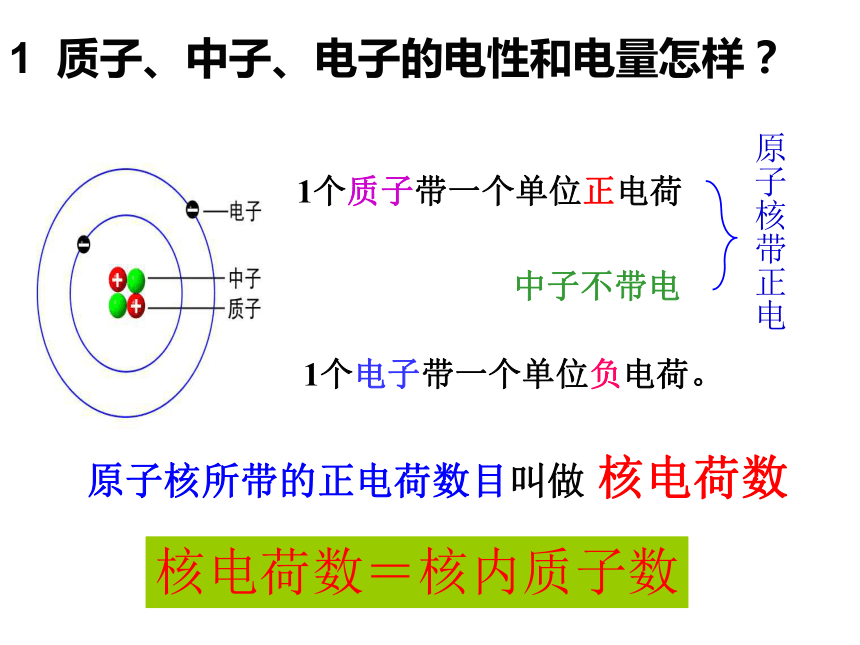
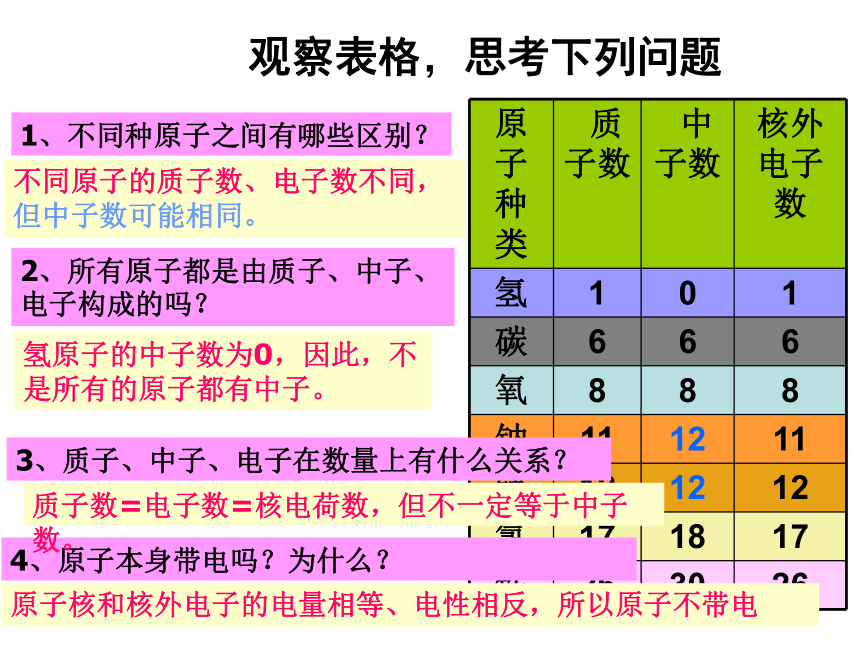
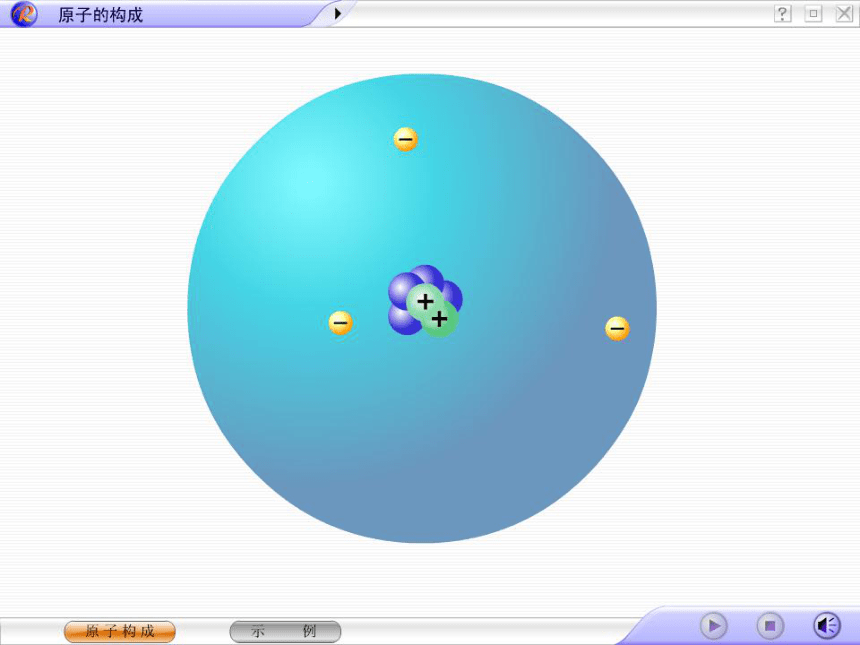
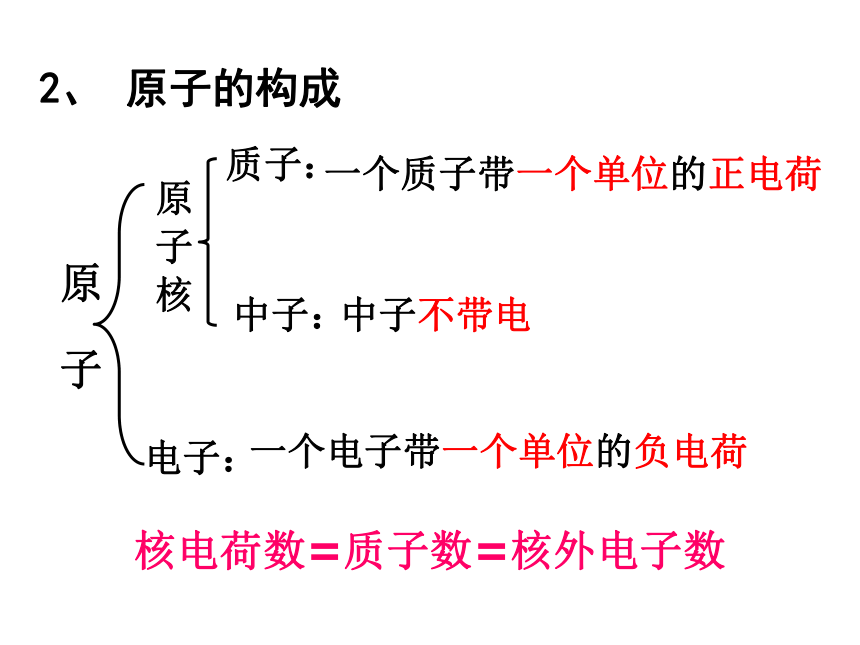
(N.Bohr,1885~1962)原子原子核核外电子质子 中子一、原子的构成1 质子、中子、电子的电性和电量怎样?1个质子带一个单位正电荷1个电子带一个单位负电荷。中子不带电原子核带正电原子核所带的正电荷数目叫做 核电荷数核电荷数=核内质子数观察表格,思考下列问题2、所有原子都是由质子、中子、电子构成的吗?3、质子、中子、电子在数量上有什么关系?1、不同种原子之间有哪些区别?4、原子本身带电吗?为什么?不同原子的质子数、电子数不同,但中子数可能相同。氢原子的中子数为0,因此,不是所有的原子都有中子。 质子数=电子数=核电荷数,但不一定等于中子数。 原子核和核外电子的电量相等、电性相反,所以原子不带电质子:一个质子带一个单位的正电荷中子:中子不带电 电子:一个电子带一个单位的负电荷2、 原子的构成核电荷数=质子数=核外电子数一、下列关于原子的说法正确的是( )
A.原子不显电性是因为原子中不存在带电的粒子
B.原子是由质子和电子构成的,呈电中性
C.原子核都是由质子和中子构成的
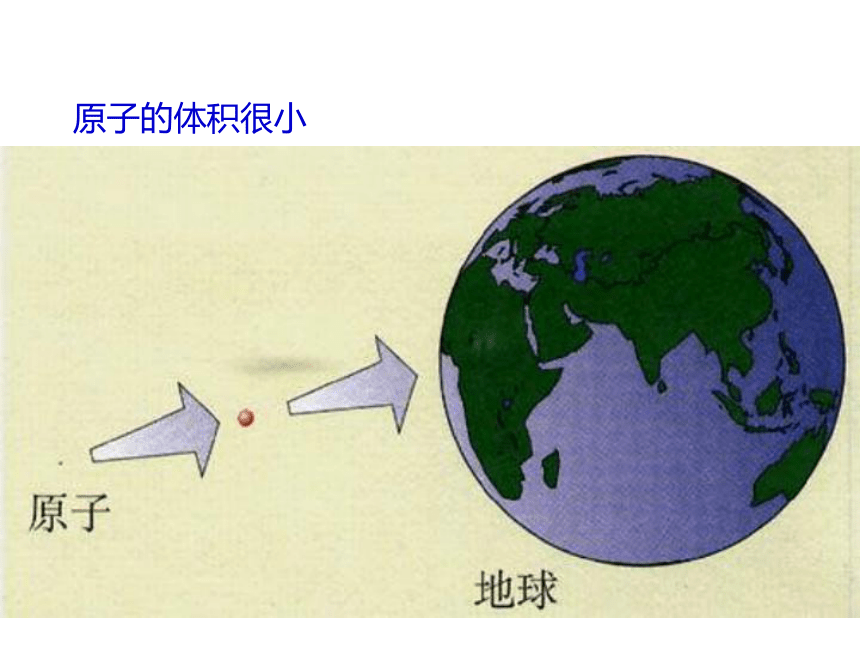
D.原子中原子核内质子数一定等于核外电子数D原子的体积很小 原子核原子原子核比原子小得多 电子在原子核外一定区域内出现,这些区域叫作叫做“电子层”,核外电子是在不同的电子层内运动的,此现象叫做核外电子的分层排布。原子核外电子的运动与排布原子核外电子的运动与排布原子核外电子的运动与排布原子核外电子的运动与排布原子核外电子的运动与排布原子核外电子的运动与排布原子核外电子的运动与排布一、核外电子的排布1、核外电子是分层排布的人们发现原子核外电子,最少的有1层,最多的有7层.电子层 一 二 三 四 五 六 七离核远近:近远能量高低:低高2、原子结构示意图如: 钠原子的结构示意图1、每一电子层上最多排2n2个电子(n为电子层数)。
第一层最多2个电子,第二层最多8个电子。2、最外层上的电子数不能超过8个(只有一个
电子层时不能超过2个)。 原子核核电荷数(质子数)第一电子层第二电子层第三电子层电子层上的电子数带正电Cl: 17Mg: 12O: 8H: 1画出下列原子的结构示意图+11-----------+17-----------------钠原子氯原子质子数=电子数=11质子数=电子数=17不带电不带电NaCl+11+17-----------------钠原子氯原子+17-----------------钠原子氯原子-----------+17-----------------钠原子氯原子+17------------------钠原子氯原子我稳定了我也稳定了,谢谢!钠离子氯离子质子数= 电子数=质子数= 电子数=11101718><带一个单位正电荷带一个单位负电荷Na+Cl-NaCl静电作用形成化合物食盐晶体 NaCl带正电荷的原子叫做阳离子
带负电荷的原子叫做阴离子钠与氯气反应生成氯化钠示意图二、离子的形成1、离子带电的原子2、离子分类 阴离子
阳离子3、离子的表示——离子符号(电子数>质子数)(电子数<质子数)Xn±元素符号离子所带电荷数(得失电子数;当n=1时略去不写 )离子带正或负电+11281+1128质子数核外电子数=质子数核外电子数>+17287+17288NaCl质子数核外电子数=质子数核外电子数<失去一个电子得到一个电子离子的形成阳离子阴离子氯化钠(NaCl)的形成过程分子、原子、离子的比较都是构成物质的粒子,都很小、不停运动、微粒间有间隔在化学变化中不能再分,且种类不变。在化学变化中可以再分且种类改变。带电的微粒分子是由原子构成,分子又可以再分为原子,原子得失电子后变为离子。交流共享 1、下列微粒是阳离子的有( );
是阴离子的有 ( )
是原子的有 ( );
为稳定结构的有 ( )ABCDABCDBCD练一练2、下列原子的电子层排布相同的是 ( )2.3.63.决定元素化学性质的是( )
A质子数 B最外层电子数 C中子数 D原子量
4.同种元素的原子和离子一定具有相同的( )
A核电荷数 B电子层数 C最外层电子数 D带电量
5.根据4种粒子结构示意图,下列说法正确的是( )
①它们都带有电荷 ②它们都具有稳定结构 ③它
们核外电子排布相同 ④它们属于不同种元素
A①② B②③ C②④ D③④
BAC部分稀有气体元素的原子结构示意图相对稳定结构部分金属元素的原子结构示意图钠:镁:铝:锂:部分非金属元素的原子结构示意图碳:磷:硫:氯:三类元素原子最外层电子数目的特点<4个在化学反应中易失去电子≥4个在化学反应中易得到电子不易得失电子8个(He为2个)总结:元素的性质,特别是化学性质,跟它的原
子的 关系密切。
最外层电子数 2、下列具有相似化学性质的元素组别 是: 。ABCDCD3.某元素原子核外有3个电子层,最外层上有1个电
子,该元素的核电荷数为 ( )
A 5 B 11 C 1 D 18B课后作业:1、将①分子②原子③质子④中子⑤电子⑥离子等粒子用序号分别填 入下列适当空格中:
(1)构成物质的基本粒子是________________
(2)构成原子的基本粒子是________________
(3)显示电中性的粒子是________________
(4)带正电的粒子是________________
(5)参加化学反应一定发生变化的粒子是____________
(6)原子中数目一定相等的粒子是_______________
挑战自我1、将①分子②原子③质子④中子⑤电子⑥离子等粒子用序号分别填 入下列适当空格中:
(1)构成物质的基本粒子是________________
(2)构成原子的基本粒子是________________
(3)显示电中性的粒子是________________
(4)带正电的粒子是________________
(5)参加化学反应一定发生变化的粒子是____________
(6)原子中数目一定相等的粒子是_______________
①②⑥③④⑤①②④③①③⑤
原子模型:原子是坚实的、不可再分的实心球。英国化学家道尔顿
(J.Dalton , 1766~1844)原子并不是构成物质的最小微粒 ——汤姆生发现了电子(1897年)英国物理学家汤姆生
(J.J.Thomson ,1856~1940)α粒子散射实验(1909年) ——原子有核英国科学家卢瑟福
(E.Rutherford,1871~1937) 行星绕太阳旋转玻尔原子模型(1913年)丹麦物理学家玻尔
(N.Bohr,1885~1962)原子原子核核外电子质子 中子一、原子的构成1 质子、中子、电子的电性和电量怎样?1个质子带一个单位正电荷1个电子带一个单位负电荷。中子不带电原子核带正电原子核所带的正电荷数目叫做 核电荷数核电荷数=核内质子数观察表格,思考下列问题2、所有原子都是由质子、中子、电子构成的吗?3、质子、中子、电子在数量上有什么关系?1、不同种原子之间有哪些区别?4、原子本身带电吗?为什么?不同原子的质子数、电子数不同,但中子数可能相同。氢原子的中子数为0,因此,不是所有的原子都有中子。 质子数=电子数=核电荷数,但不一定等于中子数。 原子核和核外电子的电量相等、电性相反,所以原子不带电质子:一个质子带一个单位的正电荷中子:中子不带电 电子:一个电子带一个单位的负电荷2、 原子的构成核电荷数=质子数=核外电子数一、下列关于原子的说法正确的是( )
A.原子不显电性是因为原子中不存在带电的粒子
B.原子是由质子和电子构成的,呈电中性
C.原子核都是由质子和中子构成的
D.原子中原子核内质子数一定等于核外电子数D原子的体积很小 原子核原子原子核比原子小得多 电子在原子核外一定区域内出现,这些区域叫作叫做“电子层”,核外电子是在不同的电子层内运动的,此现象叫做核外电子的分层排布。原子核外电子的运动与排布原子核外电子的运动与排布原子核外电子的运动与排布原子核外电子的运动与排布原子核外电子的运动与排布原子核外电子的运动与排布原子核外电子的运动与排布一、核外电子的排布1、核外电子是分层排布的人们发现原子核外电子,最少的有1层,最多的有7层.电子层 一 二 三 四 五 六 七离核远近:近远能量高低:低高2、原子结构示意图如: 钠原子的结构示意图1、每一电子层上最多排2n2个电子(n为电子层数)。
第一层最多2个电子,第二层最多8个电子。2、最外层上的电子数不能超过8个(只有一个
电子层时不能超过2个)。 原子核核电荷数(质子数)第一电子层第二电子层第三电子层电子层上的电子数带正电Cl: 17Mg: 12O: 8H: 1画出下列原子的结构示意图+11-----------+17-----------------钠原子氯原子质子数=电子数=11质子数=电子数=17不带电不带电NaCl+11+17-----------------钠原子氯原子+17-----------------钠原子氯原子-----------+17-----------------钠原子氯原子+17------------------钠原子氯原子我稳定了我也稳定了,谢谢!钠离子氯离子质子数= 电子数=质子数= 电子数=11101718><带一个单位正电荷带一个单位负电荷Na+Cl-NaCl静电作用形成化合物食盐晶体 NaCl带正电荷的原子叫做阳离子
带负电荷的原子叫做阴离子钠与氯气反应生成氯化钠示意图二、离子的形成1、离子带电的原子2、离子分类 阴离子
阳离子3、离子的表示——离子符号(电子数>质子数)(电子数<质子数)Xn±元素符号离子所带电荷数(得失电子数;当n=1时略去不写 )离子带正或负电+11281+1128质子数核外电子数=质子数核外电子数>+17287+17288NaCl质子数核外电子数=质子数核外电子数<失去一个电子得到一个电子离子的形成阳离子阴离子氯化钠(NaCl)的形成过程分子、原子、离子的比较都是构成物质的粒子,都很小、不停运动、微粒间有间隔在化学变化中不能再分,且种类不变。在化学变化中可以再分且种类改变。带电的微粒分子是由原子构成,分子又可以再分为原子,原子得失电子后变为离子。交流共享 1、下列微粒是阳离子的有( );
是阴离子的有 ( )
是原子的有 ( );
为稳定结构的有 ( )ABCDABCDBCD练一练2、下列原子的电子层排布相同的是 ( )2.3.63.决定元素化学性质的是( )
A质子数 B最外层电子数 C中子数 D原子量
4.同种元素的原子和离子一定具有相同的( )
A核电荷数 B电子层数 C最外层电子数 D带电量
5.根据4种粒子结构示意图,下列说法正确的是( )
①它们都带有电荷 ②它们都具有稳定结构 ③它
们核外电子排布相同 ④它们属于不同种元素
A①② B②③ C②④ D③④
BAC部分稀有气体元素的原子结构示意图相对稳定结构部分金属元素的原子结构示意图钠:镁:铝:锂:部分非金属元素的原子结构示意图碳:磷:硫:氯:三类元素原子最外层电子数目的特点<4个在化学反应中易失去电子≥4个在化学反应中易得到电子不易得失电子8个(He为2个)总结:元素的性质,特别是化学性质,跟它的原
子的 关系密切。
最外层电子数 2、下列具有相似化学性质的元素组别 是: 。ABCDCD3.某元素原子核外有3个电子层,最外层上有1个电
子,该元素的核电荷数为 ( )
A 5 B 11 C 1 D 18B课后作业:1、将①分子②原子③质子④中子⑤电子⑥离子等粒子用序号分别填 入下列适当空格中:
(1)构成物质的基本粒子是________________
(2)构成原子的基本粒子是________________
(3)显示电中性的粒子是________________
(4)带正电的粒子是________________
(5)参加化学反应一定发生变化的粒子是____________
(6)原子中数目一定相等的粒子是_______________
挑战自我1、将①分子②原子③质子④中子⑤电子⑥离子等粒子用序号分别填 入下列适当空格中:
(1)构成物质的基本粒子是________________
(2)构成原子的基本粒子是________________
(3)显示电中性的粒子是________________
(4)带正电的粒子是________________
(5)参加化学反应一定发生变化的粒子是____________
(6)原子中数目一定相等的粒子是_______________
①②⑥③④⑤①②④③①③⑤
同课章节目录
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的构成
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题1 质量守恒定律
- 课题2 如何正确书写化学方程式
- 课题3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动3 燃烧的条件
- 旧版目录
- 第五单元 物质组成的表示
- 课题2 燃料和热量
- 课题3 使用燃料对环境的影响
