2016江西省九江市中考化学试卷分析
图片预览







文档简介
课件57张PPT。 2016年江西省九江市
中考化学试卷分析
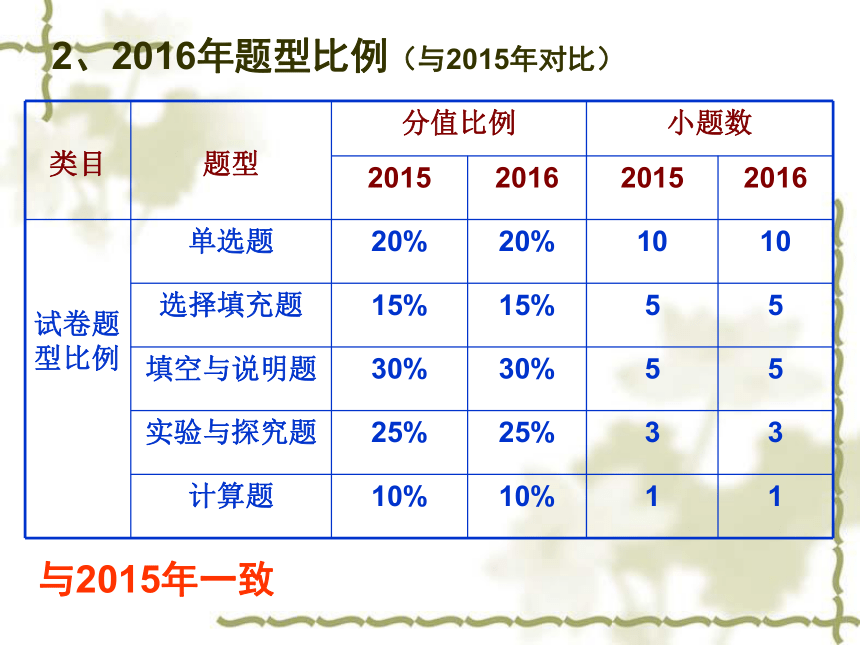
题型:单项选择题、选择填充题、填空与说明题、实验与探究题、计算题1、试卷结构:
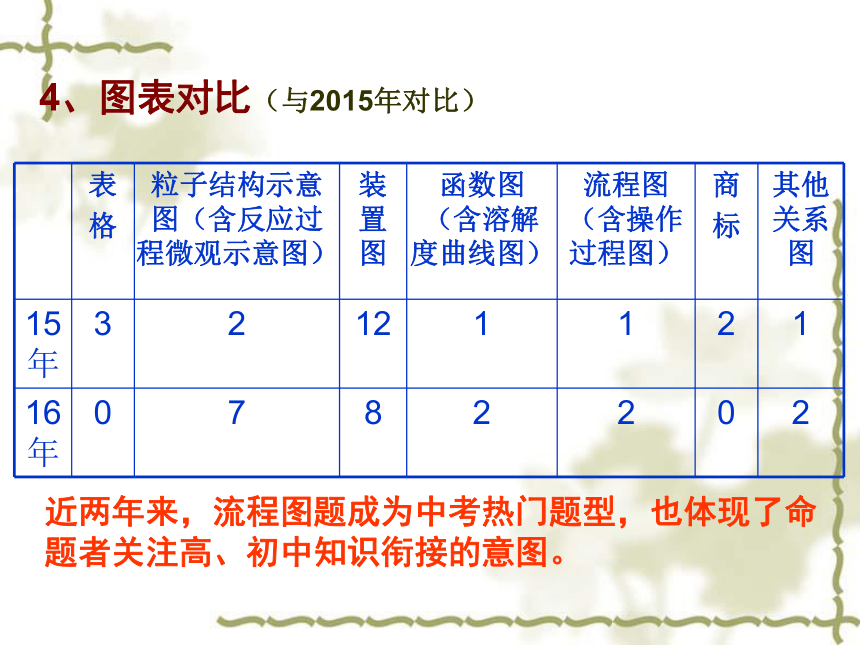
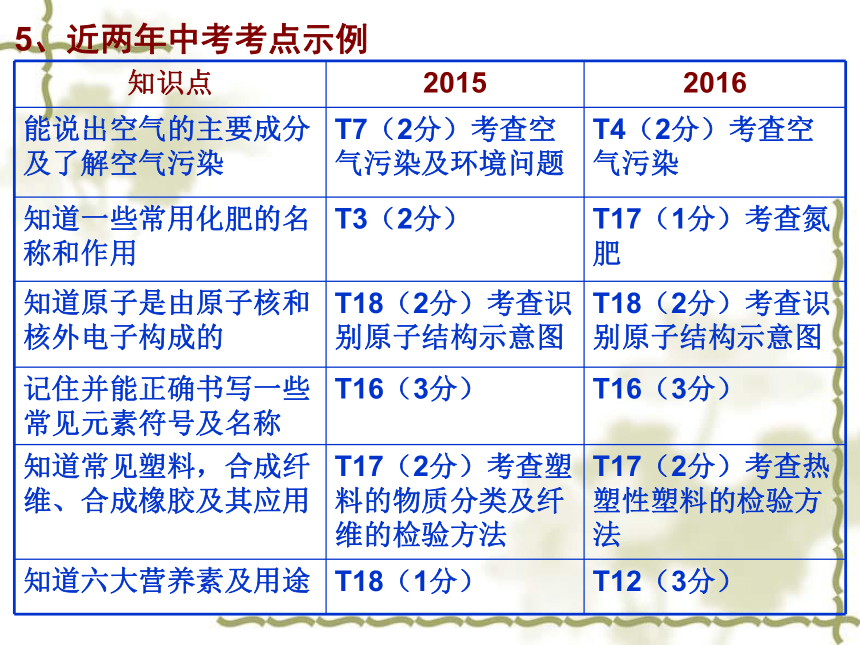
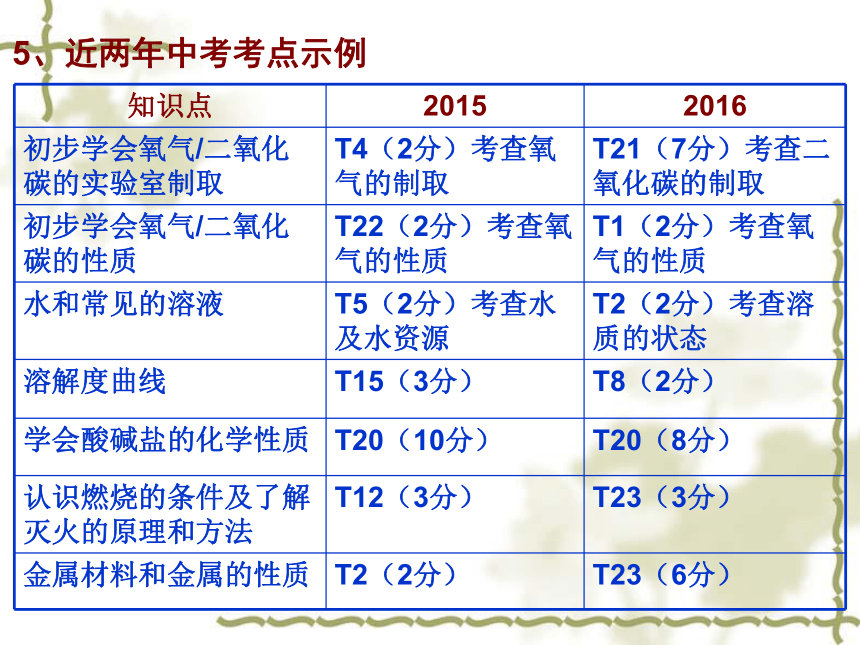
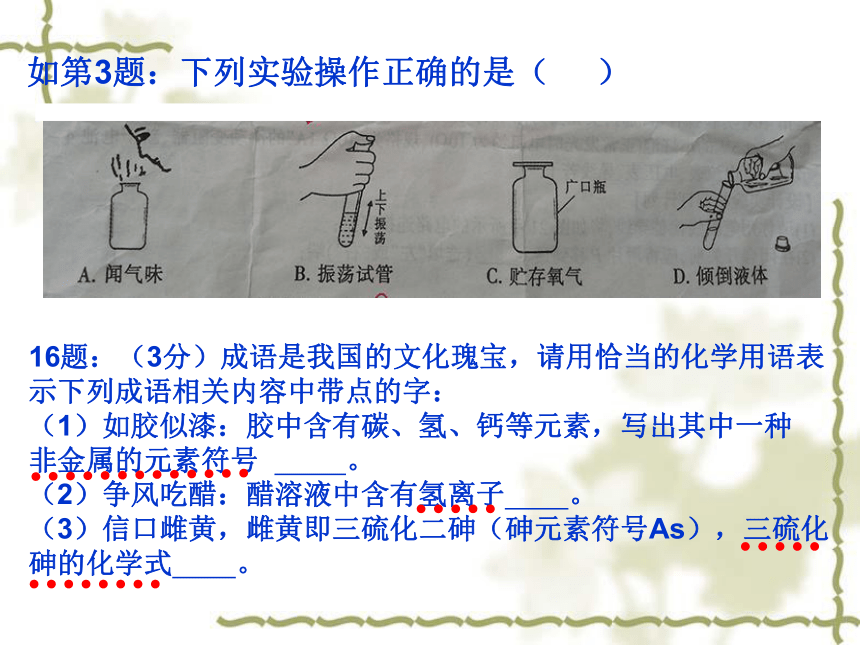
试题满分:100分,考试时间:70分钟,试卷版面:16开5面一、试题概况2、2016年题型比例(与2015年对比)与2015年一致3、试题内容分布及占分比例(与2015年对比) 4、图表对比(与2015年对比)近两年来,流程图题成为中考热门题型,也体现了命题者关注高、初中知识衔接的意图。5、近两年中考考点示例5、近两年中考考点示例二、试题主要特点 2016年江西省中考化学试卷在2015年的基础上稳中求变、变中求新。试卷中知识点覆盖面广,侧重考查对最基础的化学知识和技能的掌握情况,与课本和新课程标准紧密结合,以生产、生活、科技的知识设置情境,难度适中,突出化学核心观念和主干知识的考查,充分体现了《义务教育化学课程标准》中对化学学科思想和学科方法的最新要求,具体表现在以下几个方面:1、注重基础,体现了面向全体学生的理念 知识点覆盖面广,难度适中。 如第1题考查氧气的检验方法;第3题考查闻气体气味、液体的取用、气体的贮存、仪器的洗涤等实验基本操作;第12题考察营养素;第13题考查化学式的相关计算;第16题考查化学用语;第17题考察化石燃料、化学肥料;第18题考察元素周期表的信息识别、原子结构示意图等均源自教材。如第3题:下列实验操作正确的是( ) (1)更加突出了对学生思维能力的考察2、突出主干,体现了考察学生能力例如:第22题【反思与交流】(1)乙组同学认真分析甲组实验后,一致认为不需要通过实验就能判断猜2不成立,理由是甲组实验中也有硫酸钠生成等;
例如第19题(3):
4KOH+2MnO2+O2===2K2MnO4+2H2O
这个方程式要理解质量守恒定律才能完成的。(2)2016年中考化学试卷上没有出现大量需要记忆的化学方程式,而是出现了一些需要通过思考的化学方程式的书写。例如第23题:2Al+3ZnCl2=3Zn+2AlCl3也是要理解置换反应的本质才能完成的。(3)图表结合,考察学生获取信息的能力2016年中考图表多达21个。 考察学生对溶解度曲线、元素及原子结构、物质发生化学反应的微观过程、化学实验基本操作、物质间的相互转化、实验室中制取二氧化碳、常见酸碱盐的化学性质、溶液的酸碱性等知识的理解及实验分析和处理能力。3、注重实验,体现了化学学科的特点 实验能力的考察内容有:闻气体气味、液体的取用、气体的贮存、仪器的洗涤等实验基本操作;二氧化碳的制取和干燥;物质的分离;物质的鉴别;除杂;灭火的方法等内容,共计21分。 考查学生实验方法(包括操作、现象描述)选择;实验仪器或装置选择及理由;实验分析等4、关注社会,体现了化学的应用性 2016年中考化学试卷中有9道题紧密联系生产生活实际,分值高达41分,内容涉及物质的用途、能源和资源的开发利用、化学与科技、化学与工业、化学与农业、化学与医药学、化学与材料、化学与文学、社会热点问题、化学与健康问题、化学与环境问题等多个方面,较好的体现了化学知识的实用性原则。 如第17题:(6分)化学是造福人类的科学。
(1) 能源化学——使用新能源汽车可节约化石燃料。化石燃料包括煤、天然气和 。
(2)农业化学——化肥对提高农作物产量具有重要作用。尿素[CO(NH2)2]属于 (填氮、磷或钾)肥;
(3)医药化学——我国药学家屠呦呦因研制抗疟新药青蒿素获得诺贝尔奖。由青蒿酸(C15H22O2)合成青蒿素(C15H22O5)的过程中主要发生了 (填物理或化学)变化;
(4)材料化学——为防止食物变质常采用真空包装,目的是隔绝 ;检验塑料包装袋是否为热塑性塑料的方法(包括操作和现象) 。试题综合评述(单选题不计在内)难度适中,梯级分布,结构合理。三、九江市份试卷统计
1、九江市2016年中考化学各分数段分布情况2、2016年中考化学试题难度(P)结果统计2、2016年中考化学试题难度(P)结果统计(表5)2、2016年中考化学试题难度(P)结果统计目前均分:47.5(除单选题外)
2016年中考化学预计难度系数为0.6左右四、学生答题情况统计
学生答题常见错误汇总表(表6) T11:下列物质属于混合物的是( A )
A、锰钢 B、红磷 C、硝酸钾 D、
T12:下列基本营养素中能给人体提供能量的是( C )
A、水 B、维生素 C、油脂 D、
T13:南昌汉代海昏候墓出土的文物中,保存完好的玉器非常罕见。对玉石主要成份(化学式为NaAlSi2O6 )的描述正确的是( B )
A、含有3个氧分子
B、钠元素与铝元素的质量比为23:27
C、钠元素的质量分数为13.4%
D、
T14:下列实验方案能达到预期目的的是( C )
A、向盐酸和氯化钙的混合溶液中逐滴加入碳酸钾溶液
B、实验室中用一氧化碳还原氧化铁
C、加热氯酸钾和二氧化锰的混合物
D、往氢氧化钙溶液中逐滴加入物质X的溶液,则物质X
可能为 T15:下列实验方案能达到预期目的的是( B )
A、分离食盐和泥沙——蒸发结晶
B、除去氧化钙中的碳酸钙——高温煅烧
C、检验露置于空气中的氢氧化钠溶液是否变
质——滴入无色酚酞溶液
D、鉴别氯化钠固体和硝酸铵固体—— +-T17:(6分)化学是造福人类的科学。
(1) 能源化学——使用新能源汽车可节约化石燃料。化石燃料包括煤、天然气和 石油。
(2)农业化学——化肥对提高农作物产量具有重要作用。尿素[CO(NH2)2]属于氮(填氮、磷或钾)肥;
(3)医药化学——我国药学家屠呦呦因研制抗疟新药青蒿素获得诺贝尔奖。由青蒿酸(C15H22O2)合成青蒿素(C15H22O5)的过程中主要发生了 化学(填物理或化学)变化;
(4)材料化学——为防止食物变质常采用真空包装,目的是隔绝氧气(空气);检验塑料包装袋是否为热塑性塑料的方法(包括操作和现象)取样加热后是否熔化,冷却后是否凝固。T18:(7分)南昌大家研发的“硅衬底高光效GaN基蓝色发光二极管技术”获得2015年国家技术发明一等奖。请回答下列问题:
(1) 右图是镓在元素周期表中的信息以及原子结构示意图。镓的相对原子质量为 69.72,下列原子结构示意图所对应的元素与镓元素的化学性质相似的是B(填序号);
(2)氮化镓(GaN)中镓元素的化合价为
+3价,则氮元素的化合价为-3价;
(3)传统制备氮化镓的化学原理是:
GaCl3+NH3===GaN+3X其中X的化学式为HCl一定条件Ga
镓
69.72T19:(6分)高锰酸钾是常用的氧化剂。下图是实验室模拟工业上制备高锰酸钾晶体的操作流程:
(1)完成操作 3所需要的玻璃仪器是烧杯(玻璃棒或漏斗)( 填一种即可);实验中通过操作2析出高锰酸钾晶体,说明高锰酸钾的溶解度随温度的升高而增大;
(2)操作流程中可循环利用的物质是二氧化锰;
(3)氢氧化钾、二氧化锰和氧气在高温条件下煅烧,生成锰酸钾和水,该反应的化学方程式为: 4KOH+2MnO2+O2===2K2MnO4+2H2O高温T19T20:(8分)赣南的客家围屋如同城堡,
可以抵御外敌入侵。现在五种物质盐酸、
硫酸、氢氧化钠、氯化钡和碳酸钠作为围
屋的守护“卫士”,只有相邻物质之间能发
生反应才能组成守护的防线(如右图所示
)。其中物质A常用于铅酸蓄电池中,其
浓溶液有脱水性;物质C是人体胃液中的
主要成分。(提示:碳酸钡不溶液于水)
(1)A物质是H2SO4;
(2)B与C反应的化学方程式为:NaOH+HCl=NaCl+H2O,A与E反应的实验现象是生成白色沉淀;
(3)现在下列物质作为“外敌”分别对围屋发起进攻,若该物质与两位相邻的守护“卫士”都能发生反应才能攻破防线,那么能攻入围屋的物质是4(填序号)
1、铁 2、氧化铁 3、二氧化碳 4、氢氧化钡T20T21:(8分)请你根据下图回答有关问题T22:(8分)下图是两个实验小组分别进行“加热硫酸铜和氢氧化钠溶液反应后生成物”的实验过程示意图:
【甲组】氢氧化钠与硫酸铜反应的化学方程式为2NaOH+CuSO4=Na2SO4+Cu(OH)2 ,加热后产生黑色的氧化铜。
【乙组】为寻找实验中没有产生氧化铜的原因,他们进行了以下实验探究:
【查阅资料】在酸性条件下,氢氧化钠与硫酸铜在溶液中可发生如下反应:6NaOH+4CuSO4=3Na2SO4+Cu4(OH)6SO4 ,生成的碱式硫酸铜是不溶于水的蓝白色固体,加热不易发生分解。
【提出猜想】根据资料分析,同学们针对试管中溶液呈酸性的原因作出以下猜想:
猜想1.硫酸铜溶液呈酸性; 猜想2.生成的硫酸钠使溶液呈酸性。
【实验与结论】
实验①:用pH试纸测定硫酸铜溶液的酸碱度,得出其pH〈 (填〉、〈或=)7,硫酸铜溶液呈酸性,猜想1成立。
实验②:向盛有硫酸钠溶液的试管中滴加石蕊溶液,观察到溶液显紫色,硫酸钠溶液呈
中(填酸、中或碱)性,猜想2不成立。
【交流与反思】(1)乙组同学认真分析甲组实验后,一致认为不需要通过实验就能判断猜2不成立,理由是甲组实验中也有硫酸钠生成等;
(2)在化学反应中,相同的反应物因其质量比不同可能会导致生成物不同,请另举一例木炭和氧气 (写出反应物即可)。T22T23:(9分)央视频道《是真的吗?》栏目中有一段视频:将“锡纸”剪成一段两头宽中间窄的纸条,然后两头分别连接电池的正负极,观察到“锡纸”立即燃烧。据此,小晟同学取某种“锡纸”进行了以下探究:
(1)“锡纸”燃烧的原因:“锡纸”两端接入电池两极后造成短路致使“锡纸”燃烧,从燃烧的条件分析:开始“锡纸”不燃烧但短路却能燃烧的原因是温度达到
着火点(填 “与氧气接触”或“温度达到着火点”)。
(2)探究“锡纸”中金属的成分:“锡纸”中的金属是锡吗?
【查阅资料】 ① ‘锡纸”是锡箔或铝箔和纸粘合而成; ②锌粉是一种深灰色固体;③锡(Sn)与酸或盐溶液反应生成正二价的锡盐
【提出猜想】猜想1. “锡纸”中的金属是锡; 猜想2. “锡纸”中的金属是铝。
【进行实验】设计方案并进行实验
【交流讨论】 ① 实验中打磨“锡纸”目的是除去表面氧化物等;
②下列物质的溶液可以替代氯化锌溶液完成上述实验的是D(填序号)。
A、氯化铜 B、硝酸银 C、硫酸钠 D、硫酸亚铁
【拓展应用】电器短路会引起火灾,我们要严加防范。如果电器着火应该采取的灭火方法是切断电源后用干粉灭火器(或二氧化碳灭火器)灭火等 。T23T24:(10分)小新用20g含碳酸钠53%的天然碱制取氢氧化钠用于制作“叶脉书签”(杂质不参加反应)。操作过程如下:
(1)20g样品中碳酸钠的质量为 g;
(2)反应后所得滤液中氢氧化钠的质量分数为多少?(写出计算过程)
(3)将200g滤液浓缩成制作“叶脉书签”所需要质量分数为10%的氢氧化钠溶液,需蒸发水 g.五、错误归类及教学建议汇总1、化学用语书写不熟练不规范
例如:第16、18(3)、19(3)、20(2)、21(2)、22(第1空)、23表格(第2空)、24题都是考察化学用语的知识,共有16分。教学建议:教师在平时教学中,对化学用语的教学要采取新颖而有效的训练方法,不能再用机械而又枯燥的学习方法,要最大限度的调动全体学生学习化学用语的兴趣。这样才能又牢又好的学好化学用语。例如打破教材顺序,提前学习元素符号;每学期举行一到两次化学用语比赛等五、错误归类及教学建议汇总2、双基掌握不扎实,基本概念混淆不清
学生对常见物质的组成、结构、性质、用途、俗称记忆不清,出现混淆;仪器名称、化学概念等基本化学术语书写不正确。例如:第11题“混合物”与“化合物”;12题“营养素”与“营养物质”;第19(1)题 把“漏斗”写成“长颈漏斗”或“分液漏斗”。教学建议:重视基础知识的教学,对于化学概念更要注重理解性的教学,对于易混淆的化学概念应进行对比式教学,使学生在头脑中形成清晰的概念。五、错误归类及教学建议汇总3、文字表达能力欠缺
例如:不能用简明准确的化学语言来表述有关概念、规律、现象、实验过程等一系列的化学问题,文字表述时关键词(字)出现错误或不完整等。20题(2)“有白色沉淀生成”写成“有沉淀生成”。教学建议:化学教师在教学过程中要注意自身规范语言描述,注重对学生进行相关描述性语言的训练,例如:要在课堂上多提问,对学生作业中的文字表述精批细改,对实验设计、物质分离、物质鉴别等可进行模仿性表达训练。在讲评作业中多强调答题要注意规范性,尽可能使语言文字表达做到准确、精炼。五、错误归类及教学建议汇总4、审题能力及获取信息能力欠缺
审题马虎;不能准确理解题意; 审题时不能将题目中的陌生情景读懂、读透,挖掘出情景中的隐含条件;不能很好的将试题中的情景与学过的知识进行关联;不能将题中的信息和需要解决的问题结合起来进行分析;不能将所学知识与生活经验、劳动经验和社会热点问题联合起来。19题完成操作3所需要的玻璃仪器是 。有的学生没注意到“玻璃仪器”四个字,填“滤纸”。23题【交流讨论】②下列物质的溶液可以替代氯化锌溶液完成上述实验的是 (填序号)。A、氯化铜 B、硝酸银 C、硫酸钠D、硫酸亚铁,有的学生理解成能与铝发生置换反应的就行,于是多选了A和B。
教学建议:让学生学会审题。在认真读题的同时用笔在关键词下面圈点标记,养成自我提示的好习惯。平时在课堂上多举学生的错例,让他们自己分析原因,属于审题不清的予以强调,让学生意识到“磨刀不误砍柴工”。
五、错误归类及教学建议汇总5、实验能力和实验探究能力的欠缺
在大多数学校,教师做演示实验多,学生分组实验少,课外学生独立做探究实验的就更少。学生缺乏对实验过程的体验,更谈不上实验的技能技巧,对实验仪器、操作方法不熟悉。
教学建议:加强实验教学,但要杜绝在黑板上讲实验、在练习中做实验。要通过一些探究性的实验培养学生的实验设计能力、创新思维品质。老师要多鼓励学生对实验中遇到的异常现象进行分析、假设、实验探究,得出结论。我们在教学过程中对于实验探究题自始至终都要予以特别的关注,而不应等到中考复习时才加以关注。五、错误归类及教学建议汇总6、错别字、简单计算错误严重
例如:17题(4)熔化写成“融化”、“溶化”、“溶解”。23题“灭火器”写“灭火气”、“灭火剂”。24题氢氧化钠的相对分子质量计算错误,百分数的小数点出错。
教学建议:在平常教学过程中也要注重培养学生其他方面的能力,如严格要求学生书写工整;强化错别字的矫正;计算的准确,不要在考试中因为这些小问题而失分。五、错误归类及教学建议汇总7、学生的学习态度不端正,存在厌学情绪。
具体表现为:部分学生在胡乱涂完选择题的答题卡后,填空部分就一个也不做,即使是简简单单的题目也不动笔,看都懒得去看。本来一些送分的题目也没办法送到这样的学生手中。说明这样的学生处于一种完全放弃学习的状态,这可能是致使中考化学低分率越来越高的主要原因之一。
教学建议:在平时教学中要关注学生的学习兴趣的激发和保持,在开始学习化学时大多数学生还是抱有很大的学习热情和兴趣,但有些学生无法保持长久,于是出现“三天新鲜”甚至到了下半学期成绩大幅下降的情况。在教学中要利用化学学学科实验多的优势,从各方面调动学生学习化学的兴趣。
在教学中要关注后进生,防止出现大面积级低分数。六、试题对今后中考复习的启示我校2016年中考化学学科复习情况1、中考复习时间:4月14日—6月14日
3、复习方法:单元复习与分块复习相结合
争取一轮复习完
2、复习依据:课本上下册、新课标、中考说明、《新评价》、省中考模拟试卷(6套)、金太阳卷(后3套)等4、考查复习效果方式:月考(两次)
本校老师自主命题,按中考考试要求进行测试
六、试题对今后中考复习的启示1、关注中考说明中的考点
2、关注难度变化六、试题对今后中考复习的启示3、注重“双基”的复习,基础知识是考查的重点。常考查的基础知识和主干知识有:
(1)涉及的主要16种物质的性质和用途
二种酸(HCl和H2SO4),二种碱NaOH和[Ca(0H)2],
四种单质(C、H2、O2、Fe),四种氧化物(CO、CO2、H2O、CuO),四种盐(NaCl、Na2CO3、CaCO3、CuSO4)
(2)涉及到的常见概念及知识:物理变化、化学变化、质量守恒定律、化学用语、溶解度曲线、燃烧与灭火、铁生锈、常见方程式书写
(3)常见气体的制备,常用仪器的名称、用途和基本操作
(4)与相对分子质量和溶液配制有关的计算,与方程式和质量分数有关的计算六、试题对今后中考复习的启示4、关注元素化合物
元素化合物作为化学课程的骨架,承载了化学概念和理论、化学计算和化学实验的相关知识,它以基本概念和基本理论为指导,以实验研究为手段渗透化学计量的定量要求,它在中考化学试卷中占有重要的位置(约占40%的分值)。
元素化合物的重点把握以下几类趋势:(1)以元素化合物的性质角度切入,考查元素化合物在生产和生活中的用途。
(2)根据题目给定的陌生的元素化合物的信息,结合已有知识合理迁移,推断对应元素化合物的性质。
(3)开展实验研究,对元素化合物可能具有的性质进行探究。 专题复习可按照以下几个专题进行:“化学用语专题”、“基本实验与基本操作专题”、“推断专题”、 “实验探究专题”、“计算专题”“物质的分离与除杂专题”等。在进行这些专题训练时,应根据中考命题的特点,精心选择一些新颖的、有代表性的题目进行专题训练,真正把握其命题方向和规律,要注意体会、归纳题目中的化学方法和化学思想。5、做好专题复习。(1)通过实验活动过程的分解,考查基本实验操作。
例如:实验探究题是中考的重点,它主要考察学生设计和实施科学实验的能力。一般说来,规律类习题有以下几类:(2)通过演示实验过程及现象描述,考查有关的化学用语。(3)通过多个实验的集合,考察探究过程中思维方法的形成。如对比实验的思维方法考查,守恒思想的考查、实验现象、实验结论的考查等。(4)通过实验活动,重现实验过程,体验实验过程中基本仪器使用基本操作方法和化学探究的思维,对猜想与假设、方案设计、交流讨论、反思与评价、事故分析处理等。例(2013年江西T23)某实验小组开展了如下有关碱的化学性质探究活动:
(1)实验1的目的是 ;
(2)实验2中发生反应的化学方程式是 ;
(3)实验3中观察到溶液由红色变为无色后,小萍想知道反应后溶液中除NaCl外,是否还含有其他溶质(不考虑酚酞),于是她向反应后的溶液中加入一种试剂,从而得出了结论。小萍加入的试剂可能是 ;(4)通过上述实验探究活动,可以总结出碱的化学性质是:
①碱能与酸发生中和反应;
② ;
……
(5)准备实验时,小英发现药品室有两瓶未标注浓度的氢氧化钠溶液,经询问老师得知,该两瓶溶液的溶质质量分数分别为5%和l0%。请你设计实验方案完成对这两瓶溶液的鉴别(仅限以下实验用品:试管、量筒、滴管、酚酞溶液、10%盐酸)
六、试题对今后中考复习的启示7、复习中不要脱离了化学与社会、科学、生活的关系。
9、提高老师自身的知识水平,精选题目、不猜题押宝,不搞题海战6、注重培养学生的基本学科素养和基本学科思想10、除了注重知识点内容掌握外,还要学生学习一些应试要领。做题时一定要细心,端正心态,避免眼高手低,注意题目中的关键词,题目注释等等。做题时把握好做题的速度和物理与化学考试时间的分配。
化学学习过程中,化学思想的培养等学科素养往往比化学知识本身更为重要,如:化学推理、规律提炼、实验的规范性、实验的安全意识等。8、关注初、高中衔接。 谢 谢
中考化学试卷分析
题型:单项选择题、选择填充题、填空与说明题、实验与探究题、计算题1、试卷结构:
试题满分:100分,考试时间:70分钟,试卷版面:16开5面一、试题概况2、2016年题型比例(与2015年对比)与2015年一致3、试题内容分布及占分比例(与2015年对比) 4、图表对比(与2015年对比)近两年来,流程图题成为中考热门题型,也体现了命题者关注高、初中知识衔接的意图。5、近两年中考考点示例5、近两年中考考点示例二、试题主要特点 2016年江西省中考化学试卷在2015年的基础上稳中求变、变中求新。试卷中知识点覆盖面广,侧重考查对最基础的化学知识和技能的掌握情况,与课本和新课程标准紧密结合,以生产、生活、科技的知识设置情境,难度适中,突出化学核心观念和主干知识的考查,充分体现了《义务教育化学课程标准》中对化学学科思想和学科方法的最新要求,具体表现在以下几个方面:1、注重基础,体现了面向全体学生的理念 知识点覆盖面广,难度适中。 如第1题考查氧气的检验方法;第3题考查闻气体气味、液体的取用、气体的贮存、仪器的洗涤等实验基本操作;第12题考察营养素;第13题考查化学式的相关计算;第16题考查化学用语;第17题考察化石燃料、化学肥料;第18题考察元素周期表的信息识别、原子结构示意图等均源自教材。如第3题:下列实验操作正确的是( ) (1)更加突出了对学生思维能力的考察2、突出主干,体现了考察学生能力例如:第22题【反思与交流】(1)乙组同学认真分析甲组实验后,一致认为不需要通过实验就能判断猜2不成立,理由是甲组实验中也有硫酸钠生成等;
例如第19题(3):
4KOH+2MnO2+O2===2K2MnO4+2H2O
这个方程式要理解质量守恒定律才能完成的。(2)2016年中考化学试卷上没有出现大量需要记忆的化学方程式,而是出现了一些需要通过思考的化学方程式的书写。例如第23题:2Al+3ZnCl2=3Zn+2AlCl3也是要理解置换反应的本质才能完成的。(3)图表结合,考察学生获取信息的能力2016年中考图表多达21个。 考察学生对溶解度曲线、元素及原子结构、物质发生化学反应的微观过程、化学实验基本操作、物质间的相互转化、实验室中制取二氧化碳、常见酸碱盐的化学性质、溶液的酸碱性等知识的理解及实验分析和处理能力。3、注重实验,体现了化学学科的特点 实验能力的考察内容有:闻气体气味、液体的取用、气体的贮存、仪器的洗涤等实验基本操作;二氧化碳的制取和干燥;物质的分离;物质的鉴别;除杂;灭火的方法等内容,共计21分。 考查学生实验方法(包括操作、现象描述)选择;实验仪器或装置选择及理由;实验分析等4、关注社会,体现了化学的应用性 2016年中考化学试卷中有9道题紧密联系生产生活实际,分值高达41分,内容涉及物质的用途、能源和资源的开发利用、化学与科技、化学与工业、化学与农业、化学与医药学、化学与材料、化学与文学、社会热点问题、化学与健康问题、化学与环境问题等多个方面,较好的体现了化学知识的实用性原则。 如第17题:(6分)化学是造福人类的科学。
(1) 能源化学——使用新能源汽车可节约化石燃料。化石燃料包括煤、天然气和 。
(2)农业化学——化肥对提高农作物产量具有重要作用。尿素[CO(NH2)2]属于 (填氮、磷或钾)肥;
(3)医药化学——我国药学家屠呦呦因研制抗疟新药青蒿素获得诺贝尔奖。由青蒿酸(C15H22O2)合成青蒿素(C15H22O5)的过程中主要发生了 (填物理或化学)变化;
(4)材料化学——为防止食物变质常采用真空包装,目的是隔绝 ;检验塑料包装袋是否为热塑性塑料的方法(包括操作和现象) 。试题综合评述(单选题不计在内)难度适中,梯级分布,结构合理。三、九江市份试卷统计
1、九江市2016年中考化学各分数段分布情况2、2016年中考化学试题难度(P)结果统计2、2016年中考化学试题难度(P)结果统计(表5)2、2016年中考化学试题难度(P)结果统计目前均分:47.5(除单选题外)
2016年中考化学预计难度系数为0.6左右四、学生答题情况统计
学生答题常见错误汇总表(表6) T11:下列物质属于混合物的是( A )
A、锰钢 B、红磷 C、硝酸钾 D、
T12:下列基本营养素中能给人体提供能量的是( C )
A、水 B、维生素 C、油脂 D、
T13:南昌汉代海昏候墓出土的文物中,保存完好的玉器非常罕见。对玉石主要成份(化学式为NaAlSi2O6 )的描述正确的是( B )
A、含有3个氧分子
B、钠元素与铝元素的质量比为23:27
C、钠元素的质量分数为13.4%
D、
T14:下列实验方案能达到预期目的的是( C )
A、向盐酸和氯化钙的混合溶液中逐滴加入碳酸钾溶液
B、实验室中用一氧化碳还原氧化铁
C、加热氯酸钾和二氧化锰的混合物
D、往氢氧化钙溶液中逐滴加入物质X的溶液,则物质X
可能为 T15:下列实验方案能达到预期目的的是( B )
A、分离食盐和泥沙——蒸发结晶
B、除去氧化钙中的碳酸钙——高温煅烧
C、检验露置于空气中的氢氧化钠溶液是否变
质——滴入无色酚酞溶液
D、鉴别氯化钠固体和硝酸铵固体—— +-T17:(6分)化学是造福人类的科学。
(1) 能源化学——使用新能源汽车可节约化石燃料。化石燃料包括煤、天然气和 石油。
(2)农业化学——化肥对提高农作物产量具有重要作用。尿素[CO(NH2)2]属于氮(填氮、磷或钾)肥;
(3)医药化学——我国药学家屠呦呦因研制抗疟新药青蒿素获得诺贝尔奖。由青蒿酸(C15H22O2)合成青蒿素(C15H22O5)的过程中主要发生了 化学(填物理或化学)变化;
(4)材料化学——为防止食物变质常采用真空包装,目的是隔绝氧气(空气);检验塑料包装袋是否为热塑性塑料的方法(包括操作和现象)取样加热后是否熔化,冷却后是否凝固。T18:(7分)南昌大家研发的“硅衬底高光效GaN基蓝色发光二极管技术”获得2015年国家技术发明一等奖。请回答下列问题:
(1) 右图是镓在元素周期表中的信息以及原子结构示意图。镓的相对原子质量为 69.72,下列原子结构示意图所对应的元素与镓元素的化学性质相似的是B(填序号);
(2)氮化镓(GaN)中镓元素的化合价为
+3价,则氮元素的化合价为-3价;
(3)传统制备氮化镓的化学原理是:
GaCl3+NH3===GaN+3X其中X的化学式为HCl一定条件Ga
镓
69.72T19:(6分)高锰酸钾是常用的氧化剂。下图是实验室模拟工业上制备高锰酸钾晶体的操作流程:
(1)完成操作 3所需要的玻璃仪器是烧杯(玻璃棒或漏斗)( 填一种即可);实验中通过操作2析出高锰酸钾晶体,说明高锰酸钾的溶解度随温度的升高而增大;
(2)操作流程中可循环利用的物质是二氧化锰;
(3)氢氧化钾、二氧化锰和氧气在高温条件下煅烧,生成锰酸钾和水,该反应的化学方程式为: 4KOH+2MnO2+O2===2K2MnO4+2H2O高温T19T20:(8分)赣南的客家围屋如同城堡,
可以抵御外敌入侵。现在五种物质盐酸、
硫酸、氢氧化钠、氯化钡和碳酸钠作为围
屋的守护“卫士”,只有相邻物质之间能发
生反应才能组成守护的防线(如右图所示
)。其中物质A常用于铅酸蓄电池中,其
浓溶液有脱水性;物质C是人体胃液中的
主要成分。(提示:碳酸钡不溶液于水)
(1)A物质是H2SO4;
(2)B与C反应的化学方程式为:NaOH+HCl=NaCl+H2O,A与E反应的实验现象是生成白色沉淀;
(3)现在下列物质作为“外敌”分别对围屋发起进攻,若该物质与两位相邻的守护“卫士”都能发生反应才能攻破防线,那么能攻入围屋的物质是4(填序号)
1、铁 2、氧化铁 3、二氧化碳 4、氢氧化钡T20T21:(8分)请你根据下图回答有关问题T22:(8分)下图是两个实验小组分别进行“加热硫酸铜和氢氧化钠溶液反应后生成物”的实验过程示意图:
【甲组】氢氧化钠与硫酸铜反应的化学方程式为2NaOH+CuSO4=Na2SO4+Cu(OH)2 ,加热后产生黑色的氧化铜。
【乙组】为寻找实验中没有产生氧化铜的原因,他们进行了以下实验探究:
【查阅资料】在酸性条件下,氢氧化钠与硫酸铜在溶液中可发生如下反应:6NaOH+4CuSO4=3Na2SO4+Cu4(OH)6SO4 ,生成的碱式硫酸铜是不溶于水的蓝白色固体,加热不易发生分解。
【提出猜想】根据资料分析,同学们针对试管中溶液呈酸性的原因作出以下猜想:
猜想1.硫酸铜溶液呈酸性; 猜想2.生成的硫酸钠使溶液呈酸性。
【实验与结论】
实验①:用pH试纸测定硫酸铜溶液的酸碱度,得出其pH〈 (填〉、〈或=)7,硫酸铜溶液呈酸性,猜想1成立。
实验②:向盛有硫酸钠溶液的试管中滴加石蕊溶液,观察到溶液显紫色,硫酸钠溶液呈
中(填酸、中或碱)性,猜想2不成立。
【交流与反思】(1)乙组同学认真分析甲组实验后,一致认为不需要通过实验就能判断猜2不成立,理由是甲组实验中也有硫酸钠生成等;
(2)在化学反应中,相同的反应物因其质量比不同可能会导致生成物不同,请另举一例木炭和氧气 (写出反应物即可)。T22T23:(9分)央视频道《是真的吗?》栏目中有一段视频:将“锡纸”剪成一段两头宽中间窄的纸条,然后两头分别连接电池的正负极,观察到“锡纸”立即燃烧。据此,小晟同学取某种“锡纸”进行了以下探究:
(1)“锡纸”燃烧的原因:“锡纸”两端接入电池两极后造成短路致使“锡纸”燃烧,从燃烧的条件分析:开始“锡纸”不燃烧但短路却能燃烧的原因是温度达到
着火点(填 “与氧气接触”或“温度达到着火点”)。
(2)探究“锡纸”中金属的成分:“锡纸”中的金属是锡吗?
【查阅资料】 ① ‘锡纸”是锡箔或铝箔和纸粘合而成; ②锌粉是一种深灰色固体;③锡(Sn)与酸或盐溶液反应生成正二价的锡盐
【提出猜想】猜想1. “锡纸”中的金属是锡; 猜想2. “锡纸”中的金属是铝。
【进行实验】设计方案并进行实验
【交流讨论】 ① 实验中打磨“锡纸”目的是除去表面氧化物等;
②下列物质的溶液可以替代氯化锌溶液完成上述实验的是D(填序号)。
A、氯化铜 B、硝酸银 C、硫酸钠 D、硫酸亚铁
【拓展应用】电器短路会引起火灾,我们要严加防范。如果电器着火应该采取的灭火方法是切断电源后用干粉灭火器(或二氧化碳灭火器)灭火等 。T23T24:(10分)小新用20g含碳酸钠53%的天然碱制取氢氧化钠用于制作“叶脉书签”(杂质不参加反应)。操作过程如下:
(1)20g样品中碳酸钠的质量为 g;
(2)反应后所得滤液中氢氧化钠的质量分数为多少?(写出计算过程)
(3)将200g滤液浓缩成制作“叶脉书签”所需要质量分数为10%的氢氧化钠溶液,需蒸发水 g.五、错误归类及教学建议汇总1、化学用语书写不熟练不规范
例如:第16、18(3)、19(3)、20(2)、21(2)、22(第1空)、23表格(第2空)、24题都是考察化学用语的知识,共有16分。教学建议:教师在平时教学中,对化学用语的教学要采取新颖而有效的训练方法,不能再用机械而又枯燥的学习方法,要最大限度的调动全体学生学习化学用语的兴趣。这样才能又牢又好的学好化学用语。例如打破教材顺序,提前学习元素符号;每学期举行一到两次化学用语比赛等五、错误归类及教学建议汇总2、双基掌握不扎实,基本概念混淆不清
学生对常见物质的组成、结构、性质、用途、俗称记忆不清,出现混淆;仪器名称、化学概念等基本化学术语书写不正确。例如:第11题“混合物”与“化合物”;12题“营养素”与“营养物质”;第19(1)题 把“漏斗”写成“长颈漏斗”或“分液漏斗”。教学建议:重视基础知识的教学,对于化学概念更要注重理解性的教学,对于易混淆的化学概念应进行对比式教学,使学生在头脑中形成清晰的概念。五、错误归类及教学建议汇总3、文字表达能力欠缺
例如:不能用简明准确的化学语言来表述有关概念、规律、现象、实验过程等一系列的化学问题,文字表述时关键词(字)出现错误或不完整等。20题(2)“有白色沉淀生成”写成“有沉淀生成”。教学建议:化学教师在教学过程中要注意自身规范语言描述,注重对学生进行相关描述性语言的训练,例如:要在课堂上多提问,对学生作业中的文字表述精批细改,对实验设计、物质分离、物质鉴别等可进行模仿性表达训练。在讲评作业中多强调答题要注意规范性,尽可能使语言文字表达做到准确、精炼。五、错误归类及教学建议汇总4、审题能力及获取信息能力欠缺
审题马虎;不能准确理解题意; 审题时不能将题目中的陌生情景读懂、读透,挖掘出情景中的隐含条件;不能很好的将试题中的情景与学过的知识进行关联;不能将题中的信息和需要解决的问题结合起来进行分析;不能将所学知识与生活经验、劳动经验和社会热点问题联合起来。19题完成操作3所需要的玻璃仪器是 。有的学生没注意到“玻璃仪器”四个字,填“滤纸”。23题【交流讨论】②下列物质的溶液可以替代氯化锌溶液完成上述实验的是 (填序号)。A、氯化铜 B、硝酸银 C、硫酸钠D、硫酸亚铁,有的学生理解成能与铝发生置换反应的就行,于是多选了A和B。
教学建议:让学生学会审题。在认真读题的同时用笔在关键词下面圈点标记,养成自我提示的好习惯。平时在课堂上多举学生的错例,让他们自己分析原因,属于审题不清的予以强调,让学生意识到“磨刀不误砍柴工”。
五、错误归类及教学建议汇总5、实验能力和实验探究能力的欠缺
在大多数学校,教师做演示实验多,学生分组实验少,课外学生独立做探究实验的就更少。学生缺乏对实验过程的体验,更谈不上实验的技能技巧,对实验仪器、操作方法不熟悉。
教学建议:加强实验教学,但要杜绝在黑板上讲实验、在练习中做实验。要通过一些探究性的实验培养学生的实验设计能力、创新思维品质。老师要多鼓励学生对实验中遇到的异常现象进行分析、假设、实验探究,得出结论。我们在教学过程中对于实验探究题自始至终都要予以特别的关注,而不应等到中考复习时才加以关注。五、错误归类及教学建议汇总6、错别字、简单计算错误严重
例如:17题(4)熔化写成“融化”、“溶化”、“溶解”。23题“灭火器”写“灭火气”、“灭火剂”。24题氢氧化钠的相对分子质量计算错误,百分数的小数点出错。
教学建议:在平常教学过程中也要注重培养学生其他方面的能力,如严格要求学生书写工整;强化错别字的矫正;计算的准确,不要在考试中因为这些小问题而失分。五、错误归类及教学建议汇总7、学生的学习态度不端正,存在厌学情绪。
具体表现为:部分学生在胡乱涂完选择题的答题卡后,填空部分就一个也不做,即使是简简单单的题目也不动笔,看都懒得去看。本来一些送分的题目也没办法送到这样的学生手中。说明这样的学生处于一种完全放弃学习的状态,这可能是致使中考化学低分率越来越高的主要原因之一。
教学建议:在平时教学中要关注学生的学习兴趣的激发和保持,在开始学习化学时大多数学生还是抱有很大的学习热情和兴趣,但有些学生无法保持长久,于是出现“三天新鲜”甚至到了下半学期成绩大幅下降的情况。在教学中要利用化学学学科实验多的优势,从各方面调动学生学习化学的兴趣。
在教学中要关注后进生,防止出现大面积级低分数。六、试题对今后中考复习的启示我校2016年中考化学学科复习情况1、中考复习时间:4月14日—6月14日
3、复习方法:单元复习与分块复习相结合
争取一轮复习完
2、复习依据:课本上下册、新课标、中考说明、《新评价》、省中考模拟试卷(6套)、金太阳卷(后3套)等4、考查复习效果方式:月考(两次)
本校老师自主命题,按中考考试要求进行测试
六、试题对今后中考复习的启示1、关注中考说明中的考点
2、关注难度变化六、试题对今后中考复习的启示3、注重“双基”的复习,基础知识是考查的重点。常考查的基础知识和主干知识有:
(1)涉及的主要16种物质的性质和用途
二种酸(HCl和H2SO4),二种碱NaOH和[Ca(0H)2],
四种单质(C、H2、O2、Fe),四种氧化物(CO、CO2、H2O、CuO),四种盐(NaCl、Na2CO3、CaCO3、CuSO4)
(2)涉及到的常见概念及知识:物理变化、化学变化、质量守恒定律、化学用语、溶解度曲线、燃烧与灭火、铁生锈、常见方程式书写
(3)常见气体的制备,常用仪器的名称、用途和基本操作
(4)与相对分子质量和溶液配制有关的计算,与方程式和质量分数有关的计算六、试题对今后中考复习的启示4、关注元素化合物
元素化合物作为化学课程的骨架,承载了化学概念和理论、化学计算和化学实验的相关知识,它以基本概念和基本理论为指导,以实验研究为手段渗透化学计量的定量要求,它在中考化学试卷中占有重要的位置(约占40%的分值)。
元素化合物的重点把握以下几类趋势:(1)以元素化合物的性质角度切入,考查元素化合物在生产和生活中的用途。
(2)根据题目给定的陌生的元素化合物的信息,结合已有知识合理迁移,推断对应元素化合物的性质。
(3)开展实验研究,对元素化合物可能具有的性质进行探究。 专题复习可按照以下几个专题进行:“化学用语专题”、“基本实验与基本操作专题”、“推断专题”、 “实验探究专题”、“计算专题”“物质的分离与除杂专题”等。在进行这些专题训练时,应根据中考命题的特点,精心选择一些新颖的、有代表性的题目进行专题训练,真正把握其命题方向和规律,要注意体会、归纳题目中的化学方法和化学思想。5、做好专题复习。(1)通过实验活动过程的分解,考查基本实验操作。
例如:实验探究题是中考的重点,它主要考察学生设计和实施科学实验的能力。一般说来,规律类习题有以下几类:(2)通过演示实验过程及现象描述,考查有关的化学用语。(3)通过多个实验的集合,考察探究过程中思维方法的形成。如对比实验的思维方法考查,守恒思想的考查、实验现象、实验结论的考查等。(4)通过实验活动,重现实验过程,体验实验过程中基本仪器使用基本操作方法和化学探究的思维,对猜想与假设、方案设计、交流讨论、反思与评价、事故分析处理等。例(2013年江西T23)某实验小组开展了如下有关碱的化学性质探究活动:
(1)实验1的目的是 ;
(2)实验2中发生反应的化学方程式是 ;
(3)实验3中观察到溶液由红色变为无色后,小萍想知道反应后溶液中除NaCl外,是否还含有其他溶质(不考虑酚酞),于是她向反应后的溶液中加入一种试剂,从而得出了结论。小萍加入的试剂可能是 ;(4)通过上述实验探究活动,可以总结出碱的化学性质是:
①碱能与酸发生中和反应;
② ;
……
(5)准备实验时,小英发现药品室有两瓶未标注浓度的氢氧化钠溶液,经询问老师得知,该两瓶溶液的溶质质量分数分别为5%和l0%。请你设计实验方案完成对这两瓶溶液的鉴别(仅限以下实验用品:试管、量筒、滴管、酚酞溶液、10%盐酸)
六、试题对今后中考复习的启示7、复习中不要脱离了化学与社会、科学、生活的关系。
9、提高老师自身的知识水平,精选题目、不猜题押宝,不搞题海战6、注重培养学生的基本学科素养和基本学科思想10、除了注重知识点内容掌握外,还要学生学习一些应试要领。做题时一定要细心,端正心态,避免眼高手低,注意题目中的关键词,题目注释等等。做题时把握好做题的速度和物理与化学考试时间的分配。
化学学习过程中,化学思想的培养等学科素养往往比化学知识本身更为重要,如:化学推理、规律提炼、实验的规范性、实验的安全意识等。8、关注初、高中衔接。 谢 谢
同课章节目录
