3.1.2 氯气的性质及应用(一) 课件 (共21张PPT)_高中化学苏教版(2019)必修一
文档属性
| 名称 | 3.1.2 氯气的性质及应用(一) 课件 (共21张PPT)_高中化学苏教版(2019)必修一 |  | |
| 格式 | pptx | ||
| 文件大小 | 25.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-01 19:28:22 | ||
图片预览







文档简介
3.1.2 氯气的性质及应用(一)
素养目标
宏观辨识与微观探析
能通过观察氯气与金属、水等反应的宏观现象,辨识其性质,从微观角度理解氯气与金属、水反应的本质,构建 “结构 - 性质 - 用途” 的化学思维。
科学态度与社会责任
通过了解氯气在生活、生产中的应用及含氯消毒剂的合理使用,树立科学使用化学物质的观念,增强社会责任感,关注化学对环境和生活的影响。
变化观念与平衡思想
认识氯气参与反应时的物质变化及能量变化,理解氯气相关反应的条件、方向等,形成对化学反应变化的动态、平衡认知 。
教学重难点
重点:
1. 掌握氯气与金属(钠、铁、铜 )、水的反应,明确反应现象、产物,理
解氯水成分(Cl2、HClO?等 )及性质
2. 熟知氯气及含氯化合物(次氯酸、次氯酸盐 )在消毒、漂白等生产生活
场景的应用原理
难点:
1. 理解氯气与水反应的可逆性及平衡移动,区分氯水、液氯、次氯酸概
念与性质差异
2. 分析含氯消毒剂(漂白液、漂白粉)制备、使用的化学反应,把握
其作用机制与合理使用方法 。
新课导入
夏天游泳时,泳池里会有淡淡的 “消毒水味”,这其实和氯气消毒有关;家里用的漂白剂,能让衣服洁白如新,也离不开氯气相关的化学知识。在工业上,氯气更是制备多种重要化工产品的基础原料。可氯气一旦泄漏,又会对环境和人体造成严重危害。那么,氯气究竟有着怎样独特的性质,能在生产生活中发挥这么多作用?
1
氯气的物理性质
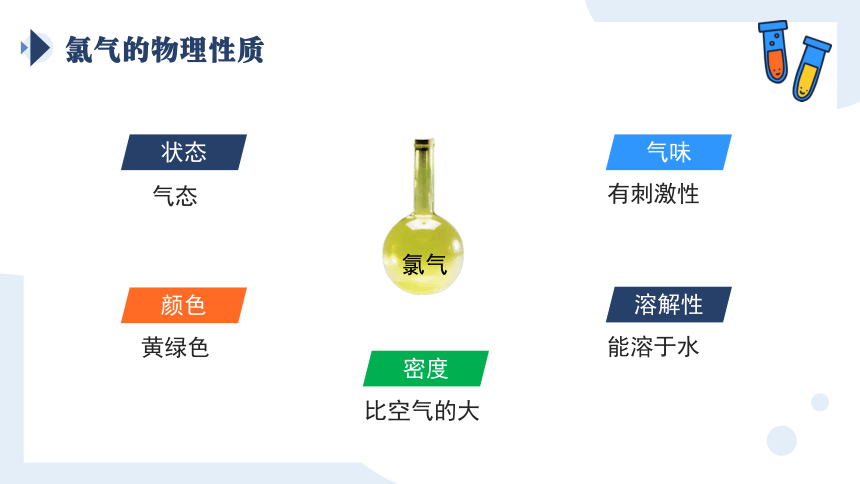
氯气的物理性质
状态
颜色
气味
溶解性
气态
黄绿色
有刺激性
能溶于水
密度
比空气的大
氯气
特别提醒
(1)闻气体的操作:用手轻轻地在试剂瓶口扇动,使极少量的气体飘进鼻孔
(2)氯气易液化,在加压的条件下,氯气可转化为液态(称为液氯),二者都是纯净物。
(3)氯气有毒,氯气的密度比空气的大,若遇到Cl2泄漏,逃生时可用湿毛巾或蘸有肥皂水等弱碱性溶液的毛巾捂住口鼻,并逆风向高处转移。
2
氯气的化学性质
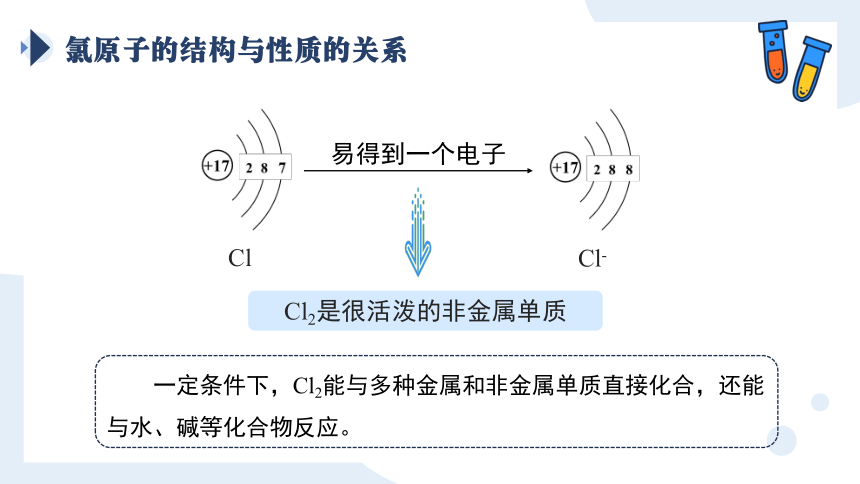
氯原子的结构与性质的关系
一定条件下,Cl2能与多种金属和非金属单质直接化合,还能与水、碱等化合物反应。
易得到一个电子
Cl-
Cl2是很活泼的非金属单质
Cl
实验探究——氯气与铁单质反应
实验现象:
剧烈反应,产生棕褐色的烟,溶于水后溶液呈棕黄色
化学方程式:
2Fe + 3Cl2 === 2FeCl3
点燃
氯气与金属单质反应
归纳:氯气与除金、铂以外的绝大多数金属都能反应。Cl2与Cu、Fe 反应时,生成高价态的金属氯化物。如Cl2与Fe反应生成 FeCl3而不是FeCl2。
常温下,液氯与干燥的铁不反应,故工业上常用钢瓶储存液氯。
氯气与非金属单质(H2)的反应
{10A1B5D5-9B99-4C35-A422-299274C87663}实验装置
实验现象
实验结论
纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,瓶口有大量白雾产生
H2 + Cl2 ====== 2HCl
点燃或光照
工业上利用电解饱和食盐水得到的氯气和氢气制取盐酸
思考讨论
通过H2在Cl2中燃烧的实验,你对燃烧的条件及其本质有什么新的认识?
燃烧不一定要有氧气参加
燃烧的本质是氧化还原反应
任何发光发热的剧烈的化学反应叫做燃烧
易错辨析
化学现象中烟、雾、气的区别
{C34123BC-ABDB-4F42-A839-AC3DB432A791}
状态
举例
烟
雾
气
固体小颗粒
Fe、Cu在氯气中燃烧分别产生棕褐色的烟—FeCl3固体颗粒、棕黄色的烟—CuCl2固体颗粒
小液滴
H2在 Cl2中燃烧生成的 HCI 气体遇水蒸气形成白雾—盐酸小液滴
气态物质
MnO2和浓盐酸在加热条件下反应生成黄绿色气体;若气体无色时,肉眼看不到
3
随堂练习
1. 下列说法不正确的是( )
A. 氯气的密度比空气的密度大
B. 氯气是黄绿色气体
C. 可用鼻子对着盛有氯气的集气瓶瓶口闻氯气的气味
D. 氯气可用于自来水杀菌、消毒
C
2. 工业制备盐酸以H2和Cl2为原料。实验室将在空气中点燃的气体a缓慢伸入集气瓶中模拟制备少量HCl(如图所示),下列说法不合理的是( )
A. 气体a是Cl2
B. 工业上不能采用混合光照的方法制备HCl
C. 反应过程中集气瓶口有白雾生成
D. 实验方案会用到 、 等图标进行提示
A
3. 为了探究氯气的性质进行以下四个实验。下列说法错误的是( )
A. 用集气瓶收集Cl2时可采用向上排空气法
B. 可以用坩埚钳夹住灼烧后的钠立刻放入充满氯气的集气瓶中
C. 金属铁和铜在燃烧实验中均得到高价态的金属氯化物
D.氢气需要先验纯,再点燃,然后通入装有氯气的集气瓶中
B
4. 某实验小组利用长柄V形管设计如图所示的Na与氯气的反应实验(“△”代表酒精灯加热),方法是先通入一段时间的氯气,然后再加热长柄中的钠块至其熔化,撤掉酒精灯,再通入Cl2。下列判断错误的是( )
A. 长柄中有白烟生成,逐渐凝聚在玻璃内壁上
B. X溶液可为浓NaOH溶液
C. V形管的“消膜泡”的作用主要是消除泡沫
D. 钠在氯气中燃烧的火焰为黄色
C
5. 下列关于氯气的说法中正确的是( )
A. 氯气在常温下能与铁反应,故不能用铁罐存放液氯
B. 点燃氢气和氯气的混合气体可以制取氯化氢
C. 氯气氧化性很强,一般都能将金属氧化为它的最高价态
D. 氯原子最外层有7个电子,所以氯元素只有-1和+7价
C
感谢您的观看
“THANK YOU”
素养目标
宏观辨识与微观探析
能通过观察氯气与金属、水等反应的宏观现象,辨识其性质,从微观角度理解氯气与金属、水反应的本质,构建 “结构 - 性质 - 用途” 的化学思维。
科学态度与社会责任
通过了解氯气在生活、生产中的应用及含氯消毒剂的合理使用,树立科学使用化学物质的观念,增强社会责任感,关注化学对环境和生活的影响。
变化观念与平衡思想
认识氯气参与反应时的物质变化及能量变化,理解氯气相关反应的条件、方向等,形成对化学反应变化的动态、平衡认知 。
教学重难点
重点:
1. 掌握氯气与金属(钠、铁、铜 )、水的反应,明确反应现象、产物,理
解氯水成分(Cl2、HClO?等 )及性质
2. 熟知氯气及含氯化合物(次氯酸、次氯酸盐 )在消毒、漂白等生产生活
场景的应用原理
难点:
1. 理解氯气与水反应的可逆性及平衡移动,区分氯水、液氯、次氯酸概
念与性质差异
2. 分析含氯消毒剂(漂白液、漂白粉)制备、使用的化学反应,把握
其作用机制与合理使用方法 。
新课导入
夏天游泳时,泳池里会有淡淡的 “消毒水味”,这其实和氯气消毒有关;家里用的漂白剂,能让衣服洁白如新,也离不开氯气相关的化学知识。在工业上,氯气更是制备多种重要化工产品的基础原料。可氯气一旦泄漏,又会对环境和人体造成严重危害。那么,氯气究竟有着怎样独特的性质,能在生产生活中发挥这么多作用?
1
氯气的物理性质
氯气的物理性质
状态
颜色
气味
溶解性
气态
黄绿色
有刺激性
能溶于水
密度
比空气的大
氯气
特别提醒
(1)闻气体的操作:用手轻轻地在试剂瓶口扇动,使极少量的气体飘进鼻孔
(2)氯气易液化,在加压的条件下,氯气可转化为液态(称为液氯),二者都是纯净物。
(3)氯气有毒,氯气的密度比空气的大,若遇到Cl2泄漏,逃生时可用湿毛巾或蘸有肥皂水等弱碱性溶液的毛巾捂住口鼻,并逆风向高处转移。
2
氯气的化学性质
氯原子的结构与性质的关系
一定条件下,Cl2能与多种金属和非金属单质直接化合,还能与水、碱等化合物反应。
易得到一个电子
Cl-
Cl2是很活泼的非金属单质
Cl
实验探究——氯气与铁单质反应
实验现象:
剧烈反应,产生棕褐色的烟,溶于水后溶液呈棕黄色
化学方程式:
2Fe + 3Cl2 === 2FeCl3
点燃
氯气与金属单质反应
归纳:氯气与除金、铂以外的绝大多数金属都能反应。Cl2与Cu、Fe 反应时,生成高价态的金属氯化物。如Cl2与Fe反应生成 FeCl3而不是FeCl2。
常温下,液氯与干燥的铁不反应,故工业上常用钢瓶储存液氯。
氯气与非金属单质(H2)的反应
{10A1B5D5-9B99-4C35-A422-299274C87663}实验装置
实验现象
实验结论
纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,瓶口有大量白雾产生
H2 + Cl2 ====== 2HCl
点燃或光照
工业上利用电解饱和食盐水得到的氯气和氢气制取盐酸
思考讨论
通过H2在Cl2中燃烧的实验,你对燃烧的条件及其本质有什么新的认识?
燃烧不一定要有氧气参加
燃烧的本质是氧化还原反应
任何发光发热的剧烈的化学反应叫做燃烧
易错辨析
化学现象中烟、雾、气的区别
{C34123BC-ABDB-4F42-A839-AC3DB432A791}
状态
举例
烟
雾
气
固体小颗粒
Fe、Cu在氯气中燃烧分别产生棕褐色的烟—FeCl3固体颗粒、棕黄色的烟—CuCl2固体颗粒
小液滴
H2在 Cl2中燃烧生成的 HCI 气体遇水蒸气形成白雾—盐酸小液滴
气态物质
MnO2和浓盐酸在加热条件下反应生成黄绿色气体;若气体无色时,肉眼看不到
3
随堂练习
1. 下列说法不正确的是( )
A. 氯气的密度比空气的密度大
B. 氯气是黄绿色气体
C. 可用鼻子对着盛有氯气的集气瓶瓶口闻氯气的气味
D. 氯气可用于自来水杀菌、消毒
C
2. 工业制备盐酸以H2和Cl2为原料。实验室将在空气中点燃的气体a缓慢伸入集气瓶中模拟制备少量HCl(如图所示),下列说法不合理的是( )
A. 气体a是Cl2
B. 工业上不能采用混合光照的方法制备HCl
C. 反应过程中集气瓶口有白雾生成
D. 实验方案会用到 、 等图标进行提示
A
3. 为了探究氯气的性质进行以下四个实验。下列说法错误的是( )
A. 用集气瓶收集Cl2时可采用向上排空气法
B. 可以用坩埚钳夹住灼烧后的钠立刻放入充满氯气的集气瓶中
C. 金属铁和铜在燃烧实验中均得到高价态的金属氯化物
D.氢气需要先验纯,再点燃,然后通入装有氯气的集气瓶中
B
4. 某实验小组利用长柄V形管设计如图所示的Na与氯气的反应实验(“△”代表酒精灯加热),方法是先通入一段时间的氯气,然后再加热长柄中的钠块至其熔化,撤掉酒精灯,再通入Cl2。下列判断错误的是( )
A. 长柄中有白烟生成,逐渐凝聚在玻璃内壁上
B. X溶液可为浓NaOH溶液
C. V形管的“消膜泡”的作用主要是消除泡沫
D. 钠在氯气中燃烧的火焰为黄色
C
5. 下列关于氯气的说法中正确的是( )
A. 氯气在常温下能与铁反应,故不能用铁罐存放液氯
B. 点燃氢气和氯气的混合气体可以制取氯化氢
C. 氯气氧化性很强,一般都能将金属氧化为它的最高价态
D. 氯原子最外层有7个电子,所以氯元素只有-1和+7价
C
感谢您的观看
“THANK YOU”
