2026高考化学一轮复习 第一章 第1讲 物质的组成、性质和转化 教学课件(91张)
文档属性
| 名称 | 2026高考化学一轮复习 第一章 第1讲 物质的组成、性质和转化 教学课件(91张) |

|
|
| 格式 | pptx | ||
| 文件大小 | 24.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-04 00:00:00 | ||
图片预览









文档简介
(共91张PPT)
化学大一轮复习
第一章 第1讲
物质的组成、性质和转化
复习目标
1.认识元素可以组成不同种类的物质,根据物质的组成和性质可以对物质进行分类。
2.熟知同类物质具有相似的性质,一定条件下各类物质可以相互转化。
3.了解胶体是一种常见的分散系,了解溶液和胶体的区别。
课时精练
考点一 物质的组成与分类
考点二 物质的性质与转化
考点三 分散系 胶体
练真题 明考向
内容索引
考点一
物质的组成与分类
1.物质的组成——元素与物质的关系
整合必备知识
游离
原子
分子
化合
原子
分子
离子
(1)同素异形体
①定义:由同一种元素形成的 。
②性质:物理性质不同,化学性质有差异。同素异形体之间在一定条件下可以相互转化,这种转化是 变化。
③常见元素的同素异形体
氧元素: ;碳元素: ;磷元素: 。
(2)纯净物和混合物
纯净物:由同种单质或化合物组成的物质。
混合物:由几种不同的单质或化合物组成的物质。
几种性质不同的单质
化学
O2、O3
金刚石、石墨、C60
白磷、红磷
[应用举例]
现有下列物质:
①冰水混合物 ②爆鸣气 ③铝热剂 ④普通玻璃 ⑤水玻璃 ⑥有机玻璃 ⑦漂白粉 ⑧TNT ⑨H2SO4 ⑩含氧40%的氧化镁 花生油 福尔马林 密封保存的NO2气体 液氯 王水
KAl(SO4)2·12H2O 分子式为C5H10的烃 分子式为C7H8的芳香烃
其中一定为纯净物的是 (填序号,下同);一定为混合物的是 ;可能是纯净物,也可能是混合物的是 。
①⑧⑨⑩
②③④⑤⑥⑦
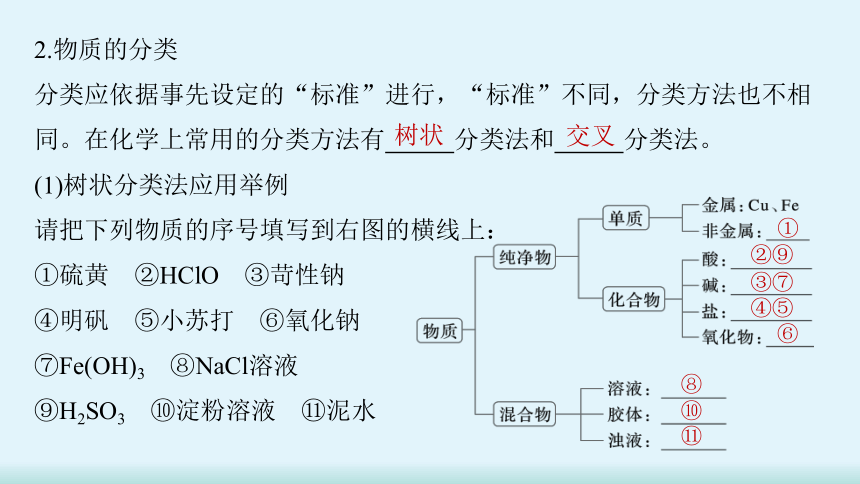
2.物质的分类
分类应依据事先设定的“标准”进行,“标准”不同,分类方法也不相同。在化学上常用的分类方法有 分类法和 分类法。
(1)树状分类法应用举例
请把下列物质的序号填写到右图的横线上:
①硫黄 ②HClO ③苛性钠
④明矾 ⑤小苏打 ⑥氧化钠
⑦Fe(OH)3 ⑧NaCl溶液
⑨H2SO3 ⑩淀粉溶液 泥水
树状
交叉
①
②⑨
③⑦
④⑤
⑥
⑧
⑩
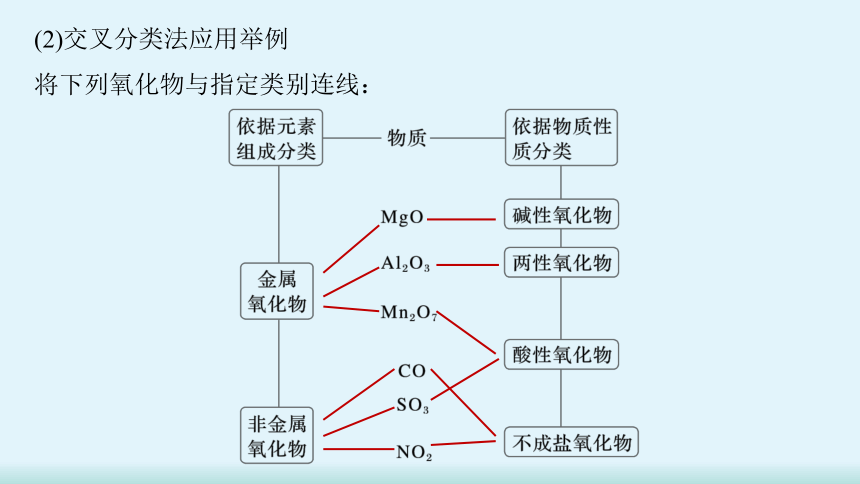
(2)交叉分类法应用举例
将下列氧化物与指定类别连线:
1.由同一种元素组成的物质一定是单质( )
2.Cu、NaCl、SiO2、H2SO4都称为分子式( )
3.金属氧化物一定是碱性氧化物,非金属氧化物一定是酸性氧化物
( )
4.酸性氧化物、碱性氧化物不一定都能与水反应生成相应的酸、碱
( )
5.酸溶于水一定能电离出H+,但能电离出H+的不一定是酸( )
6.CO2、NO2都能和水反应生成酸,故两者都是酸性氧化物( )
×
√
√
×
×
×
氧化物的再分类
(1)酸性氧化物:与碱作用只生成一种盐和水的氧化物。(2)碱性氧化物。(3)两性氧化物。(4)不成盐氧化物:既不能与酸也不能与碱反应生成(相应价态的)盐和水的氧化物。例如NO、CO等。(5)过氧化物:含有过氧键(—O—O—)的氧化物。例如H2O2、Na2O2、CaO2等。
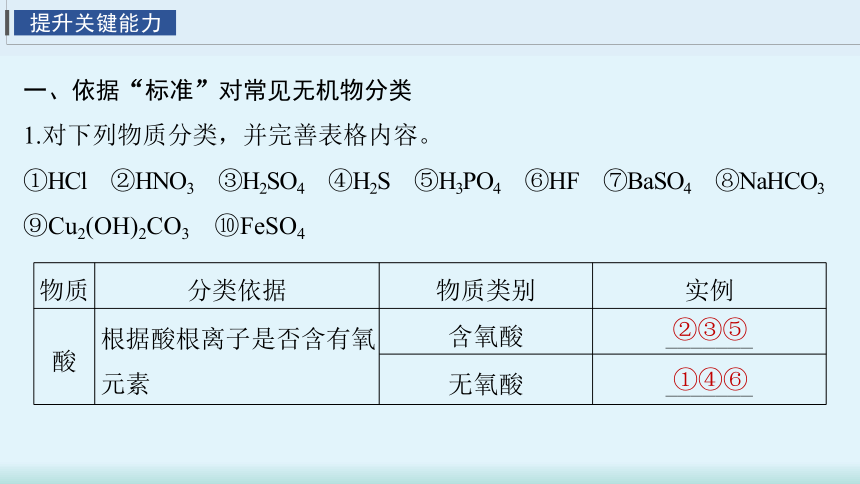
一、依据“标准”对常见无机物分类
1.对下列物质分类,并完善表格内容。
①HCl ②HNO3 ③H2SO4 ④H2S ⑤H3PO4 ⑥HF ⑦BaSO4 ⑧NaHCO3 ⑨Cu2(OH)2CO3 ⑩FeSO4
提升关键能力
物质 分类依据 物质类别 实例
酸 根据酸根离子是否含有氧元素 含氧酸 _______
无氧酸 _______
②③⑤
①④⑥
①HCl ②HNO3 ③H2SO4 ④H2S ⑤H3PO4 ⑥HF ⑦BaSO4 ⑧NaHCO3 ⑨Cu2(OH)2CO3 ⑩FeSO4
物质 分类依据 物质类别 实例
酸 根据一定条件下能电离出H+的数目 一元酸 _______
二元酸 _____
三元酸 ___
根据电离程度 强酸 _______
弱酸 _______
根据沸点高低 高沸点酸 _____
低沸点酸 ________
①②⑥
③④
⑤
①②③
④⑤⑥
③⑤
①②④⑥
①HCl ②HNO3 ③H2SO4 ④H2S ⑤H3PO4 ⑥HF ⑦BaSO4 ⑧NaHCO3 ⑨Cu2(OH)2CO3 ⑩FeSO4
物质 分类依据 物质类别 实例
盐 根据生成盐时酸、碱中和反应进行的程度 正盐 _____
酸式盐 ___
碱式盐 ___
⑦⑩
⑧
⑨
二、各物质类别及包含关系判断
2.下列各组物质的分类都正确的是(括号里的是类别) (填字母,下同),都不正确的是 。
A.NaClO(碱式盐)、C2H5OH(碱)、H2SO4(离子化合物)、玻璃钢(金属材料)
B.液氨(氢化物)、NH4Cl(铵盐)、HNO3(含氧酸)、NaOH(强碱)
C.HCl(共价化合物)、CH3COOH(羧酸)、Na2O2(碱性氧化物)、CH3I(卤代烃)
D.NO2(酸性氧化物)、CH3CHO(有机物)、CO(有机物)、CH3COOCH3(酯)
B
A
NaClO不是碱式盐,C2H5OH属于醇类,硫酸是共价化合物,玻璃钢属于复合材料,A全不正确;
C项中Na2O2属于过氧化物,不是碱性氧化物;
D项中NO2和水反应生成硝酸和NO,不属于酸性氧化物,一氧化碳虽然含有碳元素,但属于无机物。
3.如图表示了一些概念之间的从属关系,下列各项不符合图示关系的是
选项 X Y Z
A 硫酸铜 盐 纯净物
B 碱性氧化物 金属氧化物 氧化物
C 酸性氧化物 非金属氧化物 氧化物
D 强电解质 电解质 化合物
√
从组成上分类,氧化物包括金属氧化物和非金属氧化物,但酸性氧化物不一定是非金属氧化物,如Mn2O7等,C项错误。
返回
考点二
物质的性质与转化
1.物质的变化与物质性质的关系
整合必备知识
2.多角度认识物理变化与化学变化
(1)分别从物质变化(宏观)和化学键变化(微观)的视角说明化学变化的特征。
答案
宏观 有新物质生成的是化学变化,反之是物理变化
微观 有旧化学键断裂,同时有新化学键形成的是化学变化,本质是原子的重新组合
(2)通过对比物理变化和化学变化的不同,回答下列问题:
①石油的分馏 ②煤的干馏 ③钠的焰色试验 ④碘的升华 ⑤氯化铵分解 ⑥蛋白质的变性 ⑦蛋白质的显色反应 ⑧电解食盐水 ⑨CaCl2的潮解 ⑩冰的融化 FeCl3的水解 石油的裂化、裂解 蛋白质的盐析 食物的缓慢氧化 同素异形体间的转化
其中属于物理变化的是 (填序号,下同);属于化学变化的是 。
①③④⑨⑩
②⑤⑥⑦⑧
3.化学反应的分类
(1)按反应物、生成物的种类及数目:化合反应、分解反应、置换反应、复分解反应。
(2)按反应中 :离子反应、非离子反应。
(3)按反应中 :氧化还原反应、非氧化还原反应。
(4)按反应进行的程度和方向: 、 。
(5)按反应的能量变化: 、 。
有无离子参与
有无电子转移
可逆反应
不可逆反应
吸热反应
放热反应
4.不同类别的无机物之间的转化
(1)金属单质及其化合物的转化
金属单质 碱性氧化物 碱 盐
如:Na Na2O NaOH Na2SO4
符合上述转化关系的常见金属有Na、K、Ca、Ba等,但Mg、Fe、Al、Cu等不符合上述转化关系。
(2)非金属单质及其化合物的转化
非金属单质 酸性氧化物 酸 盐
如:S SO2 H2SO3 Na2SO3
符合上述转化关系的常见非金属有C、S、P等,但N、Si等不符合上述转化关系。
1.从海水中提取物质都必须通过化学反应才能实现( )
2.点燃爆竹后,硫燃烧生成SO3( )
3.232Th转化成233Th是化学变化( )
4.石墨在一定条件下转化为金刚石是化学变化( )
5.判断下列转化能否实现,能实现的打“√”,不能实现的打“×”。
①SiO2 H2SiO3( )
②SO3 H2SO4( )
③Fe2O3 Fe(OH)3( )
④BaO Ba(OH)2( )
×
√
×
×
×
×
√
√
一、生产、生活中的物质变化
1.(2024·连云港模拟)化学与生活息息相关。下列做法不涉及化学变化的是
A.用过氧乙酸对居住环境杀菌消毒
B.用活性炭除去冰箱里的异味
C.用去氧剂保鲜食品袋里的食品
D.用食醋清洗金属器皿表面的锈迹
√
提升关键能力
用过氧乙酸对居住环境杀菌消毒,利用过氧乙酸的强氧化性,发生化学变化,A不符合题意;
活性炭具有强吸附性,可吸附异味气体分子,不涉及化学变化,B符合题意;
用去氧剂保鲜食品袋里的食品,去氧剂能与氧气反应,防止食品被氧化,发生化学变化,C不符合题意;
用食醋清洗金属器皿表面的锈迹,发生化学变化,D不符合题意。
2.古诗词富载化学知识,下列古诗词的描述中不涉及化学变化的是
A.《诗经·周颂·良耜》中描述农民生产的情形:“荼蓼(杂草)朽(腐烂)止,
黍稷茂止”
B.岑参在《白雪歌送武判官归京》中描述雪景:“忽如一夜春风来,千
树万树梨花开”
C.李白在《秋浦歌》中描述冶炼工人夜间劳动的场景:“炉火照天地,
红星乱紫烟”
D.李商隐在《无题》中感言:“春蚕到死丝方尽,蜡炬成灰泪始干”
√
“荼蓼(杂草)朽(腐烂)止,黍稷茂止”,杂草腐烂过程中有新物质生成,属于化学变化,故A不符合题意;
“忽如一夜春风来,千树万树梨花开”,过程中无新物质生成,属于物理变化,故B符合题意;
“炉火照天地,红星乱紫烟”是我国古代劳动人民“冶炼金属”的过程,有新物质生成,属于化学变化,故C不符合题意;
“春蚕到死丝方尽,蜡炬成灰泪始干”,蜡烛燃烧有新物质生成,属于化学变化,故D不符合题意。
二、物质间的转化
3.(2020·江苏,10)下列选项所示的物质间转化均能实现的是
A.NaCl(aq) Cl2(g) 漂白粉(s)
B.NaCl(aq) NaHCO3(s) Na2CO3(s)
C.NaBr(aq) Br2(aq) I2(aq)
D.Mg(OH)2(s) MgCl2(aq) Mg(s)
√
由Cl2制备漂白粉应通入石灰乳而不是石灰水中,A项错误;
向氯化钠溶液中通入二氧化碳,无法制取碳酸氢钠固体,B项错误;
电解MgCl2溶液得不到Mg,D项错误。
三、基于物质类别预测陌生物质的性质
4.已知次磷酸(H3PO2)是一元中强酸,请写出其与足量氢氧化钠溶液反应的化学方程式: 。
H3PO2+NaOH===NaH2PO2+H2O
5.已知Be(OH)2与Al(OH)3都属于两性氢氧化物,写出Be(OH)2分别溶于NaOH溶液、盐酸的化学方程式:
(1) 。
(2) 。
Be(OH)2+2NaOH===Na2[Be(OH)4]
Be(OH)2+2HCl===BeCl2+2H2O
返回
考点三
分散系 胶体
1.分散系
(1)概念:把一种(或多种)物质以粒子形式分散到另一种(或多种)物质中所形成的混合物。
(2)分类:根据 的大小。
整合必备知识
分散质粒子直径
溶液
胶体
浊液
2.胶体
(1)分类
请把下列物质的序号填到对应的横线上:
①Fe(OH)3胶体 ②云 ③烟水晶 ④雾 ⑤蛋白质溶液 ⑥烟 ⑦有色玻璃
气溶胶: ;液溶胶: ;固溶胶: 。
②④⑥
①⑤
③⑦
(2)性质与应用
3.三种分散系的比较
分散系 溶液 胶体 浊液
分散质微粒成分 离子或小分子 大分子或离子集合体 巨大分子或离子集合体
分散质粒子直径大小 ______ _________ ________
稳定性 稳定 介稳定 不稳定
分散质能否透过滤纸或半透膜 均能 能透过滤纸,不能透过半透膜 均不能
鉴别 _____________ _____________ _______________
<1 nm
1~100 nm
>100 nm
无丁达尔效应
有丁达尔效应
静置沉淀或分层
1.可用过滤的方法将胶体粒子与分散剂分开( )
2.胶体不一定是液态,胶体的丁达尔效应属于物理变化( )
3.将1 mL 1 mol·L-1 FeCl3溶液滴入沸水中制备Fe(OH)3胶体,若FeCl3完全水解,则可制得的Fe(OH)3胶体粒子数少于0.001NA
( )
4.利用丁达尔效应可区分蛋白质溶液和食盐水( )
×
√
√
√
1.Fe(OH)3胶体的制备。
(1)制备方法:向沸水中逐滴加入 ,继续煮沸至液体呈 ,停止加热,即制得Fe(OH)3胶体。
(2)制备原理: (用化学方程式表示)。
提升关键能力
饱和FeCl3溶液
红褐色
FeCl3+3H2O Fe(OH)3(胶体)+3HCl
2.用Fe(OH)3胶体进行下列实验。
(1)判断是否为Fe(OH)3胶体的简单方法是 。
(2)将其装入U形管中,用石墨电极接通直流电,通电一段时间后,发现阴极附近的颜色加深,这说明 ,这种现象称为 。
(3)向其中加入饱和(NH4)2SO4溶液发生的现象是 ,原因是 。
丁达尔效应
Fe(OH)3胶体粒子带正电荷
电泳
产生红褐色沉淀
电解质溶液使胶体发生了聚沉
(4)向其中滴入过量稀硫酸,现象是 ,其原因是______________________________________________________
。
(5)提纯此分散系常用的方法是 。
先出现红褐色沉淀,后沉淀溶解
开始加入稀硫酸时,胶体发生聚沉生成Fe(OH)3沉淀,硫酸过量时又会使沉淀溶解
渗析
返回
LIANZHENTI MINGKAOXIANG
练真题 明考向
1.(2024·新课标卷,7)文房四宝是中华传统文化的瑰宝。下列有关叙述错误的是
A.羊毛可用于制毛笔,主要成分为蛋白质
B.松木可用于制墨,墨的主要成分是单质碳
C.竹子可用于造纸,纸的主要成分是纤维素
D.大理石可用于制砚台,主要成分为硅酸盐
√
羊毛的主要成分是蛋白质,A正确;
松木燃烧产生的烟灰可用来制墨,墨的主要成分是炭黑,是碳元素的一种单质,B正确;
竹子的主要成分是纤维素,可用于造纸,则纸的主要成分也是纤维素,C正确;
大理石的主要成分为碳酸钙,D错误。
2.(2025·云南1月适应性测试)科学使用化学品可提升人们生产生活质量。下列说法正确的是
A.有机氯农药防虫害效率高,可大量使用
B.BaCO3可用于中和过多的胃酸,缓解胃部不适
C.苯甲酸钠是一种常用的增味剂,能增加食品的鲜味
D.卤水能使豆浆中的蛋白质聚沉,是制作豆腐常用的凝固剂
√
有机氯农药防虫害效率高,但有机氯有毒,危害人体健康,应该合理使用有机氯农药,不能大量使用,故A错误;
BaCO3溶于盐酸,钡离子能使蛋白质变性,引起人体中毒,不能用BaCO3中和过多的胃酸,故B错误;
苯甲酸钠是一种防腐剂,可以抑制细菌的滋生,防止食品变质,不是增味剂,不能增加食品的鲜味,故C错误;
卤水中含电解质,在豆浆中加入卤水能使蛋白质发生聚沉,从而使豆浆凝固,是制作豆腐常用的凝固剂,故D正确。
3.(2024·天津,1)关于天津博物馆典藏文物的相关化学知识,判断错误的是
A.太保鼎(西周)的材质是青铜,青铜属于合金
B.《雪景寒林图》(北宋)的材质是绢(蚕丝织品),绢属于天然高分子制品
C.白釉龙柄联腹传瓶(隋),其材质是陶瓷,陶瓷属于无机非金属材料
D.乾隆款珐琅彩芍药雉鸡图玉壶春瓶(清),其珐琅彩由矿物颜料经高温
烧制而成,该颜料属于有机化合物
√
青铜是铜锡合金,A正确;
绢(蚕丝织品)主要成分是蛋白质,属于天然有机高分子,B正确;
陶瓷是硅酸盐产品,属于无机非金属材料,C正确;
珐琅彩由矿物颜料经高温烧制而成,属于无机化合物,D错误。
4.(2024·安徽,4)下列选项中的物质能按图示路径在自然界中转化。且甲和水可以直接生成乙的是
选项 甲 乙 丙
A Cl2 NaClO NaCl
B SO2 H2SO4 CaSO4
C Fe2O3 Fe(OH)3 FeCl3
D CO2 H2CO3 Ca(HCO3)2
√
NaClO(乙)与浓盐酸反应生成NaCl(丙)、Cl2和H2O,NaCl(丙)电解生成Cl2(甲),Cl2(甲)与水反应生成HClO和HCl,无法直接生成NaClO(乙),故A项不符合;
H2SO4(乙)与Ca(OH)2反应生成CaSO4(丙)和水,
CaSO4(丙)很稳定,加热至1 200 ℃以上分解,生成CaO、SO2(甲)和O2,SO2(甲)与水反应生成H2SO3而不是H2SO4(乙),故B项不符合;
Fe(OH)3(乙)与盐酸反应生成FeCl3(丙)和水,FeCl3(丙)不能直接转化为Fe2O3(甲),Fe2O3(甲)与水不反应,不能生成Fe(OH)3沉淀,故C项不符合;CO2(甲)与水反应生成H2CO3(乙),H2CO3(乙)与CaCO3反应生成Ca(HCO3)2(丙),Ca(HCO3)2受热分解生成CO2气体,故D项符合。
A.a可使灼热的铜变黑 B.b可与红热的铁产生气体
C.c可使燃烧的镁条熄灭 D.d可使湿润的淀粉碘化钾试纸变蓝
5.(2024·重庆,8)单质M的相关转化如下所示。下列说法错误的是
√
碱溶液与单质d反应生成漂白液,故单质d为Cl2,碱溶液是NaOH溶液;NaOH溶液与氧化物c(适量)反应得纯碱溶液,故氧化物c为CO2;单质M与氧化物b反应得NaOH,故单质M为Na,氧化物b为H2O;Na与单质a反应得氧化物,因此单质a为O2,据此回答。a为O2,O2可与灼热的铜反应生成黑色的氧化铜,A正确;
b为H2O,水蒸气可与红热的铁在高温下反应生成四氧化三铁和氢气,B正确;
c为CO2,镁条在CO2中燃烧生成氧化镁和碳,燃烧的镁条不熄灭,C错误;
d为Cl2,Cl2可与碘化钾反应生成碘单质,碘单质能使湿润的淀粉碘化钾试纸变蓝,D正确。
返回
KESHIJINGLIAN
课时精练
对一对
题号 1 2 3 4 5 6 7 8
答案 A B B B D C D C
题号 9 10 11 12 13 答案 B C D C B 答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
14.
(1)都是氧化物(答案合理即可)
(2)二氧化碳是由不同种元素组成的纯净物,而氮气是由同种元素组成的纯净物
(3)2NO+2CO 2CO2+N2 15∶22
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
15.
(1)盐、铜盐、碱式盐(或碳酸盐)
(2)Cu2(OH)2CO3+4HCl===2CuCl2+3H2O+CO2↑
(3)Cu(OH)2 CuO+H2O CuO+H2 Cu+H2O (4)① ②③ ④
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
16.
(1)FeCl2、Fe(OH)2 (2)②③⑤ 4Fe(OH)2+O2+2H2O===4Fe(OH)3 (3)1~100 nm 丁达尔效应 (4)Fe2O3或Fe3O4 FeSO4·7H2O分解生成SO2、SO3、H2O和X,部分S元素被还原,则Fe元素应被氧化,所以X可能为Fe2O3或Fe3O4 (5)bc
1.(2022·浙江6月选考,1)下列消毒剂的有效成分属于盐的是
A.高锰酸钾溶液 B.过氧乙酸溶液
C.双氧水 D.医用酒精
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
2.(2024·吉林模拟预测)中华文化源远流长,化学与文化传承密不可分。下列说法正确的是
A.“曾青涂铁,铁赤色如铜”,涉及的反应能证明氧化性:Fe3+>Cu2+
B.“绿蚁新醅酒,红泥小火炉”,制作火炉的“红泥”中含氧化铁
C.古陶瓷修复时所用的熟石膏,其成分为Ca(OH)2
D.“九秋风露越窑开,夺得千峰翠色来”,“翠色”是因为成分中含有
氧化亚铜
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
“曾青涂铁,铁赤色如铜”,涉及的反应为铁和铜离子反应生成铜和亚铁离子,能证明氧化性:Cu2+>Fe2+,A错误;
氧化铁为红棕色固体,火炉的“红泥”中含氧化铁,B正确;
古陶瓷修复所用的熟石膏,其化学成分为2CaSO4·H2O,C错误;
“翠色”为青色或绿色,而氧化亚铜为砖红色,“翠色”不可能来自氧化亚铜,D错误。
答案
3.下列物质分类正确的组合是
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
选项 混合物 化合物 单质 盐
A 稀盐酸 NaOH溶液 石墨 NaCl
B 水玻璃 KNO3晶体 O2 Na2CO3
C 空气 澄清石灰水 铁 CaCO3
D CuSO4·5H2O CaCl2 水银 CaO
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
氢氧化钠溶液属于混合物,故A错误;
澄清石灰水为氢氧化钙的水溶液,属于混合物,故C错误;
CuSO4·5H2O属于纯净物,CaO不属于盐,故D错误。
答案
4.(2024·武汉一模)化学创造美好生活,下列说法错误的是
A.化妆品中添加甘油可起到保湿作用
B.手机芯片与光导纤维化学成分相同
C.折叠手机柔性屏使用的原材料聚酰亚胺属于有机高分子材料
D.节日绚丽的烟花与原子核外电子跃迁过程中的能量变化有关
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
手机芯片材质是硅单质,光导纤维材质是二氧化硅,故B错误;
折叠手机柔性屏使用的原材料聚酰亚胺是聚合物,属于有机高分子材料,故C正确;
当电子由较高能量的激发态跃迁到较低能量的激发态乃至基态时,多余的能量以光的形式释放出来,因此可以看到绚丽的烟花,故D正确。
5.2023年诺贝尔化学奖授予发现和合成量子点材料的三位科学家。将富含维生素、蛋白质、糖类的有机物经高温碳化后可以获得直径为2~10 nm碳量子点材料。下列说法正确的是
A.维生素、蛋白质、糖类组成元素相同
B.碳量子点材料属于有机高分子材料
C.高温碳化有机物属于物理变化
D.将碳量子点材料分散到溶液中所形成的分散系为胶体
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
6.(2024·西安统考一模)某病毒由蛋白质外壳和单链核酸组成,如图所示,直径为60~140 nm。下列说法错误的是
A.病毒扩散到空气中可能形成胶体
B.病毒的蛋白质外壳中存在氢键
C.止咳祛痰药盐酸氨溴索的化学式为
C13H18Br2N2O·HCl,属于混合物
D.ClO2泡腾片和酒精均可灭杀该病毒,二者消毒原理不同
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
分散质粒子直径在1~100 nm之间的分散系是胶体,
该病毒直径为60~140 nm,扩散到空气中可能形成
胶体,A正确;
蛋白质分子中有氢键,如两个氨基酸之间的氢键、
二级结构后的盘旋和折叠,B正确;
盐酸氨溴索属于纯净物,C错误;
ClO2利用强氧化性消毒杀菌,酒精的杀菌原理主要是使蛋白质变性,二者消毒原理不同,D正确。
7.《本草述钩元》中的“石碱”条目下记载“采蒿蓼之属,开窖浸水,漉起,晒干烧灰,以原水淋汁……连汁货之四方,浣衣发面”。下列说法正确的是
A.“石碱”是一种强碱,成分为NaOH
B.蒿蓼中含有纤维素,分子式为(C6H10O5)n,属于纯净物
C.制取过程中包括浸取、灼烧、过滤、萃取等操作
D.“石碱”可用于浣衣,是由于其溶液显碱性,可以洗去油污
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
“晒干烧灰”说明“石碱”成分来源于植物烧成的灰中,“以原水淋汁”证明是溶于水的碳酸盐,故A错误;
纤维素的分子式为(C6H10O5)n,属于高分子,属于混合物,故B错误;
制取过程中包括浸取、灼烧、过滤等操作,没有萃取,故C错误;
“石碱”可用于浣衣,是由于碳酸根离子水解,溶液显碱性,油污在碱性溶液中水解生成易溶于水的物质,可以洗去油污,故D正确。
8.(2025·郑州模拟)科学研究发现液态水或存在第二形态,当水被加热到40~60 ℃时,它的导热性、折射率、导电性等属性也会发生改变。下列说法正确的是
A.氢、氧两种元素只能组成H2O
B.导热性、折射率、导电性属于水的化学性质
C.0 ℃时冰的密度比液态水的密度小
D.液态水两种形态间的转化属于化学变化
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
A项,氢、氧两种元素除组成H2O外还可以组成H2O2,错误;
B项,导热性、折射率、导电性属于水的物理性质,错误;
C项,冰浮在水上,说明冰的密度小于液态水,正确;
D项,液态水两种形态间的转化属于物理变化,错误。
9.(2024·河北模拟预测)化学在生产、生活、能源、环境等领域应用广泛,下列说法错误的是
A.工业上电解熔融态的氯化镁制取单质镁
B.发酵粉中的碳酸钠与固态酸发生反应生成二氧化碳使食品变膨松
C.钠离子电池储能电站的投运有利于解决光伏发电的间歇性、波动性等
问题
D.发展太阳能制氢技术,减少化石燃料的使用,有利于减缓温室效应
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
工业上从海水中提取氯化镁,再电解熔融态的氯化镁制取单质镁,故A项正确;
发酵粉的主要成分为碳酸氢钠、酒石酸,使用时,碳酸氢钠与固态酸发生反应生成二氧化碳使食品变膨松,故B项错误;
光伏发电受昼夜交替、天气阴晴等因素的影响,具有间歇性、波动性等问题,钠离子电池储能电站的投运有利于解决这些问题,故C项正确;发展太阳能制氢技术,减少化石燃料的使用,可控制二氧化碳的排放,有利于减缓温室效应,故D项正确。
10.下列关于各物质的所属类别及性质的描述正确的是
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
选项 A B C D
物质 NO2 NaCl 生铁 氢氧化铁胶体
类别 酸性氧化物 离子化合物 合金 电解质
性质 与水反应 熔融态不导电 易发生电化学腐蚀 能产生丁达尔效应
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
NO2不是酸性氧化物,故A错误;
NaCl是离子化合物,熔融态能导电,故B错误;
生铁是铁碳合金,在潮湿环境中构成原电池,易发生电化学腐蚀,故C正确;
氢氧化铁胶体是混合物,既不是电解质也不是非电解质,故D错误。
11.我国科学家研制出的“全碳气凝胶”固体材料“碳海绵”,是迄今世界上最轻的材料。下列关于“碳海绵”的说法错误的是
A.光束照射时可观察到丁达尔效应
B.常温下具有良好的耐酸、耐碱性
C.可用于处理海面的漏油
D.其净水过程是化学变化
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
“全碳气凝胶”固体材料“碳海绵”属于胶体,因此光束照射时可观察到丁达尔效应,A正确;
由于胶体具有吸附性,因此可用于处理海面的漏油,C正确;
其净水过程利用的是吸附原理,没有产生新物质,因此是物理变化,D错误。
12.已知甲、乙、丙有如图所示的转化关系(部分物质和反应条件已略去,“→”表示一步反应即可实现),下列各组物质不满足图示转化关系的是
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
选项 甲 乙 丙
A NaHCO3 Na2CO3 NaOH
B SiO2 Si Na2SiO3
C Fe2O3 Fe(OH)3 FeCl3
D S Na2SO3 Na2SO4
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
由2NaHCO3 Na2CO3+CO2↑+H2O,Na2CO3+CO2+H2O===2NaHCO3,Na2CO3+Ba(OH)2===2NaOH+BaCO3↓,满足图示关系,选项A不符合题意;
由SiO2+2C Si+2CO↑,Si+O2 SiO2,Si+
2NaOH+H2O===Na2SiO3+2H2↑,满足图示关系,选项B不符合题意;
Fe2O3无法直接生成Fe(OH)3,不满足图示关系,选项C符合题意;
由3S+6NaOH===Na2SO3+2Na2S+3H2O,Na2SO3+3H2S===Na2S+3S↓+
3H2O,2Na2SO3+O2===2Na2SO4,满足图示关系,选项D不符合题意。
13.(2025·保定模拟)下列说法错误的是
A.氦气属于稀有气体,是空气的成分
之一
B.由硅、碳、氧、硫等元素经过一系
列变化能变成铁,该过程属于化学变化
C.固定太空电梯的缆绳材料最有可能是碳纳米管(如图1),碳纳米管与C60
互为同素异形体
D.取a g偏二甲肼(火箭推进剂)在6.4 g氧气中恰好完全反应,如图2,则偏
二甲肼中不含氧
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
原子是化学变化中的最小微粒,化学变化中原子核不会变,由硅、碳、氧、硫等元素经过一系列变化能变成铁,该过程属于核聚变,故B错误;
碳纳米管与C60属于碳的不同单质,互为同素异形体,故C正确;
水中氧元素的质量为3.6 g×=3.2 g,二氧化碳中氧元素的质量为4.4 g
×=3.2 g,3.2 g+3.2 g=6.4 g,故偏二甲肼中不含氧元素,故D正确。
14.在宏观—微观—符号之间建立联系,是化学学科特有的思维方式。汽车尾气是造成大气污染的主要原因之一,在汽车排气管上安装“催化转换器”便可以使汽车的尾气转换成无毒气体。用 表示碳原子,用○表示氧原子,用 表示氮原子,如图为气体转换的微观过程。请根据图示回答下列问题:
(1)A、B、C三种物质可以归为一类的依
据是 。
(2)将C归为化合物,将D归为单质的理由是_________________________
。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
都是氧化物(答案合理即可)
二氧化碳是由不同种元素组成的纯净物,而氮气是由同种元素组成的纯净物
(3)图示反应用化学方程式表示为 。化学变化过程中消耗的A物质和生成的C物质的质量比为 。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
2NO+2CO 2CO2+N2
15∶22
根据题意及图示可知,A为NO、B为CO、C为CO2、D为N2。
15.铜器久置于空气中会和空气中的水蒸气、CO2、O2作用产生“绿锈”,该“绿锈”俗称“铜绿”,又称“孔雀石”[化学式为Cu2(OH)2CO3],“铜绿”能与酸反应生成铜盐、CO2和H2O。某同学利用下述系列反应实现了“铜→铜绿→……→铜”的转化。
铜 铜绿 A Cu(OH)2 B Cu
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
(1)从三种不同分类标准回答,“铜绿”属于哪类物质:______________
。
(2)请写出“铜绿”与盐酸反应的化学方程式:______________________
。
盐、铜盐、碱
式盐(或碳酸盐)
Cu2(OH)2CO3+4HCl===
2CuCl2+3H2O+CO2↑
铜 铜绿 A Cu(OH)2 B Cu
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
(3)写出④、⑤的化学方程式:
④ ;⑤ 。
(4)上述转化过程中属于化合反应的是 (填序号,下同),属于复分解反应的是 ,属于分解反应的是 。
Cu(OH)2 CuO+H2O
CuO+H2 Cu+H2O
①
②③
④
16.铁广泛应用于人类的生产、生活。
Ⅰ.铁及其化合物存在如图甲转化关系(部分反应物和反应条件已略去),回答下列问题。
(1)a、b、c三种物质中属于电解质的是______
(填化学式)。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
FeCl2、
Fe(OH)2
根据物质类别和铁元素的化合价可知,a为Fe,b为FeCl2,e为FeCl3,c为Fe(OH)2,d为Fe(OH)3。a、b、c三种物质中属于电解质的是FeCl2、Fe(OH)2。
(2)①~⑤反应中,既是化合反应又是氧化还原反应的是 (填序号)。写出⑤的化学方程式: 。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
②③⑤
4Fe(OH)2+O2+2H2O===4Fe(OH)3
①置换反应;②氯气与氯化亚铁反应生成氯化铁;③铁在氯气中点燃生成氯化铁;④反应中Fe的化合价没有发生变化;⑤氢氧化亚铁与氧气、水反应生成氢氧化铁;故①~⑤反应中,既是化合反应又是氧化还原反应的有②③⑤。
(3)将e的浓溶液滴加到沸水中可得到红褐色液体,该液体属于一种特殊的分散系。该分散系中分散质的微粒直径为 。鉴别e的浓溶液与该分散系所用方法的原理为
。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
1~100 nm
丁达尔效应
Ⅱ.明代《徐光启手迹》记载了以绿矾(FeSO4·7H2O)为原料制备硝酸的方法,其主要流程如图乙。
(4)X为铁的氧化物,X的化学式可能为
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
,判断依据为______________________________________
。
(5)③利用浓硫酸的性质为 (填字母)。
a.强氧化性 b.高沸点
c.酸性 d.脱水性
FeSO4·7H2O分解生成SO2、SO3、H2O和X,部分S元素被还原,则Fe元素应被氧化,所以X可能为Fe2O3或Fe3O4
Fe2O3或Fe3O4
bc
返回
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
③中浓硫酸与硝酸钾发生复分解反应生成硝酸,硝酸沸点低,易挥发,浓硫酸的沸点高,难挥发,利用了浓硫酸的高沸点和酸性。
本课结束
化学大一轮复习
第一章 第1讲
物质的组成、性质和转化
复习目标
1.认识元素可以组成不同种类的物质,根据物质的组成和性质可以对物质进行分类。
2.熟知同类物质具有相似的性质,一定条件下各类物质可以相互转化。
3.了解胶体是一种常见的分散系,了解溶液和胶体的区别。
课时精练
考点一 物质的组成与分类
考点二 物质的性质与转化
考点三 分散系 胶体
练真题 明考向
内容索引
考点一
物质的组成与分类
1.物质的组成——元素与物质的关系
整合必备知识
游离
原子
分子
化合
原子
分子
离子
(1)同素异形体
①定义:由同一种元素形成的 。
②性质:物理性质不同,化学性质有差异。同素异形体之间在一定条件下可以相互转化,这种转化是 变化。
③常见元素的同素异形体
氧元素: ;碳元素: ;磷元素: 。
(2)纯净物和混合物
纯净物:由同种单质或化合物组成的物质。
混合物:由几种不同的单质或化合物组成的物质。
几种性质不同的单质
化学
O2、O3
金刚石、石墨、C60
白磷、红磷
[应用举例]
现有下列物质:
①冰水混合物 ②爆鸣气 ③铝热剂 ④普通玻璃 ⑤水玻璃 ⑥有机玻璃 ⑦漂白粉 ⑧TNT ⑨H2SO4 ⑩含氧40%的氧化镁 花生油 福尔马林 密封保存的NO2气体 液氯 王水
KAl(SO4)2·12H2O 分子式为C5H10的烃 分子式为C7H8的芳香烃
其中一定为纯净物的是 (填序号,下同);一定为混合物的是 ;可能是纯净物,也可能是混合物的是 。
①⑧⑨⑩
②③④⑤⑥⑦
2.物质的分类
分类应依据事先设定的“标准”进行,“标准”不同,分类方法也不相同。在化学上常用的分类方法有 分类法和 分类法。
(1)树状分类法应用举例
请把下列物质的序号填写到右图的横线上:
①硫黄 ②HClO ③苛性钠
④明矾 ⑤小苏打 ⑥氧化钠
⑦Fe(OH)3 ⑧NaCl溶液
⑨H2SO3 ⑩淀粉溶液 泥水
树状
交叉
①
②⑨
③⑦
④⑤
⑥
⑧
⑩
(2)交叉分类法应用举例
将下列氧化物与指定类别连线:
1.由同一种元素组成的物质一定是单质( )
2.Cu、NaCl、SiO2、H2SO4都称为分子式( )
3.金属氧化物一定是碱性氧化物,非金属氧化物一定是酸性氧化物
( )
4.酸性氧化物、碱性氧化物不一定都能与水反应生成相应的酸、碱
( )
5.酸溶于水一定能电离出H+,但能电离出H+的不一定是酸( )
6.CO2、NO2都能和水反应生成酸,故两者都是酸性氧化物( )
×
√
√
×
×
×
氧化物的再分类
(1)酸性氧化物:与碱作用只生成一种盐和水的氧化物。(2)碱性氧化物。(3)两性氧化物。(4)不成盐氧化物:既不能与酸也不能与碱反应生成(相应价态的)盐和水的氧化物。例如NO、CO等。(5)过氧化物:含有过氧键(—O—O—)的氧化物。例如H2O2、Na2O2、CaO2等。
一、依据“标准”对常见无机物分类
1.对下列物质分类,并完善表格内容。
①HCl ②HNO3 ③H2SO4 ④H2S ⑤H3PO4 ⑥HF ⑦BaSO4 ⑧NaHCO3 ⑨Cu2(OH)2CO3 ⑩FeSO4
提升关键能力
物质 分类依据 物质类别 实例
酸 根据酸根离子是否含有氧元素 含氧酸 _______
无氧酸 _______
②③⑤
①④⑥
①HCl ②HNO3 ③H2SO4 ④H2S ⑤H3PO4 ⑥HF ⑦BaSO4 ⑧NaHCO3 ⑨Cu2(OH)2CO3 ⑩FeSO4
物质 分类依据 物质类别 实例
酸 根据一定条件下能电离出H+的数目 一元酸 _______
二元酸 _____
三元酸 ___
根据电离程度 强酸 _______
弱酸 _______
根据沸点高低 高沸点酸 _____
低沸点酸 ________
①②⑥
③④
⑤
①②③
④⑤⑥
③⑤
①②④⑥
①HCl ②HNO3 ③H2SO4 ④H2S ⑤H3PO4 ⑥HF ⑦BaSO4 ⑧NaHCO3 ⑨Cu2(OH)2CO3 ⑩FeSO4
物质 分类依据 物质类别 实例
盐 根据生成盐时酸、碱中和反应进行的程度 正盐 _____
酸式盐 ___
碱式盐 ___
⑦⑩
⑧
⑨
二、各物质类别及包含关系判断
2.下列各组物质的分类都正确的是(括号里的是类别) (填字母,下同),都不正确的是 。
A.NaClO(碱式盐)、C2H5OH(碱)、H2SO4(离子化合物)、玻璃钢(金属材料)
B.液氨(氢化物)、NH4Cl(铵盐)、HNO3(含氧酸)、NaOH(强碱)
C.HCl(共价化合物)、CH3COOH(羧酸)、Na2O2(碱性氧化物)、CH3I(卤代烃)
D.NO2(酸性氧化物)、CH3CHO(有机物)、CO(有机物)、CH3COOCH3(酯)
B
A
NaClO不是碱式盐,C2H5OH属于醇类,硫酸是共价化合物,玻璃钢属于复合材料,A全不正确;
C项中Na2O2属于过氧化物,不是碱性氧化物;
D项中NO2和水反应生成硝酸和NO,不属于酸性氧化物,一氧化碳虽然含有碳元素,但属于无机物。
3.如图表示了一些概念之间的从属关系,下列各项不符合图示关系的是
选项 X Y Z
A 硫酸铜 盐 纯净物
B 碱性氧化物 金属氧化物 氧化物
C 酸性氧化物 非金属氧化物 氧化物
D 强电解质 电解质 化合物
√
从组成上分类,氧化物包括金属氧化物和非金属氧化物,但酸性氧化物不一定是非金属氧化物,如Mn2O7等,C项错误。
返回
考点二
物质的性质与转化
1.物质的变化与物质性质的关系
整合必备知识
2.多角度认识物理变化与化学变化
(1)分别从物质变化(宏观)和化学键变化(微观)的视角说明化学变化的特征。
答案
宏观 有新物质生成的是化学变化,反之是物理变化
微观 有旧化学键断裂,同时有新化学键形成的是化学变化,本质是原子的重新组合
(2)通过对比物理变化和化学变化的不同,回答下列问题:
①石油的分馏 ②煤的干馏 ③钠的焰色试验 ④碘的升华 ⑤氯化铵分解 ⑥蛋白质的变性 ⑦蛋白质的显色反应 ⑧电解食盐水 ⑨CaCl2的潮解 ⑩冰的融化 FeCl3的水解 石油的裂化、裂解 蛋白质的盐析 食物的缓慢氧化 同素异形体间的转化
其中属于物理变化的是 (填序号,下同);属于化学变化的是 。
①③④⑨⑩
②⑤⑥⑦⑧
3.化学反应的分类
(1)按反应物、生成物的种类及数目:化合反应、分解反应、置换反应、复分解反应。
(2)按反应中 :离子反应、非离子反应。
(3)按反应中 :氧化还原反应、非氧化还原反应。
(4)按反应进行的程度和方向: 、 。
(5)按反应的能量变化: 、 。
有无离子参与
有无电子转移
可逆反应
不可逆反应
吸热反应
放热反应
4.不同类别的无机物之间的转化
(1)金属单质及其化合物的转化
金属单质 碱性氧化物 碱 盐
如:Na Na2O NaOH Na2SO4
符合上述转化关系的常见金属有Na、K、Ca、Ba等,但Mg、Fe、Al、Cu等不符合上述转化关系。
(2)非金属单质及其化合物的转化
非金属单质 酸性氧化物 酸 盐
如:S SO2 H2SO3 Na2SO3
符合上述转化关系的常见非金属有C、S、P等,但N、Si等不符合上述转化关系。
1.从海水中提取物质都必须通过化学反应才能实现( )
2.点燃爆竹后,硫燃烧生成SO3( )
3.232Th转化成233Th是化学变化( )
4.石墨在一定条件下转化为金刚石是化学变化( )
5.判断下列转化能否实现,能实现的打“√”,不能实现的打“×”。
①SiO2 H2SiO3( )
②SO3 H2SO4( )
③Fe2O3 Fe(OH)3( )
④BaO Ba(OH)2( )
×
√
×
×
×
×
√
√
一、生产、生活中的物质变化
1.(2024·连云港模拟)化学与生活息息相关。下列做法不涉及化学变化的是
A.用过氧乙酸对居住环境杀菌消毒
B.用活性炭除去冰箱里的异味
C.用去氧剂保鲜食品袋里的食品
D.用食醋清洗金属器皿表面的锈迹
√
提升关键能力
用过氧乙酸对居住环境杀菌消毒,利用过氧乙酸的强氧化性,发生化学变化,A不符合题意;
活性炭具有强吸附性,可吸附异味气体分子,不涉及化学变化,B符合题意;
用去氧剂保鲜食品袋里的食品,去氧剂能与氧气反应,防止食品被氧化,发生化学变化,C不符合题意;
用食醋清洗金属器皿表面的锈迹,发生化学变化,D不符合题意。
2.古诗词富载化学知识,下列古诗词的描述中不涉及化学变化的是
A.《诗经·周颂·良耜》中描述农民生产的情形:“荼蓼(杂草)朽(腐烂)止,
黍稷茂止”
B.岑参在《白雪歌送武判官归京》中描述雪景:“忽如一夜春风来,千
树万树梨花开”
C.李白在《秋浦歌》中描述冶炼工人夜间劳动的场景:“炉火照天地,
红星乱紫烟”
D.李商隐在《无题》中感言:“春蚕到死丝方尽,蜡炬成灰泪始干”
√
“荼蓼(杂草)朽(腐烂)止,黍稷茂止”,杂草腐烂过程中有新物质生成,属于化学变化,故A不符合题意;
“忽如一夜春风来,千树万树梨花开”,过程中无新物质生成,属于物理变化,故B符合题意;
“炉火照天地,红星乱紫烟”是我国古代劳动人民“冶炼金属”的过程,有新物质生成,属于化学变化,故C不符合题意;
“春蚕到死丝方尽,蜡炬成灰泪始干”,蜡烛燃烧有新物质生成,属于化学变化,故D不符合题意。
二、物质间的转化
3.(2020·江苏,10)下列选项所示的物质间转化均能实现的是
A.NaCl(aq) Cl2(g) 漂白粉(s)
B.NaCl(aq) NaHCO3(s) Na2CO3(s)
C.NaBr(aq) Br2(aq) I2(aq)
D.Mg(OH)2(s) MgCl2(aq) Mg(s)
√
由Cl2制备漂白粉应通入石灰乳而不是石灰水中,A项错误;
向氯化钠溶液中通入二氧化碳,无法制取碳酸氢钠固体,B项错误;
电解MgCl2溶液得不到Mg,D项错误。
三、基于物质类别预测陌生物质的性质
4.已知次磷酸(H3PO2)是一元中强酸,请写出其与足量氢氧化钠溶液反应的化学方程式: 。
H3PO2+NaOH===NaH2PO2+H2O
5.已知Be(OH)2与Al(OH)3都属于两性氢氧化物,写出Be(OH)2分别溶于NaOH溶液、盐酸的化学方程式:
(1) 。
(2) 。
Be(OH)2+2NaOH===Na2[Be(OH)4]
Be(OH)2+2HCl===BeCl2+2H2O
返回
考点三
分散系 胶体
1.分散系
(1)概念:把一种(或多种)物质以粒子形式分散到另一种(或多种)物质中所形成的混合物。
(2)分类:根据 的大小。
整合必备知识
分散质粒子直径
溶液
胶体
浊液
2.胶体
(1)分类
请把下列物质的序号填到对应的横线上:
①Fe(OH)3胶体 ②云 ③烟水晶 ④雾 ⑤蛋白质溶液 ⑥烟 ⑦有色玻璃
气溶胶: ;液溶胶: ;固溶胶: 。
②④⑥
①⑤
③⑦
(2)性质与应用
3.三种分散系的比较
分散系 溶液 胶体 浊液
分散质微粒成分 离子或小分子 大分子或离子集合体 巨大分子或离子集合体
分散质粒子直径大小 ______ _________ ________
稳定性 稳定 介稳定 不稳定
分散质能否透过滤纸或半透膜 均能 能透过滤纸,不能透过半透膜 均不能
鉴别 _____________ _____________ _______________
<1 nm
1~100 nm
>100 nm
无丁达尔效应
有丁达尔效应
静置沉淀或分层
1.可用过滤的方法将胶体粒子与分散剂分开( )
2.胶体不一定是液态,胶体的丁达尔效应属于物理变化( )
3.将1 mL 1 mol·L-1 FeCl3溶液滴入沸水中制备Fe(OH)3胶体,若FeCl3完全水解,则可制得的Fe(OH)3胶体粒子数少于0.001NA
( )
4.利用丁达尔效应可区分蛋白质溶液和食盐水( )
×
√
√
√
1.Fe(OH)3胶体的制备。
(1)制备方法:向沸水中逐滴加入 ,继续煮沸至液体呈 ,停止加热,即制得Fe(OH)3胶体。
(2)制备原理: (用化学方程式表示)。
提升关键能力
饱和FeCl3溶液
红褐色
FeCl3+3H2O Fe(OH)3(胶体)+3HCl
2.用Fe(OH)3胶体进行下列实验。
(1)判断是否为Fe(OH)3胶体的简单方法是 。
(2)将其装入U形管中,用石墨电极接通直流电,通电一段时间后,发现阴极附近的颜色加深,这说明 ,这种现象称为 。
(3)向其中加入饱和(NH4)2SO4溶液发生的现象是 ,原因是 。
丁达尔效应
Fe(OH)3胶体粒子带正电荷
电泳
产生红褐色沉淀
电解质溶液使胶体发生了聚沉
(4)向其中滴入过量稀硫酸,现象是 ,其原因是______________________________________________________
。
(5)提纯此分散系常用的方法是 。
先出现红褐色沉淀,后沉淀溶解
开始加入稀硫酸时,胶体发生聚沉生成Fe(OH)3沉淀,硫酸过量时又会使沉淀溶解
渗析
返回
LIANZHENTI MINGKAOXIANG
练真题 明考向
1.(2024·新课标卷,7)文房四宝是中华传统文化的瑰宝。下列有关叙述错误的是
A.羊毛可用于制毛笔,主要成分为蛋白质
B.松木可用于制墨,墨的主要成分是单质碳
C.竹子可用于造纸,纸的主要成分是纤维素
D.大理石可用于制砚台,主要成分为硅酸盐
√
羊毛的主要成分是蛋白质,A正确;
松木燃烧产生的烟灰可用来制墨,墨的主要成分是炭黑,是碳元素的一种单质,B正确;
竹子的主要成分是纤维素,可用于造纸,则纸的主要成分也是纤维素,C正确;
大理石的主要成分为碳酸钙,D错误。
2.(2025·云南1月适应性测试)科学使用化学品可提升人们生产生活质量。下列说法正确的是
A.有机氯农药防虫害效率高,可大量使用
B.BaCO3可用于中和过多的胃酸,缓解胃部不适
C.苯甲酸钠是一种常用的增味剂,能增加食品的鲜味
D.卤水能使豆浆中的蛋白质聚沉,是制作豆腐常用的凝固剂
√
有机氯农药防虫害效率高,但有机氯有毒,危害人体健康,应该合理使用有机氯农药,不能大量使用,故A错误;
BaCO3溶于盐酸,钡离子能使蛋白质变性,引起人体中毒,不能用BaCO3中和过多的胃酸,故B错误;
苯甲酸钠是一种防腐剂,可以抑制细菌的滋生,防止食品变质,不是增味剂,不能增加食品的鲜味,故C错误;
卤水中含电解质,在豆浆中加入卤水能使蛋白质发生聚沉,从而使豆浆凝固,是制作豆腐常用的凝固剂,故D正确。
3.(2024·天津,1)关于天津博物馆典藏文物的相关化学知识,判断错误的是
A.太保鼎(西周)的材质是青铜,青铜属于合金
B.《雪景寒林图》(北宋)的材质是绢(蚕丝织品),绢属于天然高分子制品
C.白釉龙柄联腹传瓶(隋),其材质是陶瓷,陶瓷属于无机非金属材料
D.乾隆款珐琅彩芍药雉鸡图玉壶春瓶(清),其珐琅彩由矿物颜料经高温
烧制而成,该颜料属于有机化合物
√
青铜是铜锡合金,A正确;
绢(蚕丝织品)主要成分是蛋白质,属于天然有机高分子,B正确;
陶瓷是硅酸盐产品,属于无机非金属材料,C正确;
珐琅彩由矿物颜料经高温烧制而成,属于无机化合物,D错误。
4.(2024·安徽,4)下列选项中的物质能按图示路径在自然界中转化。且甲和水可以直接生成乙的是
选项 甲 乙 丙
A Cl2 NaClO NaCl
B SO2 H2SO4 CaSO4
C Fe2O3 Fe(OH)3 FeCl3
D CO2 H2CO3 Ca(HCO3)2
√
NaClO(乙)与浓盐酸反应生成NaCl(丙)、Cl2和H2O,NaCl(丙)电解生成Cl2(甲),Cl2(甲)与水反应生成HClO和HCl,无法直接生成NaClO(乙),故A项不符合;
H2SO4(乙)与Ca(OH)2反应生成CaSO4(丙)和水,
CaSO4(丙)很稳定,加热至1 200 ℃以上分解,生成CaO、SO2(甲)和O2,SO2(甲)与水反应生成H2SO3而不是H2SO4(乙),故B项不符合;
Fe(OH)3(乙)与盐酸反应生成FeCl3(丙)和水,FeCl3(丙)不能直接转化为Fe2O3(甲),Fe2O3(甲)与水不反应,不能生成Fe(OH)3沉淀,故C项不符合;CO2(甲)与水反应生成H2CO3(乙),H2CO3(乙)与CaCO3反应生成Ca(HCO3)2(丙),Ca(HCO3)2受热分解生成CO2气体,故D项符合。
A.a可使灼热的铜变黑 B.b可与红热的铁产生气体
C.c可使燃烧的镁条熄灭 D.d可使湿润的淀粉碘化钾试纸变蓝
5.(2024·重庆,8)单质M的相关转化如下所示。下列说法错误的是
√
碱溶液与单质d反应生成漂白液,故单质d为Cl2,碱溶液是NaOH溶液;NaOH溶液与氧化物c(适量)反应得纯碱溶液,故氧化物c为CO2;单质M与氧化物b反应得NaOH,故单质M为Na,氧化物b为H2O;Na与单质a反应得氧化物,因此单质a为O2,据此回答。a为O2,O2可与灼热的铜反应生成黑色的氧化铜,A正确;
b为H2O,水蒸气可与红热的铁在高温下反应生成四氧化三铁和氢气,B正确;
c为CO2,镁条在CO2中燃烧生成氧化镁和碳,燃烧的镁条不熄灭,C错误;
d为Cl2,Cl2可与碘化钾反应生成碘单质,碘单质能使湿润的淀粉碘化钾试纸变蓝,D正确。
返回
KESHIJINGLIAN
课时精练
对一对
题号 1 2 3 4 5 6 7 8
答案 A B B B D C D C
题号 9 10 11 12 13 答案 B C D C B 答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
14.
(1)都是氧化物(答案合理即可)
(2)二氧化碳是由不同种元素组成的纯净物,而氮气是由同种元素组成的纯净物
(3)2NO+2CO 2CO2+N2 15∶22
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
15.
(1)盐、铜盐、碱式盐(或碳酸盐)
(2)Cu2(OH)2CO3+4HCl===2CuCl2+3H2O+CO2↑
(3)Cu(OH)2 CuO+H2O CuO+H2 Cu+H2O (4)① ②③ ④
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
16.
(1)FeCl2、Fe(OH)2 (2)②③⑤ 4Fe(OH)2+O2+2H2O===4Fe(OH)3 (3)1~100 nm 丁达尔效应 (4)Fe2O3或Fe3O4 FeSO4·7H2O分解生成SO2、SO3、H2O和X,部分S元素被还原,则Fe元素应被氧化,所以X可能为Fe2O3或Fe3O4 (5)bc
1.(2022·浙江6月选考,1)下列消毒剂的有效成分属于盐的是
A.高锰酸钾溶液 B.过氧乙酸溶液
C.双氧水 D.医用酒精
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
2.(2024·吉林模拟预测)中华文化源远流长,化学与文化传承密不可分。下列说法正确的是
A.“曾青涂铁,铁赤色如铜”,涉及的反应能证明氧化性:Fe3+>Cu2+
B.“绿蚁新醅酒,红泥小火炉”,制作火炉的“红泥”中含氧化铁
C.古陶瓷修复时所用的熟石膏,其成分为Ca(OH)2
D.“九秋风露越窑开,夺得千峰翠色来”,“翠色”是因为成分中含有
氧化亚铜
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
“曾青涂铁,铁赤色如铜”,涉及的反应为铁和铜离子反应生成铜和亚铁离子,能证明氧化性:Cu2+>Fe2+,A错误;
氧化铁为红棕色固体,火炉的“红泥”中含氧化铁,B正确;
古陶瓷修复所用的熟石膏,其化学成分为2CaSO4·H2O,C错误;
“翠色”为青色或绿色,而氧化亚铜为砖红色,“翠色”不可能来自氧化亚铜,D错误。
答案
3.下列物质分类正确的组合是
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
选项 混合物 化合物 单质 盐
A 稀盐酸 NaOH溶液 石墨 NaCl
B 水玻璃 KNO3晶体 O2 Na2CO3
C 空气 澄清石灰水 铁 CaCO3
D CuSO4·5H2O CaCl2 水银 CaO
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
氢氧化钠溶液属于混合物,故A错误;
澄清石灰水为氢氧化钙的水溶液,属于混合物,故C错误;
CuSO4·5H2O属于纯净物,CaO不属于盐,故D错误。
答案
4.(2024·武汉一模)化学创造美好生活,下列说法错误的是
A.化妆品中添加甘油可起到保湿作用
B.手机芯片与光导纤维化学成分相同
C.折叠手机柔性屏使用的原材料聚酰亚胺属于有机高分子材料
D.节日绚丽的烟花与原子核外电子跃迁过程中的能量变化有关
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
手机芯片材质是硅单质,光导纤维材质是二氧化硅,故B错误;
折叠手机柔性屏使用的原材料聚酰亚胺是聚合物,属于有机高分子材料,故C正确;
当电子由较高能量的激发态跃迁到较低能量的激发态乃至基态时,多余的能量以光的形式释放出来,因此可以看到绚丽的烟花,故D正确。
5.2023年诺贝尔化学奖授予发现和合成量子点材料的三位科学家。将富含维生素、蛋白质、糖类的有机物经高温碳化后可以获得直径为2~10 nm碳量子点材料。下列说法正确的是
A.维生素、蛋白质、糖类组成元素相同
B.碳量子点材料属于有机高分子材料
C.高温碳化有机物属于物理变化
D.将碳量子点材料分散到溶液中所形成的分散系为胶体
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
6.(2024·西安统考一模)某病毒由蛋白质外壳和单链核酸组成,如图所示,直径为60~140 nm。下列说法错误的是
A.病毒扩散到空气中可能形成胶体
B.病毒的蛋白质外壳中存在氢键
C.止咳祛痰药盐酸氨溴索的化学式为
C13H18Br2N2O·HCl,属于混合物
D.ClO2泡腾片和酒精均可灭杀该病毒,二者消毒原理不同
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
分散质粒子直径在1~100 nm之间的分散系是胶体,
该病毒直径为60~140 nm,扩散到空气中可能形成
胶体,A正确;
蛋白质分子中有氢键,如两个氨基酸之间的氢键、
二级结构后的盘旋和折叠,B正确;
盐酸氨溴索属于纯净物,C错误;
ClO2利用强氧化性消毒杀菌,酒精的杀菌原理主要是使蛋白质变性,二者消毒原理不同,D正确。
7.《本草述钩元》中的“石碱”条目下记载“采蒿蓼之属,开窖浸水,漉起,晒干烧灰,以原水淋汁……连汁货之四方,浣衣发面”。下列说法正确的是
A.“石碱”是一种强碱,成分为NaOH
B.蒿蓼中含有纤维素,分子式为(C6H10O5)n,属于纯净物
C.制取过程中包括浸取、灼烧、过滤、萃取等操作
D.“石碱”可用于浣衣,是由于其溶液显碱性,可以洗去油污
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
“晒干烧灰”说明“石碱”成分来源于植物烧成的灰中,“以原水淋汁”证明是溶于水的碳酸盐,故A错误;
纤维素的分子式为(C6H10O5)n,属于高分子,属于混合物,故B错误;
制取过程中包括浸取、灼烧、过滤等操作,没有萃取,故C错误;
“石碱”可用于浣衣,是由于碳酸根离子水解,溶液显碱性,油污在碱性溶液中水解生成易溶于水的物质,可以洗去油污,故D正确。
8.(2025·郑州模拟)科学研究发现液态水或存在第二形态,当水被加热到40~60 ℃时,它的导热性、折射率、导电性等属性也会发生改变。下列说法正确的是
A.氢、氧两种元素只能组成H2O
B.导热性、折射率、导电性属于水的化学性质
C.0 ℃时冰的密度比液态水的密度小
D.液态水两种形态间的转化属于化学变化
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
A项,氢、氧两种元素除组成H2O外还可以组成H2O2,错误;
B项,导热性、折射率、导电性属于水的物理性质,错误;
C项,冰浮在水上,说明冰的密度小于液态水,正确;
D项,液态水两种形态间的转化属于物理变化,错误。
9.(2024·河北模拟预测)化学在生产、生活、能源、环境等领域应用广泛,下列说法错误的是
A.工业上电解熔融态的氯化镁制取单质镁
B.发酵粉中的碳酸钠与固态酸发生反应生成二氧化碳使食品变膨松
C.钠离子电池储能电站的投运有利于解决光伏发电的间歇性、波动性等
问题
D.发展太阳能制氢技术,减少化石燃料的使用,有利于减缓温室效应
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
工业上从海水中提取氯化镁,再电解熔融态的氯化镁制取单质镁,故A项正确;
发酵粉的主要成分为碳酸氢钠、酒石酸,使用时,碳酸氢钠与固态酸发生反应生成二氧化碳使食品变膨松,故B项错误;
光伏发电受昼夜交替、天气阴晴等因素的影响,具有间歇性、波动性等问题,钠离子电池储能电站的投运有利于解决这些问题,故C项正确;发展太阳能制氢技术,减少化石燃料的使用,可控制二氧化碳的排放,有利于减缓温室效应,故D项正确。
10.下列关于各物质的所属类别及性质的描述正确的是
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
选项 A B C D
物质 NO2 NaCl 生铁 氢氧化铁胶体
类别 酸性氧化物 离子化合物 合金 电解质
性质 与水反应 熔融态不导电 易发生电化学腐蚀 能产生丁达尔效应
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
NO2不是酸性氧化物,故A错误;
NaCl是离子化合物,熔融态能导电,故B错误;
生铁是铁碳合金,在潮湿环境中构成原电池,易发生电化学腐蚀,故C正确;
氢氧化铁胶体是混合物,既不是电解质也不是非电解质,故D错误。
11.我国科学家研制出的“全碳气凝胶”固体材料“碳海绵”,是迄今世界上最轻的材料。下列关于“碳海绵”的说法错误的是
A.光束照射时可观察到丁达尔效应
B.常温下具有良好的耐酸、耐碱性
C.可用于处理海面的漏油
D.其净水过程是化学变化
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
“全碳气凝胶”固体材料“碳海绵”属于胶体,因此光束照射时可观察到丁达尔效应,A正确;
由于胶体具有吸附性,因此可用于处理海面的漏油,C正确;
其净水过程利用的是吸附原理,没有产生新物质,因此是物理变化,D错误。
12.已知甲、乙、丙有如图所示的转化关系(部分物质和反应条件已略去,“→”表示一步反应即可实现),下列各组物质不满足图示转化关系的是
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
选项 甲 乙 丙
A NaHCO3 Na2CO3 NaOH
B SiO2 Si Na2SiO3
C Fe2O3 Fe(OH)3 FeCl3
D S Na2SO3 Na2SO4
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
由2NaHCO3 Na2CO3+CO2↑+H2O,Na2CO3+CO2+H2O===2NaHCO3,Na2CO3+Ba(OH)2===2NaOH+BaCO3↓,满足图示关系,选项A不符合题意;
由SiO2+2C Si+2CO↑,Si+O2 SiO2,Si+
2NaOH+H2O===Na2SiO3+2H2↑,满足图示关系,选项B不符合题意;
Fe2O3无法直接生成Fe(OH)3,不满足图示关系,选项C符合题意;
由3S+6NaOH===Na2SO3+2Na2S+3H2O,Na2SO3+3H2S===Na2S+3S↓+
3H2O,2Na2SO3+O2===2Na2SO4,满足图示关系,选项D不符合题意。
13.(2025·保定模拟)下列说法错误的是
A.氦气属于稀有气体,是空气的成分
之一
B.由硅、碳、氧、硫等元素经过一系
列变化能变成铁,该过程属于化学变化
C.固定太空电梯的缆绳材料最有可能是碳纳米管(如图1),碳纳米管与C60
互为同素异形体
D.取a g偏二甲肼(火箭推进剂)在6.4 g氧气中恰好完全反应,如图2,则偏
二甲肼中不含氧
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
原子是化学变化中的最小微粒,化学变化中原子核不会变,由硅、碳、氧、硫等元素经过一系列变化能变成铁,该过程属于核聚变,故B错误;
碳纳米管与C60属于碳的不同单质,互为同素异形体,故C正确;
水中氧元素的质量为3.6 g×=3.2 g,二氧化碳中氧元素的质量为4.4 g
×=3.2 g,3.2 g+3.2 g=6.4 g,故偏二甲肼中不含氧元素,故D正确。
14.在宏观—微观—符号之间建立联系,是化学学科特有的思维方式。汽车尾气是造成大气污染的主要原因之一,在汽车排气管上安装“催化转换器”便可以使汽车的尾气转换成无毒气体。用 表示碳原子,用○表示氧原子,用 表示氮原子,如图为气体转换的微观过程。请根据图示回答下列问题:
(1)A、B、C三种物质可以归为一类的依
据是 。
(2)将C归为化合物,将D归为单质的理由是_________________________
。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
都是氧化物(答案合理即可)
二氧化碳是由不同种元素组成的纯净物,而氮气是由同种元素组成的纯净物
(3)图示反应用化学方程式表示为 。化学变化过程中消耗的A物质和生成的C物质的质量比为 。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
2NO+2CO 2CO2+N2
15∶22
根据题意及图示可知,A为NO、B为CO、C为CO2、D为N2。
15.铜器久置于空气中会和空气中的水蒸气、CO2、O2作用产生“绿锈”,该“绿锈”俗称“铜绿”,又称“孔雀石”[化学式为Cu2(OH)2CO3],“铜绿”能与酸反应生成铜盐、CO2和H2O。某同学利用下述系列反应实现了“铜→铜绿→……→铜”的转化。
铜 铜绿 A Cu(OH)2 B Cu
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
(1)从三种不同分类标准回答,“铜绿”属于哪类物质:______________
。
(2)请写出“铜绿”与盐酸反应的化学方程式:______________________
。
盐、铜盐、碱
式盐(或碳酸盐)
Cu2(OH)2CO3+4HCl===
2CuCl2+3H2O+CO2↑
铜 铜绿 A Cu(OH)2 B Cu
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
(3)写出④、⑤的化学方程式:
④ ;⑤ 。
(4)上述转化过程中属于化合反应的是 (填序号,下同),属于复分解反应的是 ,属于分解反应的是 。
Cu(OH)2 CuO+H2O
CuO+H2 Cu+H2O
①
②③
④
16.铁广泛应用于人类的生产、生活。
Ⅰ.铁及其化合物存在如图甲转化关系(部分反应物和反应条件已略去),回答下列问题。
(1)a、b、c三种物质中属于电解质的是______
(填化学式)。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
FeCl2、
Fe(OH)2
根据物质类别和铁元素的化合价可知,a为Fe,b为FeCl2,e为FeCl3,c为Fe(OH)2,d为Fe(OH)3。a、b、c三种物质中属于电解质的是FeCl2、Fe(OH)2。
(2)①~⑤反应中,既是化合反应又是氧化还原反应的是 (填序号)。写出⑤的化学方程式: 。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
②③⑤
4Fe(OH)2+O2+2H2O===4Fe(OH)3
①置换反应;②氯气与氯化亚铁反应生成氯化铁;③铁在氯气中点燃生成氯化铁;④反应中Fe的化合价没有发生变化;⑤氢氧化亚铁与氧气、水反应生成氢氧化铁;故①~⑤反应中,既是化合反应又是氧化还原反应的有②③⑤。
(3)将e的浓溶液滴加到沸水中可得到红褐色液体,该液体属于一种特殊的分散系。该分散系中分散质的微粒直径为 。鉴别e的浓溶液与该分散系所用方法的原理为
。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
1~100 nm
丁达尔效应
Ⅱ.明代《徐光启手迹》记载了以绿矾(FeSO4·7H2O)为原料制备硝酸的方法,其主要流程如图乙。
(4)X为铁的氧化物,X的化学式可能为
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
,判断依据为______________________________________
。
(5)③利用浓硫酸的性质为 (填字母)。
a.强氧化性 b.高沸点
c.酸性 d.脱水性
FeSO4·7H2O分解生成SO2、SO3、H2O和X,部分S元素被还原,则Fe元素应被氧化,所以X可能为Fe2O3或Fe3O4
Fe2O3或Fe3O4
bc
返回
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答案
③中浓硫酸与硝酸钾发生复分解反应生成硝酸,硝酸沸点低,易挥发,浓硫酸的沸点高,难挥发,利用了浓硫酸的高沸点和酸性。
本课结束
同课章节目录
