3.2.1醇 课件 (共23张PPT) 高中化学 人教版(2019) 选择性必修3
文档属性
| 名称 | 3.2.1醇 课件 (共23张PPT) 高中化学 人教版(2019) 选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 18.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-05 00:00:00 | ||
图片预览



文档简介
(共23张PPT)
人教版2019 高二
第2节 醇 酚
第1课时:醇
第三章 烃的衍生物
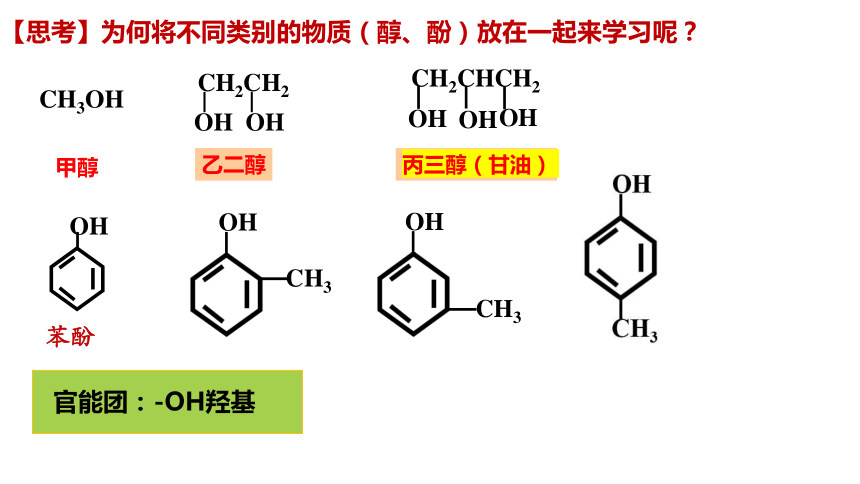
【思考】为何将不同类别的物质(醇、酚)放在一起来学习呢?
CH3OH
甲醇
CH2CH2
OH OH
乙二醇
丙三醇(甘油)
苯酚
OH
OH
CH3
OH
CH3
官能团:-OH羟基
CH2CHCH2
OH
OH
OH
CH3OH
甲醇
CH2CH2
OH OH
乙二醇
丙三醇(甘油)
苯酚
OH
OH
CH3
OH
CH3
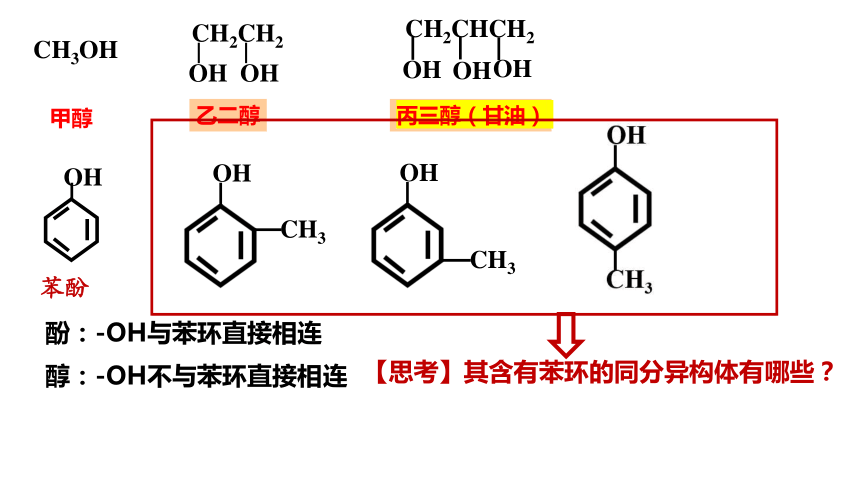
酚:-OH与苯环直接相连
CH2CHCH2
OH
OH
OH
醇:-OH不与苯环直接相连
【思考】其含有苯环的同分异构体有哪些?
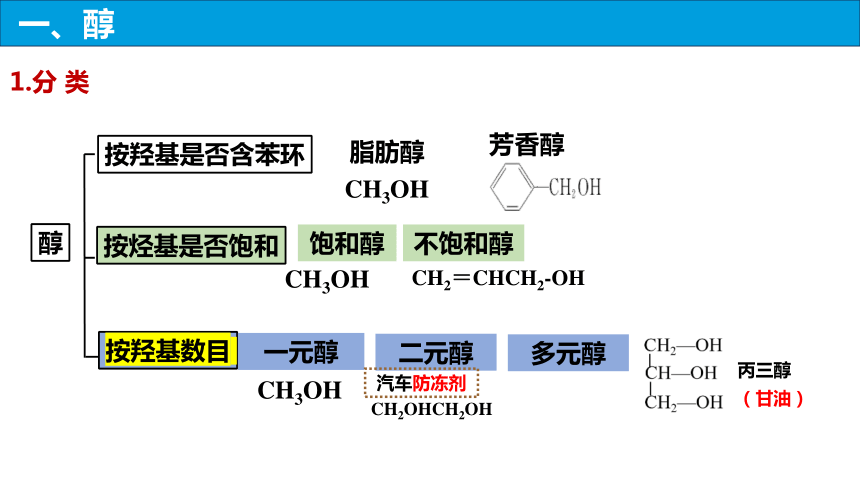
一、醇
醇
按羟基是否含苯环
按羟基数目
脂肪醇
芳香醇
一元醇
二元醇
CH3OH
按烃基是否饱和
饱和醇
不饱和醇
CH2=CHCH2-OH
多元醇
CH2OHCH2OH
丙三醇
(甘油)
汽车防冻剂
CH3OH
CH3OH
1.分 类
一、醇
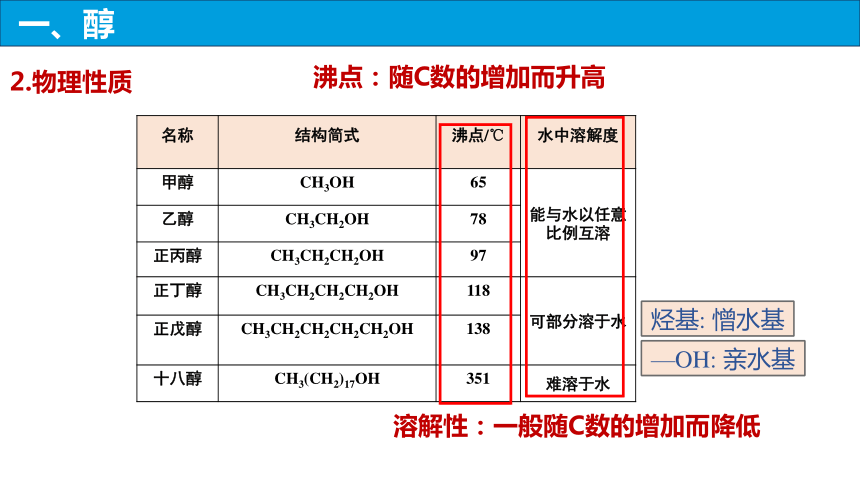
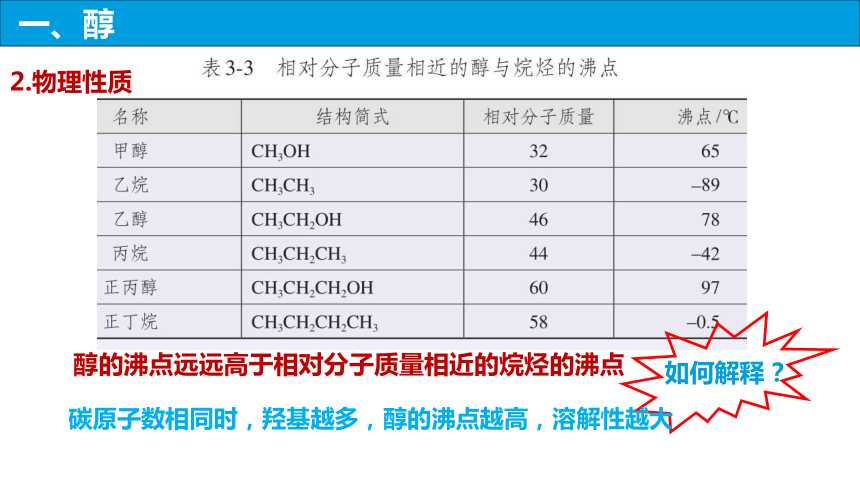
2.物理性质
名称 结构简式 沸点/℃ 水中溶解度
甲醇 CH3OH 65 能与水以任意比例互溶
乙醇 CH3CH2OH 78 正丙醇 CH3CH2CH2OH 97 正丁醇 CH3CH2CH2CH2OH 118 可部分溶于水
正戊醇 CH3CH2CH2CH2CH2OH 138 十八醇 CH3(CH2)17OH 351 难溶于水
溶解性:一般随C数的增加而降低
沸点:随C数的增加而升高
烃基: 憎水基
—OH: 亲水基
一、醇
2.物理性质
醇的沸点远远高于相对分子质量相近的烷烃的沸点
如何解释?
碳原子数相同时,羟基越多,醇的沸点越高,溶解性越大
一、醇
3.化学性质
①中的O-H键易断裂,使羟基氢原子被取代发生取代反应
②中的C-O键易断裂,使羟基被取代或脱去,发生取代反应/消去反应
R-C- C-O-H
H
H
H
H
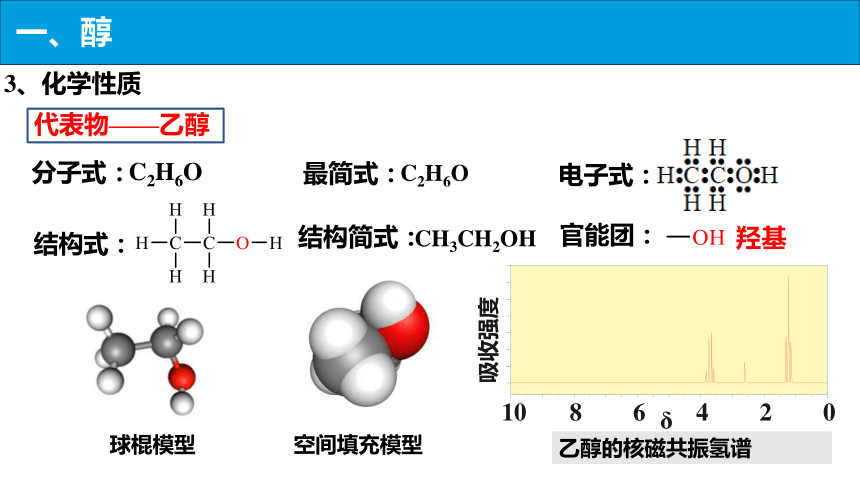
3、化学性质
代表物——乙醇
C2H6O
分子式:
电子式:
结构式:
结构简式:
官能团:
C2H6O
最简式:
空间填充模型
CH3CH2OH
羟基
8
10
0
6
2
4
吸收强度
乙醇的核磁共振氢谱
δ
球棍模型
一、醇
一、醇
3.化学性质
1>置换反应:与活泼金属(Na K Ca Mg等)
CH3CH2OH + Na
现象:先沉后浮,不熔、不游、不响,反应缓慢
乙醇-OH上的H不如H-OH中H原子活泼
3.化学性质
2>乙醇的化性:脱水(因为-OH)
酯化反应:酸脱羟基醇脱氢
CH3 CH2 OH+H Br CH3 CH2 Br+H2O
△
-Br取代了-OH,-OH和-H结合生成H2O
CH3CH2-OH + H-OCH2CH3 CH3CH2-O-CH2CH3 + H2O
浓H2SO4
140℃
分子间脱水成醚
CH2= CH2↑+H2O
浓H2SO4
浓H2SO4
170℃
分子内脱水成烯
消去反应
【思考】从反应类型辨析上述4个反应?
反应条件有何异同?
3.化学性质
注意:
浓硫酸的作用:催化剂和吸水剂
饱和碳酸钠溶液的作用:
①反应乙酸
②溶解乙醇
③降低乙酸乙酯的溶解度
④增大水溶液密度便于分层
[酯化反应:取代反应]
酸脱羟基醇脱氢
3.化学性质
[消去反应:醇 vs 卤代烃]
CH2= CH2↑+HBr
NaOH,乙醇
Δ
醇 和 卤代烃的消去反应有和异同点
5.为何使液体温度迅速升到170℃?
1.试剂添加顺序?
3.沸石作用是什么?
2.浓硫酸的作用?
6.温度计的位置?
7.作用?
催化剂和脱水剂
防止在140℃时生成乙醚。
除SO2和乙醇
液面以下
浓硫酸缓慢
加入乙醇中
褪色
4.混合液颜色变黑,
为什么?
考点小结:(笔记)
浓硫酸170℃,
乙醇脱水变乙烯,
产生气体用碱洗,
液面以下温度计
消去反应<实验3-2>
3.化学性质
消去反应<实验3-2>
断键:C-O和β-C上的C-H键
【思考】写出下列物质发生消去反应的方程式
醇消去反应的条件是?
浓硫酸,加热。有β—H
3.化学性质
酒精在人体内的代谢过程
3.化学性质
【思考】乙醇到乙醛结构发生了怎样的变化?
CH3- C-H
O
=
乙醇
乙醛
断键:O-H和α-C上的C-H键
3.化学性质
乙醇的氧化反应
A.乙醇的催化氧化
2CH3CH2OH+O2 2CH3CHO+2H2O
△
Cu
现象:
Cu:紫红色→黑色→紫红色
乙醇转化为有刺激性气味的液体
合成路线
CH3CH2OH
O2
Cu,Δ
CH3CHO
3.化学性质
[思考]乙醇的催化氧化属于消去反应吗?
O2
Cu,Δ
O2
Cu,Δ
断键:O-H和α-C上的C-H键
3.化学性质
[思考]乙醇的催化氧化分几种情况,规律如何?
小结:
醇中
α-C上有2-3个H→醛
α-C上有1个H→酮
α-C上无H→难以氧化
A.乙醇的催化氧化
乙醇的氧化反应
B.乙醇→乙酸
CH3CH2OH
酸性KMnO4溶液
现象:
酸性K2Cr2O7溶液
CH3COOH
酸性KMnO4溶液的紫红色褪去
K2Cr2O7溶液(橙色) → Cr3+ (绿色)
乙醇的氧化反应
B.乙醇→乙酸
CH3CH2OH
酸性KMnO4溶液
酸性K2Cr2O7溶液
CH3COOH
思考:
CH3OH
R-CH2OH
R-CHOH
酸性KMnO4溶液
乙醇的氧化反应
C.乙醇(彻底氧化)→CO2+H2O
CH3CH2OH + O2
点燃
氧化反应
还原反应
归纳小结:乙醇在不同反应中的断键位置
人教版2019 高二
第2节 醇 酚
第1课时:醇
第三章 烃的衍生物
【思考】为何将不同类别的物质(醇、酚)放在一起来学习呢?
CH3OH
甲醇
CH2CH2
OH OH
乙二醇
丙三醇(甘油)
苯酚
OH
OH
CH3
OH
CH3
官能团:-OH羟基
CH2CHCH2
OH
OH
OH
CH3OH
甲醇
CH2CH2
OH OH
乙二醇
丙三醇(甘油)
苯酚
OH
OH
CH3
OH
CH3
酚:-OH与苯环直接相连
CH2CHCH2
OH
OH
OH
醇:-OH不与苯环直接相连
【思考】其含有苯环的同分异构体有哪些?
一、醇
醇
按羟基是否含苯环
按羟基数目
脂肪醇
芳香醇
一元醇
二元醇
CH3OH
按烃基是否饱和
饱和醇
不饱和醇
CH2=CHCH2-OH
多元醇
CH2OHCH2OH
丙三醇
(甘油)
汽车防冻剂
CH3OH
CH3OH
1.分 类
一、醇
2.物理性质
名称 结构简式 沸点/℃ 水中溶解度
甲醇 CH3OH 65 能与水以任意比例互溶
乙醇 CH3CH2OH 78 正丙醇 CH3CH2CH2OH 97 正丁醇 CH3CH2CH2CH2OH 118 可部分溶于水
正戊醇 CH3CH2CH2CH2CH2OH 138 十八醇 CH3(CH2)17OH 351 难溶于水
溶解性:一般随C数的增加而降低
沸点:随C数的增加而升高
烃基: 憎水基
—OH: 亲水基
一、醇
2.物理性质
醇的沸点远远高于相对分子质量相近的烷烃的沸点
如何解释?
碳原子数相同时,羟基越多,醇的沸点越高,溶解性越大
一、醇
3.化学性质
①中的O-H键易断裂,使羟基氢原子被取代发生取代反应
②中的C-O键易断裂,使羟基被取代或脱去,发生取代反应/消去反应
R-C- C-O-H
H
H
H
H
3、化学性质
代表物——乙醇
C2H6O
分子式:
电子式:
结构式:
结构简式:
官能团:
C2H6O
最简式:
空间填充模型
CH3CH2OH
羟基
8
10
0
6
2
4
吸收强度
乙醇的核磁共振氢谱
δ
球棍模型
一、醇
一、醇
3.化学性质
1>置换反应:与活泼金属(Na K Ca Mg等)
CH3CH2OH + Na
现象:先沉后浮,不熔、不游、不响,反应缓慢
乙醇-OH上的H不如H-OH中H原子活泼
3.化学性质
2>乙醇的化性:脱水(因为-OH)
酯化反应:酸脱羟基醇脱氢
CH3 CH2 OH+H Br CH3 CH2 Br+H2O
△
-Br取代了-OH,-OH和-H结合生成H2O
CH3CH2-OH + H-OCH2CH3 CH3CH2-O-CH2CH3 + H2O
浓H2SO4
140℃
分子间脱水成醚
CH2= CH2↑+H2O
浓H2SO4
浓H2SO4
170℃
分子内脱水成烯
消去反应
【思考】从反应类型辨析上述4个反应?
反应条件有何异同?
3.化学性质
注意:
浓硫酸的作用:催化剂和吸水剂
饱和碳酸钠溶液的作用:
①反应乙酸
②溶解乙醇
③降低乙酸乙酯的溶解度
④增大水溶液密度便于分层
[酯化反应:取代反应]
酸脱羟基醇脱氢
3.化学性质
[消去反应:醇 vs 卤代烃]
CH2= CH2↑+HBr
NaOH,乙醇
Δ
醇 和 卤代烃的消去反应有和异同点
5.为何使液体温度迅速升到170℃?
1.试剂添加顺序?
3.沸石作用是什么?
2.浓硫酸的作用?
6.温度计的位置?
7.作用?
催化剂和脱水剂
防止在140℃时生成乙醚。
除SO2和乙醇
液面以下
浓硫酸缓慢
加入乙醇中
褪色
4.混合液颜色变黑,
为什么?
考点小结:(笔记)
浓硫酸170℃,
乙醇脱水变乙烯,
产生气体用碱洗,
液面以下温度计
消去反应<实验3-2>
3.化学性质
消去反应<实验3-2>
断键:C-O和β-C上的C-H键
【思考】写出下列物质发生消去反应的方程式
醇消去反应的条件是?
浓硫酸,加热。有β—H
3.化学性质
酒精在人体内的代谢过程
3.化学性质
【思考】乙醇到乙醛结构发生了怎样的变化?
CH3- C-H
O
=
乙醇
乙醛
断键:O-H和α-C上的C-H键
3.化学性质
乙醇的氧化反应
A.乙醇的催化氧化
2CH3CH2OH+O2 2CH3CHO+2H2O
△
Cu
现象:
Cu:紫红色→黑色→紫红色
乙醇转化为有刺激性气味的液体
合成路线
CH3CH2OH
O2
Cu,Δ
CH3CHO
3.化学性质
[思考]乙醇的催化氧化属于消去反应吗?
O2
Cu,Δ
O2
Cu,Δ
断键:O-H和α-C上的C-H键
3.化学性质
[思考]乙醇的催化氧化分几种情况,规律如何?
小结:
醇中
α-C上有2-3个H→醛
α-C上有1个H→酮
α-C上无H→难以氧化
A.乙醇的催化氧化
乙醇的氧化反应
B.乙醇→乙酸
CH3CH2OH
酸性KMnO4溶液
现象:
酸性K2Cr2O7溶液
CH3COOH
酸性KMnO4溶液的紫红色褪去
K2Cr2O7溶液(橙色) → Cr3+ (绿色)
乙醇的氧化反应
B.乙醇→乙酸
CH3CH2OH
酸性KMnO4溶液
酸性K2Cr2O7溶液
CH3COOH
思考:
CH3OH
R-CH2OH
R-CHOH
酸性KMnO4溶液
乙醇的氧化反应
C.乙醇(彻底氧化)→CO2+H2O
CH3CH2OH + O2
点燃
氧化反应
还原反应
归纳小结:乙醇在不同反应中的断键位置
