陕西省咸阳市2024-2025学年高二下学期期末质量检测化学试卷(含答案)
文档属性
| 名称 | 陕西省咸阳市2024-2025学年高二下学期期末质量检测化学试卷(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 4.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-04 17:23:41 | ||
图片预览


文档简介
陕西省咸阳市2024-2025学年高二下学期7月期末质量检测化学试题
一、单选题
1.近年我国在科学技术领域取得了举世瞩目的成就。对下列成就所涉及的化学知识判断错误的是
A.“鲲龙”水陆两栖飞机实现海上首飞:其所用燃料“航空煤油”属于混合物
B.大型液化天然气运输船成功建造:天然气液化过程中形成了新的化学键
C.“歼20战斗机”完美亮相:机身所使用的隐形材料石墨烯与金刚石互为同素异形体
D.“天问一号”探测器着陆火星:过程中使用了芳纶制作的降落伞,芳纶是高分子材料
2.下列化学用语表示错误的是
A.乙炔的空间填充模型为 B.异丁烷的键线式为
C.乙烯的实验式为 D.乙醚的结构简式为
3.美好生活要靠劳动创造。下列劳动过程没有发生酯化反应的是
A.以油脂为原料制取肥皂
B.用纤维素和醋酸制取醋酸纤维
C.由乳酸制取聚乳酸
D.白酒陈化过程中会产生香味
4.从我国南海的柳珊瑚中分离得到的柳珊瑚酸(如图),具有独特的环系结构。下列关于柳珊瑚酸的说法错误的是
A.能使溴水褪色 B.属于烃的含氧衍生物
C.能与烧碱溶液发生反应 D.其环系结构中3个五元环共平面
5.下列各有机化合物的命名正确的是
A.:1,3-二丁烯-乙基丁烷
B.:2-乙基丁烷
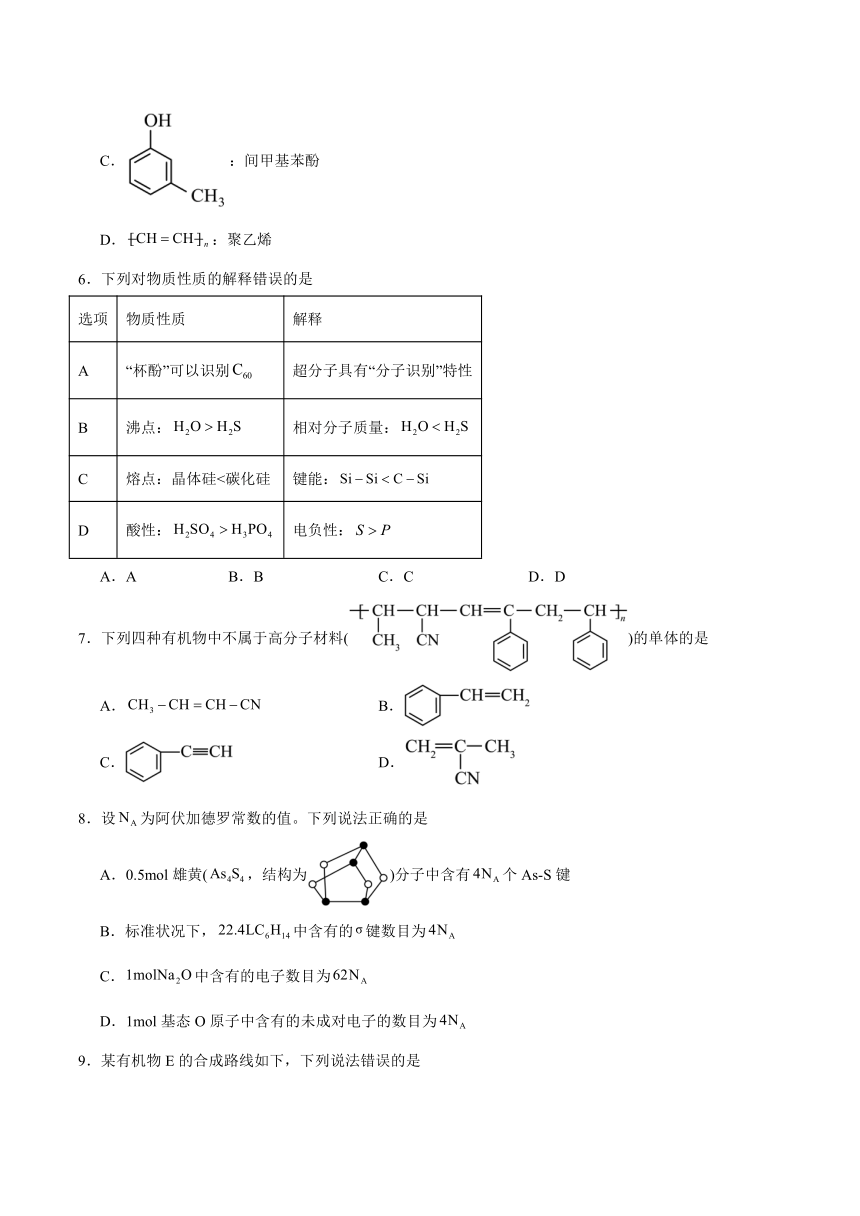
C.:间甲基苯酚
D.:聚乙烯
6.下列对物质性质的解释错误的是
选项 物质性质 解释
A “杯酚”可以识别 超分子具有“分子识别”特性
B 沸点: 相对分子质量:
C 熔点:晶体硅<碳化硅 键能:
D 酸性: 电负性:
A.A B.B C.C D.D
7.下列四种有机物中不属于高分子材料()的单体的是
A. B.
C. D.
8.设为阿伏加德罗常数的值。下列说法正确的是
A.0.5mol雄黄(,结构为)分子中含有个As-S键
B.标准状况下,中含有的键数目为
C.中含有的电子数目为
D.1mol基态O原子中含有的未成对电子的数目为
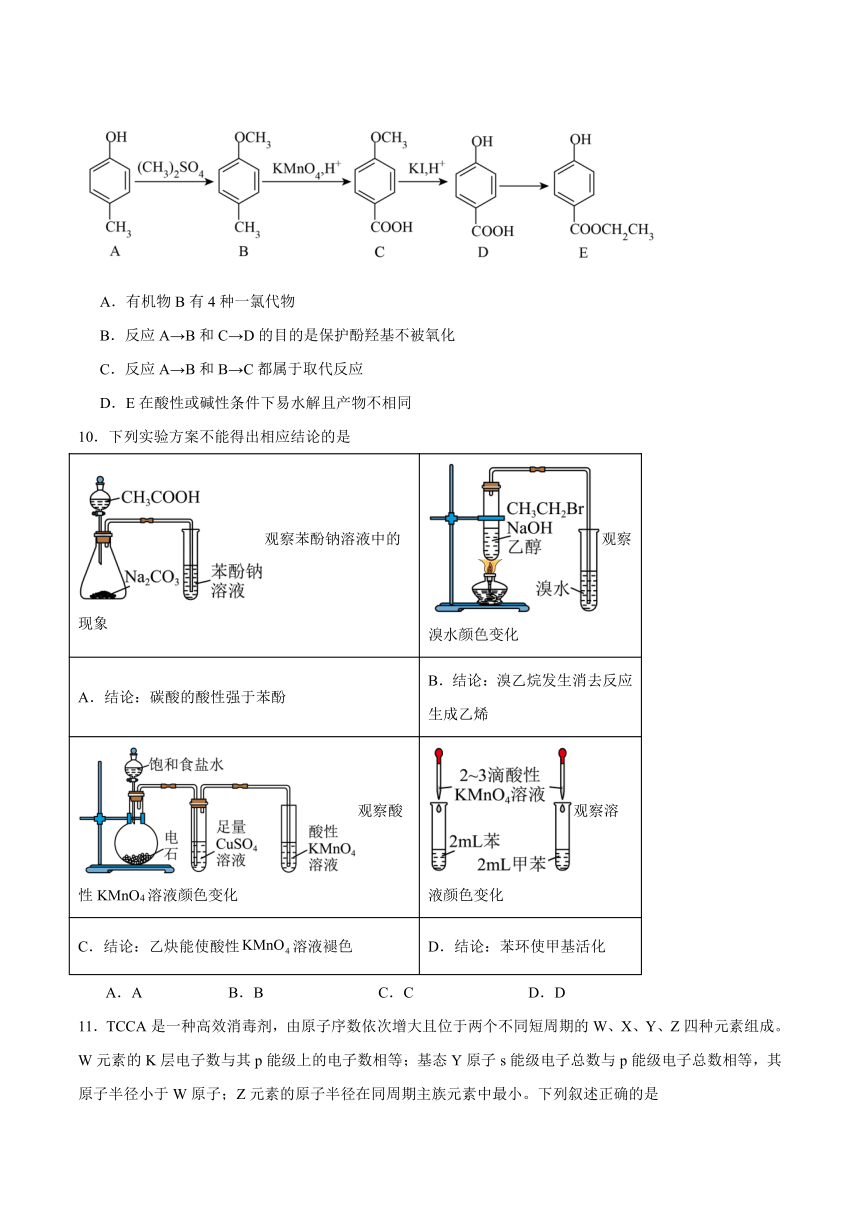
9.某有机物E的合成路线如下,下列说法错误的是
A.有机物B有4种一氯代物
B.反应A→B和C→D的目的是保护酚羟基不被氧化
C.反应A→B和B→C都属于取代反应
D.E在酸性或碱性条件下易水解且产物不相同
10.下列实验方案不能得出相应结论的是
观察苯酚钠溶液中的现象 观察溴水颜色变化
A.结论:碳酸的酸性强于苯酚 B.结论:溴乙烷发生消去反应生成乙烯
观察酸性KMnO4溶液颜色变化 观察溶液颜色变化
C.结论:乙炔能使酸性溶液褪色 D.结论:苯环使甲基活化
A.A B.B C.C D.D
11.TCCA是一种高效消毒剂,由原子序数依次增大且位于两个不同短周期的W、X、Y、Z四种元素组成。W元素的K层电子数与其p能级上的电子数相等;基态Y原子s能级电子总数与p能级电子总数相等,其原子半径小于W原子;Z元素的原子半径在同周期主族元素中最小。下列叙述正确的是
A.电负性大小:
B.简单离子半径:
C.化合物中,W原子为sp杂化
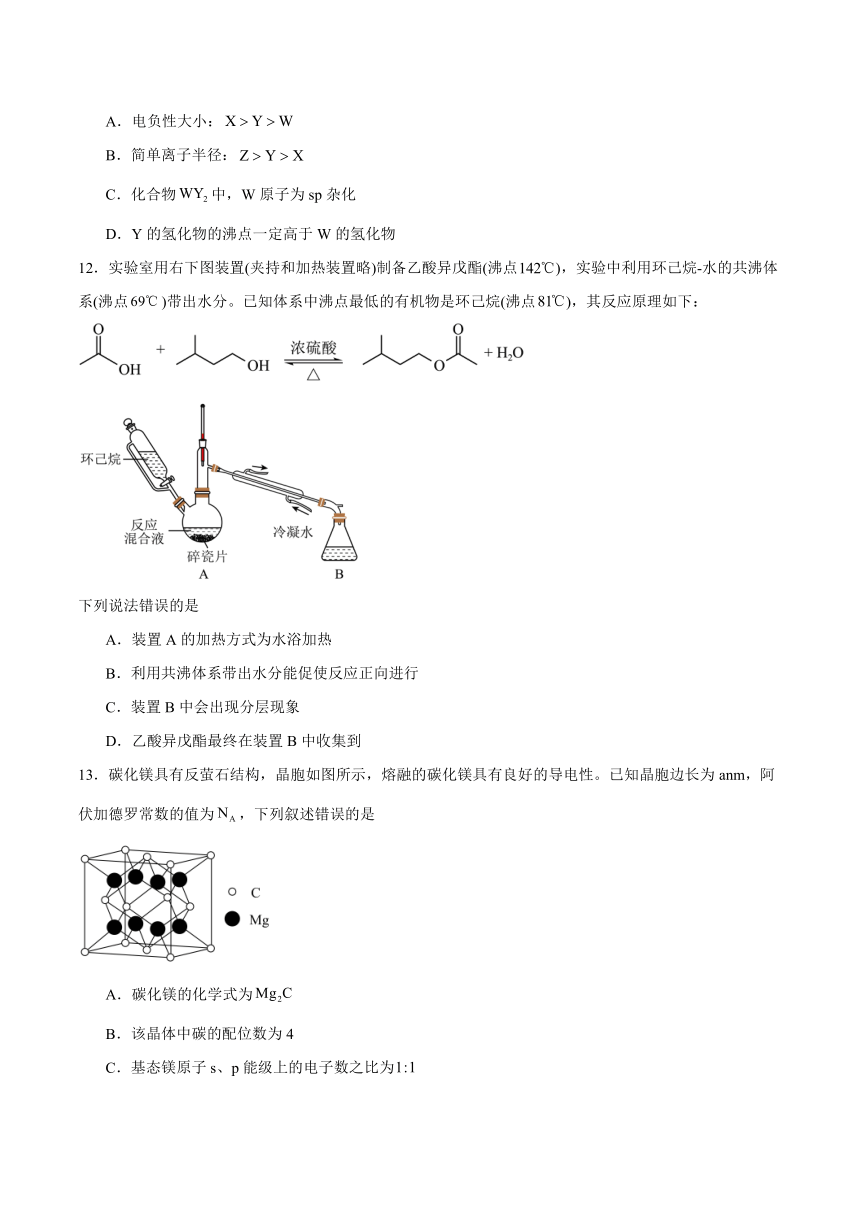
D.Y的氢化物的沸点一定高于W的氢化物
12.实验室用右下图装置(夹持和加热装置略)制备乙酸异戊酯(沸点),实验中利用环己烷-水的共沸体系(沸点)带出水分。已知体系中沸点最低的有机物是环己烷(沸点),其反应原理如下:
下列说法错误的是
A.装置A的加热方式为水浴加热
B.利用共沸体系带出水分能促使反应正向进行
C.装置B中会出现分层现象
D.乙酸异戊酯最终在装置B中收集到
13.碳化镁具有反萤石结构,晶胞如图所示,熔融的碳化镁具有良好的导电性。已知晶胞边长为anm,阿伏加德罗常数的值为,下列叙述错误的是
A.碳化镁的化学式为
B.该晶体中碳的配位数为4
C.基态镁原子s、p能级上的电子数之比为
D.该晶体的密度为
14.对羟基苯乙酮()可作化妆品的防腐剂。某实验小组用乙酸乙酯从水溶液中提取对羟基苯乙酮,进行如下实验,虽操作规范,但所得产品中混有较多的乙酸乙酯。已知:对羟基苯乙酮的沸点为;乙酸乙酯的沸点为。下列叙述正确的是
A.分液时,水层、有机层依次从分液漏斗下口放出
B.萃取剂总量相同,分两次萃取的优点是提高萃取率
C.操作X为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
D.可在得到的水层中用银氨溶液检查对羟基苯乙酮是否残留
二、解答题
15.锌及其化合物在科学技术发展和人类生产生活中发挥着重要作用。回答下列问题:
(1)《天工开物》中记载了关于火法炼锌的工艺:以炉甘石和木炭为原料高温制取锌。基态Zn原子价层电子的轨道表示式为 ,其原子核外电子共有 种空间运动状态,中阴离子的空间结构名称为 。
(2)锌是人体必需的微量元素,下列现代分析方法中,可用于检验水中痕量锌元素的是 (填字母)。
a.X射线衍射 b.原子光谱 c.核磁共振氢谱 d.红外光谱
(3)黄铜是由铜和锌所组成的合金,是人类最早使用的合金之一。
①第一电离能:Zn (填“>”或“<”)Cu。
②Cu、Zn等金属具有良好导电性的原因是 。
(4)立方ZnS晶体常用作半导体材料,其晶胞结构如图,则ZnS晶胞的俯视投影图是 (填字母)。
16.M是常用的医用胶,在常温下可以快速固化实现黏合。其相关信息如下:
试样30.6g 氧气流中燃烧测得生成、
CuO作用下,二氧化碳气流中燃烧测得生成标准状况下
质谱法测得相对分子质量为153
红外光谱如图所示
回答下列问题:
(1)M的分子式为 。M可以由有机物A和B()通过酯化反应得到,已知A中含有4种不同化学环境的氢原子,且个数比为,可推测M的结构简式为 。
(2)M中 (填“存在”或“不存在”,下同)顺反异构, 对映异构。
(3)M具有黏合性的原因是发生了加聚反应(在微量水蒸气作用下),加聚反应的化学方程式为 。
(4)医用胶固化的具体机理如下:(R表示烃基,表示微观粒子带负电荷)
①该过程中的杂化方式为 。
②已知氰基和酯基能够活化碳碳双键,故医用胶比 (填“更易”或“更难”)发生加聚反应进行固化。
(5)医用胶使用后能够发生 (填“水解反应”或“加成反应”),最终在组织内降解被人体吸收。
17.某同学在实验室以某甲醛()为原料制备间溴苯甲醛()。
已知:①温度过高,间溴苯甲醛易被氧化。
②溴、苯甲醛、1,2-二氯乙烷、间溴苯甲醛的相关性质见下表:
物质 溴 苯甲醛 1,2-二氯乙烷 间溴苯甲醛
沸点 58.8℃ 179℃ 83.5℃ 229℃
溶解性 微溶于水 微溶于水 难溶于水 难溶于水
相对分子质量 160 106 99 185
实验步骤如下:
步骤1:将一定配比的无水(催化剂)、1,2-二氯乙烷(有机溶剂)和苯甲醛(5.3g)充分混合后装入三颈烧瓶(如下图所示,加热及夹持装置已省略),缓慢滴加足量经浓硫酸干燥过的液溴,控温反应一段时间,冷却。
步骤2:将反应后的混合物缓慢加入至一定量的稀盐酸中,搅拌、静置、分液。有机层用溶液洗涤。
步骤3:向经洗涤的有机层加入适量无水固体,放置一段时间后过滤出晶体。
步骤4:分离有机层,减压蒸馏有机相,收集相应馏分。
(1)仪器X的名称是 ,锥形瓶中的试剂为NaOH溶液,其作用是吸收 (填化学式)。与本实验安全注意事项有关的图标有 (填字母)。
A.护目镜 B.洗手 C.锐器 D.排风
(2)步骤1反应过程中,为提高原料利用率,适宜的温度范围为 (填字母)。
A. B.5 C.
(3)生成间溴苯甲醛的化学方程式为 ;其中催化剂的晶体类型为 。
(4)步骤2分液时有机相处于 (填“上层”或“下层”)。
(5)减压能够降低蒸馏温度,则步骤4中采用减压蒸馏是为了防止 。
(6)若实验结束后得到3.7g间溴苯甲醛,则本实验中间溴苯甲醛的产率为 %。
18.二甲双酮是一种抗惊厥药,以丙烯为起始原料的合成路线如下:
回答下列问题:
(1)丙烯→A的反应中,丙烯中断裂的是 (填“”或“”)键,A的名称为 。
(2)A→B的反应类型为 ,B的结构简式为 。
(3)C中包含的含氧官能团的名称为 。
(4)写出D→E的化学方程式 。
(5)关于上述的有机物,下列说法正确的是_____(填字母)。
A.丙烯分子中3个碳原子共直线 B.试剂X是
C.E能发生水解、氧化、加成反应 D.二甲双酮的分子式为
(6)在D的同分异构体中,与D含有相同官能团的有 种(不含D本身,不含立体异构)。
(7)结合上述信息,以为原料,设计丙烯酸的合成路线如下:
该合成路线中反应所需试剂X为 (填化学式),物质Y的结构简式为 。
参考答案
1.B
2.B
3.A
4.D
5.C
6.B
7.D
8.A
9.C
10.A
11.C
12.D
13.B
14.B
15.(1) 15或十五 平面三角形
(2)b
(3) > 金属晶体中的自由电子(或离域电子)在外加电场作用下可发生定向移动
(4)b
16.(1) 或
(2) 不存在 不存在
(3)
(4) 更易
(5)水解反应
17.(1) 球形冷凝管 和HBr ABD
(2)C
(3) 分子晶体
(4)下层
(5)间溴苯甲醛因温度过高被氧化或醛基因温度过高被氧化
(6)40或40.0或40.00
18.(1) 异丙醇或2-丙醇
(2) 氧化反应
(3)羟基
(4)
(5)BD
(6)4或四
(7) HCN
一、单选题
1.近年我国在科学技术领域取得了举世瞩目的成就。对下列成就所涉及的化学知识判断错误的是
A.“鲲龙”水陆两栖飞机实现海上首飞:其所用燃料“航空煤油”属于混合物
B.大型液化天然气运输船成功建造:天然气液化过程中形成了新的化学键
C.“歼20战斗机”完美亮相:机身所使用的隐形材料石墨烯与金刚石互为同素异形体
D.“天问一号”探测器着陆火星:过程中使用了芳纶制作的降落伞,芳纶是高分子材料
2.下列化学用语表示错误的是
A.乙炔的空间填充模型为 B.异丁烷的键线式为
C.乙烯的实验式为 D.乙醚的结构简式为
3.美好生活要靠劳动创造。下列劳动过程没有发生酯化反应的是
A.以油脂为原料制取肥皂
B.用纤维素和醋酸制取醋酸纤维
C.由乳酸制取聚乳酸
D.白酒陈化过程中会产生香味
4.从我国南海的柳珊瑚中分离得到的柳珊瑚酸(如图),具有独特的环系结构。下列关于柳珊瑚酸的说法错误的是
A.能使溴水褪色 B.属于烃的含氧衍生物
C.能与烧碱溶液发生反应 D.其环系结构中3个五元环共平面
5.下列各有机化合物的命名正确的是
A.:1,3-二丁烯-乙基丁烷
B.:2-乙基丁烷
C.:间甲基苯酚
D.:聚乙烯
6.下列对物质性质的解释错误的是
选项 物质性质 解释
A “杯酚”可以识别 超分子具有“分子识别”特性
B 沸点: 相对分子质量:
C 熔点:晶体硅<碳化硅 键能:
D 酸性: 电负性:
A.A B.B C.C D.D
7.下列四种有机物中不属于高分子材料()的单体的是
A. B.
C. D.
8.设为阿伏加德罗常数的值。下列说法正确的是
A.0.5mol雄黄(,结构为)分子中含有个As-S键
B.标准状况下,中含有的键数目为
C.中含有的电子数目为
D.1mol基态O原子中含有的未成对电子的数目为
9.某有机物E的合成路线如下,下列说法错误的是
A.有机物B有4种一氯代物
B.反应A→B和C→D的目的是保护酚羟基不被氧化
C.反应A→B和B→C都属于取代反应
D.E在酸性或碱性条件下易水解且产物不相同
10.下列实验方案不能得出相应结论的是
观察苯酚钠溶液中的现象 观察溴水颜色变化
A.结论:碳酸的酸性强于苯酚 B.结论:溴乙烷发生消去反应生成乙烯
观察酸性KMnO4溶液颜色变化 观察溶液颜色变化
C.结论:乙炔能使酸性溶液褪色 D.结论:苯环使甲基活化
A.A B.B C.C D.D
11.TCCA是一种高效消毒剂,由原子序数依次增大且位于两个不同短周期的W、X、Y、Z四种元素组成。W元素的K层电子数与其p能级上的电子数相等;基态Y原子s能级电子总数与p能级电子总数相等,其原子半径小于W原子;Z元素的原子半径在同周期主族元素中最小。下列叙述正确的是
A.电负性大小:
B.简单离子半径:
C.化合物中,W原子为sp杂化
D.Y的氢化物的沸点一定高于W的氢化物
12.实验室用右下图装置(夹持和加热装置略)制备乙酸异戊酯(沸点),实验中利用环己烷-水的共沸体系(沸点)带出水分。已知体系中沸点最低的有机物是环己烷(沸点),其反应原理如下:
下列说法错误的是
A.装置A的加热方式为水浴加热
B.利用共沸体系带出水分能促使反应正向进行
C.装置B中会出现分层现象
D.乙酸异戊酯最终在装置B中收集到
13.碳化镁具有反萤石结构,晶胞如图所示,熔融的碳化镁具有良好的导电性。已知晶胞边长为anm,阿伏加德罗常数的值为,下列叙述错误的是
A.碳化镁的化学式为
B.该晶体中碳的配位数为4
C.基态镁原子s、p能级上的电子数之比为
D.该晶体的密度为
14.对羟基苯乙酮()可作化妆品的防腐剂。某实验小组用乙酸乙酯从水溶液中提取对羟基苯乙酮,进行如下实验,虽操作规范,但所得产品中混有较多的乙酸乙酯。已知:对羟基苯乙酮的沸点为;乙酸乙酯的沸点为。下列叙述正确的是
A.分液时,水层、有机层依次从分液漏斗下口放出
B.萃取剂总量相同,分两次萃取的优点是提高萃取率
C.操作X为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
D.可在得到的水层中用银氨溶液检查对羟基苯乙酮是否残留
二、解答题
15.锌及其化合物在科学技术发展和人类生产生活中发挥着重要作用。回答下列问题:
(1)《天工开物》中记载了关于火法炼锌的工艺:以炉甘石和木炭为原料高温制取锌。基态Zn原子价层电子的轨道表示式为 ,其原子核外电子共有 种空间运动状态,中阴离子的空间结构名称为 。
(2)锌是人体必需的微量元素,下列现代分析方法中,可用于检验水中痕量锌元素的是 (填字母)。
a.X射线衍射 b.原子光谱 c.核磁共振氢谱 d.红外光谱
(3)黄铜是由铜和锌所组成的合金,是人类最早使用的合金之一。
①第一电离能:Zn (填“>”或“<”)Cu。
②Cu、Zn等金属具有良好导电性的原因是 。
(4)立方ZnS晶体常用作半导体材料,其晶胞结构如图,则ZnS晶胞的俯视投影图是 (填字母)。
16.M是常用的医用胶,在常温下可以快速固化实现黏合。其相关信息如下:
试样30.6g 氧气流中燃烧测得生成、
CuO作用下,二氧化碳气流中燃烧测得生成标准状况下
质谱法测得相对分子质量为153
红外光谱如图所示
回答下列问题:
(1)M的分子式为 。M可以由有机物A和B()通过酯化反应得到,已知A中含有4种不同化学环境的氢原子,且个数比为,可推测M的结构简式为 。
(2)M中 (填“存在”或“不存在”,下同)顺反异构, 对映异构。
(3)M具有黏合性的原因是发生了加聚反应(在微量水蒸气作用下),加聚反应的化学方程式为 。
(4)医用胶固化的具体机理如下:(R表示烃基,表示微观粒子带负电荷)
①该过程中的杂化方式为 。
②已知氰基和酯基能够活化碳碳双键,故医用胶比 (填“更易”或“更难”)发生加聚反应进行固化。
(5)医用胶使用后能够发生 (填“水解反应”或“加成反应”),最终在组织内降解被人体吸收。
17.某同学在实验室以某甲醛()为原料制备间溴苯甲醛()。
已知:①温度过高,间溴苯甲醛易被氧化。
②溴、苯甲醛、1,2-二氯乙烷、间溴苯甲醛的相关性质见下表:
物质 溴 苯甲醛 1,2-二氯乙烷 间溴苯甲醛
沸点 58.8℃ 179℃ 83.5℃ 229℃
溶解性 微溶于水 微溶于水 难溶于水 难溶于水
相对分子质量 160 106 99 185
实验步骤如下:
步骤1:将一定配比的无水(催化剂)、1,2-二氯乙烷(有机溶剂)和苯甲醛(5.3g)充分混合后装入三颈烧瓶(如下图所示,加热及夹持装置已省略),缓慢滴加足量经浓硫酸干燥过的液溴,控温反应一段时间,冷却。
步骤2:将反应后的混合物缓慢加入至一定量的稀盐酸中,搅拌、静置、分液。有机层用溶液洗涤。
步骤3:向经洗涤的有机层加入适量无水固体,放置一段时间后过滤出晶体。
步骤4:分离有机层,减压蒸馏有机相,收集相应馏分。
(1)仪器X的名称是 ,锥形瓶中的试剂为NaOH溶液,其作用是吸收 (填化学式)。与本实验安全注意事项有关的图标有 (填字母)。
A.护目镜 B.洗手 C.锐器 D.排风
(2)步骤1反应过程中,为提高原料利用率,适宜的温度范围为 (填字母)。
A. B.5 C.
(3)生成间溴苯甲醛的化学方程式为 ;其中催化剂的晶体类型为 。
(4)步骤2分液时有机相处于 (填“上层”或“下层”)。
(5)减压能够降低蒸馏温度,则步骤4中采用减压蒸馏是为了防止 。
(6)若实验结束后得到3.7g间溴苯甲醛,则本实验中间溴苯甲醛的产率为 %。
18.二甲双酮是一种抗惊厥药,以丙烯为起始原料的合成路线如下:
回答下列问题:
(1)丙烯→A的反应中,丙烯中断裂的是 (填“”或“”)键,A的名称为 。
(2)A→B的反应类型为 ,B的结构简式为 。
(3)C中包含的含氧官能团的名称为 。
(4)写出D→E的化学方程式 。
(5)关于上述的有机物,下列说法正确的是_____(填字母)。
A.丙烯分子中3个碳原子共直线 B.试剂X是
C.E能发生水解、氧化、加成反应 D.二甲双酮的分子式为
(6)在D的同分异构体中,与D含有相同官能团的有 种(不含D本身,不含立体异构)。
(7)结合上述信息,以为原料,设计丙烯酸的合成路线如下:
该合成路线中反应所需试剂X为 (填化学式),物质Y的结构简式为 。
参考答案
1.B
2.B
3.A
4.D
5.C
6.B
7.D
8.A
9.C
10.A
11.C
12.D
13.B
14.B
15.(1) 15或十五 平面三角形
(2)b
(3) > 金属晶体中的自由电子(或离域电子)在外加电场作用下可发生定向移动
(4)b
16.(1) 或
(2) 不存在 不存在
(3)
(4) 更易
(5)水解反应
17.(1) 球形冷凝管 和HBr ABD
(2)C
(3) 分子晶体
(4)下层
(5)间溴苯甲醛因温度过高被氧化或醛基因温度过高被氧化
(6)40或40.0或40.00
18.(1) 异丙醇或2-丙醇
(2) 氧化反应
(3)羟基
(4)
(5)BD
(6)4或四
(7) HCN
同课章节目录
