山西省吕梁市2024-2025学年高二下学期期末调研测试化学试卷(含答案)
文档属性
| 名称 | 山西省吕梁市2024-2025学年高二下学期期末调研测试化学试卷(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 911.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-04 00:00:00 | ||
图片预览





文档简介
山西省吕梁市2024-2025学年高二下学期期末调研测试化学试题
一、单选题
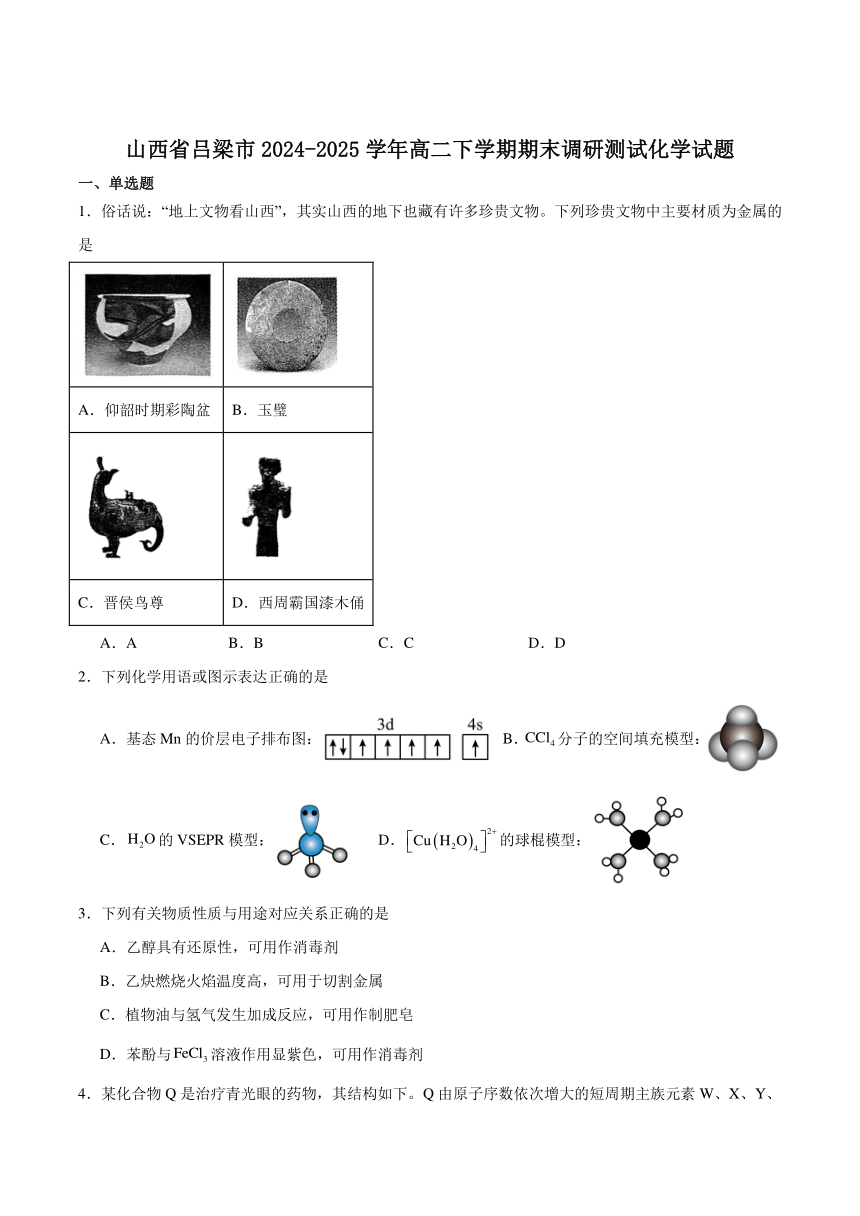
1.俗话说:“地上文物看山西”,其实山西的地下也藏有许多珍贵文物。下列珍贵文物中主要材质为金属的是
A.仰韶时期彩陶盆 B.玉璧
C.晋侯鸟尊 D.西周霸国漆木俑
A.A B.B C.C D.D
2.下列化学用语或图示表达正确的是
A.基态Mn的价层电子排布图: B.分子的空间填充模型:
C.的VSEPR模型: D.的球棍模型:
3.下列有关物质性质与用途对应关系正确的是
A.乙醇具有还原性,可用作消毒剂
B.乙炔燃烧火焰温度高,可用于切割金属
C.植物油与氢气发生加成反应,可用作制肥皂
D.苯酚与溶液作用显紫色,可用作消毒剂
4.某化合物Q是治疗青光眼的药物,其结构如下。Q由原子序数依次增大的短周期主族元素W、X、Y、Z、M组成,只有X、Y、Z同周期,下列说法正确的是
A.同周期第一电离能大于M的元素只有2种
B.含氧酸的酸性:M>Y>X
C.氢化物的沸点:XD.W与X、Y、Z、M均可形成18电子微粒
5.硫代硫酸盐是具有应用前景的浸金试剂。硫代硫酸根离子()可看作中的一个O原子被S原子替代的产物。的晶胞形状为长方体,棱长分别为nm、nm、nm,其结构如图所示,已知的摩尔质量是,为阿伏加德罗常数的值,下列说法正确的是
A.中H-O-H的键角大于中H-O-H的键角
B.浸金时,与形成配离子,中的中心S原子提供孤电子对
C.的中心硫原子的杂化方式为
D.该晶体的密度为
6.氢气是清洁能源之一,解决氢气的存储问题是当今科学界需要攻克的课题。是新型环烯类储氢材料,利用物理吸附的方法来储存氢分子,其分子结构如图所示,下列说法正确的是
A.的熔点高是因为分子中共价键的键能大
B.完全燃烧的产物均为非极性分子
C.1个分子中含有32个键
D.储氢时与间的作用力为分子间氢键
7.托伐普坦是一种治疗心血管疾病的药物,其结构如图所示,下列说法错误的是
A.L的分子式为C26H23N2O3Cl
B.L中的含氧官能团有酰胺基和酮羰基
C.L与足量H2完全加成的产物中有1个手性碳原子
D.L与酸或碱反应都可生成盐
8.某香料N的合成路线如下:。下列说法正确的是
A.试剂X可能为或溶液
B.与足量的NaOH水溶液反应的化学方程式为
C.等物质的量的M、N分别与足量的反应,最多消耗的物质的量比为1:1
D.Y中所有原子可能在同一平面
9.由有机化合物制备的合成路线中,最合理的路线涉及的反应类型依次是
A.加成反应、消去反应、氧化反应 B.加成反应、取代反应、氧化反应
C.加成反应、氧化反应、消去反应 D.氧化反应、取代反应、加成反应
10.下列实验方案、现象及结论不相符的是
选项 实验方案 现象 结论
A 取少许有机物滴入盛有银氨溶液的试管中,水浴加热 产生光亮的银镜 该有机物属于醛类物质
B 加热溴乙烷与NaOH的混合溶液,冷却后滴加溶液 产生沉淀 不能直接证明溴乙烷中含有溴元素
C 乙醇与浓硫酸共热至170℃,将产生的气体先通过NaOH溶液,再通入溴水中 溴水褪色 乙醇发生了消去反应
D 向某溶液中加入几滴浓硝酸,加热 先有白色沉淀,加热后沉淀变黄 该溶液中含蛋白质
A.A B.B C.C D.D
11.某种聚碳酸酯的透光性好,可制成车、船的挡风玻璃,以及眼镜镜片、光盘等,其结构可表示为:。原来合成聚碳酸酯的一种原料是有毒的光气(,又称碳酰氯),为贯彻绿色化学理念可以用碳酸二甲酯()与某种物质M聚合生产聚碳酸酯。下列说法正确的是
A.M可能是二酚类物质 B.该聚合反应为加成聚合反应
C.反应过程中一定生成小分子物质 D.该聚碳酸酯具有良好的亲水性
12.下列说法正确的是
A.一氯乙烷、一氯乙烯、一氯乙炔中C—Cl键长逐渐增长
B.氢键是一种特殊的化学键,蛋白质的二级结构与其有密切关系
C.金属能导电是因为金属阳离子在外加电场的作用下发生定向移动
D.平面形分子酞菁的结构见上图,则p轨道能提供一对电子的N原子是③
13.下列各组有机物只用一种试剂无法进行鉴别的是
A.乙醇 乙酸 葡萄糖 B.甲苯 溴苯 苯
C.苯酚 乙酸 1-己烯 D.苯 1-己烯 环己烷
14.物质结构决定其性质,下列实例与解释不相符的是
选项 实例 解释
A 利用“杯酚”可分离和 “杯酚”是超分子,具有分子识别的特性
B 酸性: 的极性大于,使的羧基中羟基的极性更大,更易电离出
C 离子液体难挥发 组成离子液体的粒子全都是带电荷的离子
D 纳米晶体有不同于大块晶体的特性,如熔点会随晶粒的减小而降低 纳米晶体的表面积比大块晶体的大
A.A B.B C.C D.D
二、解答题
15.有机化学实验室大量制备乙酸乙酯通常经过反应回流和产物蒸馏提纯两个步骤。
步骤一:反应回流
在圆底烧瓶中加入体积比为1:1的乙醇和冰醋酸各57mL,再加入乙醇和浓硫酸的混合物14.5mL。将圆底烧瓶与球形冷凝管连接,加热圆底烧瓶,并保持温度为110~120℃。
步骤二:产物蒸馏提纯
反应后将回流装置改装成蒸馏装置,加热圆底烧瓶,控制温度在80℃以下,获得粗产品。在获得的粗产品中缓慢加入饱和溶液至无二氧化碳逸出,分液保留酯层;在酯层中加入等体积的饱和NaCl溶液,充分混匀,酯层用pH试纸检验呈中性,分液保留酯层;向产品中继续加入饱和溶液,充分混匀,以去除酯层中的乙醇,分液保留酯层;向产品中加入无水硫酸镁,干燥;对产品再次蒸馏,收集馏分。几种有机化合物的沸点
物质 乙醇 乙酸 乙酸乙酯
沸点/℃ 78.5 117.9 77.1
(1)选用圆底烧瓶的规格为 。
A.100mL B.250mL C.500mL
(2)混合乙醇和浓硫酸的操作是 。
(3)步骤一中,加热方式是 。
(4)球形冷凝管的作用是 。
(5)加入饱和NaCl溶液的目的是 ,收集 ℃左右馏分。
(6)写出制备乙酸乙酯的方程式 。
16.X、Y、Z、T四种元素,它们的原子序数依次增大,X原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,T原子核外的M层中只有两对成对电子。请回答下列问题:
(1)Y属于 区元素,Z元素基态原子的电子排布式为 ,四种元素中电负性最大的是 (填元素符号)。
(2)相同条件下与在水中的溶解度较大的是 (写分子式),主要原因是 。
(3)的空间结构名称是 。
(4)Y可与氢原子形成离子化合物,各原子均满足2电子或8电子稳定结构,的电子式是 。
(5)Y与铁形成的晶体,其晶胞结构如图所示,对于位置的Fe原子,与其最近且距离相等的Y原子有 个,该晶体的化学式为 。
17.有机高分子A可用于生产俗称“白乳胶”的木材黏合剂,B通过加聚反应可制得A。B的燃烧产物只有和,完全燃烧21.5gB,生成22.4L(标准状况),B的蒸气对的相对密度为43。几种物质的转化关系如图所示:
已知:①羟基与碳碳双键直接相连的有机化合物会迅速转化为醛;②。
回答下列问题:
(1)A的结构简式为 。
(2)E生成D的化学方程式为 。
(3)写出属于不饱和羧酸的B的同分异构体的结构简式(不考虑立体异构) 。
(4)G生成链状缩聚物的化学方程式为 。
(5)有机化合物H是G的同系物,且相对分子质量比G的大14,两分子H反应可生成六元环状化合物,则H的结构简式为 。
18.化合物J是一种重要药物中间体,其合成路线如下(部分试剂和条件略):
已知:ⅰMe为甲基,Et为乙基,Ac为醋酸根,rt为室温。
ⅱ(为烃基或氢原子)。
ⅲ具有还原性。
根据合成路线回答下列问题:
(1)C中除含氧官能团外,还含有 。
(2)B转化为C的反应中碳酸钾的作用为 。
(3)G转化为H的化学方程式为 。
(4)M是A的同分异构体,M与溶液作用显紫色,则M的结构有 种;其中核磁共振氢谱显示有4组峰,且峰面积之比为2:2:2:1的结构简式为 。
(5)H→I经历了如图所示的多步反应:。中间产物1、中间产物2的结构简式分别是 、 。
参考答案
1.C
2.D
3.B
4.D
5.A
6.C
7.C
8.B
9.B
10.A
11.A
12.D
13.D
14.A
15.(1)B
(2)将浓硫酸缓慢加入乙醇中并不断搅拌
(3)电加热套或油浴
(4)冷凝回流反应物
(5) 洗出酯层中的少量碳酸钠,降低乙酸乙酯的溶解度 77
(6)
16.(1) p O
(2) 和都是极性分子,根据“相似相溶”原理,在中的溶解度较大
(3)平面三角形
(4)
(5) 8
17.(1)
(2)
(3)、、
(4)
(5)
18.(1)碳氟键、氰基
(2)吸收反应生成的HBr,提高产率
(3)+
(4) 16种
(5)
一、单选题
1.俗话说:“地上文物看山西”,其实山西的地下也藏有许多珍贵文物。下列珍贵文物中主要材质为金属的是
A.仰韶时期彩陶盆 B.玉璧
C.晋侯鸟尊 D.西周霸国漆木俑
A.A B.B C.C D.D
2.下列化学用语或图示表达正确的是
A.基态Mn的价层电子排布图: B.分子的空间填充模型:
C.的VSEPR模型: D.的球棍模型:
3.下列有关物质性质与用途对应关系正确的是
A.乙醇具有还原性,可用作消毒剂
B.乙炔燃烧火焰温度高,可用于切割金属
C.植物油与氢气发生加成反应,可用作制肥皂
D.苯酚与溶液作用显紫色,可用作消毒剂
4.某化合物Q是治疗青光眼的药物,其结构如下。Q由原子序数依次增大的短周期主族元素W、X、Y、Z、M组成,只有X、Y、Z同周期,下列说法正确的是
A.同周期第一电离能大于M的元素只有2种
B.含氧酸的酸性:M>Y>X
C.氢化物的沸点:X
5.硫代硫酸盐是具有应用前景的浸金试剂。硫代硫酸根离子()可看作中的一个O原子被S原子替代的产物。的晶胞形状为长方体,棱长分别为nm、nm、nm,其结构如图所示,已知的摩尔质量是,为阿伏加德罗常数的值,下列说法正确的是
A.中H-O-H的键角大于中H-O-H的键角
B.浸金时,与形成配离子,中的中心S原子提供孤电子对
C.的中心硫原子的杂化方式为
D.该晶体的密度为
6.氢气是清洁能源之一,解决氢气的存储问题是当今科学界需要攻克的课题。是新型环烯类储氢材料,利用物理吸附的方法来储存氢分子,其分子结构如图所示,下列说法正确的是
A.的熔点高是因为分子中共价键的键能大
B.完全燃烧的产物均为非极性分子
C.1个分子中含有32个键
D.储氢时与间的作用力为分子间氢键
7.托伐普坦是一种治疗心血管疾病的药物,其结构如图所示,下列说法错误的是
A.L的分子式为C26H23N2O3Cl
B.L中的含氧官能团有酰胺基和酮羰基
C.L与足量H2完全加成的产物中有1个手性碳原子
D.L与酸或碱反应都可生成盐
8.某香料N的合成路线如下:。下列说法正确的是
A.试剂X可能为或溶液
B.与足量的NaOH水溶液反应的化学方程式为
C.等物质的量的M、N分别与足量的反应,最多消耗的物质的量比为1:1
D.Y中所有原子可能在同一平面
9.由有机化合物制备的合成路线中,最合理的路线涉及的反应类型依次是
A.加成反应、消去反应、氧化反应 B.加成反应、取代反应、氧化反应
C.加成反应、氧化反应、消去反应 D.氧化反应、取代反应、加成反应
10.下列实验方案、现象及结论不相符的是
选项 实验方案 现象 结论
A 取少许有机物滴入盛有银氨溶液的试管中,水浴加热 产生光亮的银镜 该有机物属于醛类物质
B 加热溴乙烷与NaOH的混合溶液,冷却后滴加溶液 产生沉淀 不能直接证明溴乙烷中含有溴元素
C 乙醇与浓硫酸共热至170℃,将产生的气体先通过NaOH溶液,再通入溴水中 溴水褪色 乙醇发生了消去反应
D 向某溶液中加入几滴浓硝酸,加热 先有白色沉淀,加热后沉淀变黄 该溶液中含蛋白质
A.A B.B C.C D.D
11.某种聚碳酸酯的透光性好,可制成车、船的挡风玻璃,以及眼镜镜片、光盘等,其结构可表示为:。原来合成聚碳酸酯的一种原料是有毒的光气(,又称碳酰氯),为贯彻绿色化学理念可以用碳酸二甲酯()与某种物质M聚合生产聚碳酸酯。下列说法正确的是
A.M可能是二酚类物质 B.该聚合反应为加成聚合反应
C.反应过程中一定生成小分子物质 D.该聚碳酸酯具有良好的亲水性
12.下列说法正确的是
A.一氯乙烷、一氯乙烯、一氯乙炔中C—Cl键长逐渐增长
B.氢键是一种特殊的化学键,蛋白质的二级结构与其有密切关系
C.金属能导电是因为金属阳离子在外加电场的作用下发生定向移动
D.平面形分子酞菁的结构见上图,则p轨道能提供一对电子的N原子是③
13.下列各组有机物只用一种试剂无法进行鉴别的是
A.乙醇 乙酸 葡萄糖 B.甲苯 溴苯 苯
C.苯酚 乙酸 1-己烯 D.苯 1-己烯 环己烷
14.物质结构决定其性质,下列实例与解释不相符的是
选项 实例 解释
A 利用“杯酚”可分离和 “杯酚”是超分子,具有分子识别的特性
B 酸性: 的极性大于,使的羧基中羟基的极性更大,更易电离出
C 离子液体难挥发 组成离子液体的粒子全都是带电荷的离子
D 纳米晶体有不同于大块晶体的特性,如熔点会随晶粒的减小而降低 纳米晶体的表面积比大块晶体的大
A.A B.B C.C D.D
二、解答题
15.有机化学实验室大量制备乙酸乙酯通常经过反应回流和产物蒸馏提纯两个步骤。
步骤一:反应回流
在圆底烧瓶中加入体积比为1:1的乙醇和冰醋酸各57mL,再加入乙醇和浓硫酸的混合物14.5mL。将圆底烧瓶与球形冷凝管连接,加热圆底烧瓶,并保持温度为110~120℃。
步骤二:产物蒸馏提纯
反应后将回流装置改装成蒸馏装置,加热圆底烧瓶,控制温度在80℃以下,获得粗产品。在获得的粗产品中缓慢加入饱和溶液至无二氧化碳逸出,分液保留酯层;在酯层中加入等体积的饱和NaCl溶液,充分混匀,酯层用pH试纸检验呈中性,分液保留酯层;向产品中继续加入饱和溶液,充分混匀,以去除酯层中的乙醇,分液保留酯层;向产品中加入无水硫酸镁,干燥;对产品再次蒸馏,收集馏分。几种有机化合物的沸点
物质 乙醇 乙酸 乙酸乙酯
沸点/℃ 78.5 117.9 77.1
(1)选用圆底烧瓶的规格为 。
A.100mL B.250mL C.500mL
(2)混合乙醇和浓硫酸的操作是 。
(3)步骤一中,加热方式是 。
(4)球形冷凝管的作用是 。
(5)加入饱和NaCl溶液的目的是 ,收集 ℃左右馏分。
(6)写出制备乙酸乙酯的方程式 。
16.X、Y、Z、T四种元素,它们的原子序数依次增大,X原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,T原子核外的M层中只有两对成对电子。请回答下列问题:
(1)Y属于 区元素,Z元素基态原子的电子排布式为 ,四种元素中电负性最大的是 (填元素符号)。
(2)相同条件下与在水中的溶解度较大的是 (写分子式),主要原因是 。
(3)的空间结构名称是 。
(4)Y可与氢原子形成离子化合物,各原子均满足2电子或8电子稳定结构,的电子式是 。
(5)Y与铁形成的晶体,其晶胞结构如图所示,对于位置的Fe原子,与其最近且距离相等的Y原子有 个,该晶体的化学式为 。
17.有机高分子A可用于生产俗称“白乳胶”的木材黏合剂,B通过加聚反应可制得A。B的燃烧产物只有和,完全燃烧21.5gB,生成22.4L(标准状况),B的蒸气对的相对密度为43。几种物质的转化关系如图所示:
已知:①羟基与碳碳双键直接相连的有机化合物会迅速转化为醛;②。
回答下列问题:
(1)A的结构简式为 。
(2)E生成D的化学方程式为 。
(3)写出属于不饱和羧酸的B的同分异构体的结构简式(不考虑立体异构) 。
(4)G生成链状缩聚物的化学方程式为 。
(5)有机化合物H是G的同系物,且相对分子质量比G的大14,两分子H反应可生成六元环状化合物,则H的结构简式为 。
18.化合物J是一种重要药物中间体,其合成路线如下(部分试剂和条件略):
已知:ⅰMe为甲基,Et为乙基,Ac为醋酸根,rt为室温。
ⅱ(为烃基或氢原子)。
ⅲ具有还原性。
根据合成路线回答下列问题:
(1)C中除含氧官能团外,还含有 。
(2)B转化为C的反应中碳酸钾的作用为 。
(3)G转化为H的化学方程式为 。
(4)M是A的同分异构体,M与溶液作用显紫色,则M的结构有 种;其中核磁共振氢谱显示有4组峰,且峰面积之比为2:2:2:1的结构简式为 。
(5)H→I经历了如图所示的多步反应:。中间产物1、中间产物2的结构简式分别是 、 。
参考答案
1.C
2.D
3.B
4.D
5.A
6.C
7.C
8.B
9.B
10.A
11.A
12.D
13.D
14.A
15.(1)B
(2)将浓硫酸缓慢加入乙醇中并不断搅拌
(3)电加热套或油浴
(4)冷凝回流反应物
(5) 洗出酯层中的少量碳酸钠,降低乙酸乙酯的溶解度 77
(6)
16.(1) p O
(2) 和都是极性分子,根据“相似相溶”原理,在中的溶解度较大
(3)平面三角形
(4)
(5) 8
17.(1)
(2)
(3)、、
(4)
(5)
18.(1)碳氟键、氰基
(2)吸收反应生成的HBr,提高产率
(3)+
(4) 16种
(5)
同课章节目录
