苏教版高中化学必修第一册专题2研究物质的基本方法2.1.3物质的检验物质性质和变化的探究教学课件(共21张PPT)
文档属性
| 名称 | 苏教版高中化学必修第一册专题2研究物质的基本方法2.1.3物质的检验物质性质和变化的探究教学课件(共21张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-09 00:00:00 | ||
图片预览







文档简介
(共21张PPT)
第一单元 研究物质的基本方法
2.1.3 物质的检验
物质性质和变化的探究
白醋?
白酒?
水?
酱油?
Na2CO3?
CaCO3?
O2?
CO2?
真毛线?
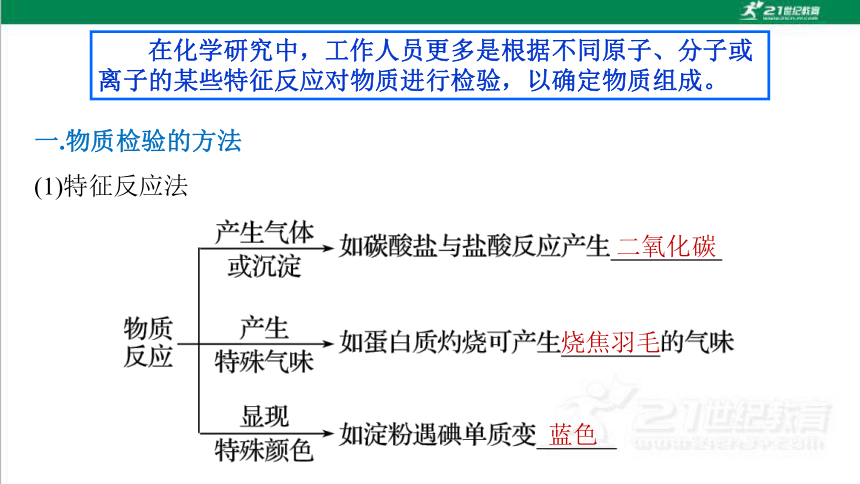
在化学研究中,工作人员更多是根据不同原子、分子或离子的某些特征反应对物质进行检验,以确定物质组成。
一.物质检验的方法
(1)特征反应法
二氧化碳
烧焦羽毛
蓝色
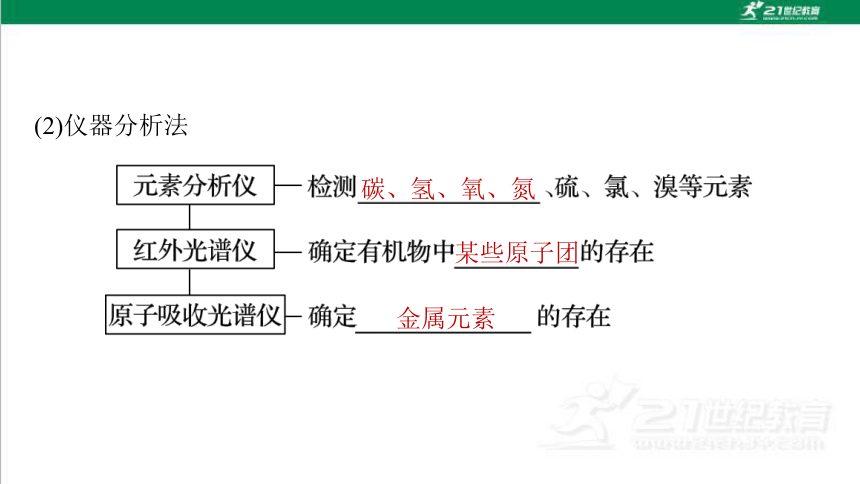
(2)仪器分析法
碳、氢、氧、氮
某些原子团
金属元素
教材P33 观察思考
检验氯化铵、硫酸铵、氯化钾、硫酸钾中的所含离子。
NH4Cl
(NH4)2SO4
KCl
K2SO4
NH4+
Cl-
K+
SO42-
二.常见离子的检验
(一)NH4+的检验方法
1、试剂:
取样加NaOH溶液,加热,将湿润的红色石蕊试纸靠近试管口
2、实验操作:
试纸变蓝色
3、现象:
(NH4)2SO4 , NH4Cl, NaOH溶液
5、检验方法:
4、化学方程式:
取样与强碱溶液加热,生成的气体使湿润的红色石蕊试纸变蓝,则含有NH4+
(二)Cl-的检验方法
1、试剂:
取样加AgNO3溶液和稀HNO3
2、实验操作:
生成白色沉淀
3、现象:
KCl, NH4Cl, 稀HNO3, AgNO3溶液
4、反应方程式:
5、检验方法:
取样加AgNO3溶液,若生成不溶于稀HNO3的白色沉淀,说明试样含Cl-
6、思考:
②不能用稀HCl,H2SO4代替:
加稀HNO3的目的:
排除CO32-、SO42-的干扰
因为会引入Cl-, SO42-
②
1、试剂:
取样加稀HCl酸化后,加入BaCl2溶液
2、实验操作:
生成白色沉淀
3、现象:
(三) SO42-的检验方法
(NH4)2SO4 , K2SO4 , 稀HCl, BaCl2溶液
4、反应方程式:
5、检验方法:
取样加稀HCl无沉淀生成,再加BaCl2溶液,若生成白色沉淀,说明该试样含SO42-
6、思考:
② 不能用稀HNO3, Ba(NO3)2代替:
加稀HCl的目的:
排除CO32-、Ag+、SO32-的干扰
在H+ 存在时,NO3-有氧化性,可将SO32-氧化为SO42-
1、焰色反应:
(四) K+,Na+的检验方法
很多金属或它们的化合物在火焰上灼烧时使火焰呈现特殊的颜色的反应。
盐酸
原火焰颜色相同
试样
火焰的颜色
盐酸
无色
2、操作
3、几种金属的焰色
①钠元素的焰色反应呈____色。
②钾元素的焰色反应呈____色(透过蓝色的钴玻璃观察)。
黄
紫
焰色反应属于 反应
② 指金属元素的性质 (如Na+ 和Na的反应现象相同)
物理
4、 注意事项
焰色反应实例:烟花
随堂练习
1、能用来区别BaCl2,Na2CO3,NaCl 溶液的试剂是( )
A. AgNO3
D. 稀盐酸
C. 稀硝酸
B. 稀硫酸
B
2、判断正误:
(1)加入AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有Cl-存在。
(2)加入BaCl2溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42-
4. 某试样的焰色反应呈黄色,下列对该试样成分的说法正确的是( )
A.肯定是钠单质
D.可能含有钾元素
C.肯定含有钠元素
B.肯定是钠的化合物
3、四瓶标签模糊的试剂: NH4Cl, (NH4)2SO4, K2SO4, NaCl
请问如何只用一种试剂鉴别它们?
Ba(OH)2溶液
C
随堂练习
三、物质性质和变化的探究
1.设计实验探究铝的性质
实验操作 主要现象 结论
打磨铝片,观察 打磨后为_____色 铝是_____色金属,铝在空气中易被氧化,形成一层氧化膜
___________________
加热未打磨的铝片 铝片内部熔融但不下滴 表层有一层Al2O3,且熔点高于Al单质
银白
银白
4Al+3O2===2Al2O3
铝片均溶解,且均有气泡产生 Al既能与盐酸反应又能与NaOH溶液反应
_____________________________、
______________________________________
2Al+6HCl===2AlCl3+3H2↑
2Al+2NaOH+2H2O===2NaAlO2+3H2↑
[方法总结]
2.设计实验方案探究影响双氧水分解速率的因素(提示:控制单一变量)
实验序号 实验方案 现象 结论
① 气泡产生较慢 ①浓度越大,H2O2分解速率_____
②温度越高,H2O2分解速率_____
③加催化剂,H2O2分解速率_____
② 气泡产生非常慢
③ 气泡产生较快
④ 气泡产生非常快
越快
越快
加快
认识物质的性质和变化的一般思路
归纳总结
第一单元 研究物质的基本方法
2.1.3 物质的检验
物质性质和变化的探究
白醋?
白酒?
水?
酱油?
Na2CO3?
CaCO3?
O2?
CO2?
真毛线?
在化学研究中,工作人员更多是根据不同原子、分子或离子的某些特征反应对物质进行检验,以确定物质组成。
一.物质检验的方法
(1)特征反应法
二氧化碳
烧焦羽毛
蓝色
(2)仪器分析法
碳、氢、氧、氮
某些原子团
金属元素
教材P33 观察思考
检验氯化铵、硫酸铵、氯化钾、硫酸钾中的所含离子。
NH4Cl
(NH4)2SO4
KCl
K2SO4
NH4+
Cl-
K+
SO42-
二.常见离子的检验
(一)NH4+的检验方法
1、试剂:
取样加NaOH溶液,加热,将湿润的红色石蕊试纸靠近试管口
2、实验操作:
试纸变蓝色
3、现象:
(NH4)2SO4 , NH4Cl, NaOH溶液
5、检验方法:
4、化学方程式:
取样与强碱溶液加热,生成的气体使湿润的红色石蕊试纸变蓝,则含有NH4+
(二)Cl-的检验方法
1、试剂:
取样加AgNO3溶液和稀HNO3
2、实验操作:
生成白色沉淀
3、现象:
KCl, NH4Cl, 稀HNO3, AgNO3溶液
4、反应方程式:
5、检验方法:
取样加AgNO3溶液,若生成不溶于稀HNO3的白色沉淀,说明试样含Cl-
6、思考:
②不能用稀HCl,H2SO4代替:
加稀HNO3的目的:
排除CO32-、SO42-的干扰
因为会引入Cl-, SO42-
②
1、试剂:
取样加稀HCl酸化后,加入BaCl2溶液
2、实验操作:
生成白色沉淀
3、现象:
(三) SO42-的检验方法
(NH4)2SO4 , K2SO4 , 稀HCl, BaCl2溶液
4、反应方程式:
5、检验方法:
取样加稀HCl无沉淀生成,再加BaCl2溶液,若生成白色沉淀,说明该试样含SO42-
6、思考:
② 不能用稀HNO3, Ba(NO3)2代替:
加稀HCl的目的:
排除CO32-、Ag+、SO32-的干扰
在H+ 存在时,NO3-有氧化性,可将SO32-氧化为SO42-
1、焰色反应:
(四) K+,Na+的检验方法
很多金属或它们的化合物在火焰上灼烧时使火焰呈现特殊的颜色的反应。
盐酸
原火焰颜色相同
试样
火焰的颜色
盐酸
无色
2、操作
3、几种金属的焰色
①钠元素的焰色反应呈____色。
②钾元素的焰色反应呈____色(透过蓝色的钴玻璃观察)。
黄
紫
焰色反应属于 反应
② 指金属元素的性质 (如Na+ 和Na的反应现象相同)
物理
4、 注意事项
焰色反应实例:烟花
随堂练习
1、能用来区别BaCl2,Na2CO3,NaCl 溶液的试剂是( )
A. AgNO3
D. 稀盐酸
C. 稀硝酸
B. 稀硫酸
B
2、判断正误:
(1)加入AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有Cl-存在。
(2)加入BaCl2溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42-
4. 某试样的焰色反应呈黄色,下列对该试样成分的说法正确的是( )
A.肯定是钠单质
D.可能含有钾元素
C.肯定含有钠元素
B.肯定是钠的化合物
3、四瓶标签模糊的试剂: NH4Cl, (NH4)2SO4, K2SO4, NaCl
请问如何只用一种试剂鉴别它们?
Ba(OH)2溶液
C
随堂练习
三、物质性质和变化的探究
1.设计实验探究铝的性质
实验操作 主要现象 结论
打磨铝片,观察 打磨后为_____色 铝是_____色金属,铝在空气中易被氧化,形成一层氧化膜
___________________
加热未打磨的铝片 铝片内部熔融但不下滴 表层有一层Al2O3,且熔点高于Al单质
银白
银白
4Al+3O2===2Al2O3
铝片均溶解,且均有气泡产生 Al既能与盐酸反应又能与NaOH溶液反应
_____________________________、
______________________________________
2Al+6HCl===2AlCl3+3H2↑
2Al+2NaOH+2H2O===2NaAlO2+3H2↑
[方法总结]
2.设计实验方案探究影响双氧水分解速率的因素(提示:控制单一变量)
实验序号 实验方案 现象 结论
① 气泡产生较慢 ①浓度越大,H2O2分解速率_____
②温度越高,H2O2分解速率_____
③加催化剂,H2O2分解速率_____
② 气泡产生非常慢
③ 气泡产生较快
④ 气泡产生非常快
越快
越快
加快
认识物质的性质和变化的一般思路
归纳总结
