苏教版高中化学必修第一册专题3从海水中获得的化学物质3.1.4氧化剂和还原剂课件(25张)
文档属性
| 名称 | 苏教版高中化学必修第一册专题3从海水中获得的化学物质3.1.4氧化剂和还原剂课件(25张) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-07 00:00:00 | ||
图片预览








文档简介
(共25张PPT)
第一单元 氯气及氯的化合物 第4课时 氧化剂和还原剂
专题3 从海水中获得的化学物质
学习目标
1.能从化学反应中元素化合价的变化认识氧化剂和还原剂、氧化产物和还原产物等概念,熟知常见的氧化剂和还原剂,理清相关概念间的关系。促进“变化观念”化学核心素养的发展。
2.认识物质的氧化性、还原性,学会分析预测物质具有的氧化性或还原性,建立判断物质氧化性、还原性强弱的“思维模型”。
氧化剂:所含元素得到电子(或电子对偏向)的反应物。
还原剂:所含元素失去电子(或电子对偏离)的反应物。
氧化剂
还原剂
口诀:氧价降
一、氧化剂 还原剂
化合价降低
化合价升高
①.氧化剂和还原剂均是指反应物质,是一种化学试剂,不是某一种元素。
②.氧化剂本身被还原,化合价降低,发生还原反应
③.还原剂本身被氧化,化合价升高,发生氧化反应
注意
2Na+Cl2===2NaCl
氧化剂
还原剂
-1
+1
0
0
一、氧化剂 还原剂
氧化剂是_____,还原剂是_____;
发生氧化反应的是_____,发生还原反应的是_____。
Cl2
Cl2
Fe
Fe
-1
+3
0
0
一、氧化剂 还原剂
常见的氧化剂
一、氧化剂 还原剂
物质种类 常见物质
氧
化
剂 部分非金属单质
含有高价态元素的化合物
某些金属活动性较弱的元素对应的高价态离子
过氧化物
O2、Cl2等
浓硫酸、HNO3、KMnO4、MnO2、KClO3、K2Cr2O7等
Fe3+、Ag+、Cu2+等
Na2O2、H2O2等
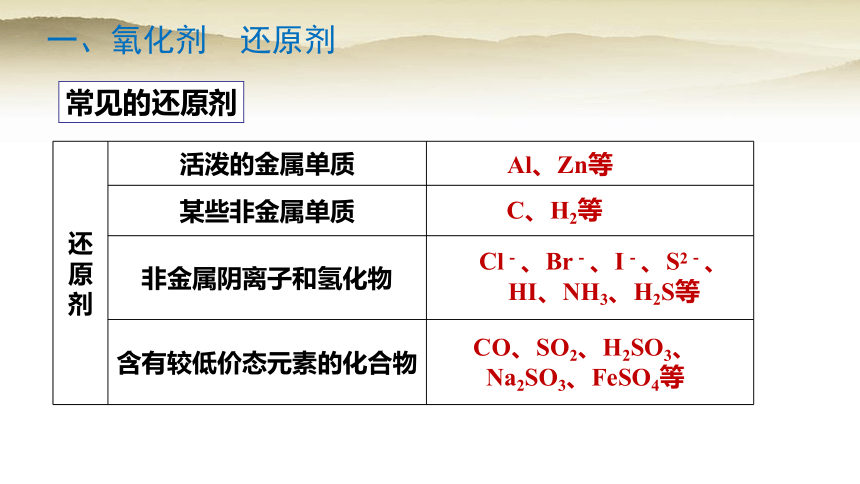
常见的还原剂
一、氧化剂 还原剂
还
原
剂 活泼的金属单质
某些非金属单质
非金属阴离子和氢化物
含有较低价态元素的化合物
Al、Zn等
C、H2等
Cl-、Br-、I-、S2-、HI、NH3、H2S等
CO、SO2、H2SO3、Na2SO3、FeSO4等
-1
+1
0
以下反应的氧化剂和还原剂是什么?
Cl2 + H2O = HCl + HClO
在反应中,氧化剂和还原剂可以是同一物质
氧化剂
还原剂
二、氧化产物 还原产物
氧化产物:还原剂失去电子被氧化的产物
还原产物:氧化剂得到电子被还原的产物
2HCl+Fe =FeCl2+H2↑
氧化剂
还原剂
氧化产物
还原产物
(元素化合价升高)生成物
(元素化合价降低)生成物
二、氧化产物 还原产物
是氧化剂 是还原剂
被氧化 被还原
氧化产物 还原产物
-1
+4
+2
MnO2
HCl
HCl
MnO2
Cl2
MnCl2
0
二、氧化产物 还原产物
氧化剂+还原剂=氧化产物+还原产物
化合价降低,得到电子,被还原,发生还原反应
化合价升高,失去电子,被氧化,发生氧化反应
降得还原氧化剂 升失氧化还原剂
口诀
二、氧化产物 还原产物
2Na+Cl2===2NaCl
氧化剂
还原剂
-1
+1
0
0
以下反应的氧化产物和还原产物是什么?
在反应中,氧化产物和还原产物可以是同一物质
氧化产物
还原产物
二、氧化产物 还原产物
判断以下反应的氧化剂、还原剂、氧化产物和还原产物
2KMnO4 K2MnO4+MnO2+O2↑
氧化剂
还原剂
氧化产物
还原产物
反应中某些物质没有“身份”
氧化剂
还原剂
0
+2
-1
+4
0
+6
+7
-2
+4
氧化产物
还原产物
还原产物
反应中某些物质“身份”相同
二、氧化产物 还原产物
二、氧化产物 还原产物
Cl-
SO2
NO或NO2
Mn2+
Fe2+或Fe
Zn2+
H+
CO2
Fe3+
典例解析
例1. 歌词“帘外芭蕉惹骤雨,门环惹铜绿”,其中的“铜绿”即是铜锈,它的化学成分是Cu2(OH)2CO3(碱式碳酸铜)。铜在潮湿的空气中生锈的化学反应为2Cu+O2+CO2+H2O===Cu2(OH)2CO3。下列有关该反应的说法中不正确的是( )
A.该反应是化合反应
B.该反应中氧气是氧化剂,单质铜是还原剂
C.该反应是氧化还原反应,只有两种元素的化合价发生了变化
D.该反应是氧化还原反应,其中Cu得电子,O2失电子
D
氧化剂具有氧化性
氧化性:物质得电子的性质或能力
还原性:物质失电子的性质或能力
即化合价降低的能力
即化合价升高的能力
还原剂具有还原性
三、氧化性 还原性
三、氧化性 还原性
物质的氧化性及还原性与核心元素化合价的关系
氧化性
氧化性
还原性
还原性
核心元素化合价 实例 性质
最高价 只有_______
中间价 既有_______
又有_______
最低价 只有_______
还原性:还原剂 还原产物;
氧化性:氧化剂 氧化产物。
(强氧化性) (强还原性) (弱还原性) (弱氧化性)
强弱规律
>
>
即“强制弱”或“前强后弱”
三、氧化性 还原性
金属还原性:Fe Cu
>
Fe+CuSO4===FeSO4+Cu
氧化剂
还原剂
氧化产物
还原产物
三、氧化性 还原性
三、氧化性 还原性
(2)根据元素的活动性顺序比较
特点:上左下右可反应,隔之愈远愈易行。
三、氧化性 还原性
氧化性:
Cl2>S
三、氧化性 还原性
氧化性:
KMnO4>MnO2
例2.根据下列反应的离子方程式:①2Fe3++2I-===2Fe2++I2;②Br2+2Fe2+===2Br-+2Fe3+,可判断各物质的氧化性由强到弱的顺序是( )
A.Fe3+、Br2、I2 B.Fe3+、I2、Br2
C.Br2、Fe3+、I2 D.Br2、I2、Fe3+
C
典例解析
课堂小结
氧化剂 还原剂
不良反应
氧化产物 还原产物
氧化性 还原性
氧化性 还原性强弱比较
随堂练习
D
第一单元 氯气及氯的化合物 第4课时 氧化剂和还原剂
专题3 从海水中获得的化学物质
学习目标
1.能从化学反应中元素化合价的变化认识氧化剂和还原剂、氧化产物和还原产物等概念,熟知常见的氧化剂和还原剂,理清相关概念间的关系。促进“变化观念”化学核心素养的发展。
2.认识物质的氧化性、还原性,学会分析预测物质具有的氧化性或还原性,建立判断物质氧化性、还原性强弱的“思维模型”。
氧化剂:所含元素得到电子(或电子对偏向)的反应物。
还原剂:所含元素失去电子(或电子对偏离)的反应物。
氧化剂
还原剂
口诀:氧价降
一、氧化剂 还原剂
化合价降低
化合价升高
①.氧化剂和还原剂均是指反应物质,是一种化学试剂,不是某一种元素。
②.氧化剂本身被还原,化合价降低,发生还原反应
③.还原剂本身被氧化,化合价升高,发生氧化反应
注意
2Na+Cl2===2NaCl
氧化剂
还原剂
-1
+1
0
0
一、氧化剂 还原剂
氧化剂是_____,还原剂是_____;
发生氧化反应的是_____,发生还原反应的是_____。
Cl2
Cl2
Fe
Fe
-1
+3
0
0
一、氧化剂 还原剂
常见的氧化剂
一、氧化剂 还原剂
物质种类 常见物质
氧
化
剂 部分非金属单质
含有高价态元素的化合物
某些金属活动性较弱的元素对应的高价态离子
过氧化物
O2、Cl2等
浓硫酸、HNO3、KMnO4、MnO2、KClO3、K2Cr2O7等
Fe3+、Ag+、Cu2+等
Na2O2、H2O2等
常见的还原剂
一、氧化剂 还原剂
还
原
剂 活泼的金属单质
某些非金属单质
非金属阴离子和氢化物
含有较低价态元素的化合物
Al、Zn等
C、H2等
Cl-、Br-、I-、S2-、HI、NH3、H2S等
CO、SO2、H2SO3、Na2SO3、FeSO4等
-1
+1
0
以下反应的氧化剂和还原剂是什么?
Cl2 + H2O = HCl + HClO
在反应中,氧化剂和还原剂可以是同一物质
氧化剂
还原剂
二、氧化产物 还原产物
氧化产物:还原剂失去电子被氧化的产物
还原产物:氧化剂得到电子被还原的产物
2HCl+Fe =FeCl2+H2↑
氧化剂
还原剂
氧化产物
还原产物
(元素化合价升高)生成物
(元素化合价降低)生成物
二、氧化产物 还原产物
是氧化剂 是还原剂
被氧化 被还原
氧化产物 还原产物
-1
+4
+2
MnO2
HCl
HCl
MnO2
Cl2
MnCl2
0
二、氧化产物 还原产物
氧化剂+还原剂=氧化产物+还原产物
化合价降低,得到电子,被还原,发生还原反应
化合价升高,失去电子,被氧化,发生氧化反应
降得还原氧化剂 升失氧化还原剂
口诀
二、氧化产物 还原产物
2Na+Cl2===2NaCl
氧化剂
还原剂
-1
+1
0
0
以下反应的氧化产物和还原产物是什么?
在反应中,氧化产物和还原产物可以是同一物质
氧化产物
还原产物
二、氧化产物 还原产物
判断以下反应的氧化剂、还原剂、氧化产物和还原产物
2KMnO4 K2MnO4+MnO2+O2↑
氧化剂
还原剂
氧化产物
还原产物
反应中某些物质没有“身份”
氧化剂
还原剂
0
+2
-1
+4
0
+6
+7
-2
+4
氧化产物
还原产物
还原产物
反应中某些物质“身份”相同
二、氧化产物 还原产物
二、氧化产物 还原产物
Cl-
SO2
NO或NO2
Mn2+
Fe2+或Fe
Zn2+
H+
CO2
Fe3+
典例解析
例1. 歌词“帘外芭蕉惹骤雨,门环惹铜绿”,其中的“铜绿”即是铜锈,它的化学成分是Cu2(OH)2CO3(碱式碳酸铜)。铜在潮湿的空气中生锈的化学反应为2Cu+O2+CO2+H2O===Cu2(OH)2CO3。下列有关该反应的说法中不正确的是( )
A.该反应是化合反应
B.该反应中氧气是氧化剂,单质铜是还原剂
C.该反应是氧化还原反应,只有两种元素的化合价发生了变化
D.该反应是氧化还原反应,其中Cu得电子,O2失电子
D
氧化剂具有氧化性
氧化性:物质得电子的性质或能力
还原性:物质失电子的性质或能力
即化合价降低的能力
即化合价升高的能力
还原剂具有还原性
三、氧化性 还原性
三、氧化性 还原性
物质的氧化性及还原性与核心元素化合价的关系
氧化性
氧化性
还原性
还原性
核心元素化合价 实例 性质
最高价 只有_______
中间价 既有_______
又有_______
最低价 只有_______
还原性:还原剂 还原产物;
氧化性:氧化剂 氧化产物。
(强氧化性) (强还原性) (弱还原性) (弱氧化性)
强弱规律
>
>
即“强制弱”或“前强后弱”
三、氧化性 还原性
金属还原性:Fe Cu
>
Fe+CuSO4===FeSO4+Cu
氧化剂
还原剂
氧化产物
还原产物
三、氧化性 还原性
三、氧化性 还原性
(2)根据元素的活动性顺序比较
特点:上左下右可反应,隔之愈远愈易行。
三、氧化性 还原性
氧化性:
Cl2>S
三、氧化性 还原性
氧化性:
KMnO4>MnO2
例2.根据下列反应的离子方程式:①2Fe3++2I-===2Fe2++I2;②Br2+2Fe2+===2Br-+2Fe3+,可判断各物质的氧化性由强到弱的顺序是( )
A.Fe3+、Br2、I2 B.Fe3+、I2、Br2
C.Br2、Fe3+、I2 D.Br2、I2、Fe3+
C
典例解析
课堂小结
氧化剂 还原剂
不良反应
氧化产物 还原产物
氧化性 还原性
氧化性 还原性强弱比较
随堂练习
D
