专题4硫与环境保护4.2.2氧化还原反应方程式的配平课件 (共30张PPT) 高中化学 苏教版(2019) 必修 第一册
文档属性
| 名称 | 专题4硫与环境保护4.2.2氧化还原反应方程式的配平课件 (共30张PPT) 高中化学 苏教版(2019) 必修 第一册 |

|
|
| 格式 | ppt | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-07 00:00:00 | ||
图片预览








文档简介
(共30张PPT)
第二单元 硫及其化合物的相互转化
苏教版高中化学(必修一)同步教学课件
专题4 硫与环境保护
第2课时 氧化还原反应方程式的配平
1.理解氧化还原反应方程式的配平的基本原则。
2.了解并掌握氧化还原反应方程式的配平方法。
3.学会氧化还原反应方程式的配平的步骤。
3.学会有关氧化还原反应的简单计算。
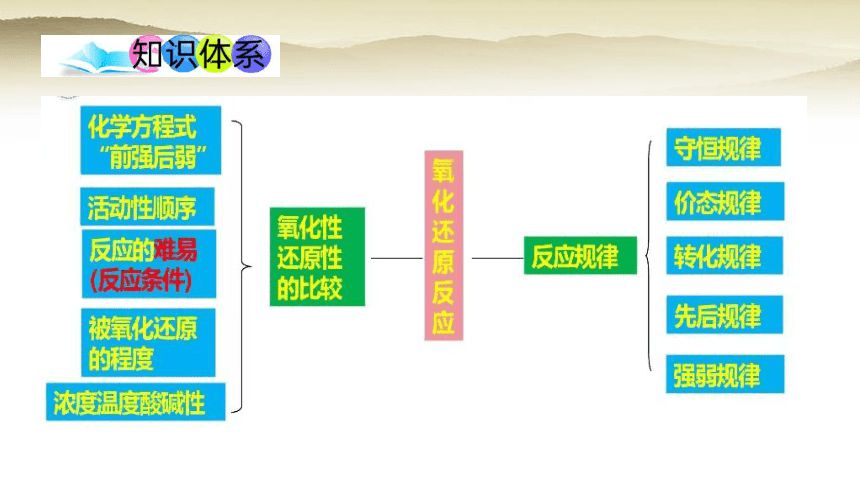
1、氧化还原反应
(1).概念:有元素化合价变化的反应
氧化反应:物质跟氧发生的化学反应/元素化合价升高的反应 2Cu +O2==2CuO
还原反应:物质失去氧的化学反应/元素化合价降低的反应 CuO+H2==H2O+Cu。
提问:氧化还原反应是否一定要有氧的参与?
并非只有得氧、失氧的反应才是氧化还原反应。得氧和失氧的反应只是氧化还原反应中的一部分,凡是有元素化合价变化的化学反应都是氧化还原反应。
一. 知识回顾
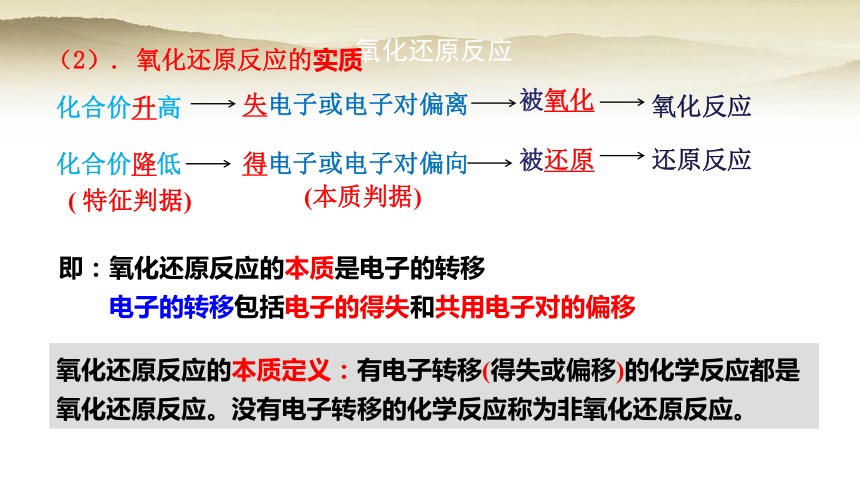
失电子或电子对偏离
化合价升高
被氧化
得电子或电子对偏向
化合价降低
被还原
(本质判据)
( 特征判据)
氧化反应
还原反应
即:氧化还原反应的本质是电子的转移
电子的转移包括电子的得失和共用电子对的偏移
氧化还原反应的本质定义:有电子转移(得失或偏移)的化学反应都是氧化还原反应。没有电子转移的化学反应称为非氧化还原反应。
氧化还原反应
(2). 氧化还原反应的实质
氧化剂:所含元素得到电子(或电子对偏向)的反应物。
还原剂:所含元素失去电子(或电子对偏离)的反应物。
氧化剂
还原剂
口诀:氧价降
2、氧化剂 还原剂
化合价降低
化合价升高
氧化产物:还原剂失去电子被氧化的产物
还原产物:氧化剂得到电子被还原的产物
2HCl+Fe =FeCl2+H2↑
氧化剂
还原剂
氧化产物
还原产物
(元素化合价升高)生成物
(元素化合价降低)生成物
3、氧化产物 还原产物
氧化剂具有氧化性
氧化性:物质得电子的性质或能力
还原性:物质失电子的性质或能力
即化合价降低的能力
即化合价升高的能力
还原剂具有还原性
4、氧化性 还原性
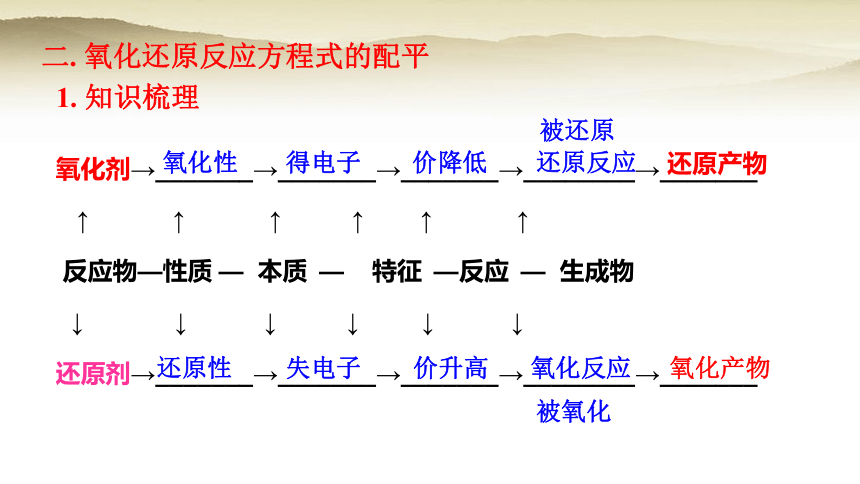
氧化剂→_______→_______→_______→________→_______
↑ ↑ ↑ ↑ ↑ ↑
反应物—性质 — 本质 — 特征 —反应 — 生成物
↓ ↓ ↓ ↓ ↓ ↓
还原剂→_______→_______→_______→________→_______
被还原
氧化性
得电子
价降低
还原反应
还原性
失电子
价升高
被氧化
氧化反应
还原产物
氧化产物
二. 氧化还原反应方程式的配平
1. 知识梳理
+2
+2
0
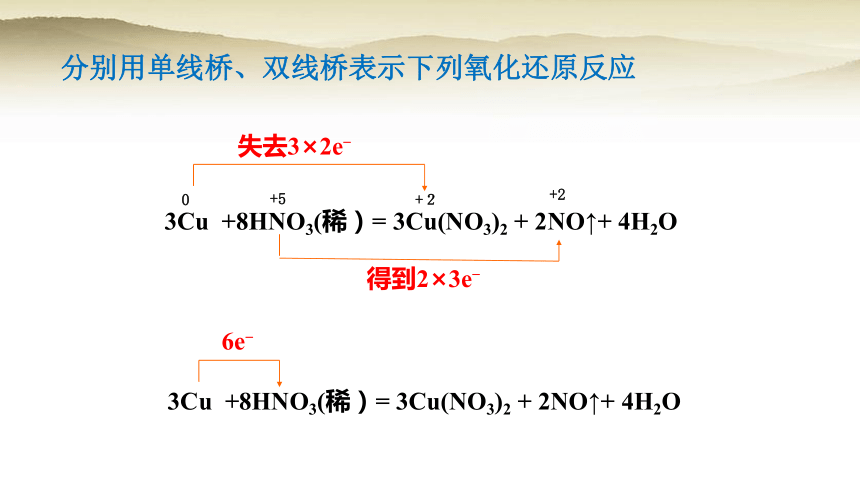
得到2×3e-
失去3×2e-
+5
3Cu +8HNO3(稀)= 3Cu(NO3)2 + 2NO↑+ 4H2O
3Cu +8HNO3(稀)= 3Cu(NO3)2 + 2NO↑+ 4H2O
6e-
分别用单线桥、双线桥表示下列氧化还原反应
2. 氧化还原反应方程式的配平三大原则
(1).得失电子守恒
还原剂失电子总数 = 氧化剂得电子总数
元素化合价升高总数 = 元素化合价降低总数
(2).质量守恒
反应前后原子的种类和个数不变
(3).电荷守恒
在离子反应方程式中,反应前后的阴、阳离子所带的电荷总数相等
(1)标变价:
正确标出反应前后化合价有变化的元素的化合价。
S + HNO3 — H2SO4 + NO2 + H2O
0
+5
+6
+4
(2)列变化:
(3)求总数:
求元素化合价升高和降低的总数
(即最小公倍数)
(4)配系数: 用观察法配平其他各物质的化学计量数。
(依据电荷守恒和原子守恒)
(5)查守恒: 即质量守恒、得失电子守恒、电荷守恒
列出元素化合价升高和降低的数值。
↑
↓
6
×1
×6
1
1
6
6
2
1
3. 氧化还原反应方程式配平的步骤
S + HNO3 — H2SO4 + NO2 + H2O
(1)标变价
(2)列变化
(3)求总数
(4)配系数
(5)查守恒
0
+5
+6
+4
↑
↓
6
1
×1
×6
1
1
6
6
2
即最小公倍数
观察法配平
[小结]配平方程式
CO2 + K2SO4 + MnSO4 + H2O
H2C2O4 + KMnO4 + H2SO4
(1)标变价
(2)列变化
(3)求总数
(4)配系数
(5)查守恒
+3
+7
+4
+2
↑
↓
2
5
×5
×2
5
10
2
2
1
即最小
公倍数
观察法
配平
找准1“分子”氧化剂化合价降低总数,1“分子”还原剂化合价升高总数
要点
3
8
强调:
“正向配平法”可以先不理会生成物中元素原子个数,只管反应物“1分子”
—
即时理解
3 8 3 2 4
FeS + HNO3(稀) — Fe(NO3)3 + H2SO4 + NO↑+ H2O
配平下列方程式
Cu + HNO3(稀) — Cu(NO3)2 + NO↑+ H2O
1 6 1 1 3 2
SO2 + H2S — S↓+ H2O
1 2 3 2
KClO3 + HCl(浓) — KCl + Cl2↑ + H2O
1 6 1 3 3
小试牛刀
(1)___ S+___KOH== ___K2S+___K2SO3+___H2O
0
-2
+4
↑
↓
2
4
×2
×1
1
2
(2+1)
6
3
1.逆向配平类一
(歧化反应)
三. 其他配平的方法
2.缺项配平:
某些反应物或生成物的化学式(或离子)未写出(缺项)
(一般缺:H2O、酸、碱、H+、OH-等)
①先利用化合价升降法配平氧化剂、还原剂及还原产物与氧化产物;
②再根据质量守恒、电荷守恒确定所缺的物质的化学式(或离子)
关键:
利用电荷守恒确定缺项物质是H2O、H+、OH-等。
→在酸性条件下,缺正电荷或多负电荷补H+;
→在碱性条件下,缺负电荷或多正电荷补OH-。
③最后观察法配平其他物质系数。
经典例题
例1.下列化学反应中,属于氧化还原反应的是( )
A.MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2
B.Na2CO3+CO2+H2O=2NaHCO3
C.SiO2+2C Si+2CO↑
D.NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl
【解析】A.MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2中无元素化合价变化,不是氧化还原反应,属于复分解反应,故A不符合题意;B.Na2CO3
+CO2+H2O=2NaHCO3中无元素化合价变化,不是氧化还原反应,属于化合反应,故B不符合题意;C.SiO2+2C Si+2CO↑中硅元素和碳元素发生化合价变化,是氧化还原反应,同时也属于置换反应,故C符合题意;D.NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl中无元素化合价变化,不是氧化还原反应,故D不符合题意;答案选C。
C
例2. 反应3Br2+6NaOH 5NaBr+NaBrO3+3H2O中,氧化产物是( )
A.Br2 B.NaBr C.NaBrO3 D.H2O
C
【解析】反应3Br2+6NaOH 5NaBr+ NaBrO3+3H2O中,Br2中的Br元素由0价变为NaBr中的-1价和NaBrO3中的+5价,化合价降低得电子,被还原,化合价升高失电子,被氧化,则Br2在该反应中既做氧化剂又做还原剂,NaBr为还原产物,NaBrO3为氧化产物,故答案选C。
例3.下列反应中,SO2作还原剂的是( )
A.SO2+NaOH===NaHSO3
B.SO2+H2O2===H2SO4
C.SO2+2H2S===3S↓+2H2O
D.2Mg+3SO2===S+2MgSO3
【解析】A.S元素化合价未改变,为非氧化还原反应,A不符合;
B.二氧化硫中硫元素化合价升高,SO2作还原剂,B符合;
C.二氧化硫中硫元素化合价降低,SO2作氧化剂, C不符合;
D.二氧化硫中硫元素化合价降低,SO2作氧化剂,D不符合;
故选B。
B
例4.下列变化中需加入氧化剂才能实现的是( )
A.S→SO2 B.Na2O2→O2 C.HNO3→NO D.2H+→H2
【解析】A.硫元素从0价升高到+4价,化合价升高被氧化,因此需要加入氧化剂才能实现,A项正确;B.Na2O2可以发生歧化反应,一部分化合价升高到0价变成O2,一部分化合价降低到-2价变成NaOH,因此不必加入其它的氧化剂,B项错误;C.氮元素从+5价降低到+2价,化合价降低被还原,因此需要加入还原剂才能实现,C项错误;D.氢元素从+1价降低到0价,化合价降低被还原,因此需要加入还原剂才能实现,D项错误;答案选A。
A
例5.配平下列方程式
(1)____HCl(浓)+____MnO2 ____Cl2↑+____MnCl2+____H2O
(2)____Cu+____HNO3(稀) == ____Cu(NO3)2+____NO↑+____H2O
(3)____KI+____KIO3+___H2SO4 == ____I2+____K2SO4+___H2O
(4)___MnO4-+___H++____Cl- == ____Mn2++____Cl2↑+___H2O
(5)_____FeS2+______O2 ______Fe2O3+______SO2
(6)___ClO-+___Fe3++___OH-===___Cl-+___FeO42-+_____H2O。
4
1
1
1
2
3
8
3
2
4
5
1
3
3
3
3
2
16
10
2
5
8
4 11 2 8
3 2 10 3 2 5
1.理解氧化还原反应方程式的配平的基本原则。
2.了解并掌握氧化还原反应方程式的配平方法。
3.学会氧化还原反应方程式的配平的步骤。
3.学会有关氧化还原反应的简单计算。
课堂小结
随堂练习
1.反应MnO2+ 4HCl(浓) MnCl2+Cl2↑+2H2O中,氧化剂与还原剂的物质的量之比是( )
A.1:2 B.1:4 C.2:1 D.1:1
【解析】A.经分析计算,氧化剂与还原剂的物质的量之比为1:2,故A正确;B.与计算不符,故B错误;C.与计算不符。故C错误;D.与计算不符,故D错误;故选A。
A
2.在电子工业中,制印刷电路时,常用氯化铁溶液作为铜的“腐蚀剂”,该过程的反应的反应为:2FeCl3 +Cu→
2FeCl2+CuCl2,该反应利用了铜的性质是( )
A.氧化性 B.还原性 C.导电性 D.酸性
【解析】A. 表现氧化性的物质,是含价态降低元素的反应物,应为FeCl3 ;B. 表现还原性的物质,是含价态升高元素的反应物,应为Cu ,符合题意;C. 导电性是物理性质,通常对金属、电解质而言;D. 酸性是H+表现出的性质,通常对酸而言。答案为B。
B
3.ClO2是一种杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+
2CO2↑+2H2O,下列说法正确的是( )
A.KClO3中氯元素被氧化 B.H2C2O4的还原性弱于ClO2
C.CO2是氧化产物 D.1molKClO3参加反应有2mol电子转移
【解析】A.反应中KClO3中氯元素的化合价由+5价降低到ClO2中的+4价,得到电子,被还原,A错误;B.根据同一氧化还原反应中还原剂的还原性强于还原产物的还原性,故有H2C2O4的还原性强于ClO2,B错误;G.反应中H2C2O4中的C由+3价升高到CO2中的+4价,失去电子,被氧化,故CO2是氧化产物,C正确;D.反应中KClO3中氯元素的化合价由+5价降低到ClO2中的+4价,1molKClO3参加反应有1mol电子转移,D错误;故答案为:C。
C
4.某温下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3的混合溶液,经测定ClO-与ClO3-的物质的量浓度之比为7:3,则Cl2与KOH反应时,被氧化的氯元素和被还原的氯元素的物质的量之比为( )
A.11:5 B.13:2 C.5:11 D.2:13
【解析】Cl2生成ClO3-与ClO-是被氧化的过程,化合价分别由0价升高为+5价和+1价,ClO-与ClO3-的物质的量浓度之比为7:3,则可设ClO3-为7mol,ClO-为3mol,被氧化的Cl共为10mol,失去电子的总物质的量为7mol×(1-0)+3mol×(5-0)=22mol,氧化还原反应中氧化剂和还原剂之间得失电子数目相等,Cl2生成KCl是被还原的过程,化合价由0价降低为-1价,则得到电子的物质的量也应为22mol,被还原的Cl的物质的量为22mol,所以被氧化的氯元素和被还原的氯元素的物质的量之比为10mol:22mol=5:11,答案选C。
C
5.对于白磷引起的中毒,硫酸铜溶液是一种解毒剂,有关反应如下:11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4,下列关于该反应说法正确的是( )
A.Cu3P既是氧化产物也是还原产物
B.11molP参与反应时,该反应中有15mol电子发生转移
C.P发生还原反应和氧化反应的物质的量之比为6∶5
D.CuSO4仅作氧化剂,发生还原反应
【解析】A.Cu3P中Cu的化合价为+1,P的化合价为-3,Cu的化合价从+2降低到+1,P的化合价从0价降低到Cu3P中的-3价,生成物Cu3P中只有元素化合价降低,所以是还原产物,故A错误;B.11molP参与反应时,其中有6molP化合价从0价升高到+5价,作还原剂,共有30mol电子发生转移,故B错误;C.11molP参与反应时,其中有5molP化合价降低,发生还原反应,6molP化合价升高,发生氧化反应,发生还原反应和氧化反应物质的量之比为5∶6,故C错误;D.反应物CuSO4中仅有Cu元素化合价降低,作氧化剂,发生还原反应,故D正确;答案选D。
D
【答案】
微生物
【答案】(1) (2)
(3)
(4)
【解析】反应Se+2H2SO4(浓)===2SO2↑+SeO2+2H2O中,Se的化合价升高,被氧化,做还原剂,浓硫酸中硫元素的化合价降低,被还原,做氧化剂;在氧化还原反应中,氧化剂的氧化性强于氧化产物的氧化性,因此依据反应①以及(1)中分析可知SeO2、浓H2SO4的氧化性强弱是SeO2小于浓H2SO4。反应②中,2 mol SO2共失去4 mol电子,失去的电子被SeO2得到,从而SeO2被还原为Se,故此反应转移4 mol电子,用双线桥法标出电子转移的方向和数目;由反应体系中物质变化可知,SeO2、KI和HNO3为反应物,Se、I2、KNO3和H2O为生成物,根据得失电子数守恒可知,SeO2的计量数为1,而KI的计量数为4,故Se的计量数为1,I2的计量数为2,根据质量守恒可知,KNO3的计量数为4,则HNO3的计量数为4,水的计量数为2
浓硫酸(或H2SO4)
硒(或Se)
小于
SeO2+4KI+4HNO3===Se+2I2+4KNO3+2H2O
第二单元 硫及其化合物的相互转化
苏教版高中化学(必修一)同步教学课件
专题4 硫与环境保护
第2课时 氧化还原反应方程式的配平
1.理解氧化还原反应方程式的配平的基本原则。
2.了解并掌握氧化还原反应方程式的配平方法。
3.学会氧化还原反应方程式的配平的步骤。
3.学会有关氧化还原反应的简单计算。
1、氧化还原反应
(1).概念:有元素化合价变化的反应
氧化反应:物质跟氧发生的化学反应/元素化合价升高的反应 2Cu +O2==2CuO
还原反应:物质失去氧的化学反应/元素化合价降低的反应 CuO+H2==H2O+Cu。
提问:氧化还原反应是否一定要有氧的参与?
并非只有得氧、失氧的反应才是氧化还原反应。得氧和失氧的反应只是氧化还原反应中的一部分,凡是有元素化合价变化的化学反应都是氧化还原反应。
一. 知识回顾
失电子或电子对偏离
化合价升高
被氧化
得电子或电子对偏向
化合价降低
被还原
(本质判据)
( 特征判据)
氧化反应
还原反应
即:氧化还原反应的本质是电子的转移
电子的转移包括电子的得失和共用电子对的偏移
氧化还原反应的本质定义:有电子转移(得失或偏移)的化学反应都是氧化还原反应。没有电子转移的化学反应称为非氧化还原反应。
氧化还原反应
(2). 氧化还原反应的实质
氧化剂:所含元素得到电子(或电子对偏向)的反应物。
还原剂:所含元素失去电子(或电子对偏离)的反应物。
氧化剂
还原剂
口诀:氧价降
2、氧化剂 还原剂
化合价降低
化合价升高
氧化产物:还原剂失去电子被氧化的产物
还原产物:氧化剂得到电子被还原的产物
2HCl+Fe =FeCl2+H2↑
氧化剂
还原剂
氧化产物
还原产物
(元素化合价升高)生成物
(元素化合价降低)生成物
3、氧化产物 还原产物
氧化剂具有氧化性
氧化性:物质得电子的性质或能力
还原性:物质失电子的性质或能力
即化合价降低的能力
即化合价升高的能力
还原剂具有还原性
4、氧化性 还原性
氧化剂→_______→_______→_______→________→_______
↑ ↑ ↑ ↑ ↑ ↑
反应物—性质 — 本质 — 特征 —反应 — 生成物
↓ ↓ ↓ ↓ ↓ ↓
还原剂→_______→_______→_______→________→_______
被还原
氧化性
得电子
价降低
还原反应
还原性
失电子
价升高
被氧化
氧化反应
还原产物
氧化产物
二. 氧化还原反应方程式的配平
1. 知识梳理
+2
+2
0
得到2×3e-
失去3×2e-
+5
3Cu +8HNO3(稀)= 3Cu(NO3)2 + 2NO↑+ 4H2O
3Cu +8HNO3(稀)= 3Cu(NO3)2 + 2NO↑+ 4H2O
6e-
分别用单线桥、双线桥表示下列氧化还原反应
2. 氧化还原反应方程式的配平三大原则
(1).得失电子守恒
还原剂失电子总数 = 氧化剂得电子总数
元素化合价升高总数 = 元素化合价降低总数
(2).质量守恒
反应前后原子的种类和个数不变
(3).电荷守恒
在离子反应方程式中,反应前后的阴、阳离子所带的电荷总数相等
(1)标变价:
正确标出反应前后化合价有变化的元素的化合价。
S + HNO3 — H2SO4 + NO2 + H2O
0
+5
+6
+4
(2)列变化:
(3)求总数:
求元素化合价升高和降低的总数
(即最小公倍数)
(4)配系数: 用观察法配平其他各物质的化学计量数。
(依据电荷守恒和原子守恒)
(5)查守恒: 即质量守恒、得失电子守恒、电荷守恒
列出元素化合价升高和降低的数值。
↑
↓
6
×1
×6
1
1
6
6
2
1
3. 氧化还原反应方程式配平的步骤
S + HNO3 — H2SO4 + NO2 + H2O
(1)标变价
(2)列变化
(3)求总数
(4)配系数
(5)查守恒
0
+5
+6
+4
↑
↓
6
1
×1
×6
1
1
6
6
2
即最小公倍数
观察法配平
[小结]配平方程式
CO2 + K2SO4 + MnSO4 + H2O
H2C2O4 + KMnO4 + H2SO4
(1)标变价
(2)列变化
(3)求总数
(4)配系数
(5)查守恒
+3
+7
+4
+2
↑
↓
2
5
×5
×2
5
10
2
2
1
即最小
公倍数
观察法
配平
找准1“分子”氧化剂化合价降低总数,1“分子”还原剂化合价升高总数
要点
3
8
强调:
“正向配平法”可以先不理会生成物中元素原子个数,只管反应物“1分子”
—
即时理解
3 8 3 2 4
FeS + HNO3(稀) — Fe(NO3)3 + H2SO4 + NO↑+ H2O
配平下列方程式
Cu + HNO3(稀) — Cu(NO3)2 + NO↑+ H2O
1 6 1 1 3 2
SO2 + H2S — S↓+ H2O
1 2 3 2
KClO3 + HCl(浓) — KCl + Cl2↑ + H2O
1 6 1 3 3
小试牛刀
(1)___ S+___KOH== ___K2S+___K2SO3+___H2O
0
-2
+4
↑
↓
2
4
×2
×1
1
2
(2+1)
6
3
1.逆向配平类一
(歧化反应)
三. 其他配平的方法
2.缺项配平:
某些反应物或生成物的化学式(或离子)未写出(缺项)
(一般缺:H2O、酸、碱、H+、OH-等)
①先利用化合价升降法配平氧化剂、还原剂及还原产物与氧化产物;
②再根据质量守恒、电荷守恒确定所缺的物质的化学式(或离子)
关键:
利用电荷守恒确定缺项物质是H2O、H+、OH-等。
→在酸性条件下,缺正电荷或多负电荷补H+;
→在碱性条件下,缺负电荷或多正电荷补OH-。
③最后观察法配平其他物质系数。
经典例题
例1.下列化学反应中,属于氧化还原反应的是( )
A.MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2
B.Na2CO3+CO2+H2O=2NaHCO3
C.SiO2+2C Si+2CO↑
D.NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl
【解析】A.MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2中无元素化合价变化,不是氧化还原反应,属于复分解反应,故A不符合题意;B.Na2CO3
+CO2+H2O=2NaHCO3中无元素化合价变化,不是氧化还原反应,属于化合反应,故B不符合题意;C.SiO2+2C Si+2CO↑中硅元素和碳元素发生化合价变化,是氧化还原反应,同时也属于置换反应,故C符合题意;D.NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl中无元素化合价变化,不是氧化还原反应,故D不符合题意;答案选C。
C
例2. 反应3Br2+6NaOH 5NaBr+NaBrO3+3H2O中,氧化产物是( )
A.Br2 B.NaBr C.NaBrO3 D.H2O
C
【解析】反应3Br2+6NaOH 5NaBr+ NaBrO3+3H2O中,Br2中的Br元素由0价变为NaBr中的-1价和NaBrO3中的+5价,化合价降低得电子,被还原,化合价升高失电子,被氧化,则Br2在该反应中既做氧化剂又做还原剂,NaBr为还原产物,NaBrO3为氧化产物,故答案选C。
例3.下列反应中,SO2作还原剂的是( )
A.SO2+NaOH===NaHSO3
B.SO2+H2O2===H2SO4
C.SO2+2H2S===3S↓+2H2O
D.2Mg+3SO2===S+2MgSO3
【解析】A.S元素化合价未改变,为非氧化还原反应,A不符合;
B.二氧化硫中硫元素化合价升高,SO2作还原剂,B符合;
C.二氧化硫中硫元素化合价降低,SO2作氧化剂, C不符合;
D.二氧化硫中硫元素化合价降低,SO2作氧化剂,D不符合;
故选B。
B
例4.下列变化中需加入氧化剂才能实现的是( )
A.S→SO2 B.Na2O2→O2 C.HNO3→NO D.2H+→H2
【解析】A.硫元素从0价升高到+4价,化合价升高被氧化,因此需要加入氧化剂才能实现,A项正确;B.Na2O2可以发生歧化反应,一部分化合价升高到0价变成O2,一部分化合价降低到-2价变成NaOH,因此不必加入其它的氧化剂,B项错误;C.氮元素从+5价降低到+2价,化合价降低被还原,因此需要加入还原剂才能实现,C项错误;D.氢元素从+1价降低到0价,化合价降低被还原,因此需要加入还原剂才能实现,D项错误;答案选A。
A
例5.配平下列方程式
(1)____HCl(浓)+____MnO2 ____Cl2↑+____MnCl2+____H2O
(2)____Cu+____HNO3(稀) == ____Cu(NO3)2+____NO↑+____H2O
(3)____KI+____KIO3+___H2SO4 == ____I2+____K2SO4+___H2O
(4)___MnO4-+___H++____Cl- == ____Mn2++____Cl2↑+___H2O
(5)_____FeS2+______O2 ______Fe2O3+______SO2
(6)___ClO-+___Fe3++___OH-===___Cl-+___FeO42-+_____H2O。
4
1
1
1
2
3
8
3
2
4
5
1
3
3
3
3
2
16
10
2
5
8
4 11 2 8
3 2 10 3 2 5
1.理解氧化还原反应方程式的配平的基本原则。
2.了解并掌握氧化还原反应方程式的配平方法。
3.学会氧化还原反应方程式的配平的步骤。
3.学会有关氧化还原反应的简单计算。
课堂小结
随堂练习
1.反应MnO2+ 4HCl(浓) MnCl2+Cl2↑+2H2O中,氧化剂与还原剂的物质的量之比是( )
A.1:2 B.1:4 C.2:1 D.1:1
【解析】A.经分析计算,氧化剂与还原剂的物质的量之比为1:2,故A正确;B.与计算不符,故B错误;C.与计算不符。故C错误;D.与计算不符,故D错误;故选A。
A
2.在电子工业中,制印刷电路时,常用氯化铁溶液作为铜的“腐蚀剂”,该过程的反应的反应为:2FeCl3 +Cu→
2FeCl2+CuCl2,该反应利用了铜的性质是( )
A.氧化性 B.还原性 C.导电性 D.酸性
【解析】A. 表现氧化性的物质,是含价态降低元素的反应物,应为FeCl3 ;B. 表现还原性的物质,是含价态升高元素的反应物,应为Cu ,符合题意;C. 导电性是物理性质,通常对金属、电解质而言;D. 酸性是H+表现出的性质,通常对酸而言。答案为B。
B
3.ClO2是一种杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+
2CO2↑+2H2O,下列说法正确的是( )
A.KClO3中氯元素被氧化 B.H2C2O4的还原性弱于ClO2
C.CO2是氧化产物 D.1molKClO3参加反应有2mol电子转移
【解析】A.反应中KClO3中氯元素的化合价由+5价降低到ClO2中的+4价,得到电子,被还原,A错误;B.根据同一氧化还原反应中还原剂的还原性强于还原产物的还原性,故有H2C2O4的还原性强于ClO2,B错误;G.反应中H2C2O4中的C由+3价升高到CO2中的+4价,失去电子,被氧化,故CO2是氧化产物,C正确;D.反应中KClO3中氯元素的化合价由+5价降低到ClO2中的+4价,1molKClO3参加反应有1mol电子转移,D错误;故答案为:C。
C
4.某温下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3的混合溶液,经测定ClO-与ClO3-的物质的量浓度之比为7:3,则Cl2与KOH反应时,被氧化的氯元素和被还原的氯元素的物质的量之比为( )
A.11:5 B.13:2 C.5:11 D.2:13
【解析】Cl2生成ClO3-与ClO-是被氧化的过程,化合价分别由0价升高为+5价和+1价,ClO-与ClO3-的物质的量浓度之比为7:3,则可设ClO3-为7mol,ClO-为3mol,被氧化的Cl共为10mol,失去电子的总物质的量为7mol×(1-0)+3mol×(5-0)=22mol,氧化还原反应中氧化剂和还原剂之间得失电子数目相等,Cl2生成KCl是被还原的过程,化合价由0价降低为-1价,则得到电子的物质的量也应为22mol,被还原的Cl的物质的量为22mol,所以被氧化的氯元素和被还原的氯元素的物质的量之比为10mol:22mol=5:11,答案选C。
C
5.对于白磷引起的中毒,硫酸铜溶液是一种解毒剂,有关反应如下:11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4,下列关于该反应说法正确的是( )
A.Cu3P既是氧化产物也是还原产物
B.11molP参与反应时,该反应中有15mol电子发生转移
C.P发生还原反应和氧化反应的物质的量之比为6∶5
D.CuSO4仅作氧化剂,发生还原反应
【解析】A.Cu3P中Cu的化合价为+1,P的化合价为-3,Cu的化合价从+2降低到+1,P的化合价从0价降低到Cu3P中的-3价,生成物Cu3P中只有元素化合价降低,所以是还原产物,故A错误;B.11molP参与反应时,其中有6molP化合价从0价升高到+5价,作还原剂,共有30mol电子发生转移,故B错误;C.11molP参与反应时,其中有5molP化合价降低,发生还原反应,6molP化合价升高,发生氧化反应,发生还原反应和氧化反应物质的量之比为5∶6,故C错误;D.反应物CuSO4中仅有Cu元素化合价降低,作氧化剂,发生还原反应,故D正确;答案选D。
D
【答案】
微生物
【答案】(1) (2)
(3)
(4)
【解析】反应Se+2H2SO4(浓)===2SO2↑+SeO2+2H2O中,Se的化合价升高,被氧化,做还原剂,浓硫酸中硫元素的化合价降低,被还原,做氧化剂;在氧化还原反应中,氧化剂的氧化性强于氧化产物的氧化性,因此依据反应①以及(1)中分析可知SeO2、浓H2SO4的氧化性强弱是SeO2小于浓H2SO4。反应②中,2 mol SO2共失去4 mol电子,失去的电子被SeO2得到,从而SeO2被还原为Se,故此反应转移4 mol电子,用双线桥法标出电子转移的方向和数目;由反应体系中物质变化可知,SeO2、KI和HNO3为反应物,Se、I2、KNO3和H2O为生成物,根据得失电子数守恒可知,SeO2的计量数为1,而KI的计量数为4,故Se的计量数为1,I2的计量数为2,根据质量守恒可知,KNO3的计量数为4,则HNO3的计量数为4,水的计量数为2
浓硫酸(或H2SO4)
硒(或Se)
小于
SeO2+4KI+4HNO3===Se+2I2+4KNO3+2H2O
