山西省临汾部分学校2024-2025学年高一下学期期末联考化学试卷(含答案)
文档属性
| 名称 | 山西省临汾部分学校2024-2025学年高一下学期期末联考化学试卷(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 936.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-06 19:45:53 | ||
图片预览



文档简介
山西省部分学校2024-2025学年高一下学期期末联考 化学试题
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列文物艺术品的主要成分属于无机非金属材料的是
艺术品
选项 A.清·丝绸团扇 B.清·茶叶锡罐 C.春秋·水晶笏板 D.清·弓弩箭
A.A B.B C.C D.D
2.化学与生产、生活、环境密切相关,下列说法错误的是
A.普通玻璃的生产以纯碱、石灰石和石英砂为主要原料
B.碳化硅具有优异的高温抗氧化性能,可用作耐高温结构材料
C.食品中添加适量的二氧化硫可以起到漂白、防腐和抗氧化等作用
D.玻璃雕刻工艺需要用到化学腐蚀试剂,可以用盐酸溶蚀玻璃生产磨砂玻璃
3.糖类、油脂、蛋白质和维生素是重要的营养物质。下列说法正确的是
A.蛋白质均能溶于水,其水解的最终产物均为氨基酸
B.工业上利用油脂在酸性条件下的水解反应获得高级脂肪酸和甘油,进行肥皂的生产
C.蔗糖、淀粉和纤维素在稀酸的催化下能发生水解反应,最终生成单糖
D.抗坏血酸(即维生素C)是水果罐头中常用的抗氧化剂,因为其具有强氧化性
4.化学与可持续发展,关系到自然资源的开发与利用,关系到化学品的合理使用,关系到人类健康和环境保护,应当引起重视。下列叙述错误的是
A.工业海水提溴技术中,吸收塔使用和水吸收溴转化为氢溴酸,其中作还原剂
B.石油的分馏可获得汽油、煤油等轻质油,煤的干馏可获得粗苯、乙烯等化工原料,二者均属于化学变化
C.绿色化学要求从源头减少或消除环境污染,改变“先污染后治理”的观念与做法
D.污水处理时,常加入硫酸亚铁、硫酸铝、聚合氯化铝等混凝剂,使污水中的细小悬浮物聚集成较大的颗粒后沉淀
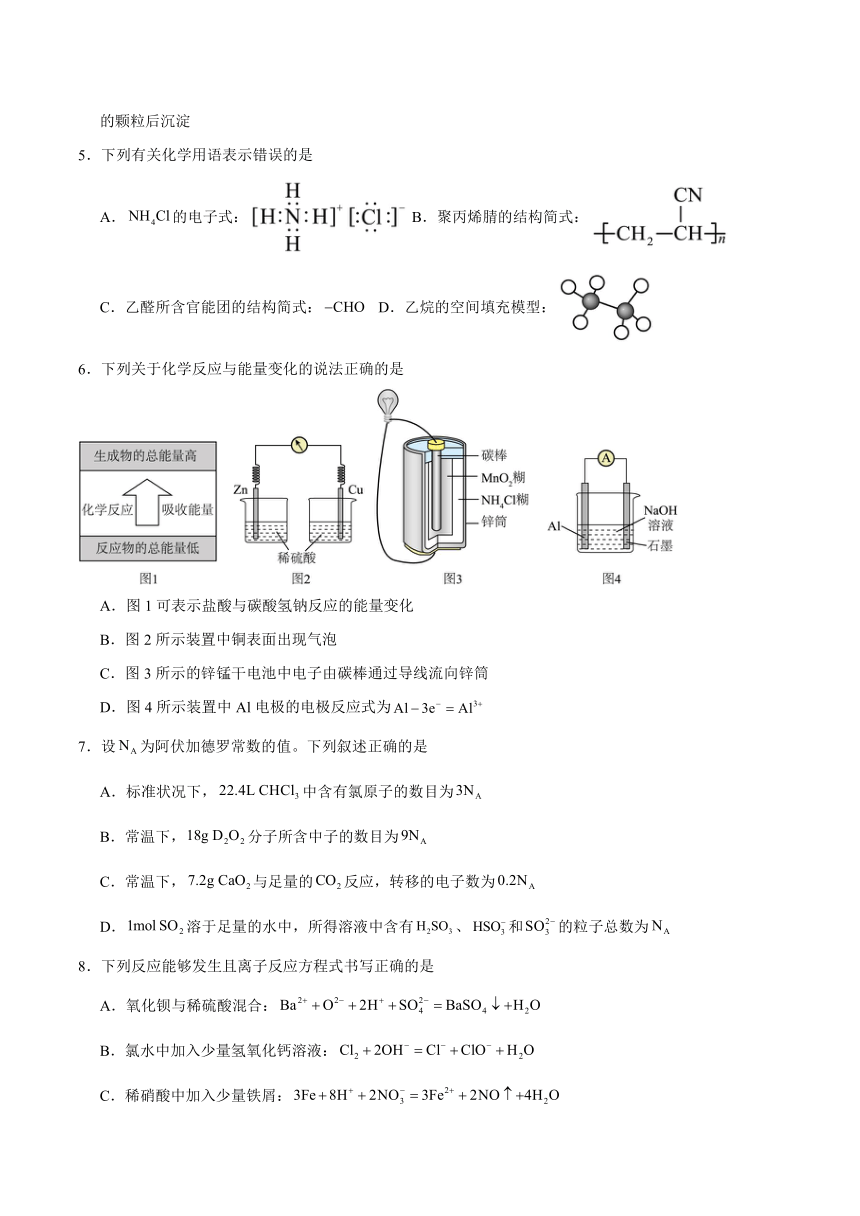
5.下列有关化学用语表示错误的是
A.的电子式: B.聚丙烯腈的结构简式:
C.乙醛所含官能团的结构简式: D.乙烷的空间填充模型:
6.下列关于化学反应与能量变化的说法正确的是
A.图1可表示盐酸与碳酸氢钠反应的能量变化
B.图2所示装置中铜表面出现气泡
C.图3所示的锌锰干电池中电子由碳棒通过导线流向锌筒
D.图4所示装置中Al电极的电极反应式为
7.设为阿伏加德罗常数的值。下列叙述正确的是
A.标准状况下,中含有氯原子的数目为
B.常温下,分子所含中子的数目为
C.常温下,与足量的反应,转移的电子数为
D.溶于足量的水中,所得溶液中含有、和的粒子总数为
8.下列反应能够发生且离子反应方程式书写正确的是
A.氧化钡与稀硫酸混合:
B.氯水中加入少量氢氧化钙溶液:
C.稀硝酸中加入少量铁屑:
D.向酸性溶液中通入气体:
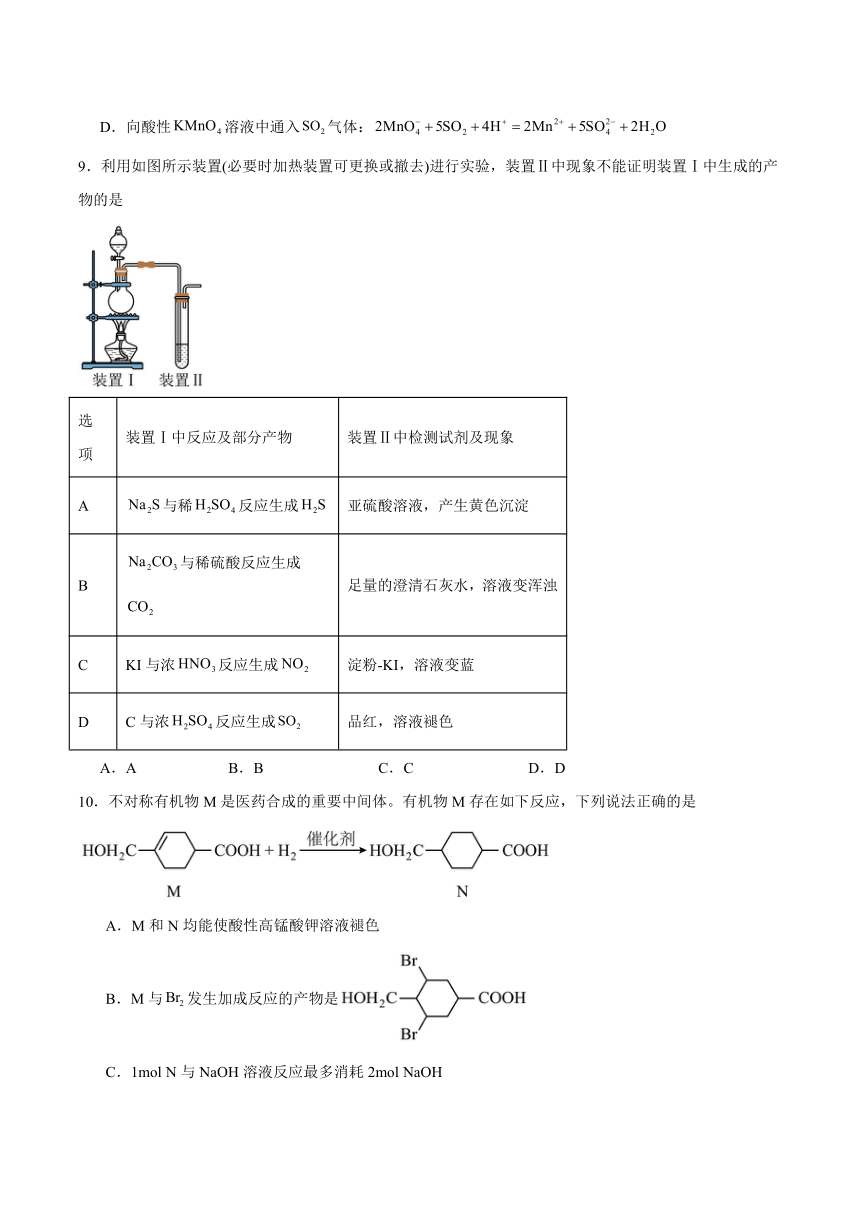
9.利用如图所示装置(必要时加热装置可更换或撤去)进行实验,装置Ⅱ中现象不能证明装置Ⅰ中生成的产物的是
选项 装置Ⅰ中反应及部分产物 装置Ⅱ中检测试剂及现象
A 与稀反应生成 亚硫酸溶液,产生黄色沉淀
B 与稀硫酸反应生成 足量的澄清石灰水,溶液变浑浊
C KI与浓反应生成 淀粉-KI,溶液变蓝
D C与浓反应生成 品红,溶液褪色
A.A B.B C.C D.D
10.不对称有机物M是医药合成的重要中间体。有机物M存在如下反应,下列说法正确的是
A.M和N均能使酸性高锰酸钾溶液褪色
B.M与发生加成反应的产物是
C.1mol N与NaOH溶液反应最多消耗2mol NaOH
D.M分子中碳原子均位于同一平面
11.下列实验操作及现象能得出相应结论的是
选项 实验操作 实验现象 实验结论
A 向硫代硫酸钠溶液中加入稀硫酸,并进行水浴加热 有乳黄色硫沉淀产生 硫酸具有氧化性
B 向溶液中通入和气体X 产生白色沉淀 气体X为
C 向盛有浓的两支试管中分别加入锌片和铝片 加入锌片的试管中迅速产生红棕色气体 金属性:
D 向盛有淀粉水解液的试管中加入过量NaOH溶液调节至碱性,再滴入3滴溶液,加热 有砖红色沉淀生成 淀粉水解液中含有葡萄糖
A.A B.B C.C D.D
12.某种重要化学合成试剂的结构如图所示。已知W、Y、Z、M、Q是原子序数依次增大的短周期主族元素,其中Q、Z同主族,Y、M同主族。下列有关说法错误的是
A.原子半径:
B.常温下,Q的单质易溶于二硫化碳
C.简单氢化物的沸点:
D.最高价氧化物对应水化物的酸性:
13.某科研兴趣小组研究Fe、石墨电极在稀硫酸亚铁和稀硫酸()混合液作电解质时的原电池反应原理,如图所示。下列说法错误的是
A.电子由Fe电极流出,石墨电极为该电池的正极
B.放电过程中,电解质溶液中的向铁电极移动
C.氧气发生的反应为:
D.当铁电极质量减少5.6g时,理论上消耗标准状况下
14.为探究草酸氢钾与酸性高锰酸钾溶液反应速率的影响因素,设计如表所示方案。下列说法错误的是
实验序号 () () () () 褪色时间t/min
① 5 5 2 0 8 8
② 10 5 2 0 a 6
③ 5 5 5 0 b 5
④ 10 5 2 3 0
A.,
B.实验①②的目的为探究溶液的浓度对化学反应速率的影响
C.实验①③的目的为探究硫酸的浓度对化学反应速率的影响
D.,说明对草酸氢钾与酸性高锰酸钾溶液的反应有催化作用
二、解答题
15.碘酸银()为白色结晶性粉末,微溶于水,光照条件下会分解,具有光敏感性。碘酸银常用作化学试剂,测定血液中的少量氯化物。此外,它还可以与碘化银、碘化铜一起作为人工降雨的成核剂。一种以海带和其他试剂为原料制备碘酸银的实验流程如下:
回答下列问题:
(1)步骤①中盛放海带的仪器为 。
(2)步骤⑥中发生反应的化学方程式为 。
(3)步骤⑦分离出的操作名称是 。
(4)已知与可发生反应:。则当有单质生成时,转移电子的物质的量为 mol。选用如下试剂或药品检验中的,可选用的物质有:
①蒸馏水 ②蓝色石蕊试纸 ③碘化钾淀粉试纸 ④淀粉 ⑤蔗糖 ⑥乙酸 ⑦乙醇
进行上述实验必须使用的物质是 (填字母)。
A.①③ B.①③⑥ C.②④⑥ D.①②④⑤⑦
(5)利用氯气与或也可制备,实验室利用氯气氧化废碘液中的或后加入KOH溶液调节pH为10获得的实验装置如图:
①仪器m的名称为 。
②饱和食盐水的作用为 。
③NaOH的作用为 。
④实验过程中,装置A中产生黄绿色气体,一段时间后,装置C中棕褐色溶液颜色逐渐变浅,当褪至无色时停止制备氯气。向装置C中加入KOH溶液调节pH为10获得。据文献报道,碘元素生成碘酸(,中强酸),装置C中和在水溶液中反应生成碘酸的化学方程式为 。
16.某含镍废料中含有NiO和稀土金属(用RE表示)的氧化物,及一定量的FeO、MgO、、、、等,利用该废料制备碱式碳酸镍[]的工艺流程如下:
已知:①“酸浸”后溶液中金属离子有、、、、、及少量的(其中代表、和等稀土元素离子)。
②室温下,溶液中金属离子开始沉淀和完全沉淀的pH如表所示。
金属离子
开始沉淀 7.5 2.2 7.2 8.9 11.9 7.8
完全沉淀 9.0 3.2 8.7 10.9 13.9 9.8
(1)“酸浸”时,将含镍废料粉碎的目的是 。
(2)滤渣1的主要成分为 。
(3)稀土复盐中 (用含y的代数式表示)。
(4)“氧化”步骤中的用量远高于理论用量的原因为 ,调pH的范围是 。检验滤渣2是否洗涤干净的操作方法为 。
(5)“除锰”时,会转化为,则发生反应的离子方程式为 。
(6)“沉镍”所得废液经处理后,可于“ ”工序循环利用。
17.2-甲基丙烯酸乙二醇酯(EDGMA)是一种重要的有机合成原料,可作交联剂及用于合成树脂。2-甲基丙烯酸乙二醇酯的一种合成路线如下:
已知:A和D互为同系物。
回答下列问题:
(1)E的结构简式为 。
(2)下列关于有机物C的说法错误的是 (填字母)。
a. C与甲醇互为同系物
b.相同物质的量的C与乙炔分别完全燃烧,二者耗氧量相同
c.0.5mol C与足量的Na反应放出标准状况下
d.C能够在Cu作催化剂加热的条件下与反应生成乙二醛
(3)F中含有的官能团名称是 。
(4)D与反应后的有机产物的化学名称为 。
(5)C与F反应生成G的化学方程式为 ,反应类型为 。
(6)有机物A和有机物D均可由分子式为的一种同分异构体通过裂解反应制得,的同分异构体中含有4个甲基的结构有 种,任写其中一种的结构简式 。
三、填空题
18.化学反应伴随着能量变化和物质的变化,其物质的变化中还存在着化学反应速率的变化与限度问题。根据下列信息分析化学反应中的变化问题。
Ⅰ.已知和反应时的能量变化关系如图1所示。
(1)和反应的离子方程式为 ;该反应属于 反应(填“吸热”或“放热”)。
(2)某实验小组设计了如图2中的两套实验装置,其中能用来证明“和反应的能量变化情况”的是装置 (填序号),可观察到的现象是 。
Ⅱ.三氯硅烷和纯净的氢气发生反应:。一定温度下,在容积为VL的恒容密闭容器中充入和,发生反应。和HCl的物质的量随时间的变化如图:
(3)下列说法能作为判断反应达到平衡状态的标志是 (填字母)。
a.容器内压强不再改变 b.体系内的气体密度不再改变
C. d.
(4)2min时,该反应的反应速率 (填“”“”或“”)。
(5)0~2min内,用表示的平均反应速率是 。
(6)该条件下,反应达到平衡时 。
(7)若将容器容积变为2V,则达到化学平衡状态所需要的时间将 (填“增长”“缩短”或“不变”)。
(8)若向该容器中充入Ne,则达到化学平衡状态所需要的时间将 (填“增长”“缩短”或“不变”)。
山西省部分学校2024-2025学年高一下学期期末联考 化学试题参考答案
题号 1 2 3 4 5 6 7 8 9 10
答案 C D C B D A B B C A
题号 11 12 13 14
答案 D D D A
15.(1)坩埚
(2)
(3)过滤
(4) B
(5) 分液漏斗 除去氯气中混有的HCl杂质 吸收未参与反应的,防止污染环境
16.(1)加快反应速率,提高浸出率
(2)和
(3)
(4) 能够催化分解,因此用量偏高 取最后一次洗涤液少许于试管中,加入盐酸酸化的溶液,若无白色沉淀生成,则已洗净,反之,未洗净
(5)
(6)沉RE
17.(1)
(2)ac
(3)碳碳双键、羧基
(4)2-甲基丙烷或异丁烷
(5) 2 取代反应或酯化反应
(6) 2 或
18.(1) 吸热
(2) Ⅰ 导管中红墨水液面上升
(3)ab
(4)
(5)
(6)
(7)增长
(8)不变
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列文物艺术品的主要成分属于无机非金属材料的是
艺术品
选项 A.清·丝绸团扇 B.清·茶叶锡罐 C.春秋·水晶笏板 D.清·弓弩箭
A.A B.B C.C D.D
2.化学与生产、生活、环境密切相关,下列说法错误的是
A.普通玻璃的生产以纯碱、石灰石和石英砂为主要原料
B.碳化硅具有优异的高温抗氧化性能,可用作耐高温结构材料
C.食品中添加适量的二氧化硫可以起到漂白、防腐和抗氧化等作用
D.玻璃雕刻工艺需要用到化学腐蚀试剂,可以用盐酸溶蚀玻璃生产磨砂玻璃
3.糖类、油脂、蛋白质和维生素是重要的营养物质。下列说法正确的是
A.蛋白质均能溶于水,其水解的最终产物均为氨基酸
B.工业上利用油脂在酸性条件下的水解反应获得高级脂肪酸和甘油,进行肥皂的生产
C.蔗糖、淀粉和纤维素在稀酸的催化下能发生水解反应,最终生成单糖
D.抗坏血酸(即维生素C)是水果罐头中常用的抗氧化剂,因为其具有强氧化性
4.化学与可持续发展,关系到自然资源的开发与利用,关系到化学品的合理使用,关系到人类健康和环境保护,应当引起重视。下列叙述错误的是
A.工业海水提溴技术中,吸收塔使用和水吸收溴转化为氢溴酸,其中作还原剂
B.石油的分馏可获得汽油、煤油等轻质油,煤的干馏可获得粗苯、乙烯等化工原料,二者均属于化学变化
C.绿色化学要求从源头减少或消除环境污染,改变“先污染后治理”的观念与做法
D.污水处理时,常加入硫酸亚铁、硫酸铝、聚合氯化铝等混凝剂,使污水中的细小悬浮物聚集成较大的颗粒后沉淀
5.下列有关化学用语表示错误的是
A.的电子式: B.聚丙烯腈的结构简式:
C.乙醛所含官能团的结构简式: D.乙烷的空间填充模型:
6.下列关于化学反应与能量变化的说法正确的是
A.图1可表示盐酸与碳酸氢钠反应的能量变化
B.图2所示装置中铜表面出现气泡
C.图3所示的锌锰干电池中电子由碳棒通过导线流向锌筒
D.图4所示装置中Al电极的电极反应式为
7.设为阿伏加德罗常数的值。下列叙述正确的是
A.标准状况下,中含有氯原子的数目为
B.常温下,分子所含中子的数目为
C.常温下,与足量的反应,转移的电子数为
D.溶于足量的水中,所得溶液中含有、和的粒子总数为
8.下列反应能够发生且离子反应方程式书写正确的是
A.氧化钡与稀硫酸混合:
B.氯水中加入少量氢氧化钙溶液:
C.稀硝酸中加入少量铁屑:
D.向酸性溶液中通入气体:
9.利用如图所示装置(必要时加热装置可更换或撤去)进行实验,装置Ⅱ中现象不能证明装置Ⅰ中生成的产物的是
选项 装置Ⅰ中反应及部分产物 装置Ⅱ中检测试剂及现象
A 与稀反应生成 亚硫酸溶液,产生黄色沉淀
B 与稀硫酸反应生成 足量的澄清石灰水,溶液变浑浊
C KI与浓反应生成 淀粉-KI,溶液变蓝
D C与浓反应生成 品红,溶液褪色
A.A B.B C.C D.D
10.不对称有机物M是医药合成的重要中间体。有机物M存在如下反应,下列说法正确的是
A.M和N均能使酸性高锰酸钾溶液褪色
B.M与发生加成反应的产物是
C.1mol N与NaOH溶液反应最多消耗2mol NaOH
D.M分子中碳原子均位于同一平面
11.下列实验操作及现象能得出相应结论的是
选项 实验操作 实验现象 实验结论
A 向硫代硫酸钠溶液中加入稀硫酸,并进行水浴加热 有乳黄色硫沉淀产生 硫酸具有氧化性
B 向溶液中通入和气体X 产生白色沉淀 气体X为
C 向盛有浓的两支试管中分别加入锌片和铝片 加入锌片的试管中迅速产生红棕色气体 金属性:
D 向盛有淀粉水解液的试管中加入过量NaOH溶液调节至碱性,再滴入3滴溶液,加热 有砖红色沉淀生成 淀粉水解液中含有葡萄糖
A.A B.B C.C D.D
12.某种重要化学合成试剂的结构如图所示。已知W、Y、Z、M、Q是原子序数依次增大的短周期主族元素,其中Q、Z同主族,Y、M同主族。下列有关说法错误的是
A.原子半径:
B.常温下,Q的单质易溶于二硫化碳
C.简单氢化物的沸点:
D.最高价氧化物对应水化物的酸性:
13.某科研兴趣小组研究Fe、石墨电极在稀硫酸亚铁和稀硫酸()混合液作电解质时的原电池反应原理,如图所示。下列说法错误的是
A.电子由Fe电极流出,石墨电极为该电池的正极
B.放电过程中,电解质溶液中的向铁电极移动
C.氧气发生的反应为:
D.当铁电极质量减少5.6g时,理论上消耗标准状况下
14.为探究草酸氢钾与酸性高锰酸钾溶液反应速率的影响因素,设计如表所示方案。下列说法错误的是
实验序号 () () () () 褪色时间t/min
① 5 5 2 0 8 8
② 10 5 2 0 a 6
③ 5 5 5 0 b 5
④ 10 5 2 3 0
A.,
B.实验①②的目的为探究溶液的浓度对化学反应速率的影响
C.实验①③的目的为探究硫酸的浓度对化学反应速率的影响
D.,说明对草酸氢钾与酸性高锰酸钾溶液的反应有催化作用
二、解答题
15.碘酸银()为白色结晶性粉末,微溶于水,光照条件下会分解,具有光敏感性。碘酸银常用作化学试剂,测定血液中的少量氯化物。此外,它还可以与碘化银、碘化铜一起作为人工降雨的成核剂。一种以海带和其他试剂为原料制备碘酸银的实验流程如下:
回答下列问题:
(1)步骤①中盛放海带的仪器为 。
(2)步骤⑥中发生反应的化学方程式为 。
(3)步骤⑦分离出的操作名称是 。
(4)已知与可发生反应:。则当有单质生成时,转移电子的物质的量为 mol。选用如下试剂或药品检验中的,可选用的物质有:
①蒸馏水 ②蓝色石蕊试纸 ③碘化钾淀粉试纸 ④淀粉 ⑤蔗糖 ⑥乙酸 ⑦乙醇
进行上述实验必须使用的物质是 (填字母)。
A.①③ B.①③⑥ C.②④⑥ D.①②④⑤⑦
(5)利用氯气与或也可制备,实验室利用氯气氧化废碘液中的或后加入KOH溶液调节pH为10获得的实验装置如图:
①仪器m的名称为 。
②饱和食盐水的作用为 。
③NaOH的作用为 。
④实验过程中,装置A中产生黄绿色气体,一段时间后,装置C中棕褐色溶液颜色逐渐变浅,当褪至无色时停止制备氯气。向装置C中加入KOH溶液调节pH为10获得。据文献报道,碘元素生成碘酸(,中强酸),装置C中和在水溶液中反应生成碘酸的化学方程式为 。
16.某含镍废料中含有NiO和稀土金属(用RE表示)的氧化物,及一定量的FeO、MgO、、、、等,利用该废料制备碱式碳酸镍[]的工艺流程如下:
已知:①“酸浸”后溶液中金属离子有、、、、、及少量的(其中代表、和等稀土元素离子)。
②室温下,溶液中金属离子开始沉淀和完全沉淀的pH如表所示。
金属离子
开始沉淀 7.5 2.2 7.2 8.9 11.9 7.8
完全沉淀 9.0 3.2 8.7 10.9 13.9 9.8
(1)“酸浸”时,将含镍废料粉碎的目的是 。
(2)滤渣1的主要成分为 。
(3)稀土复盐中 (用含y的代数式表示)。
(4)“氧化”步骤中的用量远高于理论用量的原因为 ,调pH的范围是 。检验滤渣2是否洗涤干净的操作方法为 。
(5)“除锰”时,会转化为,则发生反应的离子方程式为 。
(6)“沉镍”所得废液经处理后,可于“ ”工序循环利用。
17.2-甲基丙烯酸乙二醇酯(EDGMA)是一种重要的有机合成原料,可作交联剂及用于合成树脂。2-甲基丙烯酸乙二醇酯的一种合成路线如下:
已知:A和D互为同系物。
回答下列问题:
(1)E的结构简式为 。
(2)下列关于有机物C的说法错误的是 (填字母)。
a. C与甲醇互为同系物
b.相同物质的量的C与乙炔分别完全燃烧,二者耗氧量相同
c.0.5mol C与足量的Na反应放出标准状况下
d.C能够在Cu作催化剂加热的条件下与反应生成乙二醛
(3)F中含有的官能团名称是 。
(4)D与反应后的有机产物的化学名称为 。
(5)C与F反应生成G的化学方程式为 ,反应类型为 。
(6)有机物A和有机物D均可由分子式为的一种同分异构体通过裂解反应制得,的同分异构体中含有4个甲基的结构有 种,任写其中一种的结构简式 。
三、填空题
18.化学反应伴随着能量变化和物质的变化,其物质的变化中还存在着化学反应速率的变化与限度问题。根据下列信息分析化学反应中的变化问题。
Ⅰ.已知和反应时的能量变化关系如图1所示。
(1)和反应的离子方程式为 ;该反应属于 反应(填“吸热”或“放热”)。
(2)某实验小组设计了如图2中的两套实验装置,其中能用来证明“和反应的能量变化情况”的是装置 (填序号),可观察到的现象是 。
Ⅱ.三氯硅烷和纯净的氢气发生反应:。一定温度下,在容积为VL的恒容密闭容器中充入和,发生反应。和HCl的物质的量随时间的变化如图:
(3)下列说法能作为判断反应达到平衡状态的标志是 (填字母)。
a.容器内压强不再改变 b.体系内的气体密度不再改变
C. d.
(4)2min时,该反应的反应速率 (填“”“”或“”)。
(5)0~2min内,用表示的平均反应速率是 。
(6)该条件下,反应达到平衡时 。
(7)若将容器容积变为2V,则达到化学平衡状态所需要的时间将 (填“增长”“缩短”或“不变”)。
(8)若向该容器中充入Ne,则达到化学平衡状态所需要的时间将 (填“增长”“缩短”或“不变”)。
山西省部分学校2024-2025学年高一下学期期末联考 化学试题参考答案
题号 1 2 3 4 5 6 7 8 9 10
答案 C D C B D A B B C A
题号 11 12 13 14
答案 D D D A
15.(1)坩埚
(2)
(3)过滤
(4) B
(5) 分液漏斗 除去氯气中混有的HCl杂质 吸收未参与反应的,防止污染环境
16.(1)加快反应速率,提高浸出率
(2)和
(3)
(4) 能够催化分解,因此用量偏高 取最后一次洗涤液少许于试管中,加入盐酸酸化的溶液,若无白色沉淀生成,则已洗净,反之,未洗净
(5)
(6)沉RE
17.(1)
(2)ac
(3)碳碳双键、羧基
(4)2-甲基丙烷或异丁烷
(5) 2 取代反应或酯化反应
(6) 2 或
18.(1) 吸热
(2) Ⅰ 导管中红墨水液面上升
(3)ab
(4)
(5)
(6)
(7)增长
(8)不变
同课章节目录
