1.2 物质的酸碱性 第2课时(课件 16张PPT)
文档属性
| 名称 | 1.2 物质的酸碱性 第2课时(课件 16张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 6.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2025-08-06 00:00:00 | ||
图片预览





文档简介
(共16张PPT)
1.2.2 物质的酸碱性
【核心概念】
2.物质的变化与化学反应 结构与功能
【学习内容与要求】
1.4 常见的化合物
从微观上理解酸和碱的概念;知道常见物质的酸碱性与酸、碱的关系;认识物质的结构决定其性质。
【教学目标】
1.科学观念:知道物质酸碱性的检验方法;知道pH的变化范围,理解酸碱性与pH大小的关系。
2.科学思维:理解酸碱性与pH大小的关系。
3.探究实践:学会用酸碱指示剂检验物质的酸碱性;会用pH试纸测定物质的pH;通过对紫色石蕊试液、无色酚酞试液这两种酸碱指示剂在不同溶液中的颜色变化的探究,初步学会运用观察、实验的方法获得知识。
4.态度责任:通过一些探究活动,进一步认识与体验科学探究的过程,感受科学探究学习的快乐。
知道物质酸碱性的检验方法
1.1 酸碱指示剂
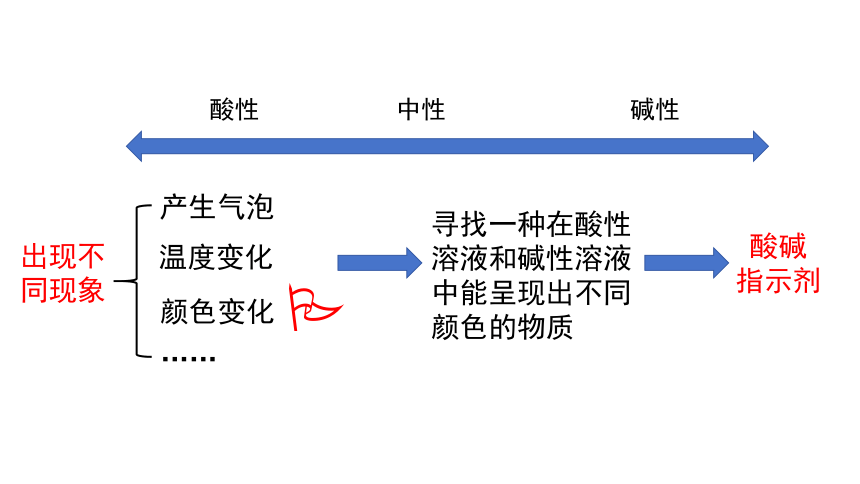
酸性
碱性
中性
出现不同现象
产生气泡
温度变化
颜色变化
……
寻找一种在酸性溶液和碱性溶液中能呈现出不同颜色的物质
酸碱
指示剂
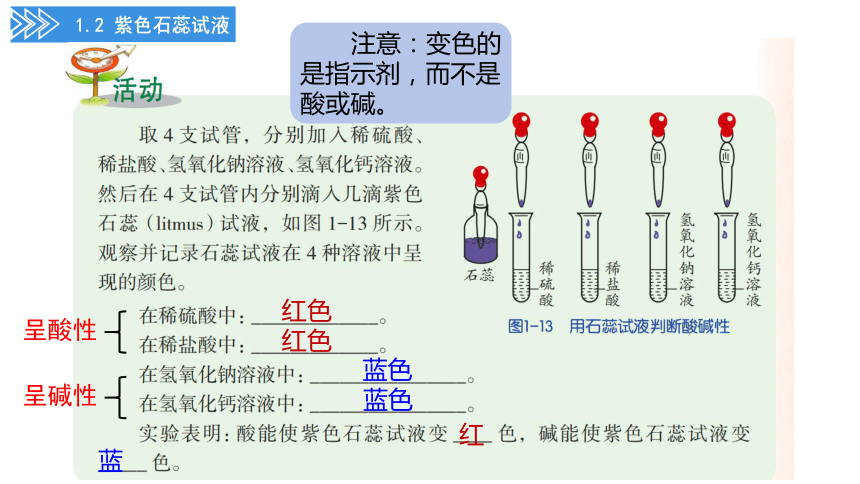
红色
红色
蓝色
蓝色
呈酸性
呈碱性
红
蓝
注意:变色的是指示剂,而不是酸或碱。
1.2 紫色石蕊试液
1.3 常见酸碱指示剂
常见指示剂和它们在酸性或碱性溶液中的颜色。
紫色石蕊试液
无色酚酞试液
蓝色石蕊试纸
红色石蕊试纸
指示剂 酸性溶液 碱性溶液
石蕊试液(紫色)
酚酞试液(无色)
蓝色石蕊试纸
红色石蕊试纸
红色
红色
红色
无色
蓝色
蓝色
不变色
不变色
变色规律:
石蕊“酸红碱蓝”
酚酞“酸无碱红”
知道pH的变化范围,理解酸碱性与pH大小的关系
2.1 pH值与酸碱性
pH 是反映物质酸碱性强弱的指标,它的范围通常在0~14 之间。
pH等于7 的物质呈中性;
pH小于7 的物质呈酸性;
pH大于7 的物质呈碱性;
酸性
碱性
中性
pH数值越大,碱性越强
pH数值越小,酸性越强
2.2 pH试纸
测定物质酸碱性强弱最常用、最简单的方法是使用pH试纸,如图所示。
pH试纸在酸碱性强弱不同的溶液里会显示出不同的颜色。
用pH试纸测试的方法比较粗略,精确的测试可使用一种称为酸度计的仪器。
pH小于7 的物质呈酸性;
pH大于7 的物质呈碱性;
酸性
碱性
中性
pH数值越大,碱性越强
pH数值越小,酸性越强
2.2 pH试纸
测定的方法:
用干燥、洁净的玻璃棒蘸取被测试的溶液,滴在pH试纸上。
将试纸显示的颜色与标准比色卡对照。
看颜色并而确定溶液的pH。
第一步:
第二步:
第三步:
注意的问题:
1.试纸不可直接伸入溶液中。
2.不能先用蒸馏水将pH试纸润湿。
(因为润湿试纸相当于稀释被检测的溶液,这会导致检测不准确)
不能“浸入”、不能“湿润”。
我们身边一些物质的pH:
1.2.2 物质的酸碱性
【核心概念】
2.物质的变化与化学反应 结构与功能
【学习内容与要求】
1.4 常见的化合物
从微观上理解酸和碱的概念;知道常见物质的酸碱性与酸、碱的关系;认识物质的结构决定其性质。
【教学目标】
1.科学观念:知道物质酸碱性的检验方法;知道pH的变化范围,理解酸碱性与pH大小的关系。
2.科学思维:理解酸碱性与pH大小的关系。
3.探究实践:学会用酸碱指示剂检验物质的酸碱性;会用pH试纸测定物质的pH;通过对紫色石蕊试液、无色酚酞试液这两种酸碱指示剂在不同溶液中的颜色变化的探究,初步学会运用观察、实验的方法获得知识。
4.态度责任:通过一些探究活动,进一步认识与体验科学探究的过程,感受科学探究学习的快乐。
知道物质酸碱性的检验方法
1.1 酸碱指示剂
酸性
碱性
中性
出现不同现象
产生气泡
温度变化
颜色变化
……
寻找一种在酸性溶液和碱性溶液中能呈现出不同颜色的物质
酸碱
指示剂
红色
红色
蓝色
蓝色
呈酸性
呈碱性
红
蓝
注意:变色的是指示剂,而不是酸或碱。
1.2 紫色石蕊试液
1.3 常见酸碱指示剂
常见指示剂和它们在酸性或碱性溶液中的颜色。
紫色石蕊试液
无色酚酞试液
蓝色石蕊试纸
红色石蕊试纸
指示剂 酸性溶液 碱性溶液
石蕊试液(紫色)
酚酞试液(无色)
蓝色石蕊试纸
红色石蕊试纸
红色
红色
红色
无色
蓝色
蓝色
不变色
不变色
变色规律:
石蕊“酸红碱蓝”
酚酞“酸无碱红”
知道pH的变化范围,理解酸碱性与pH大小的关系
2.1 pH值与酸碱性
pH 是反映物质酸碱性强弱的指标,它的范围通常在0~14 之间。
pH等于7 的物质呈中性;
pH小于7 的物质呈酸性;
pH大于7 的物质呈碱性;
酸性
碱性
中性
pH数值越大,碱性越强
pH数值越小,酸性越强
2.2 pH试纸
测定物质酸碱性强弱最常用、最简单的方法是使用pH试纸,如图所示。
pH试纸在酸碱性强弱不同的溶液里会显示出不同的颜色。
用pH试纸测试的方法比较粗略,精确的测试可使用一种称为酸度计的仪器。
pH小于7 的物质呈酸性;
pH大于7 的物质呈碱性;
酸性
碱性
中性
pH数值越大,碱性越强
pH数值越小,酸性越强
2.2 pH试纸
测定的方法:
用干燥、洁净的玻璃棒蘸取被测试的溶液,滴在pH试纸上。
将试纸显示的颜色与标准比色卡对照。
看颜色并而确定溶液的pH。
第一步:
第二步:
第三步:
注意的问题:
1.试纸不可直接伸入溶液中。
2.不能先用蒸馏水将pH试纸润湿。
(因为润湿试纸相当于稀释被检测的溶液,这会导致检测不准确)
不能“浸入”、不能“湿润”。
我们身边一些物质的pH:
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
