山西省吕梁市2024-2025学年高一下学期期末调研测试化学试卷(含答案)
文档属性
| 名称 | 山西省吕梁市2024-2025学年高一下学期期末调研测试化学试卷(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-07 00:00:00 | ||
图片预览




文档简介
山西省吕梁市2024-2025学年高一下学期期末调研测试化学试卷
一、单选题
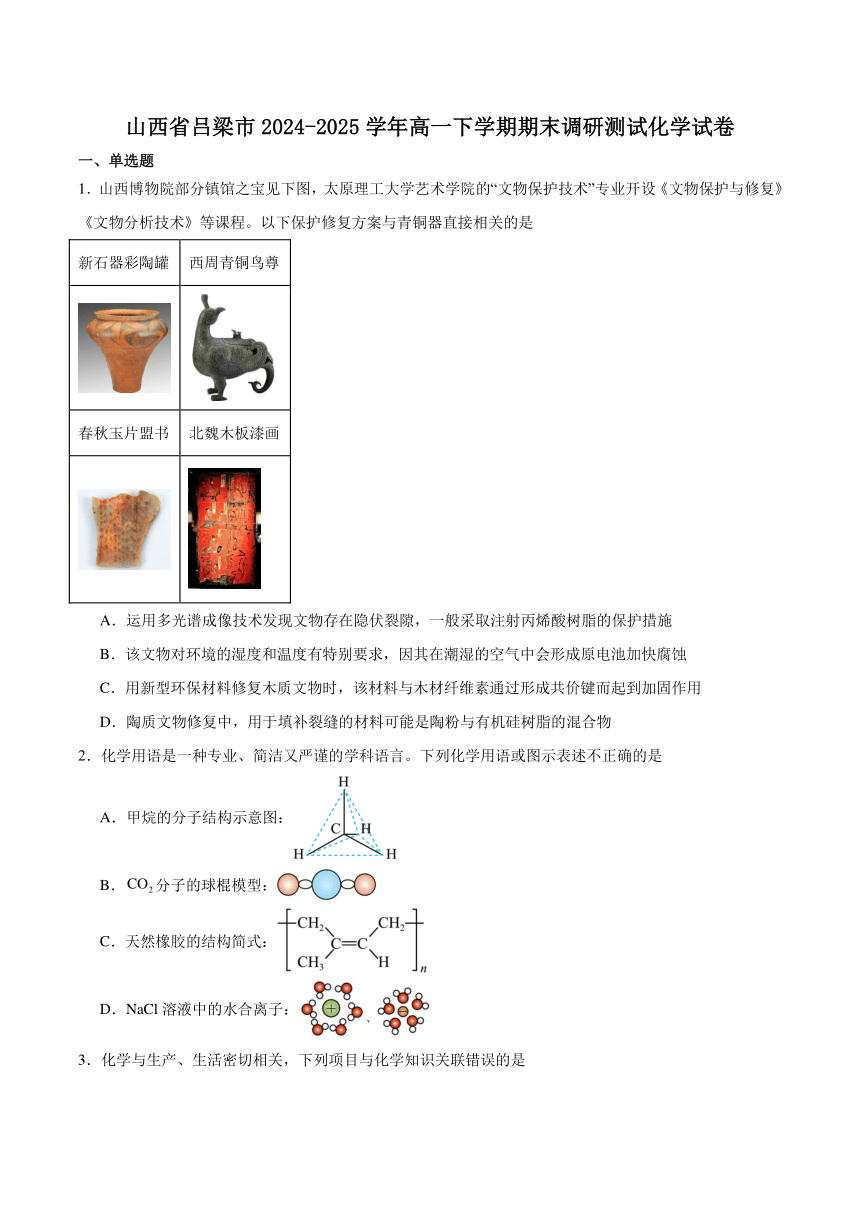
1.山西博物院部分镇馆之宝见下图,太原理工大学艺术学院的“文物保护技术”专业开设《文物保护与修复》《文物分析技术》等课程。以下保护修复方案与青铜器直接相关的是
新石器彩陶罐 西周青铜鸟尊
春秋玉片盟书 北魏木板漆画
A.运用多光谱成像技术发现文物存在隐伏裂隙,一般采取注射丙烯酸树脂的保护措施
B.该文物对环境的湿度和温度有特别要求,因其在潮湿的空气中会形成原电池加快腐蚀
C.用新型环保材料修复木质文物时,该材料与木材纤维素通过形成共价键而起到加固作用
D.陶质文物修复中,用于填补裂缝的材料可能是陶粉与有机硅树脂的混合物
2.化学用语是一种专业、简洁又严谨的学科语言。下列化学用语或图示表述不正确的是
A.甲烷的分子结构示意图:
B.分子的球棍模型:
C.天然橡胶的结构简式:
D.NaCl溶液中的水合离子:
3.化学与生产、生活密切相关,下列项目与化学知识关联错误的是
选项 项目 化学知识
A 面点师:用小苏打作膨松剂烘焙面包 可与酸反应
B 艺员助理:确保使用前暖宝宝包装完好 接触空气会形成原电池生热
C 垃圾处理站:用秸秆、树皮等生产酒精 糖类水解、发酵
D 运动会饮食顾问:指导餐饮搭配 葡萄糖是生命活动所需的主要能源物质
A.A B.B C.C D.D
根据下述材料,完成以下两个问题:
美拉德反应是一种广泛存在于食品工业中的反应,是羰基化合物(还原糖类)和氨基化合物(氨基酸和蛋白质)间的反应,生成的吡嗪类化合物能赋予食品独特的风味和色泽。某常见糖类与天门冬氨酸发生美拉德反应的部分流程如下:
已知:天门冬氨酸中-R代表
4.关于流程中出现的物质,下列说法正确的是
A.Y分子使酸性高锰酸钾溶液褪色,能证明碳碳双键的存在
B.W生成X的反应类型为加成反应
C.化合物W的链状结构中有两种含氧官能团,分别是羟基和酮羰基
D.化合物X和Y互为同分异构体
5.关于常见糖类、油脂、氨基酸和蛋白质,以下说法中不正确的是
A.葡萄糖发酵制醇阶段有产生
B.甲醛能使蛋白质变性,因此实验室常用福尔马林保存动物标本
C.甘氨酸( )和天门冬氨酸混合,在一定条件下可生成3种二肽
D.现代食品工业中通常用植物油与氢气反应生产人造奶油
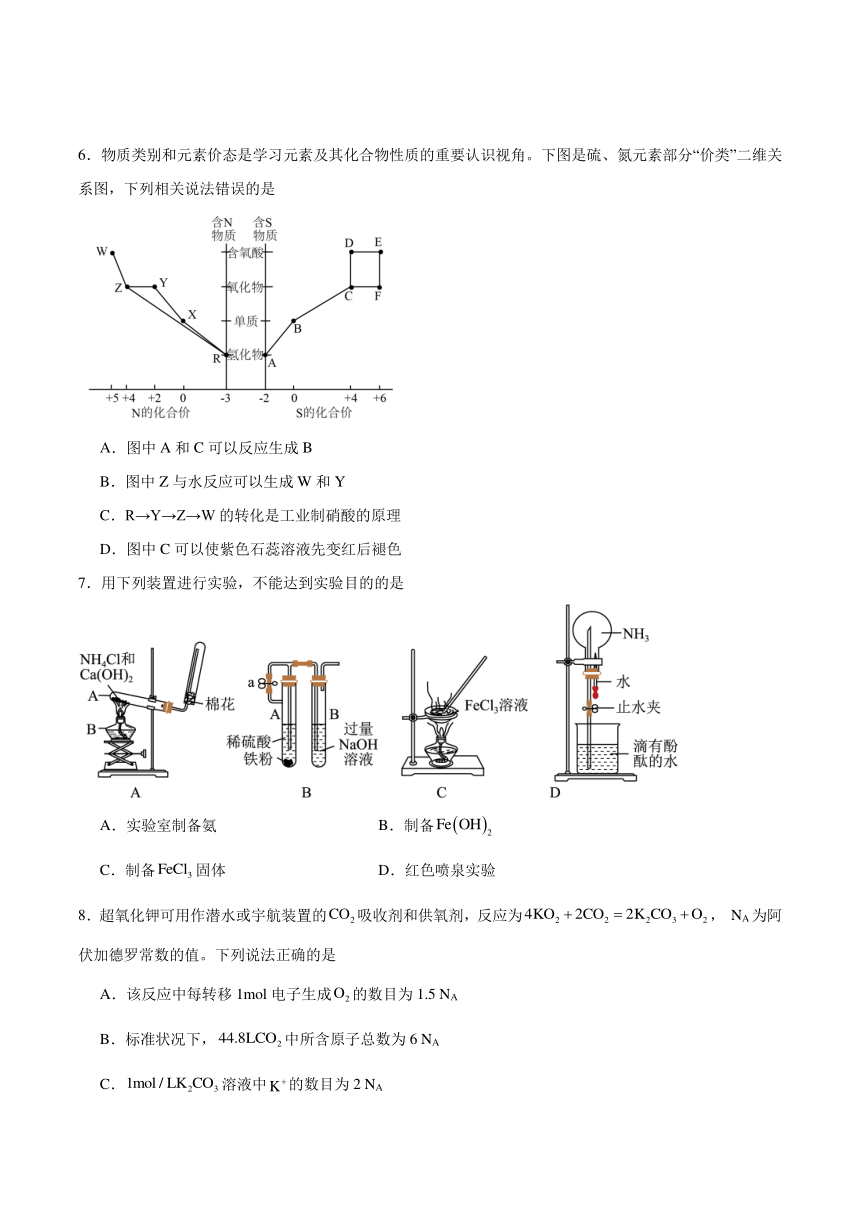
6.物质类别和元素价态是学习元素及其化合物性质的重要认识视角。下图是硫、氮元素部分“价类”二维关系图,下列相关说法错误的是
A.图中A和C可以反应生成B
B.图中Z与水反应可以生成W和Y
C.R→Y→Z→W的转化是工业制硝酸的原理
D.图中C可以使紫色石蕊溶液先变红后褪色
7.用下列装置进行实验,不能达到实验目的的是
A.实验室制备氨 B.制备
C.制备固体 D.红色喷泉实验
8.超氧化钾可用作潜水或宇航装置的吸收剂和供氧剂,反应为, NA为阿伏加德罗常数的值。下列说法正确的是
A.该反应中每转移1mol电子生成的数目为1.5 NA
B.标准状况下,中所含原子总数为6 NA
C.溶液中的数目为2 NA
D.常温常压下,晶体中离子的数目为3 NA
9.某小学科学实践课上,孩子们制做了“盐水小汽车”(图1)和“太阳能小汽车”(图2),其中“盐水小汽车”因结构简单、制作方便,深受孩子们喜爱,它的结构和原理如图3所示。下列说法错误的是
A.使用前,应将Mg片用砂纸打磨干净
B.图3食盐水中的向Cu片移动
C.两种小汽车所涉及的能量转换形式完全相同
D.正极的电极反应式为
10.下列资源的综合利用中,在给定工艺条件下转化关系正确的是
A.工业制:
B.高纯硅的制备:石英砂粗硅高纯硅
C.工业制漂白粉:NaCl溶液
D.金属Al的冶炼:铝土矿→氧化铝铝
11.化学是以实验为基础的学科。下列实验方案设计、现象和结论都正确的是
方案 现象 结论
A 向0.5g淀粉中加入的溶液,加热一段时间,冷却,再加入少量新制的悬浊液,加热 无砖红色沉淀生成 淀粉未水解
B 向溶液中加入稀硫酸 溶液变浑浊 具有氧化性
C 将粉末和Al粉混合均匀,表面撒少量氯酸钾,插入Mg条,点燃 火星四射,有熔融物滴落 该反应是放热反应
D 把浓硫酸滴到pH试纸上 试纸变红 浓硫酸具有酸性
A.A B.B C.C D.D
12.汽车尾气净化装置如图1,原理为。若在实验室中,某温度下,向5L盛有催化剂的密闭容器中投入一定量NO和CO,NO、CO的物质的量浓度随时间变化如图2所示。下列说法不正确的是
A.ab段的反应速率
B.升高温度,化学反应速率不一定加快
C.当混合气体的平均相对分子质量不再发生变化时,能表明反应已达平衡状态
D.实际汽车尾气净化时,可以通过增大压强加快反应速率
13.CO可用于处理大气污染物,在催化剂作用下该反应的机理如图1所示,反应过程中能量变化如图2所示(TS和IM分别指化学反应机理中的过渡态和中间体)。下列说法正确的是
A.总反应的催化剂为
B.中间体的稳定性顺序为:
C.反应①和反应②均为放热反应
D.整个过程中被氧化的非金属元素为N和C
14.实验室用乙醇(沸点为78.3℃)和乙酸(沸点为117.9℃),在浓硫酸的催化下,利用图1装置制取乙酸乙酯(沸点为77.1℃)某小组将右侧试管中的粗品取出,按照图2所示的步骤分离乙酸乙酯、乙醇和乙酸。下列说法错误的是
A.图1中干燥管的作用是防倒吸
B.图2中操作1是分液,操作2和3都是蒸馏
C.蒸馏时需要用到球形冷凝管
D.A是乙酸乙酯,E是乙醇,试剂a可选用硫酸
二、解答题
15.氮及其化合物对我们的生产、生活有着重要的影响。汽车发动机工作时,引发和反应生成的会对环境产生影响。
I.如图是和反应生成NO的能量变化示意图。
(1)①图中三种分子最稳定的是 (填写结构式)。
②若反应生成1molNO气体,则吸收 kJ的能量。
II.研究之间的转化具有重要意义。在2L的恒温恒容密闭容器中,通入等物质的量的NO和,发生反应,随时间的变化如下表:
t/s 0 1 2 3 4 5
2.0 1.2 0.8 0.5 0.4 0.4
(2)0~3s内, 。
(3)达到平衡时,的转化率为 。
(4)①平衡时容器内压强与反应开始时容器内压强之比为 。(忽略和间的转化)
②下列情况能表明该反应达到平衡状态的是
A.
B.密闭容器中气体的颜色不变
C.密闭容器中混合气体的密度不变
D.单位时间内消耗的同时消耗
III.为减少汽车尾气中的排放,应该开发新的车用能源。
(5)肼—空气燃料电池是一种碱性电池,能量转化率高,无污染,有广泛的应用前景。其工作原理如图所示,电池工作时,空气从 (填“A”或“B”)口通入;若肼—空气燃料电池产物为氮气和水,写出负极的电极反应式: 。
16.某化学兴趣小组用除去表面氧化物的铁钉(碳素钢)与浓硫酸共热制取并完成相关物质的性质探究(不考虑水蒸气)。
【探究一】
(1)称取铁钉3.0g,粉碎后加入装有7.5mL浓硫酸的大试管中,加热,充分反应后得到溶液X并收集气体Y。
①甲同学若要探究X溶液中是否存在,应选用 。
a.KSCN溶液和氯水 b.酸性溶液 c.KSCN溶液 d.NaOH溶液
②乙同学用注射器取448mL(已换算为标准状况)气体Y,通入足量溴水中充分反应,然后加入足量溶液,经一系列操作后得到2.33g固体,则该固体物质的化学式为 。
【探究二】
根据上述实验中体积分数的分析,丙同学认为气体Y中还可能含有和两种气体(气体在标准状况下的密度为)。设计下列实验(图中夹持类装置已省略,假设有关气体反应完全)进行探究。
(2)①若气体Y中含有,预测实验现象是 。
②装置F的作用为 。
(3)为确认的存在,需在 添加一个盛有澄清石灰水的洗气瓶M。
a.A之前 b.A~B间 c.B~C间 d.C~D间
(4)请解释生成气体的原因: (用化学方程式表示)。
【探究三】
丁同学将Y气体分别通入下列两种溶液中:
(5)试管①中的现象为紫红色褪去,写出该反应的离子反应方程式: 。
(6)试管②中没有观察到现象,此时向其中通入气体A,产生可溶于盐酸的白色沉淀,则A为 (填写化学式,下同),白色沉淀为 。
17.很多重要的化工原料都来源于石油化工,如苯、丙烯、A等,其中A的产量可以用来衡量一个国家的石油化工发展水平。用A为原料合成其它有机物的流程如图所示:
请回答下列问题:
(1)A与氢气反应得到H,下列物质与H互为同系物的有 (填写序号)。
①②③④⑤
(2)化合物G中的含氧官能团名称为 ,C的环状同分异构体的结构简式为 。
(3)写出F→G的化学方程式: 。若用代替,则生成水的摩尔质量为 。
(4)将等物质的量的D、F混合后,分别与足量Na、反应,所产生气体在相同条件下的体积比为 。
(5)有机物G能发生加成聚合反应,所得产物是一种用途广泛的树脂,该聚合物的结构简式为 。
(6)相对分子质量比有机物D大28且属于羧酸类的物质有 种。
18.海水是巨大的资源宝库。根据下图海水综合利用的工艺流程图,完成下列问题:
(1)粗盐中含有和,需提纯后才能综合利用。(i)中粗盐提纯的步骤有:①加入过量的溶液;②加入过量的溶液;③加入过量的NaOH溶液;④加入盐酸,调节溶液至中性;⑤溶解;⑥过滤;⑦蒸发。正确的操作顺序是 。
a.⑤③②①⑥④⑦ b.⑤②③①④⑥⑦ c.⑤②①③④⑥⑦ d.⑤①②③⑥④⑦
(2)上述操作过程中,判断已经沉淀完全的方法是 。
(3)为使母液中的转化为,从经济效益角度考虑,最好选用 。
a.氨水 b.氢氧化钙 c.氢氧化钠
(4)(ii)中分离与母液的操作名称是 。
(5)电解熔融氯化镁所得液态镁不能在中冷却,原因是 (结合化学反应方程式解释)。
(6)工业上常用“吹出法”提溴,(ⅳ)中主要包括吹出、吸收(用溶液)、酸化,写出碳酸钠溶液吸收溴蒸气的离子反应方程式: (溴的氧化产物为价)。
(7)欲从1000L海水(溴含量约为)中提取溴,若改用吸收热空气吹出的溴,理论上需要的质量为 g。
题号 1 2 3 4 5 6 7 8 9 10
答案 B D A D C D C B C B
题号 11 12 13 14
答案 C D B C
15.(1) N2 90kJ
(2)0.00025mol/(L s)
(3)40%
(4) 4:5 BD
(5) B
16.(1) c BaSO4
(2) D中氧化铜由黑色变为红色,E中无水硫酸铜变蓝 防止空气中水蒸气进入E干扰实验
(3)c
(4)C+2H2SO4(浓)CO2↑+2SO2↑+2H2O
(5)5SO2+2MnO+2H2O=5SO+2Mn2++4H+
(6) NH3 BaSO3
17.(1)④⑤
(2) 酯基
(3) 19g/mol
(4)1:2
(5)
(6)8
18.(1)b
(2)静置,取上层清液于试管中,滴加BaCl2溶液,若无白色沉淀产生,则证明已经沉淀完全。
(3)b
(4)过滤
(5)3Mg+N2Mg3N2,液态镁会与氮气等发生反应,生成氮化镁杂质。
(6)
(7)26
一、单选题
1.山西博物院部分镇馆之宝见下图,太原理工大学艺术学院的“文物保护技术”专业开设《文物保护与修复》《文物分析技术》等课程。以下保护修复方案与青铜器直接相关的是
新石器彩陶罐 西周青铜鸟尊
春秋玉片盟书 北魏木板漆画
A.运用多光谱成像技术发现文物存在隐伏裂隙,一般采取注射丙烯酸树脂的保护措施
B.该文物对环境的湿度和温度有特别要求,因其在潮湿的空气中会形成原电池加快腐蚀
C.用新型环保材料修复木质文物时,该材料与木材纤维素通过形成共价键而起到加固作用
D.陶质文物修复中,用于填补裂缝的材料可能是陶粉与有机硅树脂的混合物
2.化学用语是一种专业、简洁又严谨的学科语言。下列化学用语或图示表述不正确的是
A.甲烷的分子结构示意图:
B.分子的球棍模型:
C.天然橡胶的结构简式:
D.NaCl溶液中的水合离子:
3.化学与生产、生活密切相关,下列项目与化学知识关联错误的是
选项 项目 化学知识
A 面点师:用小苏打作膨松剂烘焙面包 可与酸反应
B 艺员助理:确保使用前暖宝宝包装完好 接触空气会形成原电池生热
C 垃圾处理站:用秸秆、树皮等生产酒精 糖类水解、发酵
D 运动会饮食顾问:指导餐饮搭配 葡萄糖是生命活动所需的主要能源物质
A.A B.B C.C D.D
根据下述材料,完成以下两个问题:
美拉德反应是一种广泛存在于食品工业中的反应,是羰基化合物(还原糖类)和氨基化合物(氨基酸和蛋白质)间的反应,生成的吡嗪类化合物能赋予食品独特的风味和色泽。某常见糖类与天门冬氨酸发生美拉德反应的部分流程如下:
已知:天门冬氨酸中-R代表
4.关于流程中出现的物质,下列说法正确的是
A.Y分子使酸性高锰酸钾溶液褪色,能证明碳碳双键的存在
B.W生成X的反应类型为加成反应
C.化合物W的链状结构中有两种含氧官能团,分别是羟基和酮羰基
D.化合物X和Y互为同分异构体
5.关于常见糖类、油脂、氨基酸和蛋白质,以下说法中不正确的是
A.葡萄糖发酵制醇阶段有产生
B.甲醛能使蛋白质变性,因此实验室常用福尔马林保存动物标本
C.甘氨酸( )和天门冬氨酸混合,在一定条件下可生成3种二肽
D.现代食品工业中通常用植物油与氢气反应生产人造奶油
6.物质类别和元素价态是学习元素及其化合物性质的重要认识视角。下图是硫、氮元素部分“价类”二维关系图,下列相关说法错误的是
A.图中A和C可以反应生成B
B.图中Z与水反应可以生成W和Y
C.R→Y→Z→W的转化是工业制硝酸的原理
D.图中C可以使紫色石蕊溶液先变红后褪色
7.用下列装置进行实验,不能达到实验目的的是
A.实验室制备氨 B.制备
C.制备固体 D.红色喷泉实验
8.超氧化钾可用作潜水或宇航装置的吸收剂和供氧剂,反应为, NA为阿伏加德罗常数的值。下列说法正确的是
A.该反应中每转移1mol电子生成的数目为1.5 NA
B.标准状况下,中所含原子总数为6 NA
C.溶液中的数目为2 NA
D.常温常压下,晶体中离子的数目为3 NA
9.某小学科学实践课上,孩子们制做了“盐水小汽车”(图1)和“太阳能小汽车”(图2),其中“盐水小汽车”因结构简单、制作方便,深受孩子们喜爱,它的结构和原理如图3所示。下列说法错误的是
A.使用前,应将Mg片用砂纸打磨干净
B.图3食盐水中的向Cu片移动
C.两种小汽车所涉及的能量转换形式完全相同
D.正极的电极反应式为
10.下列资源的综合利用中,在给定工艺条件下转化关系正确的是
A.工业制:
B.高纯硅的制备:石英砂粗硅高纯硅
C.工业制漂白粉:NaCl溶液
D.金属Al的冶炼:铝土矿→氧化铝铝
11.化学是以实验为基础的学科。下列实验方案设计、现象和结论都正确的是
方案 现象 结论
A 向0.5g淀粉中加入的溶液,加热一段时间,冷却,再加入少量新制的悬浊液,加热 无砖红色沉淀生成 淀粉未水解
B 向溶液中加入稀硫酸 溶液变浑浊 具有氧化性
C 将粉末和Al粉混合均匀,表面撒少量氯酸钾,插入Mg条,点燃 火星四射,有熔融物滴落 该反应是放热反应
D 把浓硫酸滴到pH试纸上 试纸变红 浓硫酸具有酸性
A.A B.B C.C D.D
12.汽车尾气净化装置如图1,原理为。若在实验室中,某温度下,向5L盛有催化剂的密闭容器中投入一定量NO和CO,NO、CO的物质的量浓度随时间变化如图2所示。下列说法不正确的是
A.ab段的反应速率
B.升高温度,化学反应速率不一定加快
C.当混合气体的平均相对分子质量不再发生变化时,能表明反应已达平衡状态
D.实际汽车尾气净化时,可以通过增大压强加快反应速率
13.CO可用于处理大气污染物,在催化剂作用下该反应的机理如图1所示,反应过程中能量变化如图2所示(TS和IM分别指化学反应机理中的过渡态和中间体)。下列说法正确的是
A.总反应的催化剂为
B.中间体的稳定性顺序为:
C.反应①和反应②均为放热反应
D.整个过程中被氧化的非金属元素为N和C
14.实验室用乙醇(沸点为78.3℃)和乙酸(沸点为117.9℃),在浓硫酸的催化下,利用图1装置制取乙酸乙酯(沸点为77.1℃)某小组将右侧试管中的粗品取出,按照图2所示的步骤分离乙酸乙酯、乙醇和乙酸。下列说法错误的是
A.图1中干燥管的作用是防倒吸
B.图2中操作1是分液,操作2和3都是蒸馏
C.蒸馏时需要用到球形冷凝管
D.A是乙酸乙酯,E是乙醇,试剂a可选用硫酸
二、解答题
15.氮及其化合物对我们的生产、生活有着重要的影响。汽车发动机工作时,引发和反应生成的会对环境产生影响。
I.如图是和反应生成NO的能量变化示意图。
(1)①图中三种分子最稳定的是 (填写结构式)。
②若反应生成1molNO气体,则吸收 kJ的能量。
II.研究之间的转化具有重要意义。在2L的恒温恒容密闭容器中,通入等物质的量的NO和,发生反应,随时间的变化如下表:
t/s 0 1 2 3 4 5
2.0 1.2 0.8 0.5 0.4 0.4
(2)0~3s内, 。
(3)达到平衡时,的转化率为 。
(4)①平衡时容器内压强与反应开始时容器内压强之比为 。(忽略和间的转化)
②下列情况能表明该反应达到平衡状态的是
A.
B.密闭容器中气体的颜色不变
C.密闭容器中混合气体的密度不变
D.单位时间内消耗的同时消耗
III.为减少汽车尾气中的排放,应该开发新的车用能源。
(5)肼—空气燃料电池是一种碱性电池,能量转化率高,无污染,有广泛的应用前景。其工作原理如图所示,电池工作时,空气从 (填“A”或“B”)口通入;若肼—空气燃料电池产物为氮气和水,写出负极的电极反应式: 。
16.某化学兴趣小组用除去表面氧化物的铁钉(碳素钢)与浓硫酸共热制取并完成相关物质的性质探究(不考虑水蒸气)。
【探究一】
(1)称取铁钉3.0g,粉碎后加入装有7.5mL浓硫酸的大试管中,加热,充分反应后得到溶液X并收集气体Y。
①甲同学若要探究X溶液中是否存在,应选用 。
a.KSCN溶液和氯水 b.酸性溶液 c.KSCN溶液 d.NaOH溶液
②乙同学用注射器取448mL(已换算为标准状况)气体Y,通入足量溴水中充分反应,然后加入足量溶液,经一系列操作后得到2.33g固体,则该固体物质的化学式为 。
【探究二】
根据上述实验中体积分数的分析,丙同学认为气体Y中还可能含有和两种气体(气体在标准状况下的密度为)。设计下列实验(图中夹持类装置已省略,假设有关气体反应完全)进行探究。
(2)①若气体Y中含有,预测实验现象是 。
②装置F的作用为 。
(3)为确认的存在,需在 添加一个盛有澄清石灰水的洗气瓶M。
a.A之前 b.A~B间 c.B~C间 d.C~D间
(4)请解释生成气体的原因: (用化学方程式表示)。
【探究三】
丁同学将Y气体分别通入下列两种溶液中:
(5)试管①中的现象为紫红色褪去,写出该反应的离子反应方程式: 。
(6)试管②中没有观察到现象,此时向其中通入气体A,产生可溶于盐酸的白色沉淀,则A为 (填写化学式,下同),白色沉淀为 。
17.很多重要的化工原料都来源于石油化工,如苯、丙烯、A等,其中A的产量可以用来衡量一个国家的石油化工发展水平。用A为原料合成其它有机物的流程如图所示:
请回答下列问题:
(1)A与氢气反应得到H,下列物质与H互为同系物的有 (填写序号)。
①②③④⑤
(2)化合物G中的含氧官能团名称为 ,C的环状同分异构体的结构简式为 。
(3)写出F→G的化学方程式: 。若用代替,则生成水的摩尔质量为 。
(4)将等物质的量的D、F混合后,分别与足量Na、反应,所产生气体在相同条件下的体积比为 。
(5)有机物G能发生加成聚合反应,所得产物是一种用途广泛的树脂,该聚合物的结构简式为 。
(6)相对分子质量比有机物D大28且属于羧酸类的物质有 种。
18.海水是巨大的资源宝库。根据下图海水综合利用的工艺流程图,完成下列问题:
(1)粗盐中含有和,需提纯后才能综合利用。(i)中粗盐提纯的步骤有:①加入过量的溶液;②加入过量的溶液;③加入过量的NaOH溶液;④加入盐酸,调节溶液至中性;⑤溶解;⑥过滤;⑦蒸发。正确的操作顺序是 。
a.⑤③②①⑥④⑦ b.⑤②③①④⑥⑦ c.⑤②①③④⑥⑦ d.⑤①②③⑥④⑦
(2)上述操作过程中,判断已经沉淀完全的方法是 。
(3)为使母液中的转化为,从经济效益角度考虑,最好选用 。
a.氨水 b.氢氧化钙 c.氢氧化钠
(4)(ii)中分离与母液的操作名称是 。
(5)电解熔融氯化镁所得液态镁不能在中冷却,原因是 (结合化学反应方程式解释)。
(6)工业上常用“吹出法”提溴,(ⅳ)中主要包括吹出、吸收(用溶液)、酸化,写出碳酸钠溶液吸收溴蒸气的离子反应方程式: (溴的氧化产物为价)。
(7)欲从1000L海水(溴含量约为)中提取溴,若改用吸收热空气吹出的溴,理论上需要的质量为 g。
题号 1 2 3 4 5 6 7 8 9 10
答案 B D A D C D C B C B
题号 11 12 13 14
答案 C D B C
15.(1) N2 90kJ
(2)0.00025mol/(L s)
(3)40%
(4) 4:5 BD
(5) B
16.(1) c BaSO4
(2) D中氧化铜由黑色变为红色,E中无水硫酸铜变蓝 防止空气中水蒸气进入E干扰实验
(3)c
(4)C+2H2SO4(浓)CO2↑+2SO2↑+2H2O
(5)5SO2+2MnO+2H2O=5SO+2Mn2++4H+
(6) NH3 BaSO3
17.(1)④⑤
(2) 酯基
(3) 19g/mol
(4)1:2
(5)
(6)8
18.(1)b
(2)静置,取上层清液于试管中,滴加BaCl2溶液,若无白色沉淀产生,则证明已经沉淀完全。
(3)b
(4)过滤
(5)3Mg+N2Mg3N2,液态镁会与氮气等发生反应,生成氮化镁杂质。
(6)
(7)26
同课章节目录
