2.1.2 原子与离子、分子 课件(共21张PPT)2025-2026学年化学鲁教版(2024)九年级上册
文档属性
| 名称 | 2.1.2 原子与离子、分子 课件(共21张PPT)2025-2026学年化学鲁教版(2024)九年级上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-07 00:00:00 | ||
图片预览






文档简介
(共21张PPT)
认识原子结构示意图和离子的形成过程,知道物质可以由原子、离子或分子构成。
会画原子结构示意图,理解离子的形成过程。
01
02
原子是由原子核由核外的电子构成,其中原子核又由质子和中子构成。
2.为什么原子不显电性?
1.原子是由上面构成的?
原子核是由带正电荷的质子和不带电的中子构成的, 原子中电子代负电,由于原子钟质子数与电子数相等,它们所带的电荷数页相等,但电性相反,所以整个原子不显电性。
课前 · 回顾
课前 · 回顾
前面我们做过原子结构模型,知道原子是呈“球”状的,电子是在原子核外“很大”的空间里运动,那么电子在原子核外电子运动时是怎么排布的呢?
原子结构示意图
一、原子与离子、分子
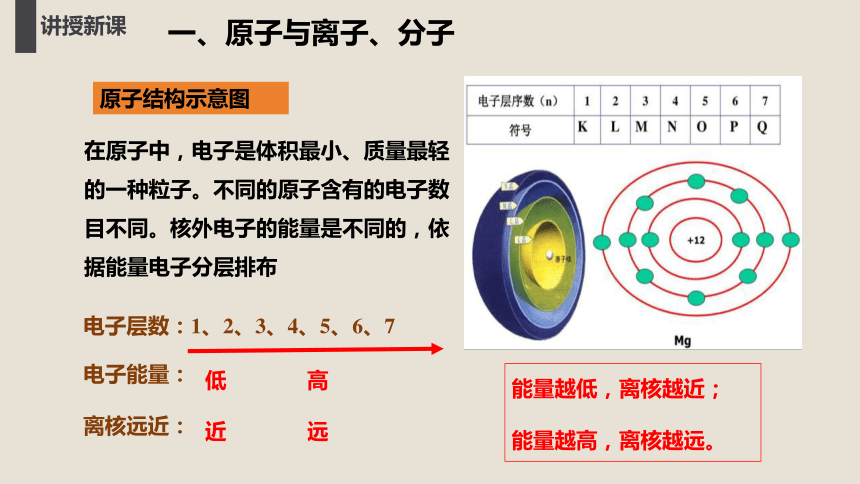
在原子中,电子是体积最小、质量最轻的一种粒子。不同的原子含有的电子数目不同。核外电子的能量是不同的,依据能量电子分层排布
电子层数:1、2、3、4、5、6、7
电子能量:
离核远近:
能量越低,离核越近;
能量越高,离核越远。
低 高
近 远
多识一点
用原子结构示意图可以方便简明地表示原子核外电子的排布。
原子结构的表示
原子核
质子数
第二层电子数
第一层
第二层最外层
原子核外电子排布规律:
(1)第一层最多排2个电子,第二层最多排8个电子,最外层子数不超过8个(第一层为最外层时,不超过2个)。
(2)排满第一层再排第二层,排满第二层再排第三层(适用于前三层)。
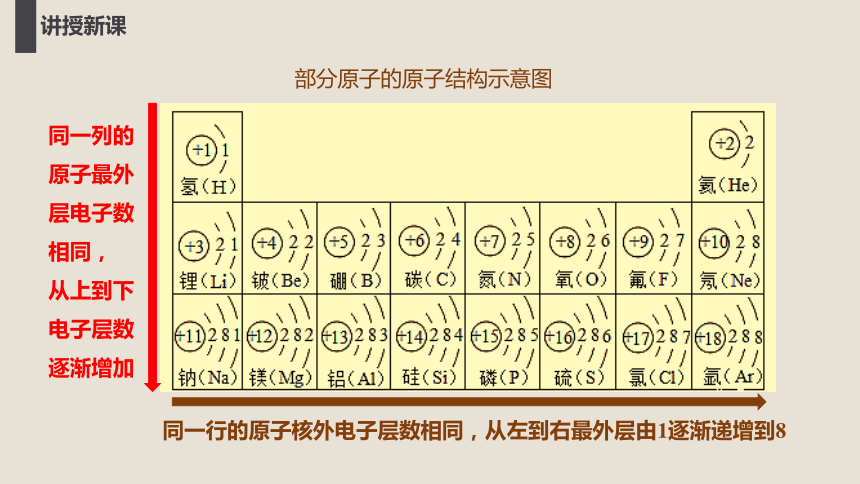
部分原子的原子结构示意图
同一列的原子最外层电子数相同,
从上到下电子层数逐渐增加
同一行的原子核外电子层数相同,从左到右最外层由1逐渐递增到8
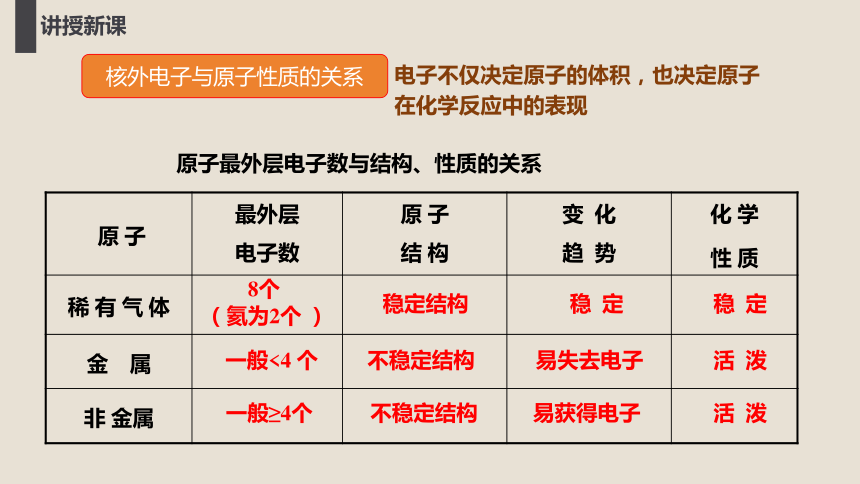
核外电子与原子性质的关系
原子最外层电子数与结构、性质的关系
原 子 最外层 电子数 原 子 结 构 变 化 趋 势 化 学
性 质
稀 有 气 体
金 属
非 金属
8个
(氦为2个 )
稳定结构
稳 定
稳 定
一般<4 个
不稳定结构
易失去电子
活 泼
一般≥4个
不稳定结构
易获得电子
活 泼
电子不仅决定原子的体积,也决定原子在化学反应中的表现
离子的形成
在化学反应中,原子核是不变的,发生改变的只是原子核外的电子。原子失去电子后变成带正电荷的阳离子,得到电子后变成带负电荷的阴离子。
由于最外层电子数为8(只有一个电子层时为2)个的结构是相对稳定结构。不具备相对稳定结构的原子有形成相对稳定结构的趋势。所以在化学反应中,原子就通过得失电子来使其达到稳定结构。
因此离子也是构成物质的一种基本粒子。原子通过得失电子后变成阴离子和阳离子,阴、阳离子通过静电作用结合成不显电性的物质。形成过程如下:
失去一个电子
得到一个电子
Na
Na+
Cl
Cl-
阴、阳离子间的静电作用
NaCl
(不显电性)
离子的概念:由原子得到或失去电子后形成的带电的原子或原子团叫作离子。
由于离子或原子的化学性质与最外层电子数有关,所以当离子或原子的最外层电子数相同时,它们的化学性质也相似。
离子的表示方法
离子符号右上角的数字表示离子所带的电荷数,正负号表示离子所带电荷的电性。
Mg2+
Cl-
Na+
O2-
镁离子
氯离子
钠离子
氧离子
每个镁离子带2个单位的正电荷
表示2个镁离子
Mg2+
2
分子物质
有些原子之间不是先转化成离子再构成物质的,而是原子之间直接结合形成分子,再由分子构成物质的。
例如,1个氢原子(H)能与1个氯原子(CI)结合,形成1个氯化氢分子(HCI),而1个氧原子(O)能与2个氢原子(H)结合,形成1个水分子(H2O)。
H2O
H2
O2
水的形成过程:
水(H2O)
O
H
H
H
H
氢原子
O
氧原子
结合
聚集
1.原子是由居于原子中心、带正电荷的原子核和核外带负电荷的电子构成的,原子不显电性。原子核所带电荷数称为核电荷数,它是由质子数决定的。
2.某原子的相对原子质量是一个该原子的质量跟一个碳-12原子质量的1/12的比值。
3.分子是由原子构成的,原子得到或失去电子后转变为离子。
原子、分子、离子都是构成物质的微观粒子。
长话短说
质子和中子还可以在分吗?
原子可以再分为质子、中子和电子,那么质子、中子和电子能否再分
1964年,科学家首次提出了夸克模型(图2-6),认为质子、中子由更小的夸克构成。这一模型的提出,成功地解释了许多事实。随着科学技术的进步,人们不仅利用大型粒子对撞机证明了夸克的存在,更发现与所有已知的质子、中子、电子等亚原子粒子不同,夸克带有分数电荷且都是两两成对或三三成群。
夸克的发现不仅刷新了人类对微观世界的认知,也再次激发了人类探索微观世界的热情。随着众多亚原子粒子不断被发现,人类逼近微观世界本质的步伐也越来越快。
图2-5 夸克模型
多识一点
1.如图为镁原子的结构示意图,下列有关镁原子的说法正确的是( )
A.镁原子的核内质子数为12
B.镁原子的核外电子数为2
C.镁原子在化学反应中易得到2个电子,形成镁离子Mg2+
D.镁原子最外电子层达到了稳定结构
A
2.下列关于粒子结构示意图的说法正确的是( )
A.第①组的原子在化学反应中都易得到电子
B.第②组的原子的化学性质相似
C.第③组原子的化学性质相似
D.第④组的粒子具有相对稳定的结构
CD
3.如图是四种粒子的结构示意图,下列有关说法不正确的是( )
A.①表示的粒子属于金属阳离子
B.③④表示的粒子化学性质相似
C.③在化学反应中易得到电子
D.原子、离子等都是构成物质的基本粒子
BC
4.通过探究物质构成的奥秘,我们了解了物质的组成与结构。
(1)物质的组成和构成关系如图所示,
图中①表示 ______,②表示 _______。
(2)电子的质量很小,可以忽略不计,
所以原子的质量主要集中在 ________上,相
对原子质量近似等于 _______与中子数之和。
(3)金属铜是由 ________(选填“原子”、
“分子”或“离子”)构成的。
质子
离子
原子核
质子数
原子
5.如下图所示,分别是钾元素、氢元素、氧元素、钠元素的原子结构示意图。
(1)A 中 X 的值为_________;
(2)A、D 化学性质相似的原因是___________________;
(3)B 形成的离子符号为____________;
(4)根据上图信息分析,1 个氢氧根离子
中含有的电子数是_______。
19
最外层电子数相同
H+
10
认识原子结构示意图和离子的形成过程,知道物质可以由原子、离子或分子构成。
会画原子结构示意图,理解离子的形成过程。
01
02
原子是由原子核由核外的电子构成,其中原子核又由质子和中子构成。
2.为什么原子不显电性?
1.原子是由上面构成的?
原子核是由带正电荷的质子和不带电的中子构成的, 原子中电子代负电,由于原子钟质子数与电子数相等,它们所带的电荷数页相等,但电性相反,所以整个原子不显电性。
课前 · 回顾
课前 · 回顾
前面我们做过原子结构模型,知道原子是呈“球”状的,电子是在原子核外“很大”的空间里运动,那么电子在原子核外电子运动时是怎么排布的呢?
原子结构示意图
一、原子与离子、分子
在原子中,电子是体积最小、质量最轻的一种粒子。不同的原子含有的电子数目不同。核外电子的能量是不同的,依据能量电子分层排布
电子层数:1、2、3、4、5、6、7
电子能量:
离核远近:
能量越低,离核越近;
能量越高,离核越远。
低 高
近 远
多识一点
用原子结构示意图可以方便简明地表示原子核外电子的排布。
原子结构的表示
原子核
质子数
第二层电子数
第一层
第二层最外层
原子核外电子排布规律:
(1)第一层最多排2个电子,第二层最多排8个电子,最外层子数不超过8个(第一层为最外层时,不超过2个)。
(2)排满第一层再排第二层,排满第二层再排第三层(适用于前三层)。
部分原子的原子结构示意图
同一列的原子最外层电子数相同,
从上到下电子层数逐渐增加
同一行的原子核外电子层数相同,从左到右最外层由1逐渐递增到8
核外电子与原子性质的关系
原子最外层电子数与结构、性质的关系
原 子 最外层 电子数 原 子 结 构 变 化 趋 势 化 学
性 质
稀 有 气 体
金 属
非 金属
8个
(氦为2个 )
稳定结构
稳 定
稳 定
一般<4 个
不稳定结构
易失去电子
活 泼
一般≥4个
不稳定结构
易获得电子
活 泼
电子不仅决定原子的体积,也决定原子在化学反应中的表现
离子的形成
在化学反应中,原子核是不变的,发生改变的只是原子核外的电子。原子失去电子后变成带正电荷的阳离子,得到电子后变成带负电荷的阴离子。
由于最外层电子数为8(只有一个电子层时为2)个的结构是相对稳定结构。不具备相对稳定结构的原子有形成相对稳定结构的趋势。所以在化学反应中,原子就通过得失电子来使其达到稳定结构。
因此离子也是构成物质的一种基本粒子。原子通过得失电子后变成阴离子和阳离子,阴、阳离子通过静电作用结合成不显电性的物质。形成过程如下:
失去一个电子
得到一个电子
Na
Na+
Cl
Cl-
阴、阳离子间的静电作用
NaCl
(不显电性)
离子的概念:由原子得到或失去电子后形成的带电的原子或原子团叫作离子。
由于离子或原子的化学性质与最外层电子数有关,所以当离子或原子的最外层电子数相同时,它们的化学性质也相似。
离子的表示方法
离子符号右上角的数字表示离子所带的电荷数,正负号表示离子所带电荷的电性。
Mg2+
Cl-
Na+
O2-
镁离子
氯离子
钠离子
氧离子
每个镁离子带2个单位的正电荷
表示2个镁离子
Mg2+
2
分子物质
有些原子之间不是先转化成离子再构成物质的,而是原子之间直接结合形成分子,再由分子构成物质的。
例如,1个氢原子(H)能与1个氯原子(CI)结合,形成1个氯化氢分子(HCI),而1个氧原子(O)能与2个氢原子(H)结合,形成1个水分子(H2O)。
H2O
H2
O2
水的形成过程:
水(H2O)
O
H
H
H
H
氢原子
O
氧原子
结合
聚集
1.原子是由居于原子中心、带正电荷的原子核和核外带负电荷的电子构成的,原子不显电性。原子核所带电荷数称为核电荷数,它是由质子数决定的。
2.某原子的相对原子质量是一个该原子的质量跟一个碳-12原子质量的1/12的比值。
3.分子是由原子构成的,原子得到或失去电子后转变为离子。
原子、分子、离子都是构成物质的微观粒子。
长话短说
质子和中子还可以在分吗?
原子可以再分为质子、中子和电子,那么质子、中子和电子能否再分
1964年,科学家首次提出了夸克模型(图2-6),认为质子、中子由更小的夸克构成。这一模型的提出,成功地解释了许多事实。随着科学技术的进步,人们不仅利用大型粒子对撞机证明了夸克的存在,更发现与所有已知的质子、中子、电子等亚原子粒子不同,夸克带有分数电荷且都是两两成对或三三成群。
夸克的发现不仅刷新了人类对微观世界的认知,也再次激发了人类探索微观世界的热情。随着众多亚原子粒子不断被发现,人类逼近微观世界本质的步伐也越来越快。
图2-5 夸克模型
多识一点
1.如图为镁原子的结构示意图,下列有关镁原子的说法正确的是( )
A.镁原子的核内质子数为12
B.镁原子的核外电子数为2
C.镁原子在化学反应中易得到2个电子,形成镁离子Mg2+
D.镁原子最外电子层达到了稳定结构
A
2.下列关于粒子结构示意图的说法正确的是( )
A.第①组的原子在化学反应中都易得到电子
B.第②组的原子的化学性质相似
C.第③组原子的化学性质相似
D.第④组的粒子具有相对稳定的结构
CD
3.如图是四种粒子的结构示意图,下列有关说法不正确的是( )
A.①表示的粒子属于金属阳离子
B.③④表示的粒子化学性质相似
C.③在化学反应中易得到电子
D.原子、离子等都是构成物质的基本粒子
BC
4.通过探究物质构成的奥秘,我们了解了物质的组成与结构。
(1)物质的组成和构成关系如图所示,
图中①表示 ______,②表示 _______。
(2)电子的质量很小,可以忽略不计,
所以原子的质量主要集中在 ________上,相
对原子质量近似等于 _______与中子数之和。
(3)金属铜是由 ________(选填“原子”、
“分子”或“离子”)构成的。
质子
离子
原子核
质子数
原子
5.如下图所示,分别是钾元素、氢元素、氧元素、钠元素的原子结构示意图。
(1)A 中 X 的值为_________;
(2)A、D 化学性质相似的原因是___________________;
(3)B 形成的离子符号为____________;
(4)根据上图信息分析,1 个氢氧根离子
中含有的电子数是_______。
19
最外层电子数相同
H+
10
同课章节目录
