2.2 元素 课件(共27张PPT) 2025-2026学年化学鲁教版(2024)九年级上册
文档属性
| 名称 | 2.2 元素 课件(共27张PPT) 2025-2026学年化学鲁教版(2024)九年级上册 |
|
|
| 格式 | pptx | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-07 00:00:00 | ||
图片预览







文档简介
(共27张PPT)
了解元素的概念,初步学会用元素描述物质的宏观组成
学会正确书写元素符号,记住一些常见的元素符号。认识并学会运用元素周期表
通过对纯净物和元素的分类,进一步体会分类的思想,学习分类的方法
01
02
03
山林川原、河池泉井、日月生辉、电闪雷鸣……我们所处的世界丰富多彩。然而,尽管外表形形色色,变化无穷,但其内部的一切物质都含有相同的最简单的组成部分——元素。
我们要进一步学习化学,还得从构成世界万物最基本的元素开始。
元素与元素符号概念
在我们的先人在战国时期就提出了“金、木、水、火、土”是组成世界万物的亘古不变的基本成分——元素。
小明认为“所有的物质都是由原子、分子、离子等基本粒子构成的,这些基本粒子才是组成物质的元素”。
小丽认为“分子在化学变化中可以再分,是容易变的;而原子是不变的,并且分子是由原子构成的,离子是由原子得失电子后形成的,所以原子才是组成世界万物的元素”。
请提出你的观点。
一、元素与元素符号
交流共享
8
8
8
8
8
8
8
1
1
1
1
1
1
1
1
1
1
6
6
6
6
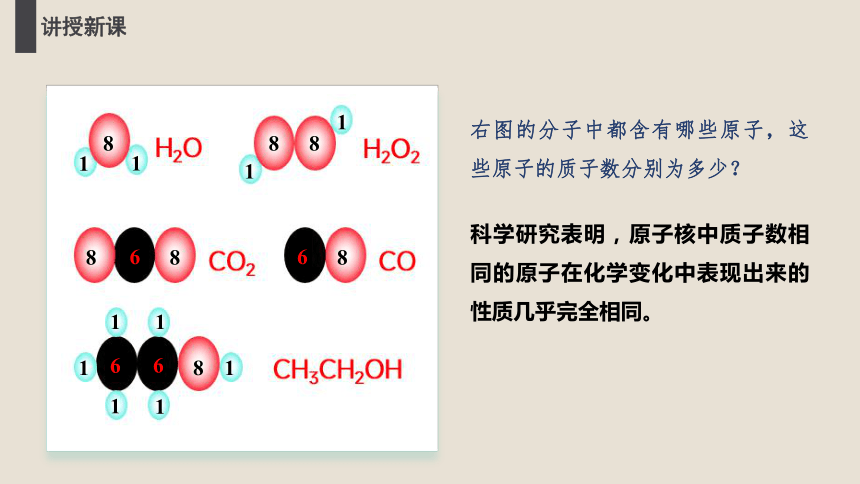
右图的分子中都含有哪些原子,这些原子的质子数分别为多少?
科学研究表明,原子核中质子数相同的原子在化学变化中表现出来的性质几乎完全相同。
科学家把具有相同质子数的原子归为一类,每一类原子称为一种元素。
质子数为1的一类原子称为氢元素;质子数为6的一类原子称为碳元素;
世界上确认的元素有118种,其中有92种为自然界中发现,有26种为人工合成。人工合成的元素主要采取做加法的方式,就是将两个质量相对较小的原子核,通过高速撞击聚变成更重的元素。人造元素并非在自然界不存在,
而是由于这些元素原子衰变太快,或者自然界太稀有,难以在自然界得到而已。
【问题】:什么是氧元素?
+11
2
8
1
Na
+11
2
8
Na
+
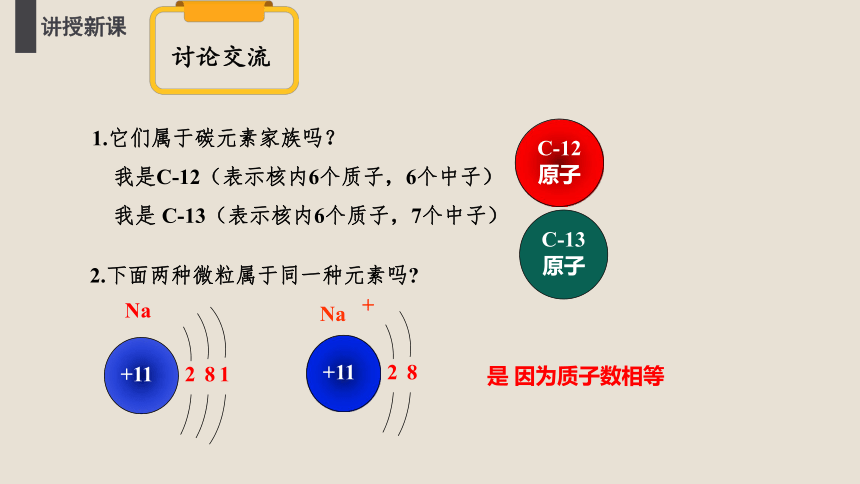
2.下面两种微粒属于同一种元素吗
C-13
原子
C-12
原子
是 因为质子数相等
讨论交流
1.它们属于碳元素家族吗?
我是C-12(表示核内6个质子,6个中子)
我是 C-13(表示核内6个质子,7个中子)
元素与原子的区别和联系
元素 原子
含义 质子数(即核电荷数)相同的一类原子的总称 化学变化中的最小粒子
区别 只讲种类,不讲个数 既讲种类,又讲个数
适用 范围 用于描述物质的宏观组成 用于描述分子或某些微粒的微观构成
联系 元素和原子是总体和个体的关系,元素是一类原子的总称 物质的宏观组成与微观构成
1.物质宏观组成的描述:物质名称+元素+组成
2.物质微观构成的描述:(1个)物质的分子+( ×个)原子+构成
例如:水是由氢元素和氧元素组成的;
水分子是由氢原子和氧原子构成的;
1个水分子是由2个氢原子和1个氧原子构成的。
以二氧化碳为例进行物质的描述?
宏观 宏观
微观 微观
个数 个数
元素在自然界中的分布并不均匀,按质量计算,地壳中含量最多的是氧元素,其他元素含量由高到低依次是硅、铝、铁、钙等。
单质与化合物
目前已发现的物质有上亿种,这上亿种物质分为混合物和纯净物两种。再根据组成物质的元素种类的多少,又把纯净物分为单质和化合物。
只由一种元素组成的纯净物叫做单质。
由两种或两种以上元素组成的纯净物叫做化合物。
比如氢气、氧气、金刚石等。
比如二氧化碳、氯化钠、水等。
单质与化合物的区别于联系:
单质 化合物
区别 概念 只由一种元素组成的纯净物 由两种或两种以上元素组成的纯净物
宏观组成 一种元素 两种或两种以上元素
微观构成 同种原子或由同种原子构成的同种分子 不同种原子构成的同种分子或不同种离子
联系 都是纯净物;单质与单质发生化合反应可以生成化合物,化合物发生分解反应可以生成单质 单质
混合物
化合物
微观探索
针对练习:下图中“ ”和“O” “ ” 分别表示不同元素的原子。
(1)表示混合物的有 (填序号,下同);
(2)表示单质的有 ,可以表示化合物的有 。
B
AD
C
为方便区分和交流,国际上规定每种元素都采用统一的符号来表示,这种符号叫作元素符号。
元素符号采用元素拉丁文名称的第一个字母来表示元素;当几种元素的拉丁文名称第一个字母相同时,就附加一个小写字母。第一个字母要大写,第二个字母要小写。
元素符号的书写
元素符号的书写
【记忆大比拼】
①按顺序背诵并能够默写出元素名称以及对应元素符号;
②其他常见元素符号熟记会默写。
①表示一种元素(宏观)
②表示该元素的一个原子(微观)
③表示一种物质(宏观,由原子直接构成的三类物质)
元素符号的书写
H
①氢元素
②一个氢原子
Fe
①铁元素
②一个铁原子
③铁
C
你知道“3H”、“5C”“7Na”、“10Mg”分别表示什么意思吗?
3个氢
原子
5个碳
原子
7个钠
原子
10个镁
原子
注意:元素符号前面加上数字,只表示微观含义,即表示原子的个数;
例如 2H 表示 。
两个氢原子
思维拓展
如:氦、氖、氩等
③稀有气体元素:“气”字头
①金属元素:“钅”字旁(汞除外)
如:铁、铜等
固态非金属元素(“石”字旁)
气态非金属元素(“气”字头)
非金属元素
②
如:碳、碘等
如:氢、氧等
元素的分类
元素周期表的结构与规律
自然界中的物质是由多种元素组成的,这些元素彼此是否有联系?有没有规律可循?在原子结构被发现之前,科学家们就已经对此进行了长期的探索。
把元素按照相对原子质量由小到大的顺序排列起来,并分成几行,使性质相似的元素排在同一列中,从而得到第一张元素周期表。
二、元素周期表
现代化学的元素周期律是1869年俄国科学家
门捷列夫(D.Mendeleev,1834-1907)在前人
研究的基础上,把当时已知的63种元素按照
相对原子质量由小到大的顺序排列起来,并
分成几行,使性质相似的元素排在同一列中,
制成元素周期表的雏形。经过多年修订后才成为如今的周期表。
目前正式命名的有118种元素,按质子数由小到大的顺序排列。
元素周期表的发展历程
原子序数
相对原子质量
元素符号
元素
名称
1 H
氢
1.008
元素周期表的结构
元素周期表中每种元素都有一个序号,称为原子序数。它的数值等于其原子核内质子数。
(1)周期表每一横行叫做一个周期,共有7个周期。(各周期电子层数相同,核电荷数逐渐增加)
(2)周期表每一个纵行叫做
一族,共有16个族(8、9、
10三个纵行共同组成一个族)。
(各族最外层电子数相同,电子
层数逐渐增加,化学性质相似)
元素所在的周期数等于原子的核外电子层数
原子序数=核内质子数=核电荷数=核外电子数
元素周期表的规律:
(1)同周期元素原子电子层数相同,且周期数=电子层数。同主族元素的最外层电子数相同,且主族序数=最外层电子数
(2)同周期元素从左到右,核电荷数逐渐增大(原子序数=核电荷数=核内质子数=核外电子数)。原子最外层电子数逐渐增多。同周期的元素从金属元素开始,逐渐过渡到非金属元素,最后以稀有气体元素结束。
(3)同族元素原子电子层数从上到下逐渐增多,原子半径逐渐增大。最外层电子数相同,化学性质相似。
1.元素是组成物质的基本成分,人们把质子数相同的一类原子称为一种元素。国际上通常采用元素符号表示每一种元素。
2.只由一种元素组成的纯净物属于单质,由两种或两种以上的元素组成的纯净物属于化合物。
3.元素周期表是学习和研究化学的重要工具。。
长话短说
1.生活中的“加碘盐”“含氟牙膏”,“加铁酱油”,其中的“碘”“氟”“铁”指的是( )
A.原子 B.离子 C.元素 D.分子
C
2.我国著名化学家张青莲为相对原子质量测定作出了卓越贡献。如图是元素周期表的一部分。下列说法正确的是( )
A.两种元素都属于非金属元素
B.锑原子的核内质子数为51
C.锑元素的相对原子质量是121.8g
D.锑原子质量比铟原子的质量小
B
3.如图是几种元素的粒子结构示意图及元素周期表的一部分。
(1)2021年2月27日,嫦娥五号采集的月壤样品在中国国家博物馆正式展出。月壤中存在着大量的氦-3(氦-3是含有2个质子和1个中子的氦原子),其原子结构示意图为图甲中的 (填序号)相对原子质量是 。A-E中位于同一主族的是 。
(2)硒是人体必需微量元素,具有防癌、抗癌作用,其原子结构示意图如图甲中的E,该元素处于元素周期表中第 周期,它与图乙中 (填元素名称)的化学性质相似.
A
3
CE
4或四
氧元素
了解元素的概念,初步学会用元素描述物质的宏观组成
学会正确书写元素符号,记住一些常见的元素符号。认识并学会运用元素周期表
通过对纯净物和元素的分类,进一步体会分类的思想,学习分类的方法
01
02
03
山林川原、河池泉井、日月生辉、电闪雷鸣……我们所处的世界丰富多彩。然而,尽管外表形形色色,变化无穷,但其内部的一切物质都含有相同的最简单的组成部分——元素。
我们要进一步学习化学,还得从构成世界万物最基本的元素开始。
元素与元素符号概念
在我们的先人在战国时期就提出了“金、木、水、火、土”是组成世界万物的亘古不变的基本成分——元素。
小明认为“所有的物质都是由原子、分子、离子等基本粒子构成的,这些基本粒子才是组成物质的元素”。
小丽认为“分子在化学变化中可以再分,是容易变的;而原子是不变的,并且分子是由原子构成的,离子是由原子得失电子后形成的,所以原子才是组成世界万物的元素”。
请提出你的观点。
一、元素与元素符号
交流共享
8
8
8
8
8
8
8
1
1
1
1
1
1
1
1
1
1
6
6
6
6
右图的分子中都含有哪些原子,这些原子的质子数分别为多少?
科学研究表明,原子核中质子数相同的原子在化学变化中表现出来的性质几乎完全相同。
科学家把具有相同质子数的原子归为一类,每一类原子称为一种元素。
质子数为1的一类原子称为氢元素;质子数为6的一类原子称为碳元素;
世界上确认的元素有118种,其中有92种为自然界中发现,有26种为人工合成。人工合成的元素主要采取做加法的方式,就是将两个质量相对较小的原子核,通过高速撞击聚变成更重的元素。人造元素并非在自然界不存在,
而是由于这些元素原子衰变太快,或者自然界太稀有,难以在自然界得到而已。
【问题】:什么是氧元素?
+11
2
8
1
Na
+11
2
8
Na
+
2.下面两种微粒属于同一种元素吗
C-13
原子
C-12
原子
是 因为质子数相等
讨论交流
1.它们属于碳元素家族吗?
我是C-12(表示核内6个质子,6个中子)
我是 C-13(表示核内6个质子,7个中子)
元素与原子的区别和联系
元素 原子
含义 质子数(即核电荷数)相同的一类原子的总称 化学变化中的最小粒子
区别 只讲种类,不讲个数 既讲种类,又讲个数
适用 范围 用于描述物质的宏观组成 用于描述分子或某些微粒的微观构成
联系 元素和原子是总体和个体的关系,元素是一类原子的总称 物质的宏观组成与微观构成
1.物质宏观组成的描述:物质名称+元素+组成
2.物质微观构成的描述:(1个)物质的分子+( ×个)原子+构成
例如:水是由氢元素和氧元素组成的;
水分子是由氢原子和氧原子构成的;
1个水分子是由2个氢原子和1个氧原子构成的。
以二氧化碳为例进行物质的描述?
宏观 宏观
微观 微观
个数 个数
元素在自然界中的分布并不均匀,按质量计算,地壳中含量最多的是氧元素,其他元素含量由高到低依次是硅、铝、铁、钙等。
单质与化合物
目前已发现的物质有上亿种,这上亿种物质分为混合物和纯净物两种。再根据组成物质的元素种类的多少,又把纯净物分为单质和化合物。
只由一种元素组成的纯净物叫做单质。
由两种或两种以上元素组成的纯净物叫做化合物。
比如氢气、氧气、金刚石等。
比如二氧化碳、氯化钠、水等。
单质与化合物的区别于联系:
单质 化合物
区别 概念 只由一种元素组成的纯净物 由两种或两种以上元素组成的纯净物
宏观组成 一种元素 两种或两种以上元素
微观构成 同种原子或由同种原子构成的同种分子 不同种原子构成的同种分子或不同种离子
联系 都是纯净物;单质与单质发生化合反应可以生成化合物,化合物发生分解反应可以生成单质 单质
混合物
化合物
微观探索
针对练习:下图中“ ”和“O” “ ” 分别表示不同元素的原子。
(1)表示混合物的有 (填序号,下同);
(2)表示单质的有 ,可以表示化合物的有 。
B
AD
C
为方便区分和交流,国际上规定每种元素都采用统一的符号来表示,这种符号叫作元素符号。
元素符号采用元素拉丁文名称的第一个字母来表示元素;当几种元素的拉丁文名称第一个字母相同时,就附加一个小写字母。第一个字母要大写,第二个字母要小写。
元素符号的书写
元素符号的书写
【记忆大比拼】
①按顺序背诵并能够默写出元素名称以及对应元素符号;
②其他常见元素符号熟记会默写。
①表示一种元素(宏观)
②表示该元素的一个原子(微观)
③表示一种物质(宏观,由原子直接构成的三类物质)
元素符号的书写
H
①氢元素
②一个氢原子
Fe
①铁元素
②一个铁原子
③铁
C
你知道“3H”、“5C”“7Na”、“10Mg”分别表示什么意思吗?
3个氢
原子
5个碳
原子
7个钠
原子
10个镁
原子
注意:元素符号前面加上数字,只表示微观含义,即表示原子的个数;
例如 2H 表示 。
两个氢原子
思维拓展
如:氦、氖、氩等
③稀有气体元素:“气”字头
①金属元素:“钅”字旁(汞除外)
如:铁、铜等
固态非金属元素(“石”字旁)
气态非金属元素(“气”字头)
非金属元素
②
如:碳、碘等
如:氢、氧等
元素的分类
元素周期表的结构与规律
自然界中的物质是由多种元素组成的,这些元素彼此是否有联系?有没有规律可循?在原子结构被发现之前,科学家们就已经对此进行了长期的探索。
把元素按照相对原子质量由小到大的顺序排列起来,并分成几行,使性质相似的元素排在同一列中,从而得到第一张元素周期表。
二、元素周期表
现代化学的元素周期律是1869年俄国科学家
门捷列夫(D.Mendeleev,1834-1907)在前人
研究的基础上,把当时已知的63种元素按照
相对原子质量由小到大的顺序排列起来,并
分成几行,使性质相似的元素排在同一列中,
制成元素周期表的雏形。经过多年修订后才成为如今的周期表。
目前正式命名的有118种元素,按质子数由小到大的顺序排列。
元素周期表的发展历程
原子序数
相对原子质量
元素符号
元素
名称
1 H
氢
1.008
元素周期表的结构
元素周期表中每种元素都有一个序号,称为原子序数。它的数值等于其原子核内质子数。
(1)周期表每一横行叫做一个周期,共有7个周期。(各周期电子层数相同,核电荷数逐渐增加)
(2)周期表每一个纵行叫做
一族,共有16个族(8、9、
10三个纵行共同组成一个族)。
(各族最外层电子数相同,电子
层数逐渐增加,化学性质相似)
元素所在的周期数等于原子的核外电子层数
原子序数=核内质子数=核电荷数=核外电子数
元素周期表的规律:
(1)同周期元素原子电子层数相同,且周期数=电子层数。同主族元素的最外层电子数相同,且主族序数=最外层电子数
(2)同周期元素从左到右,核电荷数逐渐增大(原子序数=核电荷数=核内质子数=核外电子数)。原子最外层电子数逐渐增多。同周期的元素从金属元素开始,逐渐过渡到非金属元素,最后以稀有气体元素结束。
(3)同族元素原子电子层数从上到下逐渐增多,原子半径逐渐增大。最外层电子数相同,化学性质相似。
1.元素是组成物质的基本成分,人们把质子数相同的一类原子称为一种元素。国际上通常采用元素符号表示每一种元素。
2.只由一种元素组成的纯净物属于单质,由两种或两种以上的元素组成的纯净物属于化合物。
3.元素周期表是学习和研究化学的重要工具。。
长话短说
1.生活中的“加碘盐”“含氟牙膏”,“加铁酱油”,其中的“碘”“氟”“铁”指的是( )
A.原子 B.离子 C.元素 D.分子
C
2.我国著名化学家张青莲为相对原子质量测定作出了卓越贡献。如图是元素周期表的一部分。下列说法正确的是( )
A.两种元素都属于非金属元素
B.锑原子的核内质子数为51
C.锑元素的相对原子质量是121.8g
D.锑原子质量比铟原子的质量小
B
3.如图是几种元素的粒子结构示意图及元素周期表的一部分。
(1)2021年2月27日,嫦娥五号采集的月壤样品在中国国家博物馆正式展出。月壤中存在着大量的氦-3(氦-3是含有2个质子和1个中子的氦原子),其原子结构示意图为图甲中的 (填序号)相对原子质量是 。A-E中位于同一主族的是 。
(2)硒是人体必需微量元素,具有防癌、抗癌作用,其原子结构示意图如图甲中的E,该元素处于元素周期表中第 周期,它与图乙中 (填元素名称)的化学性质相似.
A
3
CE
4或四
氧元素
同课章节目录
