内蒙古部分学校2024-2025学年高一下学期7月期末联考化学试卷 (含答案)
文档属性
| 名称 | 内蒙古部分学校2024-2025学年高一下学期7月期末联考化学试卷 (含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 999.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-08 00:00:00 | ||
图片预览



文档简介
内蒙古部分学校2024-2025学年高一下学期7月联考化学试卷
一、单选题
1.文物承载中华文明。下列文物的主要成分是金属的是
选项 A.商代后母戊鼎 B.汉代石雕 C.唐三彩 D.东晋《兰亭集序》
文物
A.A B.B C.C D.D
2.古籍中记载着大量有机物。下列记载的有机物分类正确的是
A.《天工开物》——“蜜”(果糖)——二糖
B.《本草纲目》——“酒”(乙醇)——醇类
C.《齐民要术》——“醋”(乙酸)——醛类
D.《神农本草经》——“脂”(硬脂酸甘油酯)——酸类
3.能源是社会发展的动力。下列关于能源的说法正确的是
A.煤炭是可再生能源,燃烧不会污染环境
B.氢能燃烧产物无污染,但现阶段制取成本高
C.核能属于二次能源,不会产生污染物
D.太阳能是不可再生能源,能量密度高,稳定
4.下列叙述正确的是
A.向某溶液中先加稀盐酸酸化,再滴加溶液,若产生白色沉淀,则证明原溶液含
B.向含乙酸的乙酸乙酯中加入NaOH溶液,分液得到纯净的乙酸乙酯
C.用稀盐酸洗涤银镜反应后的试管,因为稀盐酸能溶解单质银,生成可溶性银盐
D.除去溶液中的,可向溶液中加入足量的铁粉,过滤
5.豆腐是利用盐卤(含氯化镁、硫酸钙)或葡萄糖酸--内酯(结构简式如图所示)等物质将豆浆中的蛋白质聚沉而制成的。下列说法错误的是
A.固体不导电,但为电解质
B.葡萄糖酸--内酯可与热的氢氧化钠溶液反应
C.将金属钠投入氯化镁溶液中,可获得金属镁
D.葡萄糖酸--内酯中碳元素的质量分数最大
6.下列关于化学反应中能量变化的说法错误的是
A.释放热量的化学反应为放热反应
B.反应物的总键能比生成物的总键能大的反应为吸热反应
C.反应物的总能量比生成物的总能量低的反应为吸热反应
D.需要加热才能发生的反应均为吸热反应,常温下能自发进行的反应均为放热反应
7.材料是社会进步的阶梯。下列关于高分子材料的说法正确的是
A.航天服使用的聚酰胺纤维、聚丙烯腈纤维都是天然高分子材料
B.聚乙烯是天然高分子材料,由乙烯通过加聚反应制得,常用于制作食品包装袋
C.棉花、羊毛和蚕丝的主要成分均为天然高分子材料,其中棉花的主要成分是纤维素
D.聚氯乙烯(PVC)的单体是,因其无毒且化学性质稳定,可制作保鲜膜
8.《政府工作报告》明确提出“加强污染防治和生态建设”“加快发展绿色低碳经济”“积极稳妥推进碳达峰碳中和”。下列做法与报告内容相符的是
A.露天焚烧垃圾,快速处理废弃物
B.大量使用一次性塑料餐具,方便生活
C.工厂废水直接排放到河流中,节省处理成本
D.用自行车或公共交通代替私家车出行,减少尾气排放
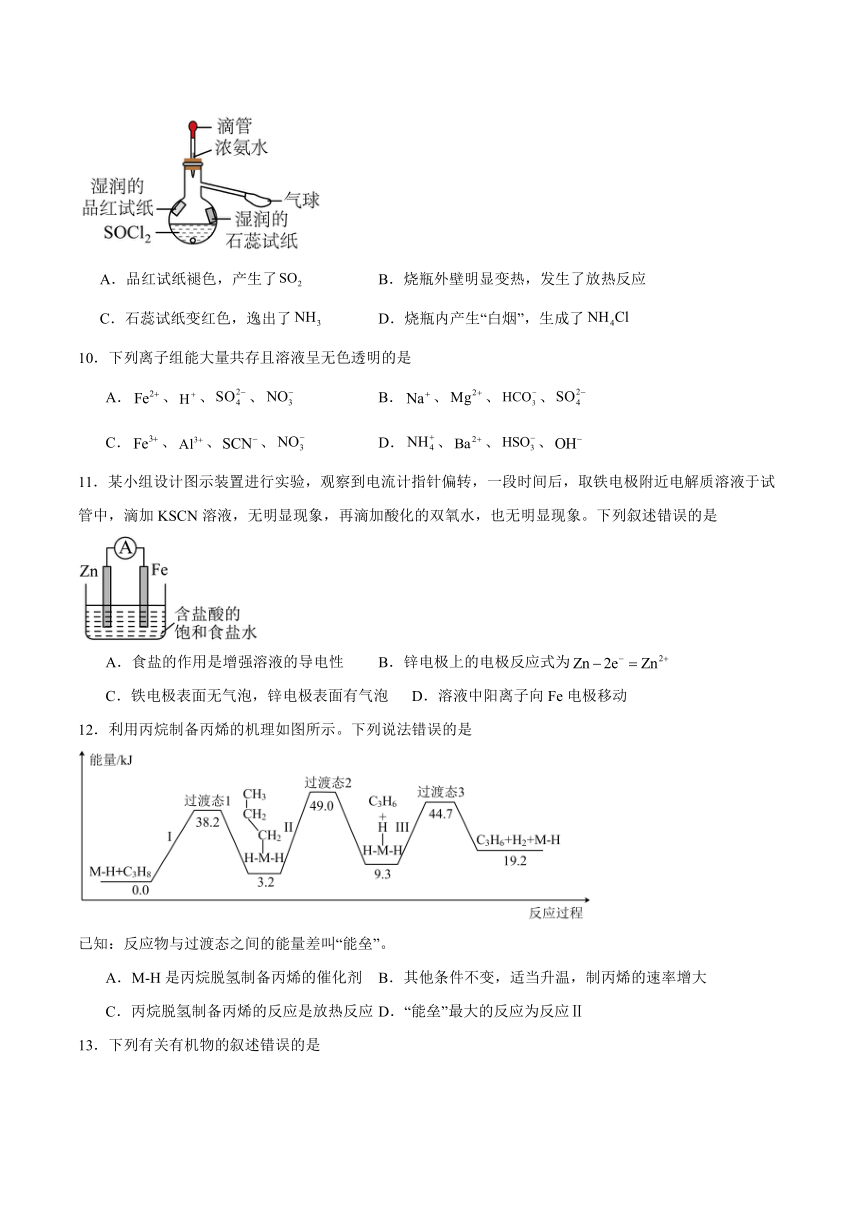
9.某实验小组设计如图装置进行实验,先在烧瓶中盛装适量,再向其中滴加浓氨水(氨水溶解的热效应很小,可忽略不计),根据现象预测的结论错误的是
A.品红试纸褪色,产生了 B.烧瓶外壁明显变热,发生了放热反应
C.石蕊试纸变红色,逸出了 D.烧瓶内产生“白烟”,生成了
10.下列离子组能大量共存且溶液呈无色透明的是
A.、、、 B.、、、
C.、、、 D.、、、
11.某小组设计图示装置进行实验,观察到电流计指针偏转,一段时间后,取铁电极附近电解质溶液于试管中,滴加KSCN溶液,无明显现象,再滴加酸化的双氧水,也无明显现象。下列叙述错误的是
A.食盐的作用是增强溶液的导电性 B.锌电极上的电极反应式为
C.铁电极表面无气泡,锌电极表面有气泡 D.溶液中阳离子向Fe电极移动
12.利用丙烷制备丙烯的机理如图所示。下列说法错误的是
已知:反应物与过渡态之间的能量差叫“能垒”。
A.M-H是丙烷脱氢制备丙烯的催化剂 B.其他条件不变,适当升温,制丙烯的速率增大
C.丙烷脱氢制备丙烯的反应是放热反应 D.“能垒”最大的反应为反应Ⅱ
13.下列有关有机物的叙述错误的是
A.和互为同分异构体
B.和均能与NaOH溶液反应
C.和均属于醇
D.和为同一种物质
14.根据下列实验操作及现象,得出的结论合理的是
选项 操作及现象 结论
A 将NaOH溶液与盐酸混合,触摸试管外壁感觉发热 该反应为放热反应
B 向乙醇中加入一小块钠,产生无色气泡 乙醇属于酸
C 在溶液中滴加KOH溶液,产生红褐色沉淀 与发生了氧化还原反应
D 在铜和稀硫酸的混合物中加入少量,产生气泡 作催化剂
A.A B.B C.C D.D
二、多选题
15.汽车尾气处理装置是现代车辆减少有害气体排放的关键系统,主要通过催化化学反应将尾气中的NO和CO污染物转化为无害物质。几种共价键的键能数据如下:
化学键
键能 630 1076 945 799
下列推断正确的是
A.加入催化剂,能增大正反应速率,也同时增大逆反应速率
B.上述反应的正反应是气体分子数减小的反应,也是吸热反应
C.物质的化学键键能越大,该物质就越不易发生化学反应
D.每生成,放出的热量为
三、解答题
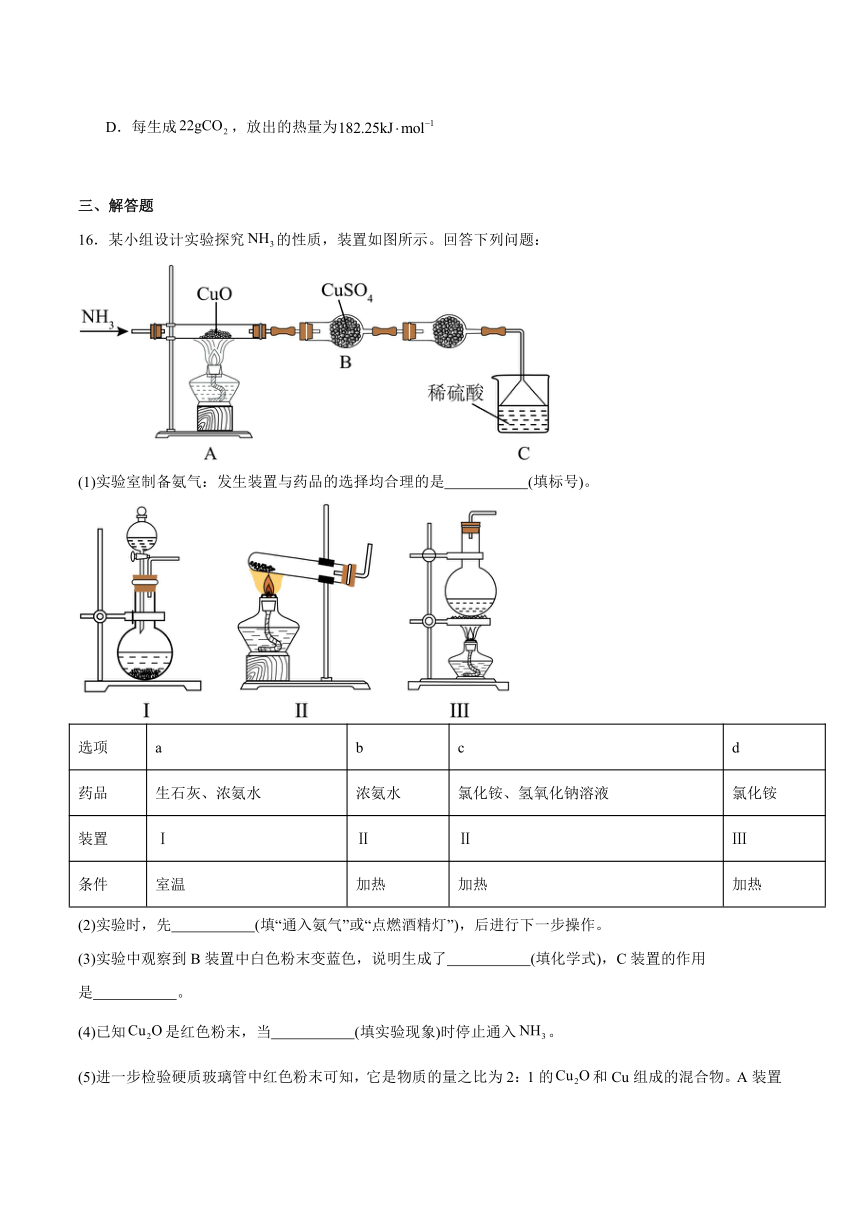
16.某小组设计实验探究的性质,装置如图所示。回答下列问题:
(1)实验室制备氨气:发生装置与药品的选择均合理的是 (填标号)。
选项 a b c d
药品 生石灰、浓氨水 浓氨水 氯化铵、氢氧化钠溶液 氯化铵
装置 Ⅰ Ⅱ Ⅱ Ⅲ
条件 室温 加热 加热 加热
(2)实验时,先 (填“通入氨气”或“点燃酒精灯”),后进行下一步操作。
(3)实验中观察到B装置中白色粉末变蓝色,说明生成了 (填化学式),C装置的作用是 。
(4)已知是红色粉末,当 (填实验现象)时停止通入。
(5)进一步检验硬质玻璃管中红色粉末可知,它是物质的量之比为2:1的和Cu组成的混合物。A装置硬质玻璃管中反应的另一种产物为气体单质,硬质玻璃管中的总反应方程式为 。
(6)收集两瓶干燥的氨气,进行喷泉实验:
利用D装置引发 色喷泉,其原理是 ;受D装置启发,小组创新设计E装置,引发E装置喷泉的操作是 。
17.硫代硫酸钠()常作氰化物中毒的解毒剂及照相行业中的定影剂。某小组以硫酸厂排放的尾气为原料制备硫代硫酸钠,工艺流程如图所示。回答下列问题:
已知:
①制备原理:。
②和的溶解度均随温度的升高显著增大,在48℃时开始分解。
③产品在酸性条件下不稳定:。
④碘量法测定样品纯度原理:。
(1)“碱吸”时,加入过量的NaOH溶液的目的是 。
(2)“趁热过滤”主要是除去 ,相比常温过滤,“趁热过滤”的优点是 。
(3)调节“溶液”pH时,若不小心加入了过量的稀硫酸,产生的后果是 。
(4)“系列操作”包括蒸发浓缩、 、过滤、洗涤、低温(<48℃)干燥,若干燥时温度过高,产生的后果是 。
(5)硫代硫酸钠在医疗领域常作氰化物中毒的解毒剂。已知和KCN反应生成两种正盐,将产物分两份:一份滴加溶液,溶液变红色;另一份滴加盐酸,将产生的气体通入品红溶液中,溶液褪色。和KCN反应的离子方程式为 。
(6)测定产品的纯度:取产品溶于蒸馏水配制成250mL溶液,取25.00mL配制的溶液于锥形瓶中,加入碘()水至恰好完全反应时消耗碘水,则该产品中的质量分数为 %。
18.《周礼》一书,有“醯人掌共五齐七菹”的记载,醯人是周王室掌管五齐、七菹的官员,从侧面反映出醋在当时帝王饮食生活中的重要地位。以玉米等粮食为原料模拟民间酿醋(F)的主要原理设计如下流程。回答下列问题:
(1)“粉碎”的目的是 。
(2)B的名称是 。
(3)写出C生成D的化学方程式: 。
(4)在新制中加入适量E共热,观察到的实验现象是 。E的环状同分异构体为 (填结构简式)。
(5)醋能提升菜肴风味,是因为生成了G,F与D生成G的反应类型是 。
(6)已知等量X分别与足量Na、反应产生和的体积比为1:1(同温同压),X分子含甲基,则X的结构简式为 ,含有的官能团有 (填名称)。
四、填空题
19.甲醇()被誉为“液态阳光”,以甲醇为载体,将间歇性可再生能源(太阳能、风能)转化为稳定、可运输的化学能,从而解决清洁能源存储与时空分布不均的难题。回答下列问题:反应原理:
ⅰ.;
ⅱ.(g代表气态)。
(1)下列图像能正确表示反应ⅰ中能量变化的是 (填标号)。
A. B.
(2)300℃时,向恒容密闭容器中充入1molCO2和仅发生反应ⅱ,下列情况能说明该反应达到平衡状态的是___________(填标号)。
A.气体密度不随时间变化 B.气体总压强不随时间变化
C.的体积分数不随时间变化 D.体系中H原子数目不随时间变化
(3)在体积可变的密闭反应器中充入适量的和,仅发生反应ⅱ,下列措施不能增大合成反应速率的是___________(填标号)。
A.增大压强 B.降低温度 C.加入催化剂 D.增大浓度
(4)250℃、条件下,向2L密闭容器中充入和,在催化剂作用下只发生反应ⅱ,测得、和的物质的量(n)与时间(t)的关系如图。
①甲代表 (填化学式), 。
②平衡时的体积分数为 (保留两位有效数字)。
(5)甲醇-空气碱性(如KOH作为电解质)燃料电池放电效率较高,在 (填“正”或“负”)极区充入空气,负极的电极反应式为 (氧化产物为)。
题号 1 2 3 4 5 6 7 8 9 10
答案 A B B D C D C D C B
题号 11 12 13 14 15
答案 C C A A AC
16.(1)a
(2)通入氨气
(3) 吸收尾气中的,防止污染环境
(4)A中黑色粉末全部变为红色粉末
(5)
(6) 红或粉红 氨气极易溶于水,烧瓶内外形成较大压强差,外压将水快速压入烧瓶中 打开止水夹K,用热毛巾捂烧瓶,当与水接触后快速移开毛巾
17.(1)将全部转化成
(2) 硫 避免硫代硫酸钠析出,减少产品损失
(3)与稀硫酸发生反应,降低产率
(4) 降温结晶 产品失去结晶水
(5)
(6)
18.(1)增大固体接触面积,提高反应速率
(2)麦芽榶
(3)
(4) 产生砖红色沉淀
(5)取代反应或酯化反应
(6) 羧基、羟基
19.(1)A
(2)BC
(3)B
(4) 0.76 6.8
(5) 正
一、单选题
1.文物承载中华文明。下列文物的主要成分是金属的是
选项 A.商代后母戊鼎 B.汉代石雕 C.唐三彩 D.东晋《兰亭集序》
文物
A.A B.B C.C D.D
2.古籍中记载着大量有机物。下列记载的有机物分类正确的是
A.《天工开物》——“蜜”(果糖)——二糖
B.《本草纲目》——“酒”(乙醇)——醇类
C.《齐民要术》——“醋”(乙酸)——醛类
D.《神农本草经》——“脂”(硬脂酸甘油酯)——酸类
3.能源是社会发展的动力。下列关于能源的说法正确的是
A.煤炭是可再生能源,燃烧不会污染环境
B.氢能燃烧产物无污染,但现阶段制取成本高
C.核能属于二次能源,不会产生污染物
D.太阳能是不可再生能源,能量密度高,稳定
4.下列叙述正确的是
A.向某溶液中先加稀盐酸酸化,再滴加溶液,若产生白色沉淀,则证明原溶液含
B.向含乙酸的乙酸乙酯中加入NaOH溶液,分液得到纯净的乙酸乙酯
C.用稀盐酸洗涤银镜反应后的试管,因为稀盐酸能溶解单质银,生成可溶性银盐
D.除去溶液中的,可向溶液中加入足量的铁粉,过滤
5.豆腐是利用盐卤(含氯化镁、硫酸钙)或葡萄糖酸--内酯(结构简式如图所示)等物质将豆浆中的蛋白质聚沉而制成的。下列说法错误的是
A.固体不导电,但为电解质
B.葡萄糖酸--内酯可与热的氢氧化钠溶液反应
C.将金属钠投入氯化镁溶液中,可获得金属镁
D.葡萄糖酸--内酯中碳元素的质量分数最大
6.下列关于化学反应中能量变化的说法错误的是
A.释放热量的化学反应为放热反应
B.反应物的总键能比生成物的总键能大的反应为吸热反应
C.反应物的总能量比生成物的总能量低的反应为吸热反应
D.需要加热才能发生的反应均为吸热反应,常温下能自发进行的反应均为放热反应
7.材料是社会进步的阶梯。下列关于高分子材料的说法正确的是
A.航天服使用的聚酰胺纤维、聚丙烯腈纤维都是天然高分子材料
B.聚乙烯是天然高分子材料,由乙烯通过加聚反应制得,常用于制作食品包装袋
C.棉花、羊毛和蚕丝的主要成分均为天然高分子材料,其中棉花的主要成分是纤维素
D.聚氯乙烯(PVC)的单体是,因其无毒且化学性质稳定,可制作保鲜膜
8.《政府工作报告》明确提出“加强污染防治和生态建设”“加快发展绿色低碳经济”“积极稳妥推进碳达峰碳中和”。下列做法与报告内容相符的是
A.露天焚烧垃圾,快速处理废弃物
B.大量使用一次性塑料餐具,方便生活
C.工厂废水直接排放到河流中,节省处理成本
D.用自行车或公共交通代替私家车出行,减少尾气排放
9.某实验小组设计如图装置进行实验,先在烧瓶中盛装适量,再向其中滴加浓氨水(氨水溶解的热效应很小,可忽略不计),根据现象预测的结论错误的是
A.品红试纸褪色,产生了 B.烧瓶外壁明显变热,发生了放热反应
C.石蕊试纸变红色,逸出了 D.烧瓶内产生“白烟”,生成了
10.下列离子组能大量共存且溶液呈无色透明的是
A.、、、 B.、、、
C.、、、 D.、、、
11.某小组设计图示装置进行实验,观察到电流计指针偏转,一段时间后,取铁电极附近电解质溶液于试管中,滴加KSCN溶液,无明显现象,再滴加酸化的双氧水,也无明显现象。下列叙述错误的是
A.食盐的作用是增强溶液的导电性 B.锌电极上的电极反应式为
C.铁电极表面无气泡,锌电极表面有气泡 D.溶液中阳离子向Fe电极移动
12.利用丙烷制备丙烯的机理如图所示。下列说法错误的是
已知:反应物与过渡态之间的能量差叫“能垒”。
A.M-H是丙烷脱氢制备丙烯的催化剂 B.其他条件不变,适当升温,制丙烯的速率增大
C.丙烷脱氢制备丙烯的反应是放热反应 D.“能垒”最大的反应为反应Ⅱ
13.下列有关有机物的叙述错误的是
A.和互为同分异构体
B.和均能与NaOH溶液反应
C.和均属于醇
D.和为同一种物质
14.根据下列实验操作及现象,得出的结论合理的是
选项 操作及现象 结论
A 将NaOH溶液与盐酸混合,触摸试管外壁感觉发热 该反应为放热反应
B 向乙醇中加入一小块钠,产生无色气泡 乙醇属于酸
C 在溶液中滴加KOH溶液,产生红褐色沉淀 与发生了氧化还原反应
D 在铜和稀硫酸的混合物中加入少量,产生气泡 作催化剂
A.A B.B C.C D.D
二、多选题
15.汽车尾气处理装置是现代车辆减少有害气体排放的关键系统,主要通过催化化学反应将尾气中的NO和CO污染物转化为无害物质。几种共价键的键能数据如下:
化学键
键能 630 1076 945 799
下列推断正确的是
A.加入催化剂,能增大正反应速率,也同时增大逆反应速率
B.上述反应的正反应是气体分子数减小的反应,也是吸热反应
C.物质的化学键键能越大,该物质就越不易发生化学反应
D.每生成,放出的热量为
三、解答题
16.某小组设计实验探究的性质,装置如图所示。回答下列问题:
(1)实验室制备氨气:发生装置与药品的选择均合理的是 (填标号)。
选项 a b c d
药品 生石灰、浓氨水 浓氨水 氯化铵、氢氧化钠溶液 氯化铵
装置 Ⅰ Ⅱ Ⅱ Ⅲ
条件 室温 加热 加热 加热
(2)实验时,先 (填“通入氨气”或“点燃酒精灯”),后进行下一步操作。
(3)实验中观察到B装置中白色粉末变蓝色,说明生成了 (填化学式),C装置的作用是 。
(4)已知是红色粉末,当 (填实验现象)时停止通入。
(5)进一步检验硬质玻璃管中红色粉末可知,它是物质的量之比为2:1的和Cu组成的混合物。A装置硬质玻璃管中反应的另一种产物为气体单质,硬质玻璃管中的总反应方程式为 。
(6)收集两瓶干燥的氨气,进行喷泉实验:
利用D装置引发 色喷泉,其原理是 ;受D装置启发,小组创新设计E装置,引发E装置喷泉的操作是 。
17.硫代硫酸钠()常作氰化物中毒的解毒剂及照相行业中的定影剂。某小组以硫酸厂排放的尾气为原料制备硫代硫酸钠,工艺流程如图所示。回答下列问题:
已知:
①制备原理:。
②和的溶解度均随温度的升高显著增大,在48℃时开始分解。
③产品在酸性条件下不稳定:。
④碘量法测定样品纯度原理:。
(1)“碱吸”时,加入过量的NaOH溶液的目的是 。
(2)“趁热过滤”主要是除去 ,相比常温过滤,“趁热过滤”的优点是 。
(3)调节“溶液”pH时,若不小心加入了过量的稀硫酸,产生的后果是 。
(4)“系列操作”包括蒸发浓缩、 、过滤、洗涤、低温(<48℃)干燥,若干燥时温度过高,产生的后果是 。
(5)硫代硫酸钠在医疗领域常作氰化物中毒的解毒剂。已知和KCN反应生成两种正盐,将产物分两份:一份滴加溶液,溶液变红色;另一份滴加盐酸,将产生的气体通入品红溶液中,溶液褪色。和KCN反应的离子方程式为 。
(6)测定产品的纯度:取产品溶于蒸馏水配制成250mL溶液,取25.00mL配制的溶液于锥形瓶中,加入碘()水至恰好完全反应时消耗碘水,则该产品中的质量分数为 %。
18.《周礼》一书,有“醯人掌共五齐七菹”的记载,醯人是周王室掌管五齐、七菹的官员,从侧面反映出醋在当时帝王饮食生活中的重要地位。以玉米等粮食为原料模拟民间酿醋(F)的主要原理设计如下流程。回答下列问题:
(1)“粉碎”的目的是 。
(2)B的名称是 。
(3)写出C生成D的化学方程式: 。
(4)在新制中加入适量E共热,观察到的实验现象是 。E的环状同分异构体为 (填结构简式)。
(5)醋能提升菜肴风味,是因为生成了G,F与D生成G的反应类型是 。
(6)已知等量X分别与足量Na、反应产生和的体积比为1:1(同温同压),X分子含甲基,则X的结构简式为 ,含有的官能团有 (填名称)。
四、填空题
19.甲醇()被誉为“液态阳光”,以甲醇为载体,将间歇性可再生能源(太阳能、风能)转化为稳定、可运输的化学能,从而解决清洁能源存储与时空分布不均的难题。回答下列问题:反应原理:
ⅰ.;
ⅱ.(g代表气态)。
(1)下列图像能正确表示反应ⅰ中能量变化的是 (填标号)。
A. B.
(2)300℃时,向恒容密闭容器中充入1molCO2和仅发生反应ⅱ,下列情况能说明该反应达到平衡状态的是___________(填标号)。
A.气体密度不随时间变化 B.气体总压强不随时间变化
C.的体积分数不随时间变化 D.体系中H原子数目不随时间变化
(3)在体积可变的密闭反应器中充入适量的和,仅发生反应ⅱ,下列措施不能增大合成反应速率的是___________(填标号)。
A.增大压强 B.降低温度 C.加入催化剂 D.增大浓度
(4)250℃、条件下,向2L密闭容器中充入和,在催化剂作用下只发生反应ⅱ,测得、和的物质的量(n)与时间(t)的关系如图。
①甲代表 (填化学式), 。
②平衡时的体积分数为 (保留两位有效数字)。
(5)甲醇-空气碱性(如KOH作为电解质)燃料电池放电效率较高,在 (填“正”或“负”)极区充入空气,负极的电极反应式为 (氧化产物为)。
题号 1 2 3 4 5 6 7 8 9 10
答案 A B B D C D C D C B
题号 11 12 13 14 15
答案 C C A A AC
16.(1)a
(2)通入氨气
(3) 吸收尾气中的,防止污染环境
(4)A中黑色粉末全部变为红色粉末
(5)
(6) 红或粉红 氨气极易溶于水,烧瓶内外形成较大压强差,外压将水快速压入烧瓶中 打开止水夹K,用热毛巾捂烧瓶,当与水接触后快速移开毛巾
17.(1)将全部转化成
(2) 硫 避免硫代硫酸钠析出,减少产品损失
(3)与稀硫酸发生反应,降低产率
(4) 降温结晶 产品失去结晶水
(5)
(6)
18.(1)增大固体接触面积,提高反应速率
(2)麦芽榶
(3)
(4) 产生砖红色沉淀
(5)取代反应或酯化反应
(6) 羧基、羟基
19.(1)A
(2)BC
(3)B
(4) 0.76 6.8
(5) 正
同课章节目录
