2025年河南省漯河市临颍县三家店镇二中、实验中学联考九年级下学期中考三模化学试卷(含答案)
文档属性
| 名称 | 2025年河南省漯河市临颍县三家店镇二中、实验中学联考九年级下学期中考三模化学试卷(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 2.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-08 00:00:00 | ||
图片预览


文档简介
2025年中招考试化学模拟试题
一、选择题(本题包括14个小题,每小题1分,共14分。每小题只有一个选项符合题意)
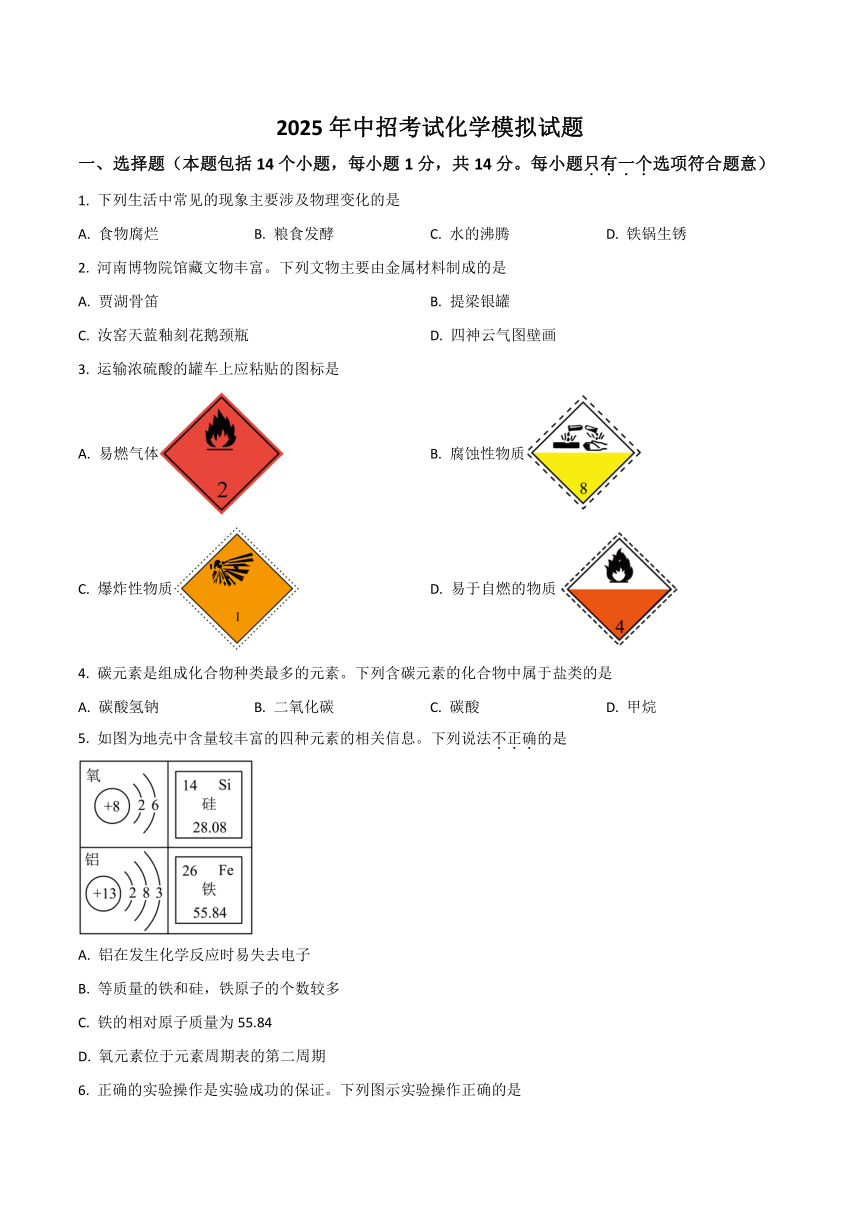
1. 下列生活中常见的现象主要涉及物理变化的是
A. 食物腐烂 B. 粮食发酵 C. 水的沸腾 D. 铁锅生锈
2. 河南博物院馆藏文物丰富。下列文物主要由金属材料制成的是
A. 贾湖骨笛 B. 提梁银罐
C. 汝窑天蓝釉刻花鹅颈瓶 D. 四神云气图壁画
3. 运输浓硫酸的罐车上应粘贴的图标是
A. 易燃气体 B. 腐蚀性物质
C. 爆炸性物质 D. 易于自燃的物质
4. 碳元素是组成化合物种类最多的元素。下列含碳元素的化合物中属于盐类的是
A. 碳酸氢钠 B. 二氧化碳 C. 碳酸 D. 甲烷
5. 如图为地壳中含量较丰富的四种元素的相关信息。下列说法不正确的是
A. 铝在发生化学反应时易失去电子
B. 等质量的铁和硅,铁原子的个数较多
C. 铁的相对原子质量为55.84
D. 氧元素位于元素周期表的第二周期
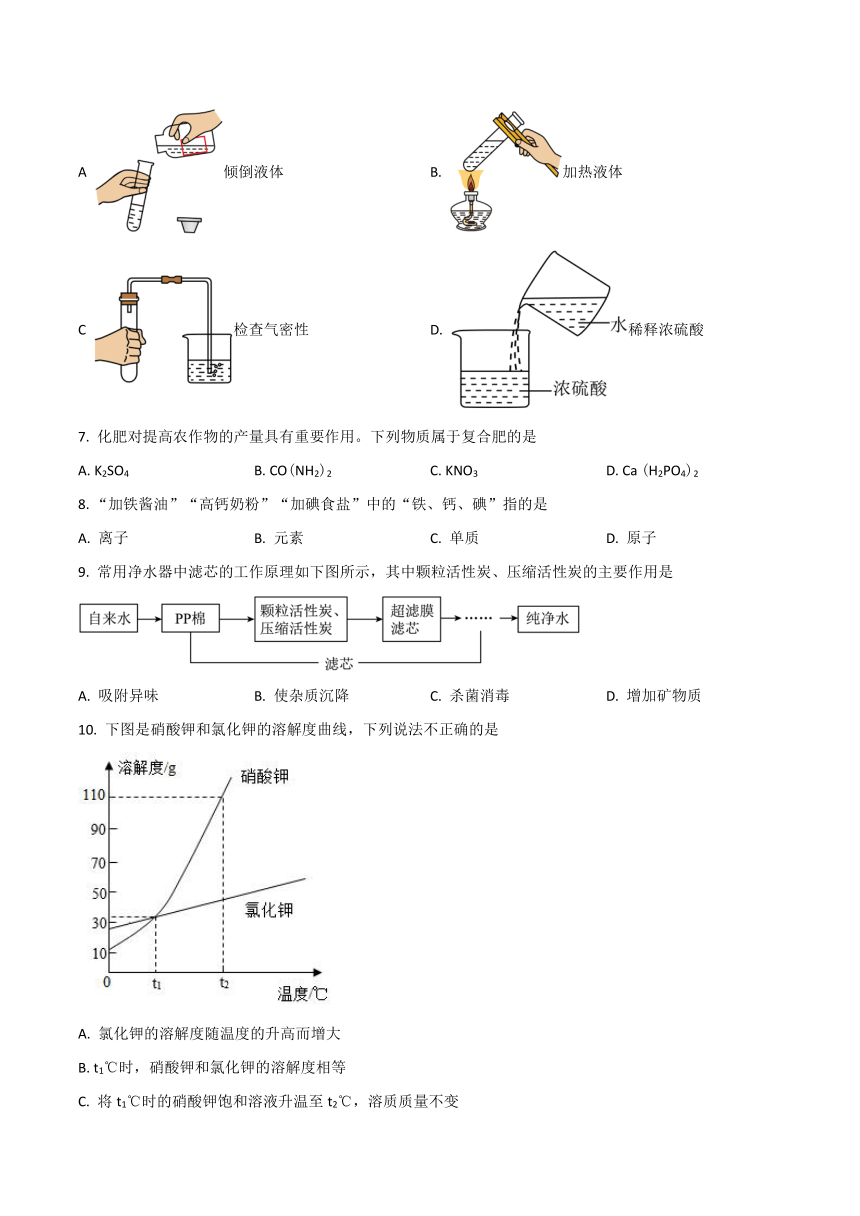
6. 正确的实验操作是实验成功的保证。下列图示实验操作正确的是
A 倾倒液体 B. 加热液体
C 检查气密性 D. 稀释浓硫酸
7. 化肥对提高农作物的产量具有重要作用。下列物质属于复合肥的是
A. K2SO4 B. CO(NH2)2 C. KNO3 D. Ca (H2PO4)2
8. “加铁酱油”“高钙奶粉”“加碘食盐”中的“铁、钙、碘”指的是
A. 离子 B. 元素 C. 单质 D. 原子
9. 常用净水器中滤芯的工作原理如下图所示,其中颗粒活性炭、压缩活性炭的主要作用是
A. 吸附异味 B. 使杂质沉降 C. 杀菌消毒 D. 增加矿物质
10. 下图是硝酸钾和氯化钾的溶解度曲线,下列说法不正确的是
A. 氯化钾的溶解度随温度的升高而增大
B. t1℃时,硝酸钾和氯化钾的溶解度相等
C. 将t1℃时的硝酸钾饱和溶液升温至t2℃,溶质质量不变
D. t2℃时,硝酸钾饱和溶液中溶质与溶剂的质量比为11:21
11. 超氧化钾常用于化学氧自救器中,其涉及的反应的化学方程式为:4KO2+2CO2=2X+3O2。关于该反应的说法正确的是
A. 该反应属于复分解反应 B. X的化学式为K2CO3
C. 反应中氧元素的化合价始终不变 D. 反应中元素的种类发生改变
12. 下列区分物质的试剂或方法不正确的是
A. 用水区分氢氧化钠固体和硝酸铵固体
B. 用闻气味的方法区分白酒和白醋
C. 用酚酞溶液区分碳酸钠溶液和氢氧化钠溶液
D. 用灼烧的方法区分黄金和黄铜(铜锌合金)
13. 高铁酸钾(K2FeO4)作净水剂时可发生反应:4K2FeO4+10H2O=4Fe(OH)3↓+8KOH+3O2↑,下列说法正确是
A. 该反应中涉及的物质有酸、碱、盐、氧化物
B. 高铁酸钾(K2FeO4)中铁元素的化合价为+7
C. 反应前后分子个数没有发生变化
D. 可用带火星的木条检验反应生成的气体
14. 现有8g氧化铁和氧化铜的混合物,与100g一定质量分数的盐酸恰好完全反应,则该盐酸中溶质的质量分数可能为
A. 7.3% B. 10% C. 12% D. 15%
二、填空题(本题包括6个小题,每空1分,共16分)
15. 请从氮气、氧气、干冰中选择适当的物质填空:焊接金属时可作保护气的是_______;可用于制造舞台烟雾效果的是_______。
16. 鱼肉味道鲜美,鱼肉中能在消化液作用下生成氨基酸的营养物质是_______。青少年缺钙会引起_______(填“贫血”或“佝偻病”)。
17. 保护环境是我国的一项基本国策。
(1)石油和天然气均属于_______(填“可再生”或“不可再生”)能源;使用含硫的煤会产生一种引起酸雨的气体是_______。
(2)氢气是理想的清洁燃料。氢气作燃料的优点是_______(写1条即可)。
(3)液氨有望成为新一代绿色能源。氨气在纯氧中燃烧生成空气中含量最多的气体和一种氧化物,且释放大量的热。该反应的化学方程式为_______。
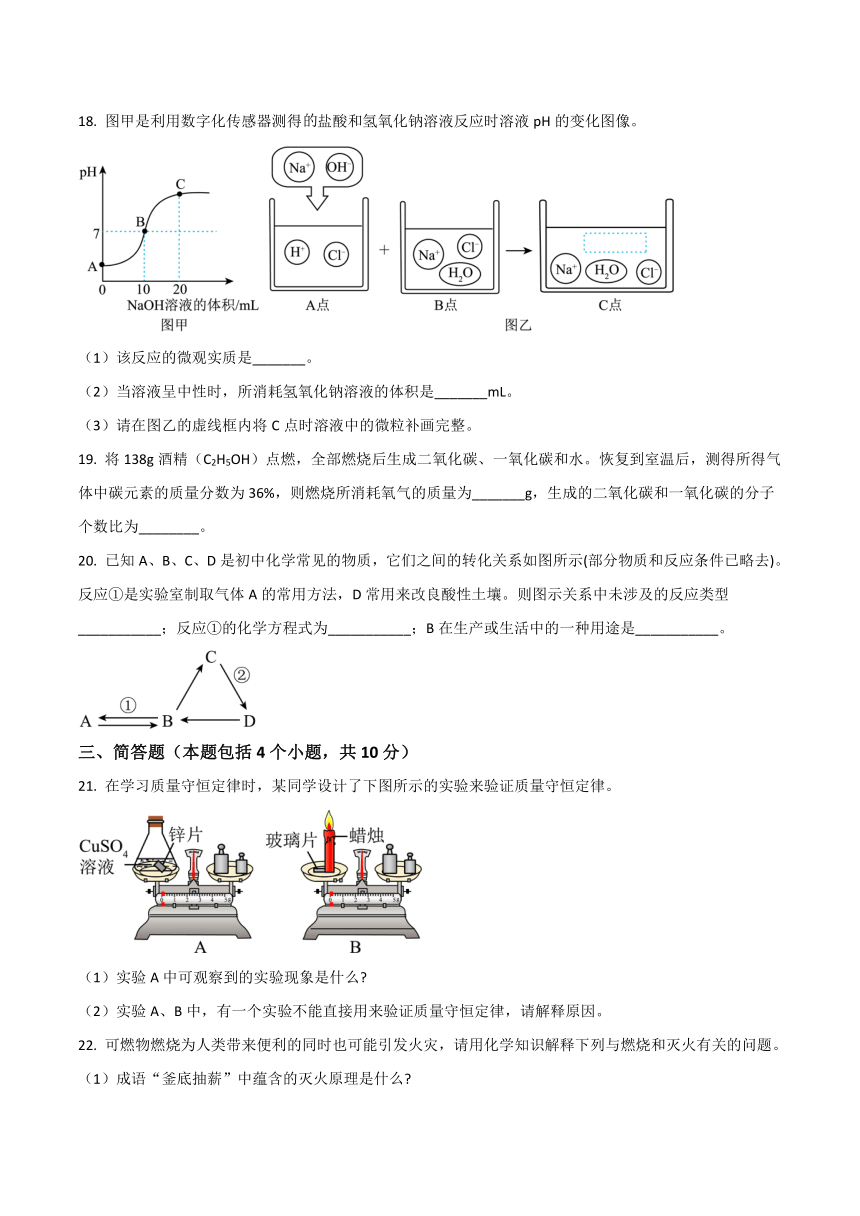
18. 图甲是利用数字化传感器测得盐酸和氢氧化钠溶液反应时溶液pH的变化图像。
(1)该反应的微观实质是_______。
(2)当溶液呈中性时,所消耗氢氧化钠溶液的体积是_______mL。
(3)请在图乙的虚线框内将C点时溶液中的微粒补画完整。
19. 将138g酒精(C2H5OH)点燃,全部燃烧后生成二氧化碳、一氧化碳和水。恢复到室温后,测得所得气体中碳元素的质量分数为36%,则燃烧所消耗氧气的质量为_______g,生成的二氧化碳和一氧化碳的分子个数比为________。
20. 已知A、B、C、D是初中化学常见的物质,它们之间的转化关系如图所示(部分物质和反应条件已略去)。反应①是实验室制取气体A的常用方法,D常用来改良酸性土壤。则图示关系中未涉及的反应类型___________;反应①的化学方程式为___________;B在生产或生活中的一种用途是___________。
三、简答题(本题包括4个小题,共10分)
21. 在学习质量守恒定律时,某同学设计了下图所示的实验来验证质量守恒定律。
(1)实验A中可观察到的实验现象是什么
(2)实验A、B中,有一个实验不能直接用来验证质量守恒定律,请解释原因。
22. 可燃物燃烧为人类带来便利的同时也可能引发火灾,请用化学知识解释下列与燃烧和灭火有关的问题。
(1)成语“釜底抽薪”中蕴含的灭火原理是什么
(2)图书档案等贵重物品着火时可用二氧化碳灭火器灭火,这体现的二氧化碳的性质有哪些
23. 掌握实验室制取气体的方法是必备的化学素养。实验室常用下图所示仪器组装制取气体的装置,据此回答问题。
(1)写出仪器⑧的名称:_______。
(2)请选择适当的仪器,组装一套实验室制取二氧化碳的发生和收集装置。(用序号表示)。
(3)实验室可利用图示仪器组装制取氧气的装置,写出加热高锰酸钾制取氧气的化学方程式。
24. 如下图所示,实验前杠杆两端分别挂着质量和体积相同的锌球,且杠杆平衡。
(1)写出烧杯乙中发生的反应的化学方程式。
(2)一段时间后,同时移走两个烧杯,发现杠杆左端下降,请解释原因(假设置换出的金属均附着在锌球上)。
(3)要验证Zn、Ag、Cu三种金属的活动性顺序,请在该实验的基础上补充一个实验,简要写出实验的步骤和现象。
四、综合应用题(共10分)
25. 酸、碱、盐是生产、生活中用途广泛的重要化合物。
(1)下列关于酸、碱、盐的说法中正确的是_______(填字母)。
a.酸和碱一定都含氢、氧元素
b.有水生成的反应一定是中和反应
c.盐可以不含金属元素
d.盐的水溶液都显中性
(2)某化学小组对碱的性质进行归纳整理,做了如下图所示的实验,请将表格填写完整。
实验序号 实验I 实验Ⅱ 实验Ⅲ 实验IV
实验操作
实验现象 溶液变红色 生成蓝色沉淀 无明显现象 无明显现象
分析与结论 Ca(OH)2能与指示剂作用 反应的化学方程式为_______ 无法确定是否发生反应 无法确定是否发生反应
(3)为证明CO2与NaOH发生了化学反应并探究反应进行的程度,化学小组做了以下实验。(已知碳酸钠溶液呈碱性)
①取少量实验Ⅲ反应后的溶液于试管中,向试管中滴加BaCl2溶液,观察到有白色沉淀生成,该过程中发生反应的化学方程式为_______,本实验是通过检验_______(填“反应物消失”或“有新物质生成”)来证明二者发生了化学反应的。
②滴加BaCl2溶液后将试管中的混合物过滤,向滤液中加入无色酚酞溶液,溶液变红。但这还不能说明溶液中含有NaOH,为什么 请说明理由:_______。
(4)取少量实验IV反应后的溶液于试管中,向试管中滴加少量的BaCl2溶液,发现有白色沉淀生成,据此不能推断反应有Na2SO4生成,为什么 请说明理由:_______。
(5)若实验IV中试管内为2g5%氢氧化钠溶液,先滴加几滴无色酚酞溶液,再逐滴滴加稀硫酸至溶液中的红色恰好消失,则可直接证明稀硫酸与氢氧化钠溶液发生了化学反应。请计算:此时已加入溶质质量分数为24.5%的稀硫酸的质量。
2025年中招考试化学模拟试题
一、选择题(本题包括14个小题,每小题1分,共14分。每小题只有一个选项符合题意)
【1题答案】
C
【2题答案】
B
【3题答案】
B
【4题答案】
A
【5题答案】
B
【6题答案】
C
【7题答案】
C
【8题答案】
B
【9题答案】
A
【10题答案】
D
【11题答案】
B
【12题答案】
C
【13题答案】
D
【14题答案】
B
二、填空题(本题包括6个小题,每空1分,共16分)
【15题答案】
①. 氮气 ②. 干冰
【16题答案】
①. 蛋白质 ②. 佝偻病
【17题答案】
(1) ①. 不可再生 ②. SO2##二氧化硫
(2)燃烧的产物是水,无污染(合理即可)
(3)4NH3+3O22N2+6H2O
【18题答案】
(1)氢离子和氢氧根离子结合生成水分子
(2)10 (3)
【19题答案】
①. 224 ②. 1:2
【20题答案】
①. 置换反应 ②. ③. 作建筑材料##作补钙剂
三、简答题(本题包括4个小题,共10分)
【21题答案】
(1)锌片表面有红色固体析出,溶液由蓝色逐渐变为无色,天平平衡。
(2)实验B不能直接用来验证质量守恒定律。因为蜡烛燃烧生成的水和二氧化碳,在敞口容器中,生成的二氧化碳和水蒸气逸散到空气中,导致反应后剩余的物质质量减少,无法直接验证质量守恒定律。
【22题答案】
(1)清除可燃物
(2)二氧化碳不可燃也不助燃,且密度比空气的大
【23题答案】
(1)酒精灯 (2)①③④⑤
(3)
【24题答案】
(1)
(2)等质量的锌置换出银的质量大于置换出铜的质量
(3)将铜丝放入硝酸银溶液中,铜丝表面析出银白色固体,溶液变成蓝色##将银丝放入硝酸铜溶液中,无明显现象
四、综合应用题(共10分)
【25题答案】
(1)c (2)2NaOH+CuSO4=Na2SO4+Cu(OH)2↓
(3) ①. Na2CO3+BaCl2=BaCO3↓+2NaCl ②. 有新物质生成 ③. 因为题目未明确所加BaCl2溶液是否足量(或过量),不能明确Na2CO3是否消耗完。Na2CO3溶液呈碱性,也能使无色酚酞溶液变红
(4)因为稀硫酸也能与BaCl2溶液反应,生成BaSO4白色沉淀
(5)解:设此时已加入稀硫酸的质量为x。
解得x=0.5g
答:此时已加入稀硫酸的质量为0.5g。
一、选择题(本题包括14个小题,每小题1分,共14分。每小题只有一个选项符合题意)
1. 下列生活中常见的现象主要涉及物理变化的是
A. 食物腐烂 B. 粮食发酵 C. 水的沸腾 D. 铁锅生锈
2. 河南博物院馆藏文物丰富。下列文物主要由金属材料制成的是
A. 贾湖骨笛 B. 提梁银罐
C. 汝窑天蓝釉刻花鹅颈瓶 D. 四神云气图壁画
3. 运输浓硫酸的罐车上应粘贴的图标是
A. 易燃气体 B. 腐蚀性物质
C. 爆炸性物质 D. 易于自燃的物质
4. 碳元素是组成化合物种类最多的元素。下列含碳元素的化合物中属于盐类的是
A. 碳酸氢钠 B. 二氧化碳 C. 碳酸 D. 甲烷
5. 如图为地壳中含量较丰富的四种元素的相关信息。下列说法不正确的是
A. 铝在发生化学反应时易失去电子
B. 等质量的铁和硅,铁原子的个数较多
C. 铁的相对原子质量为55.84
D. 氧元素位于元素周期表的第二周期
6. 正确的实验操作是实验成功的保证。下列图示实验操作正确的是
A 倾倒液体 B. 加热液体
C 检查气密性 D. 稀释浓硫酸
7. 化肥对提高农作物的产量具有重要作用。下列物质属于复合肥的是
A. K2SO4 B. CO(NH2)2 C. KNO3 D. Ca (H2PO4)2
8. “加铁酱油”“高钙奶粉”“加碘食盐”中的“铁、钙、碘”指的是
A. 离子 B. 元素 C. 单质 D. 原子
9. 常用净水器中滤芯的工作原理如下图所示,其中颗粒活性炭、压缩活性炭的主要作用是
A. 吸附异味 B. 使杂质沉降 C. 杀菌消毒 D. 增加矿物质
10. 下图是硝酸钾和氯化钾的溶解度曲线,下列说法不正确的是
A. 氯化钾的溶解度随温度的升高而增大
B. t1℃时,硝酸钾和氯化钾的溶解度相等
C. 将t1℃时的硝酸钾饱和溶液升温至t2℃,溶质质量不变
D. t2℃时,硝酸钾饱和溶液中溶质与溶剂的质量比为11:21
11. 超氧化钾常用于化学氧自救器中,其涉及的反应的化学方程式为:4KO2+2CO2=2X+3O2。关于该反应的说法正确的是
A. 该反应属于复分解反应 B. X的化学式为K2CO3
C. 反应中氧元素的化合价始终不变 D. 反应中元素的种类发生改变
12. 下列区分物质的试剂或方法不正确的是
A. 用水区分氢氧化钠固体和硝酸铵固体
B. 用闻气味的方法区分白酒和白醋
C. 用酚酞溶液区分碳酸钠溶液和氢氧化钠溶液
D. 用灼烧的方法区分黄金和黄铜(铜锌合金)
13. 高铁酸钾(K2FeO4)作净水剂时可发生反应:4K2FeO4+10H2O=4Fe(OH)3↓+8KOH+3O2↑,下列说法正确是
A. 该反应中涉及的物质有酸、碱、盐、氧化物
B. 高铁酸钾(K2FeO4)中铁元素的化合价为+7
C. 反应前后分子个数没有发生变化
D. 可用带火星的木条检验反应生成的气体
14. 现有8g氧化铁和氧化铜的混合物,与100g一定质量分数的盐酸恰好完全反应,则该盐酸中溶质的质量分数可能为
A. 7.3% B. 10% C. 12% D. 15%
二、填空题(本题包括6个小题,每空1分,共16分)
15. 请从氮气、氧气、干冰中选择适当的物质填空:焊接金属时可作保护气的是_______;可用于制造舞台烟雾效果的是_______。
16. 鱼肉味道鲜美,鱼肉中能在消化液作用下生成氨基酸的营养物质是_______。青少年缺钙会引起_______(填“贫血”或“佝偻病”)。
17. 保护环境是我国的一项基本国策。
(1)石油和天然气均属于_______(填“可再生”或“不可再生”)能源;使用含硫的煤会产生一种引起酸雨的气体是_______。
(2)氢气是理想的清洁燃料。氢气作燃料的优点是_______(写1条即可)。
(3)液氨有望成为新一代绿色能源。氨气在纯氧中燃烧生成空气中含量最多的气体和一种氧化物,且释放大量的热。该反应的化学方程式为_______。
18. 图甲是利用数字化传感器测得盐酸和氢氧化钠溶液反应时溶液pH的变化图像。
(1)该反应的微观实质是_______。
(2)当溶液呈中性时,所消耗氢氧化钠溶液的体积是_______mL。
(3)请在图乙的虚线框内将C点时溶液中的微粒补画完整。
19. 将138g酒精(C2H5OH)点燃,全部燃烧后生成二氧化碳、一氧化碳和水。恢复到室温后,测得所得气体中碳元素的质量分数为36%,则燃烧所消耗氧气的质量为_______g,生成的二氧化碳和一氧化碳的分子个数比为________。
20. 已知A、B、C、D是初中化学常见的物质,它们之间的转化关系如图所示(部分物质和反应条件已略去)。反应①是实验室制取气体A的常用方法,D常用来改良酸性土壤。则图示关系中未涉及的反应类型___________;反应①的化学方程式为___________;B在生产或生活中的一种用途是___________。
三、简答题(本题包括4个小题,共10分)
21. 在学习质量守恒定律时,某同学设计了下图所示的实验来验证质量守恒定律。
(1)实验A中可观察到的实验现象是什么
(2)实验A、B中,有一个实验不能直接用来验证质量守恒定律,请解释原因。
22. 可燃物燃烧为人类带来便利的同时也可能引发火灾,请用化学知识解释下列与燃烧和灭火有关的问题。
(1)成语“釜底抽薪”中蕴含的灭火原理是什么
(2)图书档案等贵重物品着火时可用二氧化碳灭火器灭火,这体现的二氧化碳的性质有哪些
23. 掌握实验室制取气体的方法是必备的化学素养。实验室常用下图所示仪器组装制取气体的装置,据此回答问题。
(1)写出仪器⑧的名称:_______。
(2)请选择适当的仪器,组装一套实验室制取二氧化碳的发生和收集装置。(用序号表示)。
(3)实验室可利用图示仪器组装制取氧气的装置,写出加热高锰酸钾制取氧气的化学方程式。
24. 如下图所示,实验前杠杆两端分别挂着质量和体积相同的锌球,且杠杆平衡。
(1)写出烧杯乙中发生的反应的化学方程式。
(2)一段时间后,同时移走两个烧杯,发现杠杆左端下降,请解释原因(假设置换出的金属均附着在锌球上)。
(3)要验证Zn、Ag、Cu三种金属的活动性顺序,请在该实验的基础上补充一个实验,简要写出实验的步骤和现象。
四、综合应用题(共10分)
25. 酸、碱、盐是生产、生活中用途广泛的重要化合物。
(1)下列关于酸、碱、盐的说法中正确的是_______(填字母)。
a.酸和碱一定都含氢、氧元素
b.有水生成的反应一定是中和反应
c.盐可以不含金属元素
d.盐的水溶液都显中性
(2)某化学小组对碱的性质进行归纳整理,做了如下图所示的实验,请将表格填写完整。
实验序号 实验I 实验Ⅱ 实验Ⅲ 实验IV
实验操作
实验现象 溶液变红色 生成蓝色沉淀 无明显现象 无明显现象
分析与结论 Ca(OH)2能与指示剂作用 反应的化学方程式为_______ 无法确定是否发生反应 无法确定是否发生反应
(3)为证明CO2与NaOH发生了化学反应并探究反应进行的程度,化学小组做了以下实验。(已知碳酸钠溶液呈碱性)
①取少量实验Ⅲ反应后的溶液于试管中,向试管中滴加BaCl2溶液,观察到有白色沉淀生成,该过程中发生反应的化学方程式为_______,本实验是通过检验_______(填“反应物消失”或“有新物质生成”)来证明二者发生了化学反应的。
②滴加BaCl2溶液后将试管中的混合物过滤,向滤液中加入无色酚酞溶液,溶液变红。但这还不能说明溶液中含有NaOH,为什么 请说明理由:_______。
(4)取少量实验IV反应后的溶液于试管中,向试管中滴加少量的BaCl2溶液,发现有白色沉淀生成,据此不能推断反应有Na2SO4生成,为什么 请说明理由:_______。
(5)若实验IV中试管内为2g5%氢氧化钠溶液,先滴加几滴无色酚酞溶液,再逐滴滴加稀硫酸至溶液中的红色恰好消失,则可直接证明稀硫酸与氢氧化钠溶液发生了化学反应。请计算:此时已加入溶质质量分数为24.5%的稀硫酸的质量。
2025年中招考试化学模拟试题
一、选择题(本题包括14个小题,每小题1分,共14分。每小题只有一个选项符合题意)
【1题答案】
C
【2题答案】
B
【3题答案】
B
【4题答案】
A
【5题答案】
B
【6题答案】
C
【7题答案】
C
【8题答案】
B
【9题答案】
A
【10题答案】
D
【11题答案】
B
【12题答案】
C
【13题答案】
D
【14题答案】
B
二、填空题(本题包括6个小题,每空1分,共16分)
【15题答案】
①. 氮气 ②. 干冰
【16题答案】
①. 蛋白质 ②. 佝偻病
【17题答案】
(1) ①. 不可再生 ②. SO2##二氧化硫
(2)燃烧的产物是水,无污染(合理即可)
(3)4NH3+3O22N2+6H2O
【18题答案】
(1)氢离子和氢氧根离子结合生成水分子
(2)10 (3)
【19题答案】
①. 224 ②. 1:2
【20题答案】
①. 置换反应 ②. ③. 作建筑材料##作补钙剂
三、简答题(本题包括4个小题,共10分)
【21题答案】
(1)锌片表面有红色固体析出,溶液由蓝色逐渐变为无色,天平平衡。
(2)实验B不能直接用来验证质量守恒定律。因为蜡烛燃烧生成的水和二氧化碳,在敞口容器中,生成的二氧化碳和水蒸气逸散到空气中,导致反应后剩余的物质质量减少,无法直接验证质量守恒定律。
【22题答案】
(1)清除可燃物
(2)二氧化碳不可燃也不助燃,且密度比空气的大
【23题答案】
(1)酒精灯 (2)①③④⑤
(3)
【24题答案】
(1)
(2)等质量的锌置换出银的质量大于置换出铜的质量
(3)将铜丝放入硝酸银溶液中,铜丝表面析出银白色固体,溶液变成蓝色##将银丝放入硝酸铜溶液中,无明显现象
四、综合应用题(共10分)
【25题答案】
(1)c (2)2NaOH+CuSO4=Na2SO4+Cu(OH)2↓
(3) ①. Na2CO3+BaCl2=BaCO3↓+2NaCl ②. 有新物质生成 ③. 因为题目未明确所加BaCl2溶液是否足量(或过量),不能明确Na2CO3是否消耗完。Na2CO3溶液呈碱性,也能使无色酚酞溶液变红
(4)因为稀硫酸也能与BaCl2溶液反应,生成BaSO4白色沉淀
(5)解:设此时已加入稀硫酸的质量为x。
解得x=0.5g
答:此时已加入稀硫酸的质量为0.5g。
同课章节目录
