苏教版高中化学选择性必修2专题2原子结构与元素性质2.1.1人类对原子结构的认识原子核外电子的运动特征课件(28张)
文档属性
| 名称 | 苏教版高中化学选择性必修2专题2原子结构与元素性质2.1.1人类对原子结构的认识原子核外电子的运动特征课件(28张) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-09 00:00:00 | ||
图片预览







文档简介
(共28张PPT)
第一单元
第1课时 原子核外电子的运动
专题2 原子结构与元素的性质
德谟克利特:朴素原子观
道尔顿:原子学说
汤姆生:“葡萄干面包式”模型
卢瑟福:带核原子结构模型
玻尔:原子轨道模型
现代量子力学模型
知识回顾
1803
1904
1911
1913
1926
一、人类对原子结构的认识
X
A
Z
原子
原子核
核外电子(Z)
质子(Z)
中子(N=A - Z)
质量数=质子数+ 中子数
(A=Z+N)
核电荷数=核内质子数=核外电子数=原子序数
知识回顾
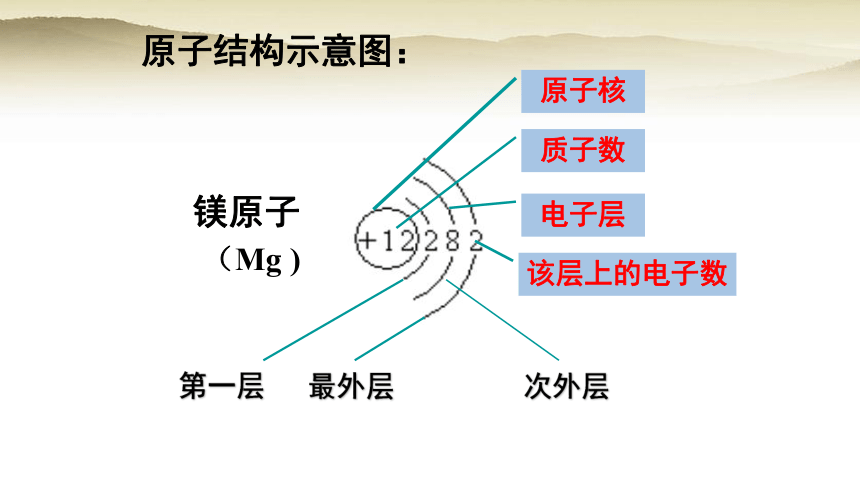
原子结构示意图:
镁原子
(Mg )
原子核
质子数
电子层
该层上的电子数
第一层 最外层 次外层
依据上页的原子结构示意图,回忆你所知道的原子的核外电子排布规律。
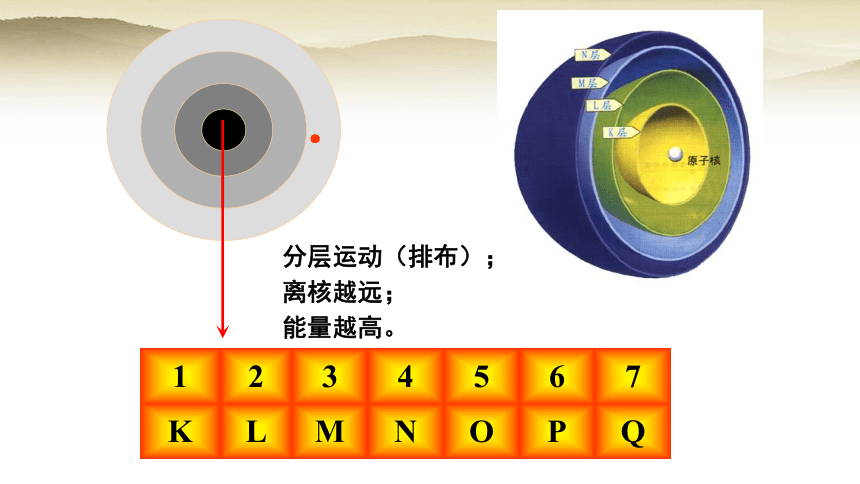
二、原子核外电子的运动特征
电子云
·
能量越高。
离核越远;
分层运动(排布);
Q
P
O
N
M
L
K
7
6
5
4
3
2
1
核外电子排布规律:
(1)能量最低原理:
电子先排布在能量较低的轨道上
(2)
每层≤2n2个。
最外层≤ 8个(K层时≤2个),如果最外层为8个(K层为2个)就达到了饱和稳定结构。
次外层≤ 18个,倒数第三层≤ 32
完成P.28【温故知新】
核外电子运动的特征
核外电子质量小,运动空间小,运动速率大。
无确定的轨道,无法描述其运动轨迹。
无法计算电子在某一刻所在的位置,只能指出其在核外空间某处出现的机会的多少。
可用统计(图示)的方法研究电子在核外出现的概率:电子云
电子云:
氢原子的电子云
①电子云的概念:
电子在原子核外空间一定范围内出现,好像带负电荷云雾笼罩在原子核周围,人们形象的称为电子云。
③小黑点疏密的含义:
离核近,小黑点密,电子云密度大,电子出现的机会多;
离核远,小黑点疏,电子云密度小,电子出现的机会少。
②小黑点的含义:
并非表示电子,而是表示:电子在此空间出现过
电子出现的机会的多少
在多电子原子中,原子核外电子的运动状态不同,我们从以下几个方面描述原子核外电子的运动状态。
一、电子层(能层)
二、原子轨道(能级)
三、电子的自旋状态
一、电子层(又称能层)n:
电子层序数(n) 1 2 3 4 5 6 7
符号 K L M N O P Q
离核越来越远,能量越来越高
在含有多个电子的原子中,电子的能量往往是不同的。人们根据电子的能量差异和主要运动区域的不同,认为核外电子分别处于不同的电子层上。
量子力学研究表明,处于同一电子层的原子核外电子,也可以在不同类型的原子轨道上运动。
二、原子轨道(能级)
轨道的类型不同,轨道的形状也不同。
用s、p、d、f分别表示不同形状的轨道。
s轨道:球形
p轨道:纺锤形
d原子轨道是花瓣形的;f轨道形状更复杂。
1.原子轨道的表示方法:
第四电子层:有四种类型轨道,记作4s,4p,4d,4f
第一电子层:只有s轨道,记作1s。
第二电子层:有二种类型轨道,分别记作2s、 2p。
第三电子层:有三种类型轨道,记作3s,3p,3d。
原子轨道种类数与电子层序数相等,即n层有n种轨道。
s轨道:球形
s 轨道是球形对称(原子核位于球心)n越大,电子能量越大(即1s<2s<3s<4s),原子轨道半径越大。
p轨道:纺锤形
P轨道纺锤形,每个P轨道有3个伸展方向,相互垂直,分别以Px,Py,Pz表示。同一电子层 Px,Py,PZ能量相同(如:2px=2py=2pz)。
2. 原子轨道的伸展方向:
(决定该种类型的轨道个数)
①s轨道是球形对称,所以只有1个轨道
②p轨道有x、y、z三个伸展方向,包括px、py、pz共3个轨道
③d轨道有5个伸展方向,f轨道有7个伸展方向
3.各原子轨道能量高低:
③电子层和形状相同的原子轨道能量相等。
①相同电子层上原子轨道能量高低:
ns < np < nd < nf
②形状相同的原子轨道能量高低:
1s < 2s < 3s < 4s……
如:2px=2py=2pz
完成P.30【学以致用】
三.电子自旋:
原子核外电子还有一种称为“自旋”的运动。
原子核外电子的自旋可以有两种不同的状态,通常人们用向上箭头“↑”和向下箭头“↓”来表示这两种不同的自旋状态。
每个轨道最多只能容纳两个自旋状态不同的电子
电子层 原子轨
道类型 原子轨道
数目 可容纳的
电子数目
1 1s
2 2s,2p
3 3s,3p,3d
4 4s,4p,4d,4f
n —
1
2
4
8
9
18
16
32
n2
2n2
总结:各电子层包含的原子轨道数目和可容纳的电子数
1、关于“电子云”的描述中,正确的是( )
A、一个小黑点表示一个电子
B、一个小黑点代表电子在此出现过
C、电子云是带正电的云雾
D、小黑点的疏密表示电子在核外空间单位体积内出现机会的多少
BD
2、有下列四种轨道:①2s②2p③3p④4d,其中能量最高的是( )
A. 2s B.2p C.3p D.4d
D
2s<2p<3P<4d
当堂巩固
3、下列轨道含有轨道数目为3的是
A.1s B.2p C.3p D.4d
4、3d轨道中最多容纳电子数为
A.2 B. 10 C.14 D.18
BC
B
5、第三电子层含有的轨道数为
A.3 B.5 C.7 D.9
D
当堂巩固
6、 S轨道是 对称,所以S轨道有 个轨道;P轨道在空间有 个伸展方向,所以P轨道包括 个轨道;d轨道有 个轨道、f轨道有 个轨道。每一个原子轨道上只能有 个自旋状态不同核外电子。
球形
1
x、y、z 3
px、py、pz 3
5
7
2
当堂巩固
第一单元
第1课时 原子核外电子的运动
专题2 原子结构与元素的性质
德谟克利特:朴素原子观
道尔顿:原子学说
汤姆生:“葡萄干面包式”模型
卢瑟福:带核原子结构模型
玻尔:原子轨道模型
现代量子力学模型
知识回顾
1803
1904
1911
1913
1926
一、人类对原子结构的认识
X
A
Z
原子
原子核
核外电子(Z)
质子(Z)
中子(N=A - Z)
质量数=质子数+ 中子数
(A=Z+N)
核电荷数=核内质子数=核外电子数=原子序数
知识回顾
原子结构示意图:
镁原子
(Mg )
原子核
质子数
电子层
该层上的电子数
第一层 最外层 次外层
依据上页的原子结构示意图,回忆你所知道的原子的核外电子排布规律。
二、原子核外电子的运动特征
电子云
·
能量越高。
离核越远;
分层运动(排布);
Q
P
O
N
M
L
K
7
6
5
4
3
2
1
核外电子排布规律:
(1)能量最低原理:
电子先排布在能量较低的轨道上
(2)
每层≤2n2个。
最外层≤ 8个(K层时≤2个),如果最外层为8个(K层为2个)就达到了饱和稳定结构。
次外层≤ 18个,倒数第三层≤ 32
完成P.28【温故知新】
核外电子运动的特征
核外电子质量小,运动空间小,运动速率大。
无确定的轨道,无法描述其运动轨迹。
无法计算电子在某一刻所在的位置,只能指出其在核外空间某处出现的机会的多少。
可用统计(图示)的方法研究电子在核外出现的概率:电子云
电子云:
氢原子的电子云
①电子云的概念:
电子在原子核外空间一定范围内出现,好像带负电荷云雾笼罩在原子核周围,人们形象的称为电子云。
③小黑点疏密的含义:
离核近,小黑点密,电子云密度大,电子出现的机会多;
离核远,小黑点疏,电子云密度小,电子出现的机会少。
②小黑点的含义:
并非表示电子,而是表示:电子在此空间出现过
电子出现的机会的多少
在多电子原子中,原子核外电子的运动状态不同,我们从以下几个方面描述原子核外电子的运动状态。
一、电子层(能层)
二、原子轨道(能级)
三、电子的自旋状态
一、电子层(又称能层)n:
电子层序数(n) 1 2 3 4 5 6 7
符号 K L M N O P Q
离核越来越远,能量越来越高
在含有多个电子的原子中,电子的能量往往是不同的。人们根据电子的能量差异和主要运动区域的不同,认为核外电子分别处于不同的电子层上。
量子力学研究表明,处于同一电子层的原子核外电子,也可以在不同类型的原子轨道上运动。
二、原子轨道(能级)
轨道的类型不同,轨道的形状也不同。
用s、p、d、f分别表示不同形状的轨道。
s轨道:球形
p轨道:纺锤形
d原子轨道是花瓣形的;f轨道形状更复杂。
1.原子轨道的表示方法:
第四电子层:有四种类型轨道,记作4s,4p,4d,4f
第一电子层:只有s轨道,记作1s。
第二电子层:有二种类型轨道,分别记作2s、 2p。
第三电子层:有三种类型轨道,记作3s,3p,3d。
原子轨道种类数与电子层序数相等,即n层有n种轨道。
s轨道:球形
s 轨道是球形对称(原子核位于球心)n越大,电子能量越大(即1s<2s<3s<4s),原子轨道半径越大。
p轨道:纺锤形
P轨道纺锤形,每个P轨道有3个伸展方向,相互垂直,分别以Px,Py,Pz表示。同一电子层 Px,Py,PZ能量相同(如:2px=2py=2pz)。
2. 原子轨道的伸展方向:
(决定该种类型的轨道个数)
①s轨道是球形对称,所以只有1个轨道
②p轨道有x、y、z三个伸展方向,包括px、py、pz共3个轨道
③d轨道有5个伸展方向,f轨道有7个伸展方向
3.各原子轨道能量高低:
③电子层和形状相同的原子轨道能量相等。
①相同电子层上原子轨道能量高低:
ns < np < nd < nf
②形状相同的原子轨道能量高低:
1s < 2s < 3s < 4s……
如:2px=2py=2pz
完成P.30【学以致用】
三.电子自旋:
原子核外电子还有一种称为“自旋”的运动。
原子核外电子的自旋可以有两种不同的状态,通常人们用向上箭头“↑”和向下箭头“↓”来表示这两种不同的自旋状态。
每个轨道最多只能容纳两个自旋状态不同的电子
电子层 原子轨
道类型 原子轨道
数目 可容纳的
电子数目
1 1s
2 2s,2p
3 3s,3p,3d
4 4s,4p,4d,4f
n —
1
2
4
8
9
18
16
32
n2
2n2
总结:各电子层包含的原子轨道数目和可容纳的电子数
1、关于“电子云”的描述中,正确的是( )
A、一个小黑点表示一个电子
B、一个小黑点代表电子在此出现过
C、电子云是带正电的云雾
D、小黑点的疏密表示电子在核外空间单位体积内出现机会的多少
BD
2、有下列四种轨道:①2s②2p③3p④4d,其中能量最高的是( )
A. 2s B.2p C.3p D.4d
D
2s<2p<3P<4d
当堂巩固
3、下列轨道含有轨道数目为3的是
A.1s B.2p C.3p D.4d
4、3d轨道中最多容纳电子数为
A.2 B. 10 C.14 D.18
BC
B
5、第三电子层含有的轨道数为
A.3 B.5 C.7 D.9
D
当堂巩固
6、 S轨道是 对称,所以S轨道有 个轨道;P轨道在空间有 个伸展方向,所以P轨道包括 个轨道;d轨道有 个轨道、f轨道有 个轨道。每一个原子轨道上只能有 个自旋状态不同核外电子。
球形
1
x、y、z 3
px、py、pz 3
5
7
2
当堂巩固
