苏教版高中化学选择性必修2专题4分子空间结构与物质性质4.2配合物的形成和应用课件(26张)
文档属性
| 名称 | 苏教版高中化学选择性必修2专题4分子空间结构与物质性质4.2配合物的形成和应用课件(26张) |

|
|
| 格式 | ppt | ||
| 文件大小 | 5.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-09 00:00:00 | ||
图片预览






文档简介
(共26张PPT)
组织建设
第二单元 配合物的形成和应用
《黄金大劫案》
Au+HNO3+4HCl=H[AuCl4]+NO↑+2H2O
实验现象:
1.滴加氨水后,试管中首先出现蓝色沉淀。
Cu2++2NH3·H2O=Cu(OH)2↓+2NH4+
2.继续滴加氨水,沉淀逐渐溶解,溶液变成深蓝色。
思考:沉淀为什么溶解?深蓝色的可溶物质是什么?
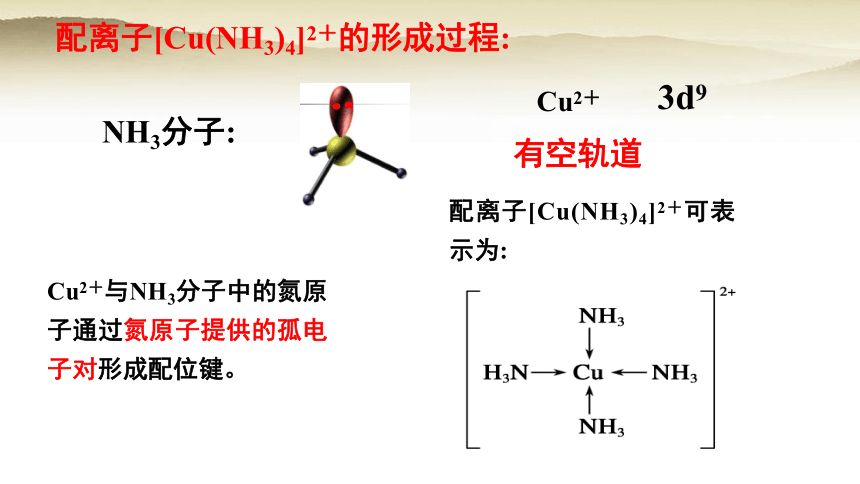
Cu2+与NH3分子中的氮原子通过氮原子提供的孤电子对形成配位键。
配离子[Cu(NH3)4]2+可表示为:
NH3分子:
Cu2+
3d9
有空轨道
配离子[Cu(NH3)4]2+的形成过程:
实验现象:
1.滴加氨水后,试管中首先出现蓝色沉淀。
Cu2++2NH3·H2O=Cu(OH)2↓+2NH4+
2.继续滴加氨水,沉淀逐渐溶解,溶液变成深蓝色。
思考:沉淀为什么溶解?深蓝色的可溶物质是什么?
Cu(OH)2+4NH3·H2O=[Cu(NH3)4]2++2OH-+4H2O
乙醇的作用:(醇析)降低[Cu(NH3)4]SO4的溶解度,利于析出[Cu(NH3)4]SO4·H2O晶体。
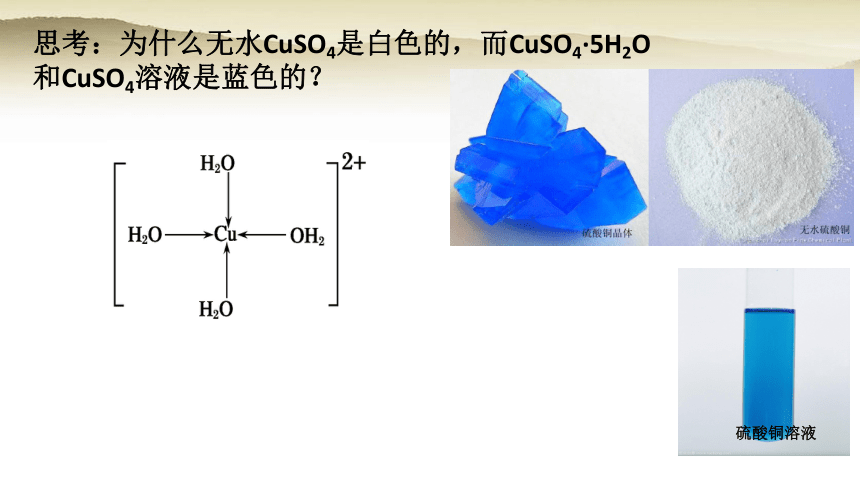
思考:为什么无水CuSO4是白色的,而CuSO4·5H2O和CuSO4溶液是蓝色的?
硫酸铜溶液
1、概念:把金属离子(或原子)与某些分子或离子(称为配体)以配位键结合形成的化合物称为配位化合物,简称配合物。
如:[Cu(NH3)4]SO4、[Ag(NH3)2]OH等均为配合物。
注意NH4Cl不是配合物。
一、配位化合物
(内外界之间是完全电离的)
[Co(NH3)6] Cl3
内界
外界
K3[Cr(CN)6]
内界
外界
(1)内界与外界
=[Cu(NH3)4]2++SO42-
[Cu(NH3)4] SO4
內界
↓
外界
↓
再例如:
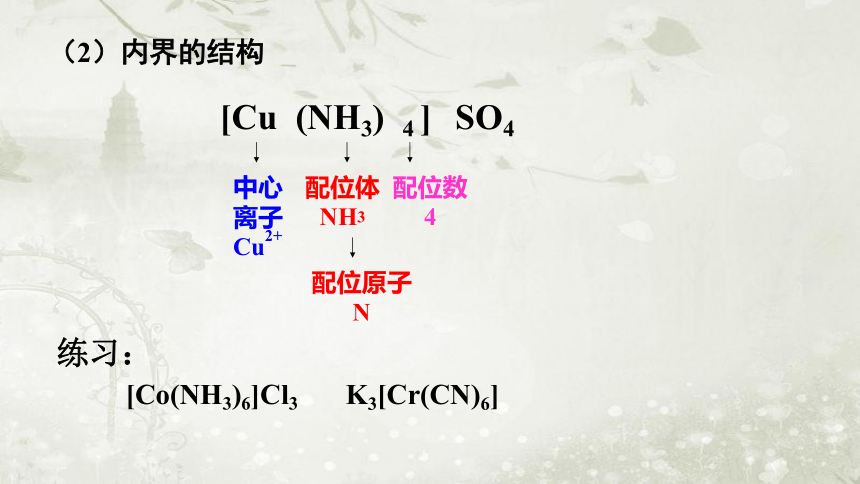
[Cu (NH3) 4 ] SO4
中心
离子
Cu2+
配位体
NH3
配位数
4
(2)内界的结构
配位原子
N
[Co(NH3)6]Cl3
K3[Cr(CN)6]
练习:
1、填空下列配合物的配位数
K[PtCl3(NH3)] 配位数为___
[Co(NH3)4Cl2]Cl 配位数是___
[Co(NH3)5Cl]Cl2 配位数是___
6
配位体不是同一分子或离子时,配位数要两者相加
4
6
3+1=4
4+2=6
5+1=6
练习:
a、中心原子:
Ni(CO)5、Fe(CO)5 中Ni和Fe都是中性原子
b、配位体:
中性分子
配位体中配位原子必须含有孤对电子的原子,如NH3中N,H2O中O。
多为过渡金属阳离子
也有中性原子
极少数阴离子
阴离子
如X-、OH-、SCN-、CN--等
如H2O、NH3、CO等
3、形成配合物的条件
学 以 致 用
现有两种配合物晶体[Co(NH3)6]Cl3和[Co(NH3)5Cl]Cl2,一种为橙黄色,另一种为紫红色。请设计实验方案将两种配合物区别开来。
取相同质量的两种晶体分别配成溶液,向两种溶液中分别滴加硝酸酸化的AgNO3溶液至不再产生沉淀,分别记录滴加的AgNO3溶液的体积。滴加体积多的为[Co(NH3)6]Cl3,滴加体积少的为[Co(NH3)5Cl]Cl2。
3、配合物的结构
(1)配合物的空间结构
一般中心原子的配位数为2、4、6。
(2)配合物的异构现象
含有两种或两种以上配位体的配合物,若配位体在空间的排列方式不同,就能形成不同的几何构型的配合物。
如:Pt(NH3)2Cl2有顺式和反式两种异构体。
极性分子
非极性分子
二、配合物的性质及应用
1.配合物性质:
具有一定的稳定性,配位键越强,配合物越稳定。过渡金属配合物远比主族金属易形成配合物。
(1)银氨溶液
银镜反应→检验葡萄糖
配制银氨溶液时,向AgNO3溶液中滴加氨水,先生成白色沉淀,后沉淀逐渐溶解,生成银氨溶液。
Ag++NH3·H2O=AgOH↓+NH4+
AgOH+2NH3·H2O=[Ag(NH3)2]++OH-+2H2O
2.配合物的应用
(2)检验Fe3+离子
Fe3+与SCN-生成[Fe(SCN)n](3-n)+
血红色
(3)做助熔剂
2 Al2O3(熔融)==4 Al+3 O2↑
电解
加冰晶石Na3[AlF6]降低熔点
在生命体中、医药、配合物与生物固氮、生产生活等中都有很重要的应用。
血红素(Fe2+ )结构示意图
血红素(Fe2+ )结构示意图
CO中毒原因
人体内血红蛋白是Fe2+卟林配合物, Fe2+与O2结合形成配合物,而CO与血红蛋白中的Fe2+能生成更稳定的配合物。发生CO中毒事故,应首先将病人移至通风处,必要时送医院抢救。
在生产中,配合物被广泛应用于染色、电镀、硬水软化、金属冶炼领域。例如,夹心配位化合物二茂铁具有高度的热稳定性,常被用作燃料的催化剂和抗爆剂,它的节能消烟效果也非常好。
配位化合物在羊毛染色过程中的作用
为了使羊毛呈现不同的色彩,同时在洗涤和光照的条件下不易褪色,我们可以在染色过程中,使用金属盐(如铬、铝、铁、铜盐等)对其进行处理。因羊毛和染料中都含有可与金属离子配位的基团(—NH2、—COOH),染色时,金属离子和染料及羊毛之间发生反应,生成体积较大、溶解度小的配合物,使染料坚固地附着在纤维上,从而改变羊毛的颜色。
在生命科学、抗癌药物、催化剂研制、激光材料、超导材料等许多尖端研究领域中,配合物发挥的作用也越来越大。
配合物在生命体中有着非常重要的作用。
许多酶的作用与其结构中含有形成配位键的金属离子有关。
生物体中能量的转换、传递或电荷转移,化学键的形成或断裂以及伴随这些过程出现的能量变化和分配等,常与金属离子和有机体生成的复杂配合物所起的作用有关。
课时小结:
一、配合物的形成条件
配体要提供孤对电子
中心原子提供空轨道
二、配合物的结构
中心原子
配位体
配位数
外界离子
内界
外界
1.(1)配合物[Ag(NH3)2]OH的中心原子是______,配位体是________,配位数是_____,发生电离的电离方程式是______________________。
(2)在配合物[Co(NH3)5Cl]Cl2中,内界是__________,配位体是________,配位数是______。
答案:(1)Ag+ NH3 2 [Ag(NH3)2]OH =[Ag(NH3)2]++OH-
(2)[Co(NH3)5Cl]2+ NH3、Cl- 6
课堂检测
2.下列关于[Cr(H2O)4Br2]Br·2H2O的说法正确的是( )
A.配体为水分子,配位原子为O,外界为Br-
B.中心离子的配位数为6
C.中心离子Cr3+采取sp3杂化
D.中心离子的化合价为+2价
B
课堂检测
3、能区别[Co(NH3)4Cl2]Cl和[Co(NH3)4Cl2]NO3两种溶液的试剂是( )。
A.AgNO3溶液 B.NaOH溶液
C.CCl4 D.浓氨水
A
课堂检测
组织建设
第二单元 配合物的形成和应用
《黄金大劫案》
Au+HNO3+4HCl=H[AuCl4]+NO↑+2H2O
实验现象:
1.滴加氨水后,试管中首先出现蓝色沉淀。
Cu2++2NH3·H2O=Cu(OH)2↓+2NH4+
2.继续滴加氨水,沉淀逐渐溶解,溶液变成深蓝色。
思考:沉淀为什么溶解?深蓝色的可溶物质是什么?
Cu2+与NH3分子中的氮原子通过氮原子提供的孤电子对形成配位键。
配离子[Cu(NH3)4]2+可表示为:
NH3分子:
Cu2+
3d9
有空轨道
配离子[Cu(NH3)4]2+的形成过程:
实验现象:
1.滴加氨水后,试管中首先出现蓝色沉淀。
Cu2++2NH3·H2O=Cu(OH)2↓+2NH4+
2.继续滴加氨水,沉淀逐渐溶解,溶液变成深蓝色。
思考:沉淀为什么溶解?深蓝色的可溶物质是什么?
Cu(OH)2+4NH3·H2O=[Cu(NH3)4]2++2OH-+4H2O
乙醇的作用:(醇析)降低[Cu(NH3)4]SO4的溶解度,利于析出[Cu(NH3)4]SO4·H2O晶体。
思考:为什么无水CuSO4是白色的,而CuSO4·5H2O和CuSO4溶液是蓝色的?
硫酸铜溶液
1、概念:把金属离子(或原子)与某些分子或离子(称为配体)以配位键结合形成的化合物称为配位化合物,简称配合物。
如:[Cu(NH3)4]SO4、[Ag(NH3)2]OH等均为配合物。
注意NH4Cl不是配合物。
一、配位化合物
(内外界之间是完全电离的)
[Co(NH3)6] Cl3
内界
外界
K3[Cr(CN)6]
内界
外界
(1)内界与外界
=[Cu(NH3)4]2++SO42-
[Cu(NH3)4] SO4
內界
↓
外界
↓
再例如:
[Cu (NH3) 4 ] SO4
中心
离子
Cu2+
配位体
NH3
配位数
4
(2)内界的结构
配位原子
N
[Co(NH3)6]Cl3
K3[Cr(CN)6]
练习:
1、填空下列配合物的配位数
K[PtCl3(NH3)] 配位数为___
[Co(NH3)4Cl2]Cl 配位数是___
[Co(NH3)5Cl]Cl2 配位数是___
6
配位体不是同一分子或离子时,配位数要两者相加
4
6
3+1=4
4+2=6
5+1=6
练习:
a、中心原子:
Ni(CO)5、Fe(CO)5 中Ni和Fe都是中性原子
b、配位体:
中性分子
配位体中配位原子必须含有孤对电子的原子,如NH3中N,H2O中O。
多为过渡金属阳离子
也有中性原子
极少数阴离子
阴离子
如X-、OH-、SCN-、CN--等
如H2O、NH3、CO等
3、形成配合物的条件
学 以 致 用
现有两种配合物晶体[Co(NH3)6]Cl3和[Co(NH3)5Cl]Cl2,一种为橙黄色,另一种为紫红色。请设计实验方案将两种配合物区别开来。
取相同质量的两种晶体分别配成溶液,向两种溶液中分别滴加硝酸酸化的AgNO3溶液至不再产生沉淀,分别记录滴加的AgNO3溶液的体积。滴加体积多的为[Co(NH3)6]Cl3,滴加体积少的为[Co(NH3)5Cl]Cl2。
3、配合物的结构
(1)配合物的空间结构
一般中心原子的配位数为2、4、6。
(2)配合物的异构现象
含有两种或两种以上配位体的配合物,若配位体在空间的排列方式不同,就能形成不同的几何构型的配合物。
如:Pt(NH3)2Cl2有顺式和反式两种异构体。
极性分子
非极性分子
二、配合物的性质及应用
1.配合物性质:
具有一定的稳定性,配位键越强,配合物越稳定。过渡金属配合物远比主族金属易形成配合物。
(1)银氨溶液
银镜反应→检验葡萄糖
配制银氨溶液时,向AgNO3溶液中滴加氨水,先生成白色沉淀,后沉淀逐渐溶解,生成银氨溶液。
Ag++NH3·H2O=AgOH↓+NH4+
AgOH+2NH3·H2O=[Ag(NH3)2]++OH-+2H2O
2.配合物的应用
(2)检验Fe3+离子
Fe3+与SCN-生成[Fe(SCN)n](3-n)+
血红色
(3)做助熔剂
2 Al2O3(熔融)==4 Al+3 O2↑
电解
加冰晶石Na3[AlF6]降低熔点
在生命体中、医药、配合物与生物固氮、生产生活等中都有很重要的应用。
血红素(Fe2+ )结构示意图
血红素(Fe2+ )结构示意图
CO中毒原因
人体内血红蛋白是Fe2+卟林配合物, Fe2+与O2结合形成配合物,而CO与血红蛋白中的Fe2+能生成更稳定的配合物。发生CO中毒事故,应首先将病人移至通风处,必要时送医院抢救。
在生产中,配合物被广泛应用于染色、电镀、硬水软化、金属冶炼领域。例如,夹心配位化合物二茂铁具有高度的热稳定性,常被用作燃料的催化剂和抗爆剂,它的节能消烟效果也非常好。
配位化合物在羊毛染色过程中的作用
为了使羊毛呈现不同的色彩,同时在洗涤和光照的条件下不易褪色,我们可以在染色过程中,使用金属盐(如铬、铝、铁、铜盐等)对其进行处理。因羊毛和染料中都含有可与金属离子配位的基团(—NH2、—COOH),染色时,金属离子和染料及羊毛之间发生反应,生成体积较大、溶解度小的配合物,使染料坚固地附着在纤维上,从而改变羊毛的颜色。
在生命科学、抗癌药物、催化剂研制、激光材料、超导材料等许多尖端研究领域中,配合物发挥的作用也越来越大。
配合物在生命体中有着非常重要的作用。
许多酶的作用与其结构中含有形成配位键的金属离子有关。
生物体中能量的转换、传递或电荷转移,化学键的形成或断裂以及伴随这些过程出现的能量变化和分配等,常与金属离子和有机体生成的复杂配合物所起的作用有关。
课时小结:
一、配合物的形成条件
配体要提供孤对电子
中心原子提供空轨道
二、配合物的结构
中心原子
配位体
配位数
外界离子
内界
外界
1.(1)配合物[Ag(NH3)2]OH的中心原子是______,配位体是________,配位数是_____,发生电离的电离方程式是______________________。
(2)在配合物[Co(NH3)5Cl]Cl2中,内界是__________,配位体是________,配位数是______。
答案:(1)Ag+ NH3 2 [Ag(NH3)2]OH =[Ag(NH3)2]++OH-
(2)[Co(NH3)5Cl]2+ NH3、Cl- 6
课堂检测
2.下列关于[Cr(H2O)4Br2]Br·2H2O的说法正确的是( )
A.配体为水分子,配位原子为O,外界为Br-
B.中心离子的配位数为6
C.中心离子Cr3+采取sp3杂化
D.中心离子的化合价为+2价
B
课堂检测
3、能区别[Co(NH3)4Cl2]Cl和[Co(NH3)4Cl2]NO3两种溶液的试剂是( )。
A.AgNO3溶液 B.NaOH溶液
C.CCl4 D.浓氨水
A
课堂检测
