鲁科版高中化学选择性必修1第1章化学反应与能量转化1.2.2化学电源课件(23张)
文档属性
| 名称 | 鲁科版高中化学选择性必修1第1章化学反应与能量转化1.2.2化学电源课件(23张) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-09 00:00:00 | ||
图片预览







文档简介
(共23张PPT)
第2节 化学能转化为电能—电池
第2课时 化学电源
学习目标
1.掌握原电池原理,能用原电池原理解释生活中的化学电源原理。
2.会分析化学电源及新型化学电源的原理,会写出电极反应,会分析离子导体中的离子移动方向。
3、会利用原电池原理设计简单的燃料电池。
*
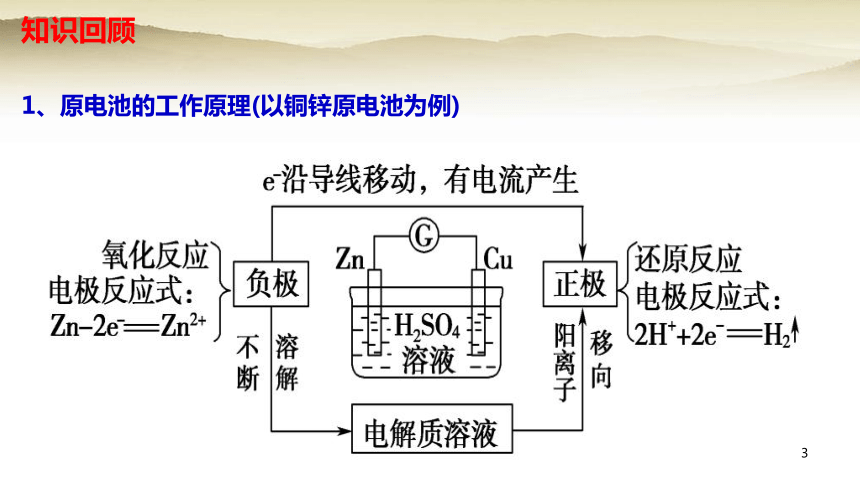
1、原电池的工作原理(以铜锌原电池为例)
知识回顾
*
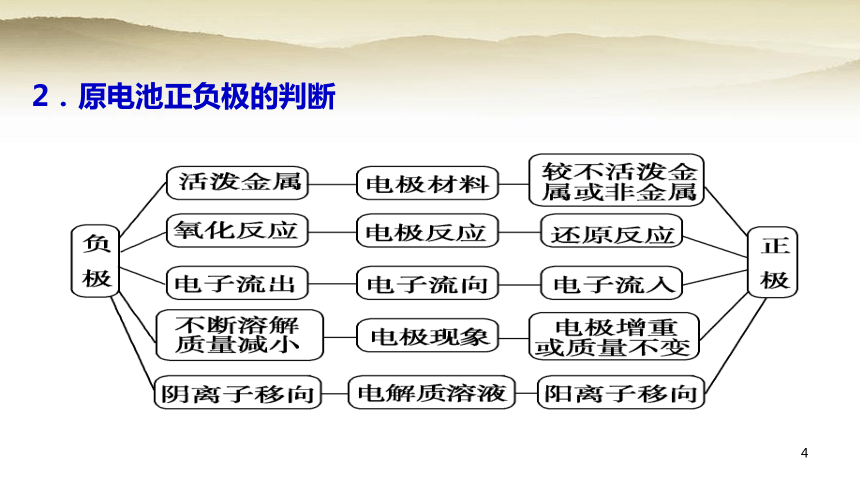
2.原电池正负极的判断
*
*
一、各种化学电源
电极反应方程式:
负极:
正极:
Zn+2OH-–2e-= ZnO+H2O
2MnO2+ 2H2O + 2e- = 2MnO(OH) + 2OH-
反应总的方程式
Zn + 2MnO2+ H2O = ZnO + 2MnO(OH)
⑴碱性锌锰干电池
⑵铅蓄电池
电极反应式:
电池总反应方程式
负极:2H2+4OH--4e-=4H2O
正极:O2+2H2O+4e-=4OH-
电池反应为:2H2+O2=2H2O
⑶碱性氢氧燃料电池
电极反应式:
*
*
1.银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故。根据电化学原理可进行如下处理:在铝质容器中加入食盐溶液,再将变黑的银器漫入该溶液中,一段时间后发现黑色会褪去。下列说法正确的是
A.处理过程中银器一直保持恒重
B.银器为正极,Ag2S被还原生成单质银
C.该过程中总反应为2Al+3Ag2S=6Ag+Al2S3
D.黑色褪去的原因是黑色Ag2S转化为白色AgCl
【答案】B
三、普通原电池
*
2.某原电池总反应的离子方程式为:2Fe3++Fe=3Fe2+,不能实现该反应的原电池是( )
A.正极为Cu,负极为Fe,电解质为FeCl3溶液
B.正极为C,负极为Fe,电解质为Fe(NO3)3溶液
C.正极为Fe,负极为Zn,电解质为Fe2(SO4)3溶液
D.正极为Ag,负极为Fe,电解质为CuSO4溶液
CD
练习
*
1、铜锌原电池(如图)工作时,下列叙述正确的是( )
A.正极反应为Zn-2e-===Zn2+
B.电池反应为Zn+Cu2+===Zn2++Cu
C.在外电路中,电子从负极流向正极
D.盐桥中的K+移向ZnSO4溶液
BC
四、盐桥原电池
*
2.为了避免锌片与Cu2+直接接触发生反应而影响原电池的放电效率,有人设计了如下装置,按要求完成以下填空:
(1)此装置工作时,可以观察到的现象是______________________________
________________________________________,
电池总反应式为_________________________。
(2)以上电池中,锌和锌盐溶液组成__ ______,铜和铜盐溶液组成 ,中间通过盐桥连接起来。
(3)电池工作时,硫酸锌溶液中SO42- 向________移动,硫酸铜溶液中SO42-向________移动。
(4)此盐桥内为饱和KCl溶液,盐桥是通过________移动来导电的。在工作时,K+移向 。
电流计指针发生偏转,
锌片逐渐溶解,铜片上有红色物质析出
Zn+Cu2+=Zn2++Cu
锌半电池
铜半电池
锌电极
盐桥
离子
正极区(CuSO4溶液)
练习
*
3.依据氧化还原反应:2Ag+(aq)+Cu(s)===Cu2+(aq)+2Ag(s)设计的原电池如下图所示。
请回答下列问题:
(1)电极X的材料是____;电解质溶液Y是__________;
(2)银电极为原电池的_ ___极,发生的电极反应为 ;
X电极上发生的电极反应为 ;
(3)外电路中的电子是从_______电极流向_______电极。
Cu
AgNO3
正
Ag+(aq)+e-=Ag(s)
Cu(s)-2e-=Cu2+(aq)
Cu
Ag
练习
*
③当在外电路中通过导线的电子的物质的量为 0.2 mol时;
铜电极质量减少 g, 银电极的质量增加 g;盐桥中有 mol
NO3-进入正极区 ;
练习
Cu-2e-=Cu2+
2Ag++2e-=2Ag
6.4
21.6
0.2
*
五、燃料原电池
*
1、一种新型的燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极通入乙烷和氧气,其总反应为:
2C2H6+7O2+8KOH==4K2CO3+10H2O
有关此电池的推断正确的是( )
A.负极反应为14H2O+7O2+28e-==28OH-
B.放电一段时间后,负极周围的pH升高
C.每消耗1molC2H6,则电路上转移的电子为14mol
D.放电过程中KOH的物质的量浓度不变
C
五、燃料原电池
*
2、乙醇燃料电池中采用磺酸类质子溶剂,在200 ℃左右时供电,电池总反应式为C2H5OH+3O2 =2CO2+3H2O,电池示意图如图所示,下列说法中正确的是( )
A.电池工作时,质子向电池的负极迁移
B.电池工作时,电流由b极沿导线流向a极
C.a极上发生的电极反应是
C2H5OH+3H2O+12e-=2CO2↑+12H+
D.b极上发生的电极反应是
2H2O+O2+4e-=4OH-
B
练习
*
3.瓦斯分析仪(如图甲)工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动。下列有关叙述中正确的是( )
A.瓦斯分析仪工作时,电池内电路中电子由电极b流向电极a
B.电极b是正极,O2-由电极a流向电极b
C.电极a的反应式为CH4+4O2--8e-===CO2+2H2O
D.当固体电解质中有1 mol O2-通过时,转移4 mol电子
C
*
4、用两根铂丝作为电极插入KOH溶液中,再分别向两极通入甲烷气体和氧气,可形成原电池—燃料电池,该电池放电时发生的反应为CH4+2KOH+2O2===K2CO3+3H2O。下列说法错误的是( )
A.通甲烷的一极为负极,通氧气的一极为正极
B.放电时,通入O2一极附近溶液的pH升高
C.放电一段时间后,KOH的物质的量不发生变化
D.通甲烷极的电极反应式是CH4+10OH--8e-=== CO32-+7H2O
C
练习
*
5、高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:
3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
A.放电时负极反应为Zn-2e-+2OH-=Zn(OH)2
B.充电时阳极反应为Fe(OH)3-3e-+5OH-=FeO42- +4H2O
C.放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化
D.放电时正极附近溶液的碱性增强
C
练习
*
6、原电池是化学对人类的一项重大贡献。
(1)如图是甲烷燃料电池原理示意图,回答下列问题:
①电池的负极是 (填“a”或“b”)电极,该极的电极
反应 。
②电池工作一段时间后电解质溶液的pH (填“增大”
“减小”或“不变”)。
CH4+10OH--8e-=CO32- +7H2O
减小
a
练习
*
六、“有膜” 原电池
离子交换膜的类型
(1)阳离子交换膜:只允许阳离子通过;
(2)阴离子交换膜:只允许阴离子通过;
(3)质子交换膜:只允许质子通过。
*
1.锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )
A.铜电极上发生氧化反应
B.电池工作一段时间后,甲池的c(SO42-)减小
C.电池工作一段时间后,乙池溶液的总质量增加
D.阴阳离子离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
C
*
1、我国科学家报道了如图所示的水溶液锂离子电池体系。下列叙述错误的是( )
A.a为电池的正极
B.电池充电反应为LiMn2O4===Li1-xMn2O4+xLi
C.放电时,a极锂的化合价发生变化
D.放电时,溶液中Li+从b向a迁移
C
七、“新型”原电池
*
第2节 化学能转化为电能—电池
第2课时 化学电源
学习目标
1.掌握原电池原理,能用原电池原理解释生活中的化学电源原理。
2.会分析化学电源及新型化学电源的原理,会写出电极反应,会分析离子导体中的离子移动方向。
3、会利用原电池原理设计简单的燃料电池。
*
1、原电池的工作原理(以铜锌原电池为例)
知识回顾
*
2.原电池正负极的判断
*
*
一、各种化学电源
电极反应方程式:
负极:
正极:
Zn+2OH-–2e-= ZnO+H2O
2MnO2+ 2H2O + 2e- = 2MnO(OH) + 2OH-
反应总的方程式
Zn + 2MnO2+ H2O = ZnO + 2MnO(OH)
⑴碱性锌锰干电池
⑵铅蓄电池
电极反应式:
电池总反应方程式
负极:2H2+4OH--4e-=4H2O
正极:O2+2H2O+4e-=4OH-
电池反应为:2H2+O2=2H2O
⑶碱性氢氧燃料电池
电极反应式:
*
*
1.银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故。根据电化学原理可进行如下处理:在铝质容器中加入食盐溶液,再将变黑的银器漫入该溶液中,一段时间后发现黑色会褪去。下列说法正确的是
A.处理过程中银器一直保持恒重
B.银器为正极,Ag2S被还原生成单质银
C.该过程中总反应为2Al+3Ag2S=6Ag+Al2S3
D.黑色褪去的原因是黑色Ag2S转化为白色AgCl
【答案】B
三、普通原电池
*
2.某原电池总反应的离子方程式为:2Fe3++Fe=3Fe2+,不能实现该反应的原电池是( )
A.正极为Cu,负极为Fe,电解质为FeCl3溶液
B.正极为C,负极为Fe,电解质为Fe(NO3)3溶液
C.正极为Fe,负极为Zn,电解质为Fe2(SO4)3溶液
D.正极为Ag,负极为Fe,电解质为CuSO4溶液
CD
练习
*
1、铜锌原电池(如图)工作时,下列叙述正确的是( )
A.正极反应为Zn-2e-===Zn2+
B.电池反应为Zn+Cu2+===Zn2++Cu
C.在外电路中,电子从负极流向正极
D.盐桥中的K+移向ZnSO4溶液
BC
四、盐桥原电池
*
2.为了避免锌片与Cu2+直接接触发生反应而影响原电池的放电效率,有人设计了如下装置,按要求完成以下填空:
(1)此装置工作时,可以观察到的现象是______________________________
________________________________________,
电池总反应式为_________________________。
(2)以上电池中,锌和锌盐溶液组成__ ______,铜和铜盐溶液组成 ,中间通过盐桥连接起来。
(3)电池工作时,硫酸锌溶液中SO42- 向________移动,硫酸铜溶液中SO42-向________移动。
(4)此盐桥内为饱和KCl溶液,盐桥是通过________移动来导电的。在工作时,K+移向 。
电流计指针发生偏转,
锌片逐渐溶解,铜片上有红色物质析出
Zn+Cu2+=Zn2++Cu
锌半电池
铜半电池
锌电极
盐桥
离子
正极区(CuSO4溶液)
练习
*
3.依据氧化还原反应:2Ag+(aq)+Cu(s)===Cu2+(aq)+2Ag(s)设计的原电池如下图所示。
请回答下列问题:
(1)电极X的材料是____;电解质溶液Y是__________;
(2)银电极为原电池的_ ___极,发生的电极反应为 ;
X电极上发生的电极反应为 ;
(3)外电路中的电子是从_______电极流向_______电极。
Cu
AgNO3
正
Ag+(aq)+e-=Ag(s)
Cu(s)-2e-=Cu2+(aq)
Cu
Ag
练习
*
③当在外电路中通过导线的电子的物质的量为 0.2 mol时;
铜电极质量减少 g, 银电极的质量增加 g;盐桥中有 mol
NO3-进入正极区 ;
练习
Cu-2e-=Cu2+
2Ag++2e-=2Ag
6.4
21.6
0.2
*
五、燃料原电池
*
1、一种新型的燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极通入乙烷和氧气,其总反应为:
2C2H6+7O2+8KOH==4K2CO3+10H2O
有关此电池的推断正确的是( )
A.负极反应为14H2O+7O2+28e-==28OH-
B.放电一段时间后,负极周围的pH升高
C.每消耗1molC2H6,则电路上转移的电子为14mol
D.放电过程中KOH的物质的量浓度不变
C
五、燃料原电池
*
2、乙醇燃料电池中采用磺酸类质子溶剂,在200 ℃左右时供电,电池总反应式为C2H5OH+3O2 =2CO2+3H2O,电池示意图如图所示,下列说法中正确的是( )
A.电池工作时,质子向电池的负极迁移
B.电池工作时,电流由b极沿导线流向a极
C.a极上发生的电极反应是
C2H5OH+3H2O+12e-=2CO2↑+12H+
D.b极上发生的电极反应是
2H2O+O2+4e-=4OH-
B
练习
*
3.瓦斯分析仪(如图甲)工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动。下列有关叙述中正确的是( )
A.瓦斯分析仪工作时,电池内电路中电子由电极b流向电极a
B.电极b是正极,O2-由电极a流向电极b
C.电极a的反应式为CH4+4O2--8e-===CO2+2H2O
D.当固体电解质中有1 mol O2-通过时,转移4 mol电子
C
*
4、用两根铂丝作为电极插入KOH溶液中,再分别向两极通入甲烷气体和氧气,可形成原电池—燃料电池,该电池放电时发生的反应为CH4+2KOH+2O2===K2CO3+3H2O。下列说法错误的是( )
A.通甲烷的一极为负极,通氧气的一极为正极
B.放电时,通入O2一极附近溶液的pH升高
C.放电一段时间后,KOH的物质的量不发生变化
D.通甲烷极的电极反应式是CH4+10OH--8e-=== CO32-+7H2O
C
练习
*
5、高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:
3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
A.放电时负极反应为Zn-2e-+2OH-=Zn(OH)2
B.充电时阳极反应为Fe(OH)3-3e-+5OH-=FeO42- +4H2O
C.放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化
D.放电时正极附近溶液的碱性增强
C
练习
*
6、原电池是化学对人类的一项重大贡献。
(1)如图是甲烷燃料电池原理示意图,回答下列问题:
①电池的负极是 (填“a”或“b”)电极,该极的电极
反应 。
②电池工作一段时间后电解质溶液的pH (填“增大”
“减小”或“不变”)。
CH4+10OH--8e-=CO32- +7H2O
减小
a
练习
*
六、“有膜” 原电池
离子交换膜的类型
(1)阳离子交换膜:只允许阳离子通过;
(2)阴离子交换膜:只允许阴离子通过;
(3)质子交换膜:只允许质子通过。
*
1.锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )
A.铜电极上发生氧化反应
B.电池工作一段时间后,甲池的c(SO42-)减小
C.电池工作一段时间后,乙池溶液的总质量增加
D.阴阳离子离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
C
*
1、我国科学家报道了如图所示的水溶液锂离子电池体系。下列叙述错误的是( )
A.a为电池的正极
B.电池充电反应为LiMn2O4===Li1-xMn2O4+xLi
C.放电时,a极锂的化合价发生变化
D.放电时,溶液中Li+从b向a迁移
C
七、“新型”原电池
*
同课章节目录
- 第1章 化学反应与能量转化
- 第1节 化学反应的热效应
- 第2节 化学能转化为电能——电池
- 第3节 电能转化为化学能——电解
- 第4节 金属的腐蚀与防护
- 微项目 设计载人航天器用化学电池与氧气再生方案——化学反应中能量及物质的转化利用
- 第2章 化学反应的方向、 限度与速率
- 第1节 化学反应的方向
- 第2节 化学反应的限度
- 第3节 化学反应的速率
- 第4节 化学反应条件的优化——工业合成氨
- 微项目 探讨如何利用工业废气中的二氧化碳合成甲醇——化学反应选择与反应条件优化
- 第3章 物质在水溶液中的行为
- 第1节 水与水溶液
- 第2节 弱电解质的电离 盐类的水解
- 第3节 沉淀溶解平衡
- 第4节 离子反应
- 微项目 揭秘索尔维制碱法和侯氏制碱法——化学平衡思想的创造性应用
