鲁科版高中化学选择性必修1第3章物质在水溶液中的行为3.2.3盐类水解平衡的移动盐类水解的应用课件(21张)
文档属性
| 名称 | 鲁科版高中化学选择性必修1第3章物质在水溶液中的行为3.2.3盐类水解平衡的移动盐类水解的应用课件(21张) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-09 00:00:00 | ||
图片预览




文档简介
(共21张PPT)
第2节 弱电解质的电离 盐类水解
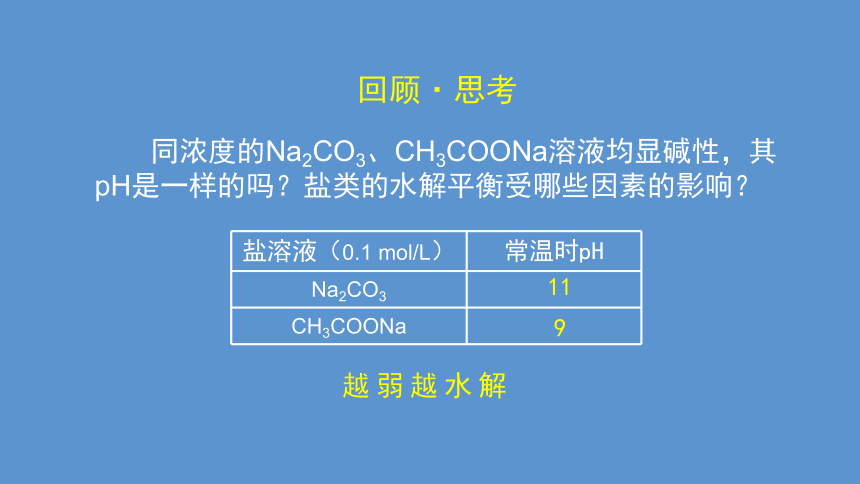
回顾·思考
越弱越水解
同浓度的Na2CO3、CH3COONa溶液均显碱性,其pH是一样的吗?盐类的水解平衡受哪些因素的影响?
盐溶液(0.1 mol/L) 常温时pH
Na2CO3
CH3COONa
11
9
水解程度影响因素
内因:盐本身的性质
外因:
?
同浓度的Na2CO3、CH3COONa溶液均显碱性,其pH是一样的吗?盐类的水解平衡受哪些因素的影响?
回顾·思考
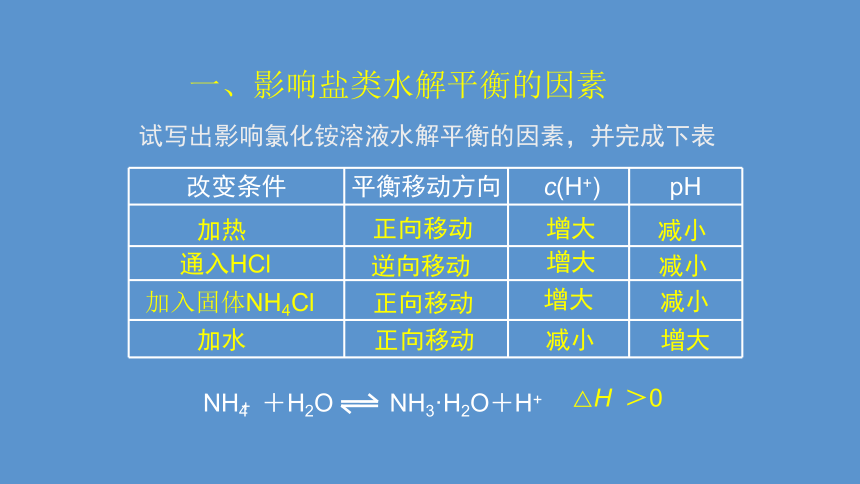
改变条件 平衡移动方向 c(H+) pH
NH4 +H2O NH3·H2O+H+
一、影响盐类水解平衡的因素
加热
通入HCl
加入固体NH4Cl
加水
正向移动
逆向移动
正向移动
增大
增大
增大
减小
减小
减小
△H >0
试写出影响氯化铵溶液水解平衡的因素,并完成下表
+
正向移动
减小
增大
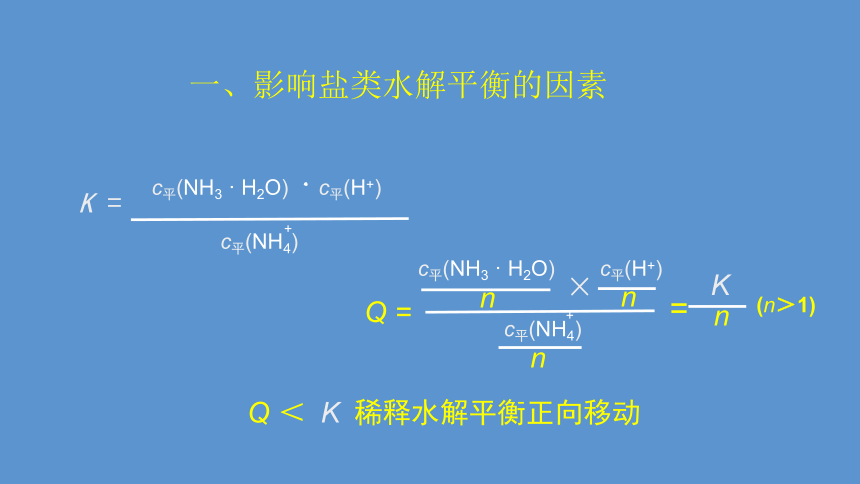
K =
c平(NH3 · H2O) · c平(H+)
c平(NH4)
Q < K 稀释水解平衡正向移动
c平(NH3 · H2O) c平(H+)
Q =
c平(NH4)
n
n
n
×
K
n
=
(n>1)
一、影响盐类水解平衡的因素
+
+
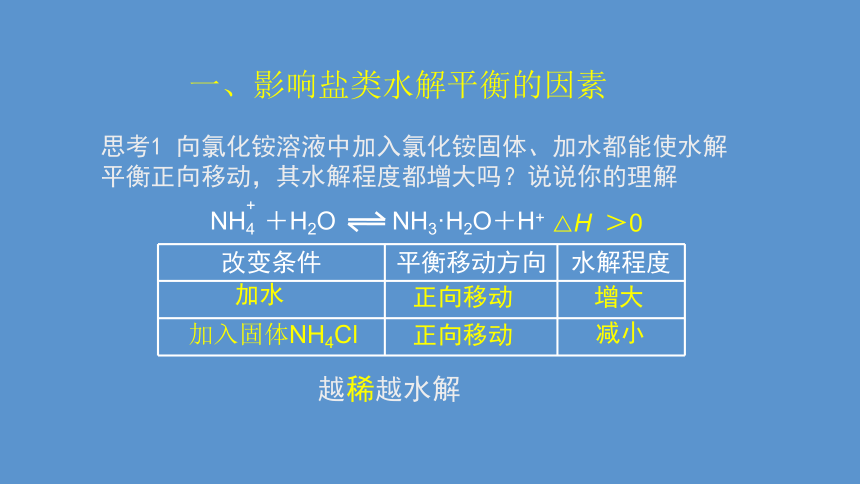
思考1 向氯化铵溶液中加入氯化铵固体、加水都能使水解平衡正向移动,其水解程度都增大吗?说说你的理解
改变条件 平衡移动方向 水解程度
加水
正向移动
增大
加入固体NH4Cl
正向移动
减小
越稀越水解
NH4 +H2O NH3·H2O+H+
△H >0
+
一、影响盐类水解平衡的因素
小结
内因:
外因:
越弱越水解
越热越水解
越稀越水解
促进或抑制水解
盐的本性
温度
盐溶液浓度
溶液酸碱性
(勒夏特列原理)
一、影响盐类水解平衡的因素
二、运用盐类水解的知识分析解决问题
思考2 你能用水解平衡的知识解释泡沫灭火器的灭火原理吗?
资料卡片
泡沫灭火器中装有NaHCO3浓溶液和Al2(SO4)3浓溶液。二者混合时会发生剧烈反应,产生气体和沉淀,在起泡剂的作用下迅速产生大量泡沫,用以灭火。
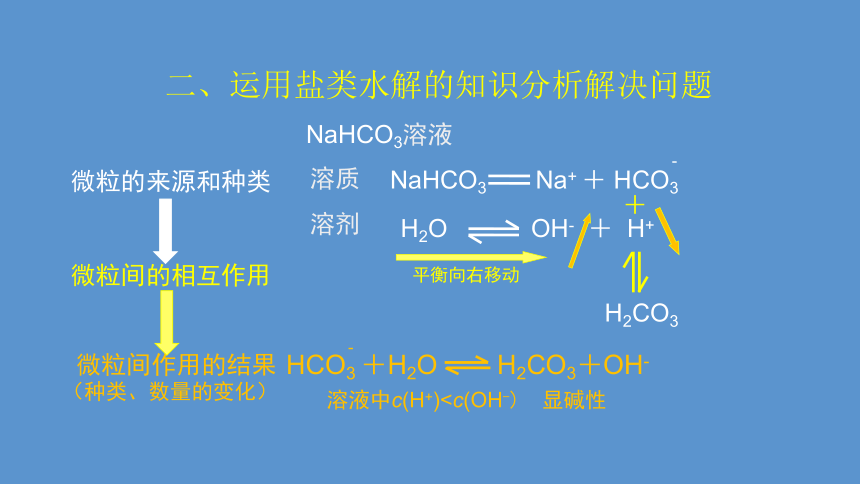
NaHCO3溶液
Al2(SO4)3溶液
H2O OH- + H+
溶剂
溶质
+
微粒的来源和种类
微粒间的相互作用
微粒间作用的结果
平衡向右移动
溶液中c(H+)H2CO3
NaHCO3溶液
(种类、数量的变化)
NaHCO3 Na+ + HCO3
-
HCO3 +H2O H2CO3+OH-
-
二、运用盐类水解的知识分析解决问题
H2O H+ + OH-
溶剂
溶质
+
微粒的来源和种类
微粒间的相互作用
微粒间作用的结果
平衡向右移动
溶液中c(H+)>c(OH-) 显酸性
Al3++3H2O Al(OH)3+3H+
Al(OH)3
Al2(SO4)3溶液
(种类、数量的变化)
Al2(SO4)3 3SO4+ 2Al3+
2-
二、运用盐类水解的知识分析解决问题
Al3++3H2O Al(OH)3 +3 H+
NaHCO3溶液
Al2(SO4)3溶液
H2O + CO2
H2O
+
NaHCO3溶液与Al2(SO4)3溶液的混合
平衡向
右移动
HCO3 +H2O H2CO3 + OH-
-
3HCO3 + Al3+ Al(OH)3 + 3CO2
-
二、运用盐类水解的知识分析解决问题
微粒的来源和种类
微粒间的相互作用
微粒间作用的结果
微观分析角度
问题解决思路
找“弱”离子,建立水解平衡。多种“弱”离子水解相互影响
溶质、溶剂的电离
平衡移动,微粒种类、数量的变化,现象变化
二、运用盐类水解的知识分析解决问题
思考3 硫化铝固体溶于水后会产生什么现象?
Al3++3H2O 3 H+ + Al(OH)3
S2-+H2O OH- + HS-
HS- +H2O OH- + H2S
H2O
Al2S3 3S2- + 2Al3+
+
+
平衡向
右移动
Al2S3 + 6H2O 2Al(OH)3 + 3H2S
二、运用盐类水解的知识分析解决问题
现象:同时产生沉淀和气体
硫化铝(Al2S3)等盐,其阴、阳离子都能水解并分别生成气体和沉淀,因此这样的盐在水中是不能存在的。
Al2S3 + 6H2O 2Al(OH)3 + 3H2S
思考3 硫化铝固体溶于水后会产生什么现象?
二、运用盐类水解的知识分析解决问题
CH3COO- + H2O CH3COOH + OH-
+
H2O
CH3COO- + NH4+ + H2O NH3·H2O + CH3COOH
思考4 醋酸铵固体溶于水后,醋酸根和铵根离子都能水解,其水溶液能稳定存在吗?
平衡向
右移动
能够稳定存在
NH4 + H2O NH3·H2O + H+
+
二、运用盐类水解的知识分析解决问题
弱酸的酸根离子和弱碱的阳离子在同一溶液中,水解反应会相互促进。当同时产生沉淀和气体时,水解完全。
Al2S3 + 6H2O 2Al(OH)3 + 3H2S
CH3COO- + NH4+ + H2O NH3·H2O + CH3COOH
部分水解
水解完全
水解完全
3HCO3 + Al3+ Al(OH)3 + 3CO2
-
二、运用盐类水解的知识分析解决问题
铵态氮肥中NH4 水解:NH4+H2O NH3·H2O+H+
当二者混合时,两个水解反应相互促进,NH4 转化为NH3·H2O,
分解产生氨气逸出,造成氮肥损失。
+
草木灰中CO3 水解:CO3 +H2O HCO3+OH-
思考·交流
铵态氮肥与草木灰(成分含有K2CO3)混合使用会大大降低氮肥的肥效,原因是什么?
结合化学用语解释下列事实:
+
2-
-
2-
+
你知道生活和生产实践中应用到的盐类的水解知识的实例吗?说说其中的原理。
三、盐类水解的应用
1.实验室制备氢氧化铁胶体
Fe3+ + 3H2O Fe(OH)3 + 3H+
Fe3+ + 3H2O Fe(OH)3(胶体)+ 3H+
加热,促进水解,生成氢氧化铁胶体
△
2.明矾净水
三、盐类水解的应用
Al3+ + 3H2O Al(OH)3 + 3H+
Al3+ + 3H2O Al(OH)3(胶体)+ 3H+
Al3+与HCO3水解互促,生成氢氧化铝胶体
-
天然水(含HCO3离子)
-
你知道生活和生产实践中应用到的盐类的水解知识的实例吗?说说其中的原理。
三、盐类水解的应用
3.热碱水除油污
CO3 水解:CO3 +H2O HCO3+OH-
2-
-
2-
HCO3 +H2O H2CO3 + OH-
-
加热促进水解,碱性增强,利用碱性除油污
你知道生活和生产实践中应用到的盐类的水解知识的实例吗?说说其中的原理。
概括·整合
内因:
外因:
盐的本性
温度
盐溶液浓度
溶液酸碱性
调控平衡
分析解决问题
实际应用
盐类的水解平衡
第2节 弱电解质的电离 盐类水解
回顾·思考
越弱越水解
同浓度的Na2CO3、CH3COONa溶液均显碱性,其pH是一样的吗?盐类的水解平衡受哪些因素的影响?
盐溶液(0.1 mol/L) 常温时pH
Na2CO3
CH3COONa
11
9
水解程度影响因素
内因:盐本身的性质
外因:
?
同浓度的Na2CO3、CH3COONa溶液均显碱性,其pH是一样的吗?盐类的水解平衡受哪些因素的影响?
回顾·思考
改变条件 平衡移动方向 c(H+) pH
NH4 +H2O NH3·H2O+H+
一、影响盐类水解平衡的因素
加热
通入HCl
加入固体NH4Cl
加水
正向移动
逆向移动
正向移动
增大
增大
增大
减小
减小
减小
△H >0
试写出影响氯化铵溶液水解平衡的因素,并完成下表
+
正向移动
减小
增大
K =
c平(NH3 · H2O) · c平(H+)
c平(NH4)
Q < K 稀释水解平衡正向移动
c平(NH3 · H2O) c平(H+)
Q =
c平(NH4)
n
n
n
×
K
n
=
(n>1)
一、影响盐类水解平衡的因素
+
+
思考1 向氯化铵溶液中加入氯化铵固体、加水都能使水解平衡正向移动,其水解程度都增大吗?说说你的理解
改变条件 平衡移动方向 水解程度
加水
正向移动
增大
加入固体NH4Cl
正向移动
减小
越稀越水解
NH4 +H2O NH3·H2O+H+
△H >0
+
一、影响盐类水解平衡的因素
小结
内因:
外因:
越弱越水解
越热越水解
越稀越水解
促进或抑制水解
盐的本性
温度
盐溶液浓度
溶液酸碱性
(勒夏特列原理)
一、影响盐类水解平衡的因素
二、运用盐类水解的知识分析解决问题
思考2 你能用水解平衡的知识解释泡沫灭火器的灭火原理吗?
资料卡片
泡沫灭火器中装有NaHCO3浓溶液和Al2(SO4)3浓溶液。二者混合时会发生剧烈反应,产生气体和沉淀,在起泡剂的作用下迅速产生大量泡沫,用以灭火。
NaHCO3溶液
Al2(SO4)3溶液
H2O OH- + H+
溶剂
溶质
+
微粒的来源和种类
微粒间的相互作用
微粒间作用的结果
平衡向右移动
溶液中c(H+)
NaHCO3溶液
(种类、数量的变化)
NaHCO3 Na+ + HCO3
-
HCO3 +H2O H2CO3+OH-
-
二、运用盐类水解的知识分析解决问题
H2O H+ + OH-
溶剂
溶质
+
微粒的来源和种类
微粒间的相互作用
微粒间作用的结果
平衡向右移动
溶液中c(H+)>c(OH-) 显酸性
Al3++3H2O Al(OH)3+3H+
Al(OH)3
Al2(SO4)3溶液
(种类、数量的变化)
Al2(SO4)3 3SO4+ 2Al3+
2-
二、运用盐类水解的知识分析解决问题
Al3++3H2O Al(OH)3 +3 H+
NaHCO3溶液
Al2(SO4)3溶液
H2O + CO2
H2O
+
NaHCO3溶液与Al2(SO4)3溶液的混合
平衡向
右移动
HCO3 +H2O H2CO3 + OH-
-
3HCO3 + Al3+ Al(OH)3 + 3CO2
-
二、运用盐类水解的知识分析解决问题
微粒的来源和种类
微粒间的相互作用
微粒间作用的结果
微观分析角度
问题解决思路
找“弱”离子,建立水解平衡。多种“弱”离子水解相互影响
溶质、溶剂的电离
平衡移动,微粒种类、数量的变化,现象变化
二、运用盐类水解的知识分析解决问题
思考3 硫化铝固体溶于水后会产生什么现象?
Al3++3H2O 3 H+ + Al(OH)3
S2-+H2O OH- + HS-
HS- +H2O OH- + H2S
H2O
Al2S3 3S2- + 2Al3+
+
+
平衡向
右移动
Al2S3 + 6H2O 2Al(OH)3 + 3H2S
二、运用盐类水解的知识分析解决问题
现象:同时产生沉淀和气体
硫化铝(Al2S3)等盐,其阴、阳离子都能水解并分别生成气体和沉淀,因此这样的盐在水中是不能存在的。
Al2S3 + 6H2O 2Al(OH)3 + 3H2S
思考3 硫化铝固体溶于水后会产生什么现象?
二、运用盐类水解的知识分析解决问题
CH3COO- + H2O CH3COOH + OH-
+
H2O
CH3COO- + NH4+ + H2O NH3·H2O + CH3COOH
思考4 醋酸铵固体溶于水后,醋酸根和铵根离子都能水解,其水溶液能稳定存在吗?
平衡向
右移动
能够稳定存在
NH4 + H2O NH3·H2O + H+
+
二、运用盐类水解的知识分析解决问题
弱酸的酸根离子和弱碱的阳离子在同一溶液中,水解反应会相互促进。当同时产生沉淀和气体时,水解完全。
Al2S3 + 6H2O 2Al(OH)3 + 3H2S
CH3COO- + NH4+ + H2O NH3·H2O + CH3COOH
部分水解
水解完全
水解完全
3HCO3 + Al3+ Al(OH)3 + 3CO2
-
二、运用盐类水解的知识分析解决问题
铵态氮肥中NH4 水解:NH4+H2O NH3·H2O+H+
当二者混合时,两个水解反应相互促进,NH4 转化为NH3·H2O,
分解产生氨气逸出,造成氮肥损失。
+
草木灰中CO3 水解:CO3 +H2O HCO3+OH-
思考·交流
铵态氮肥与草木灰(成分含有K2CO3)混合使用会大大降低氮肥的肥效,原因是什么?
结合化学用语解释下列事实:
+
2-
-
2-
+
你知道生活和生产实践中应用到的盐类的水解知识的实例吗?说说其中的原理。
三、盐类水解的应用
1.实验室制备氢氧化铁胶体
Fe3+ + 3H2O Fe(OH)3 + 3H+
Fe3+ + 3H2O Fe(OH)3(胶体)+ 3H+
加热,促进水解,生成氢氧化铁胶体
△
2.明矾净水
三、盐类水解的应用
Al3+ + 3H2O Al(OH)3 + 3H+
Al3+ + 3H2O Al(OH)3(胶体)+ 3H+
Al3+与HCO3水解互促,生成氢氧化铝胶体
-
天然水(含HCO3离子)
-
你知道生活和生产实践中应用到的盐类的水解知识的实例吗?说说其中的原理。
三、盐类水解的应用
3.热碱水除油污
CO3 水解:CO3 +H2O HCO3+OH-
2-
-
2-
HCO3 +H2O H2CO3 + OH-
-
加热促进水解,碱性增强,利用碱性除油污
你知道生活和生产实践中应用到的盐类的水解知识的实例吗?说说其中的原理。
概括·整合
内因:
外因:
盐的本性
温度
盐溶液浓度
溶液酸碱性
调控平衡
分析解决问题
实际应用
盐类的水解平衡
同课章节目录
- 第1章 化学反应与能量转化
- 第1节 化学反应的热效应
- 第2节 化学能转化为电能——电池
- 第3节 电能转化为化学能——电解
- 第4节 金属的腐蚀与防护
- 微项目 设计载人航天器用化学电池与氧气再生方案——化学反应中能量及物质的转化利用
- 第2章 化学反应的方向、 限度与速率
- 第1节 化学反应的方向
- 第2节 化学反应的限度
- 第3节 化学反应的速率
- 第4节 化学反应条件的优化——工业合成氨
- 微项目 探讨如何利用工业废气中的二氧化碳合成甲醇——化学反应选择与反应条件优化
- 第3章 物质在水溶液中的行为
- 第1节 水与水溶液
- 第2节 弱电解质的电离 盐类的水解
- 第3节 沉淀溶解平衡
- 第4节 离子反应
- 微项目 揭秘索尔维制碱法和侯氏制碱法——化学平衡思想的创造性应用
