人教版高中化学必修第一册第四章物质结构元素周期律4.1.1原子结构教学课件
文档属性
| 名称 | 人教版高中化学必修第一册第四章物质结构元素周期律4.1.1原子结构教学课件 |  | |
| 格式 | ppt | ||
| 文件大小 | 10.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-11 19:47:16 | ||
图片预览










文档简介
(共44张PPT)
第四章 第一节 第一课时
《原子结构》
春秋战国时期,墨子、惠子等哲学家同样从不同角度提出了物质有不能再分的最小单位的观点。
公元前450年以前,古希腊哲学家德谟克利特提出,宇宙万物都是由最微小、坚硬、不可入,不可分割的物质粒子所构成的。这种粒子就是原子。
化学史话/ CHEMISTRY HISTORY
道尔顿模型(1803年)
英国化学家道尔顿提出:原子是构成物质的基本粒子,它们是坚实的、不可分割的实心球体
化学史话/ CHEMISTRY HISTORY
化学史话/ CHEMISTRY HISTORY
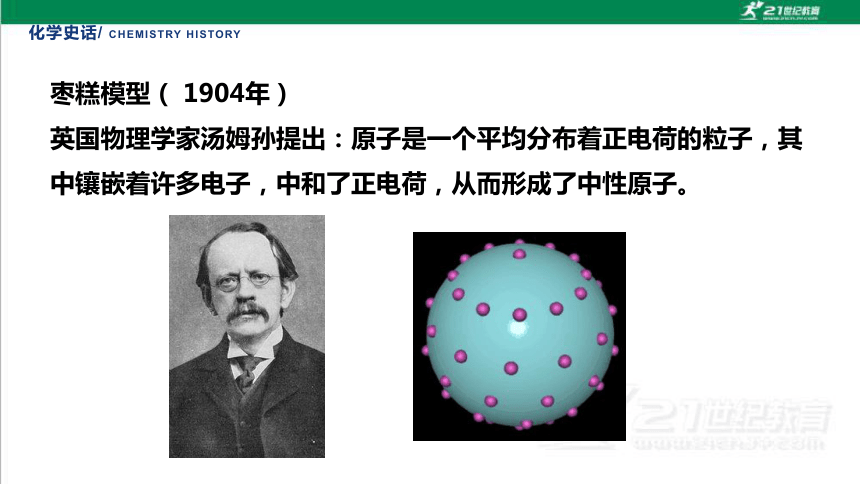
枣糕模型( 1904年)
英国物理学家汤姆孙提出:原子是一个平均分布着正电荷的粒子,其中镶嵌着许多电子,中和了正电荷,从而形成了中性原子。
卢瑟福原子模型(1911年)
物理学家卢瑟福提出:在原子的中心有一个带正电荷的核,它的质量几乎等于原子的全部质量,电子在它的周围沿着不同的轨道运转,就像行星围绕太阳运转一样。
化学史话/ CHEMISTRY HISTORY
化学史话/ CHEMISTRY HISTORY
玻尔原子结构模型(1913年)
丹麦物理学家玻尔:电子在原子核外空间的一定轨道上绕核做高速圆周运动。
化学史话/ CHEMISTRY HISTORY
电子云模型(1926年)
奥地利物理学家薛定谔等以量子力学为基础提出电子云模型
一、原子的结构
原子
原子核
核外电子:
中子:
质子:
原子序数=核电荷数=质子数=核外电子数
带1个单位正电荷
不带电
带1个单位负电荷
原子结构/ ATOM STRUCTURE
一、原子的结构
(2)质量关系:质量数(A)=质子数(Z)+中子数(N)。
1.质量数
(1)概念:将原子核内所有质子和中子的相对质量取近似整数值相加,所得的数值叫做质量数,常用A表示。
原子结构/ ATOM STRUCTURE
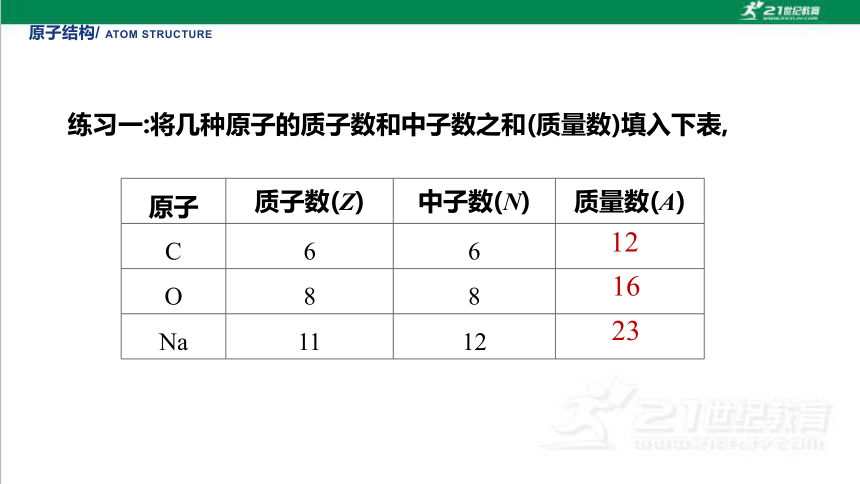
原子 质子数(Z) 中子数(N) 质量数(A)
C 6 6
O 8 8
Na 11 12
12
16
23
练习一:将几种原子的质子数和中子数之和(质量数)填入下表,
原子结构/ ATOM STRUCTURE
一、原子的结构
2.原子符号
表示的意义是质子数为Z,质量数为A的X元素的一种_____。
原子
原子结构/ ATOM STRUCTURE
2008年,冲绳科学技术大学院大学的科学家们用他们的“飞秒照相机”成功地首次拍到了材料内部电子的运动轨迹,再度实现了突破。
化学史话/ CHEMISTRY HISTORY
一、原子的结构
3.核外电子排布——能量规律
各电子层由内到外 电子层数 1 2 3 4 5 6 7
字母代号 K L M N O P Q
离核远近 由____到____
能量高低 由____到____
原子结构/ ATOM STRUCTURE
近
远
低
高
核外电子由里向外,依次排布在能量逐渐_____的电子层里,即按K→L→M→ N……顺序排列。
升高
思考并填空:
核电荷数 元素名称 元素符号 各电子层的电子数
K L M N O P
2 氦 He 2
10 氖 Ne 2 8
18 氩 Ar 2 8 8
36 氪 Kr 2 8 18 8
54 氙 Xe 2 8 18 18 8
86 氡 Rn 2 8 18 32 18 8
当K层为最外层时,最多能容纳的电子数是多少?
除了K层,其他各层为最外层时,最多能容纳的电子数是多少?
原子结构/ ATOM STRUCTURE
(2)最外层电子数目最多不能超过____个(K层为最外层时不能超过2个)。
(1)各电子层最多容纳____个电子(n表示电子层数)。
一、原子的结构
4.核外电子排布——数量规律
2n2
8
(3)次外层最多能容纳的电子数不超过____个。
18
原子结构/ ATOM STRUCTURE
将Na、K的原子结构示意图分别写成 正确吗?若不正确,请说明原因。
原子结构/ ATOM STRUCTURE
一、原子的结构
5.原子结构示意图
练习二:画出下列原子或离子的结构示意图。
①S______, S2-_______;
②Ca_______,Ca2+_______。
练习三:请同学们课下画出1-20号元素原子结构示意图
原子结构/ ATOM STRUCTURE
法国化学家拉瓦锡
(1743-1794)
1789年在《化学概要》中提出了第一张元素分类表。
一、元素周期表的发展历程
1775
1800
1825
1850
1875
1900
1925
年
法国化学家拉瓦锡
(1743-1794)
1789年在《化学概要》中提出了第一个元素分类表。
一、元素周期表的发展历程
1775
1800
1825
1850
1875
1900
1925
年
德国化学家德贝莱纳
(1780-1849)
1829年提出“三素组”的概念。
萌芽期
法国化学家拉瓦锡
(1743-1794)
1789年在《化学概要》中提出了第一个元素分类表。
一、元素周期表的发展历程
1775
1800
1825
1850
1875
1900
1925
年
德国化学家德贝莱纳
(1780-1849)
1829年提出“三素组”的概念。
俄国化学家门捷列夫
(1834-1907)
1869年2月编制了第一张元素周期表。
萌芽期
一、元素周期表的发展历程
门捷列夫编制的第一张元素周期表(手稿)
门捷列夫编制的第一张元素周期表(整理稿)
法国化学家拉瓦锡
(1743-1794)
1789年在《化学概要》中提出了第一个元素分类表。
一、元素周期表的发展历程
1775
1800
1825
1850
1875
1900
1925
年
德国化学家德贝莱纳
(1780-1849)
1829年提出“三素组”的概念。
俄国化学家门捷列夫
(1834-1907)
1869年2月编制了第一张元素周期表。
(1866-1919)
瑞士化学家维尔纳
1905年制成了现代形式的元素周期表。
萌芽期
成型期
法国化学家拉瓦锡
(1743-1794)
1789年在《化学概要》中提出了第一个元素分类表。
一、元素周期表的发展历程
1775
1800
1825
1850
1875
1900
1925
年
德国化学家德贝莱纳
(1780-1849)
1829年提出“三素组”的概念。
俄国化学家门捷列夫
(1834-1907)
1869年2月编制了第一张元素周期表。
(1866-1919)
瑞士化学家维尔纳
1905年制成了现代形式的元素周期表。
英国物理学家莫塞莱
(1887-1915)
1913年发现并证明元素的原子序数等于原子的核电荷数。
萌芽期
成型期
完善期
多姿多彩的元素周期表
多姿多彩的元素周期表
多姿多彩的元素周期表
二、元素周期表(概况)
学习任务:观察元素周期表,探寻编排规则
1、以 为原子序数,将原子序数由小到大,按照 的顺序依次排列。
1 2
3 4 5 6 7 8 9 10
11 12 13 14 15 16 17 18
1、元素周期表的编排规则
以 为原子序数,将元素按原子序数由小到大的顺序,将元素在表中 依次排列。
核电荷数
从左至右,从上至下
周期
族
二、元素周期表(概况)
16
7个横行共 个周期
18个纵行共 个族
如“第3周期”或“第三周期”
7
如“第ⅡA族”“第ⅡB族”
请写出金属铝在周期表中的位置
“第3周期第ⅢA族”或
“第三周期第ⅢA族”
2、元素周期表的表达规则。
二、元素周期表(概况)
学习任务:观察元素周期表,探寻编排规则
1、以 为原子序数,将原子序数由小到大,按照 的顺序依次排列。
1 2
3 4 5 6 7 8 9 10
11 12 13 14 15 16 17 18
3、周期的规律。
电子层数
同周期元素具有相同的 。
周期序数= 。
电子层数
二、元素周期表(周期)
3、周期的规律。
周期序数 包括元素种数
1
2
3
4
5
6
7
预测:第8周期最多可包含
种元素。
2
8
8
18
18
32
32
短
周
期
长周
期
50
2×12
2×22
2×32
2×42
2×52
二、元素周期表(族)
4、族的规律。
族的分类
7个副族(B)
7个主族(A)
Ⅷ
0
二、元素周期表(概况)
学习任务:观察元素周期表,探寻编排规则
1、以 为原子序数,将原子序数由小到大,按照 的顺序依次排列。
1 2
3 4 5 6 7 8 9 10
11 12 13 14 15 16 17 18
4、族的规律。
最外层电子层数
同族元素具有相同的 。
主族序数= 。
最外层电子层数
ⅠA
ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
试一试:
你知道 在周期表中的位置吗?
2 8 18 7
+35
第4周期第ⅦA族
二、元素周期表(规律)
5、周期和族的关系。
问题思考(1):
为什么各周期元素种类不同?
A、0族
A、B、Ⅷ、0族
镧系
锕系
·
·
·
周期序数 包括元素种数
1
2
3 2
8
8
4
5
6
7 18
18
32
32
二、元素周期表(规律)
5、周期和族的关系。
左右相邻(同周期)
上下相邻(同主族 )
·
·
1、11、25
2、8、18、32
问题思考(2):
主族相邻元素的原子序数差值规律?
二、元素周期表
7、特殊区域
过渡元素
(过渡金属)
碱
金
属
元
素
卤
族
元
素
稀
有
气
体
元
素
元素:具有相同核电荷数(即质子数)的一类原子的总称
三、核素
核素:具有一定数目的质子和一定数目的中子的一种原子
即同一元素的不同核素之间互称为同位素。
同位素:质子数相同而中子数不同的同一元素的不同原子间互称
H
1
——元素符号
原子序数——
相对原子质量——1.008
——元素名称
氢
原子
原子核
质子(Z)
核外电子
中子(N)
同位素的应用
核燃料
放射线治癌症
辐射育种
金属探伤
环保治污:辐射消毒(如紫外线、γ射线)
原子半径变大
金属性变强
还原性变强
最高价氧化物对应的水化物碱性强
原子半径变
金属性变 (非金属性变 =气态氢化物稳定性 )
还原性变 (氧化性变 )
最高价氧化物对应水化物碱性变 (酸性变 )
小
弱
弱
弱
强
强
强
强
元素周期律是学习和研究化学的重要工具。下列递变规律正确的是
A. 原子半径:PB. 稳定性:HCl>H2S>PH3
C. 金属性:NaD. 碱性:LiOH>NaOH > KOH
√
小结
元素周期表
横行:周期,7个
纵列:族,18列,16个族
周期序数=电子层数
主族序数=最外层电子数
主族:IA-VIIA
副族:IB-VIIB
0族:稀有气体
按照核电荷数(质子数)由小到大排列
短周期:1-3
长周期:4-7
元素
核素
是一种元素的三种核素,互称为同位素。
原子
原子核
质子
核外电子
中子
VIII
随堂检测
1、下列元素中,属于短周期ⅦA族的是( )
C. I D. F
A. Be B. Br
2 2
+4
2 8 18 7
+35
2 8 18 18 7
+53
2 7
+9
2、第三周期 VⅡA 族元素的原子序数为( )
A.16 B.17
C.18 D.19
随堂检测
3、铋(Bi)在医药方面有重要应用。下列关于 和 的说法正确的是( )
A. 和 都含有83个中子
B. 和 互为同位素
C. 和 的核外电子数不同
D. 和 分别含有126和127个质子
随堂检测
第四章 第一节 第一课时
《原子结构》
春秋战国时期,墨子、惠子等哲学家同样从不同角度提出了物质有不能再分的最小单位的观点。
公元前450年以前,古希腊哲学家德谟克利特提出,宇宙万物都是由最微小、坚硬、不可入,不可分割的物质粒子所构成的。这种粒子就是原子。
化学史话/ CHEMISTRY HISTORY
道尔顿模型(1803年)
英国化学家道尔顿提出:原子是构成物质的基本粒子,它们是坚实的、不可分割的实心球体
化学史话/ CHEMISTRY HISTORY
化学史话/ CHEMISTRY HISTORY
枣糕模型( 1904年)
英国物理学家汤姆孙提出:原子是一个平均分布着正电荷的粒子,其中镶嵌着许多电子,中和了正电荷,从而形成了中性原子。
卢瑟福原子模型(1911年)
物理学家卢瑟福提出:在原子的中心有一个带正电荷的核,它的质量几乎等于原子的全部质量,电子在它的周围沿着不同的轨道运转,就像行星围绕太阳运转一样。
化学史话/ CHEMISTRY HISTORY
化学史话/ CHEMISTRY HISTORY
玻尔原子结构模型(1913年)
丹麦物理学家玻尔:电子在原子核外空间的一定轨道上绕核做高速圆周运动。
化学史话/ CHEMISTRY HISTORY
电子云模型(1926年)
奥地利物理学家薛定谔等以量子力学为基础提出电子云模型
一、原子的结构
原子
原子核
核外电子:
中子:
质子:
原子序数=核电荷数=质子数=核外电子数
带1个单位正电荷
不带电
带1个单位负电荷
原子结构/ ATOM STRUCTURE
一、原子的结构
(2)质量关系:质量数(A)=质子数(Z)+中子数(N)。
1.质量数
(1)概念:将原子核内所有质子和中子的相对质量取近似整数值相加,所得的数值叫做质量数,常用A表示。
原子结构/ ATOM STRUCTURE
原子 质子数(Z) 中子数(N) 质量数(A)
C 6 6
O 8 8
Na 11 12
12
16
23
练习一:将几种原子的质子数和中子数之和(质量数)填入下表,
原子结构/ ATOM STRUCTURE
一、原子的结构
2.原子符号
表示的意义是质子数为Z,质量数为A的X元素的一种_____。
原子
原子结构/ ATOM STRUCTURE
2008年,冲绳科学技术大学院大学的科学家们用他们的“飞秒照相机”成功地首次拍到了材料内部电子的运动轨迹,再度实现了突破。
化学史话/ CHEMISTRY HISTORY
一、原子的结构
3.核外电子排布——能量规律
各电子层由内到外 电子层数 1 2 3 4 5 6 7
字母代号 K L M N O P Q
离核远近 由____到____
能量高低 由____到____
原子结构/ ATOM STRUCTURE
近
远
低
高
核外电子由里向外,依次排布在能量逐渐_____的电子层里,即按K→L→M→ N……顺序排列。
升高
思考并填空:
核电荷数 元素名称 元素符号 各电子层的电子数
K L M N O P
2 氦 He 2
10 氖 Ne 2 8
18 氩 Ar 2 8 8
36 氪 Kr 2 8 18 8
54 氙 Xe 2 8 18 18 8
86 氡 Rn 2 8 18 32 18 8
当K层为最外层时,最多能容纳的电子数是多少?
除了K层,其他各层为最外层时,最多能容纳的电子数是多少?
原子结构/ ATOM STRUCTURE
(2)最外层电子数目最多不能超过____个(K层为最外层时不能超过2个)。
(1)各电子层最多容纳____个电子(n表示电子层数)。
一、原子的结构
4.核外电子排布——数量规律
2n2
8
(3)次外层最多能容纳的电子数不超过____个。
18
原子结构/ ATOM STRUCTURE
将Na、K的原子结构示意图分别写成 正确吗?若不正确,请说明原因。
原子结构/ ATOM STRUCTURE
一、原子的结构
5.原子结构示意图
练习二:画出下列原子或离子的结构示意图。
①S______, S2-_______;
②Ca_______,Ca2+_______。
练习三:请同学们课下画出1-20号元素原子结构示意图
原子结构/ ATOM STRUCTURE
法国化学家拉瓦锡
(1743-1794)
1789年在《化学概要》中提出了第一张元素分类表。
一、元素周期表的发展历程
1775
1800
1825
1850
1875
1900
1925
年
法国化学家拉瓦锡
(1743-1794)
1789年在《化学概要》中提出了第一个元素分类表。
一、元素周期表的发展历程
1775
1800
1825
1850
1875
1900
1925
年
德国化学家德贝莱纳
(1780-1849)
1829年提出“三素组”的概念。
萌芽期
法国化学家拉瓦锡
(1743-1794)
1789年在《化学概要》中提出了第一个元素分类表。
一、元素周期表的发展历程
1775
1800
1825
1850
1875
1900
1925
年
德国化学家德贝莱纳
(1780-1849)
1829年提出“三素组”的概念。
俄国化学家门捷列夫
(1834-1907)
1869年2月编制了第一张元素周期表。
萌芽期
一、元素周期表的发展历程
门捷列夫编制的第一张元素周期表(手稿)
门捷列夫编制的第一张元素周期表(整理稿)
法国化学家拉瓦锡
(1743-1794)
1789年在《化学概要》中提出了第一个元素分类表。
一、元素周期表的发展历程
1775
1800
1825
1850
1875
1900
1925
年
德国化学家德贝莱纳
(1780-1849)
1829年提出“三素组”的概念。
俄国化学家门捷列夫
(1834-1907)
1869年2月编制了第一张元素周期表。
(1866-1919)
瑞士化学家维尔纳
1905年制成了现代形式的元素周期表。
萌芽期
成型期
法国化学家拉瓦锡
(1743-1794)
1789年在《化学概要》中提出了第一个元素分类表。
一、元素周期表的发展历程
1775
1800
1825
1850
1875
1900
1925
年
德国化学家德贝莱纳
(1780-1849)
1829年提出“三素组”的概念。
俄国化学家门捷列夫
(1834-1907)
1869年2月编制了第一张元素周期表。
(1866-1919)
瑞士化学家维尔纳
1905年制成了现代形式的元素周期表。
英国物理学家莫塞莱
(1887-1915)
1913年发现并证明元素的原子序数等于原子的核电荷数。
萌芽期
成型期
完善期
多姿多彩的元素周期表
多姿多彩的元素周期表
多姿多彩的元素周期表
二、元素周期表(概况)
学习任务:观察元素周期表,探寻编排规则
1、以 为原子序数,将原子序数由小到大,按照 的顺序依次排列。
1 2
3 4 5 6 7 8 9 10
11 12 13 14 15 16 17 18
1、元素周期表的编排规则
以 为原子序数,将元素按原子序数由小到大的顺序,将元素在表中 依次排列。
核电荷数
从左至右,从上至下
周期
族
二、元素周期表(概况)
16
7个横行共 个周期
18个纵行共 个族
如“第3周期”或“第三周期”
7
如“第ⅡA族”“第ⅡB族”
请写出金属铝在周期表中的位置
“第3周期第ⅢA族”或
“第三周期第ⅢA族”
2、元素周期表的表达规则。
二、元素周期表(概况)
学习任务:观察元素周期表,探寻编排规则
1、以 为原子序数,将原子序数由小到大,按照 的顺序依次排列。
1 2
3 4 5 6 7 8 9 10
11 12 13 14 15 16 17 18
3、周期的规律。
电子层数
同周期元素具有相同的 。
周期序数= 。
电子层数
二、元素周期表(周期)
3、周期的规律。
周期序数 包括元素种数
1
2
3
4
5
6
7
预测:第8周期最多可包含
种元素。
2
8
8
18
18
32
32
短
周
期
长周
期
50
2×12
2×22
2×32
2×42
2×52
二、元素周期表(族)
4、族的规律。
族的分类
7个副族(B)
7个主族(A)
Ⅷ
0
二、元素周期表(概况)
学习任务:观察元素周期表,探寻编排规则
1、以 为原子序数,将原子序数由小到大,按照 的顺序依次排列。
1 2
3 4 5 6 7 8 9 10
11 12 13 14 15 16 17 18
4、族的规律。
最外层电子层数
同族元素具有相同的 。
主族序数= 。
最外层电子层数
ⅠA
ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
试一试:
你知道 在周期表中的位置吗?
2 8 18 7
+35
第4周期第ⅦA族
二、元素周期表(规律)
5、周期和族的关系。
问题思考(1):
为什么各周期元素种类不同?
A、0族
A、B、Ⅷ、0族
镧系
锕系
·
·
·
周期序数 包括元素种数
1
2
3 2
8
8
4
5
6
7 18
18
32
32
二、元素周期表(规律)
5、周期和族的关系。
左右相邻(同周期)
上下相邻(同主族 )
·
·
1、11、25
2、8、18、32
问题思考(2):
主族相邻元素的原子序数差值规律?
二、元素周期表
7、特殊区域
过渡元素
(过渡金属)
碱
金
属
元
素
卤
族
元
素
稀
有
气
体
元
素
元素:具有相同核电荷数(即质子数)的一类原子的总称
三、核素
核素:具有一定数目的质子和一定数目的中子的一种原子
即同一元素的不同核素之间互称为同位素。
同位素:质子数相同而中子数不同的同一元素的不同原子间互称
H
1
——元素符号
原子序数——
相对原子质量——1.008
——元素名称
氢
原子
原子核
质子(Z)
核外电子
中子(N)
同位素的应用
核燃料
放射线治癌症
辐射育种
金属探伤
环保治污:辐射消毒(如紫外线、γ射线)
原子半径变大
金属性变强
还原性变强
最高价氧化物对应的水化物碱性强
原子半径变
金属性变 (非金属性变 =气态氢化物稳定性 )
还原性变 (氧化性变 )
最高价氧化物对应水化物碱性变 (酸性变 )
小
弱
弱
弱
强
强
强
强
元素周期律是学习和研究化学的重要工具。下列递变规律正确的是
A. 原子半径:P
C. 金属性:Na
√
小结
元素周期表
横行:周期,7个
纵列:族,18列,16个族
周期序数=电子层数
主族序数=最外层电子数
主族:IA-VIIA
副族:IB-VIIB
0族:稀有气体
按照核电荷数(质子数)由小到大排列
短周期:1-3
长周期:4-7
元素
核素
是一种元素的三种核素,互称为同位素。
原子
原子核
质子
核外电子
中子
VIII
随堂检测
1、下列元素中,属于短周期ⅦA族的是( )
C. I D. F
A. Be B. Br
2 2
+4
2 8 18 7
+35
2 8 18 18 7
+53
2 7
+9
2、第三周期 VⅡA 族元素的原子序数为( )
A.16 B.17
C.18 D.19
随堂检测
3、铋(Bi)在医药方面有重要应用。下列关于 和 的说法正确的是( )
A. 和 都含有83个中子
B. 和 互为同位素
C. 和 的核外电子数不同
D. 和 分别含有126和127个质子
随堂检测
