人教版高中化学必修第一册第四章物质结构元素周期律4.1.2元素周期表核素教学课件
文档属性
| 名称 | 人教版高中化学必修第一册第四章物质结构元素周期律4.1.2元素周期表核素教学课件 |  | |
| 格式 | ppt | ||
| 文件大小 | 10.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-11 19:47:26 | ||
图片预览









文档简介
(共37张PPT)
第一节 原子结构与元素周期表
第四章 物质结构 元素周期律
素养目标
宏观辨识与微观探析:
宏观上认识元素周期表的基本结构七行18列,分为七个周期,16个族,从微观上理解同主族元素原子核外电子排布的相似性和递变规律,初步理解结构决定性质,性质反映结构的基本规律。
证据推理与模型认知:
建立同主族、同周期元素原子结构变化的微观模型,理解根据该模型进行元素性质推理的科学思想。
科学探究与创新意识:
通过“科学史话”及“化学与职业”栏目,培养严谨求实的科学态度,增强努力学好化学知识为社会服务的责任感和使命感。
教学目标
本节重点
元素周期表的结构,核素、同位素的概念。
本节难点
元素周期表的结构。
1.了解核素、同位素的含义,认识同位素在生产、生活中的应用。
2.了解元素周期表的形成过程,并能运用归纳、概括等方法对信息进行加工,体验科学探究的过程,进一步学习科学探究的方法。
3.通知道周期和族的概念,会描述元素周期表的结构,知道元素在周期表中的位置与原子结构的关系,初步学会推导元素在周期表中的位置的基本方法。
新课导入
你知道吗?
门捷列夫怎样绘制了他的第一张元素周期律图表?
新课导入
你知道吗?
门捷列夫的元素周期表是什么样的?
1869 年2月,门捷列夫发表了他的第一张元素周期律图表,初步实现了元素的系统化和科学分类。该表包括了当时已发现的63 种元素,并大胆预言了3 种未知元素的存在,指出按照原子量排列起来的元素,在性质上呈现出明显的周期性。
门捷列夫第一张元素周期表
门捷列夫第二张元素周期表
元素周期表编排原则
元素周期表的结构
核素 同位素
课堂思考
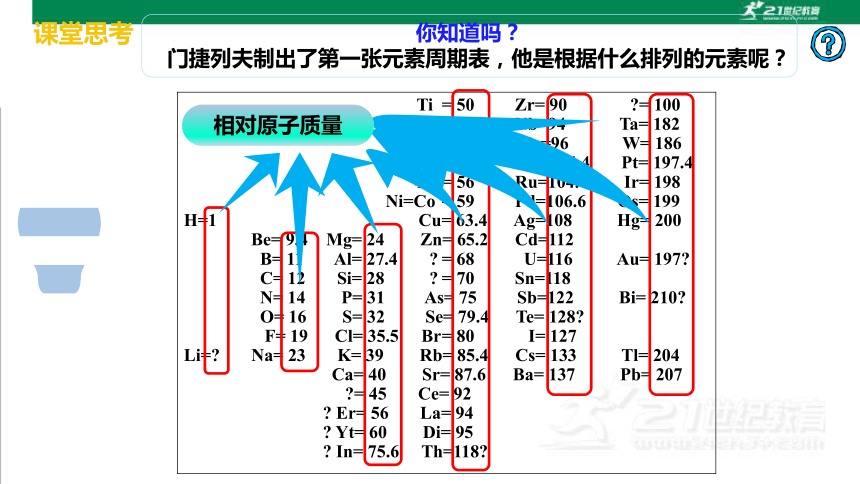
你知道吗?
门捷列夫制出了第一张元素周期表,他是根据什么排列的元素呢?
Ti = 50 Zr= 90 = 100
V = 51 Nb=94 Ta= 182
Cr = 52 Mo=96 W= 186
Mn= 55 Rh=104.4 Pt= 197.4
Fe = 56 Ru=104.4 Ir= 198
Ni=Co = 59 Pd=106.6 Os= 199
H=1 Cu= 63.4 Ag=108 Hg= 200
Be= 9.4 Mg= 24 Zn= 65.2 Cd=112
B= 11 Al= 27.4 = 68 U=116 Au= 197
C= 12 Si= 28 = 70 Sn=118
N= 14 P= 31 As= 75 Sb=122 Bi= 210
O= 16 S= 32 Se= 79.4 Te= 128
F= 19 Cl= 35.5 Br = 80 I= 127
Li= Na= 23 K= 39 Rb= 85.4 Cs= 133 Tl= 204
Ca= 40 Sr= 87.6 Ba= 137 Pb= 207
= 45 Ce= 92
Er= 56 La= 94
Yt= 60 Di= 95
In= 75.6 Th=118
相对原子质量
01
元素周期表编排原则
一、元素周期表编排原则
课堂探究
了解认识
对比学习
1.门捷列夫绘制的第一张元素周期表是按照元素的相对原子质量来排列的,随着科学家对原子结构认识的不断深入,元素周期表中元素的排列依据也由相对原子质量改为核电荷数。
2.原子序数:按照元素在周期表中的顺序给元素编号
原子序数=质子数=核电荷数=核外电子数
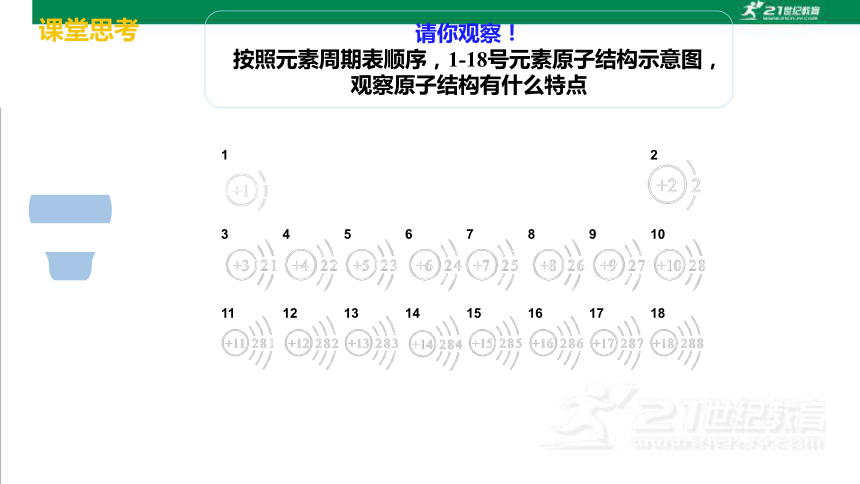
元素的性质取决于原子核外电子的排布——用原子结构示意图表示
课堂思考
请你观察!
按照元素周期表顺序,1-18号元素原子结构示意图,
观察原子结构有什么特点
1 2
3 4 5 6 7 8 9 10
11 12 13 14 15 16 17 18
课堂探究
重点理解
一、元素周期表编排原则
对比学习
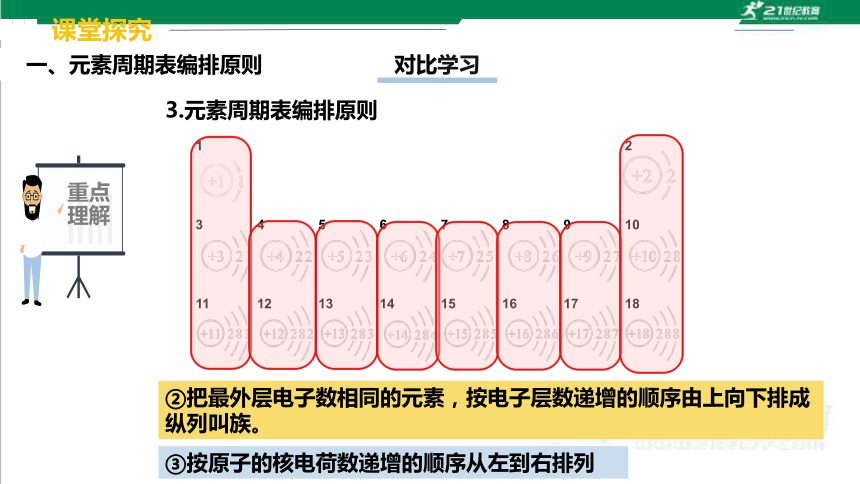
3.元素周期表编排原则
①将电子层数相同的元素按照原子序数递增的顺序由左向右排成横行叫周期。
1 2
3 4 5 6 7 8 9 10
11 12 13 14 15 16 17 18
课堂探究
重点理解
一、元素周期表编排原则
对比学习
3.元素周期表编排原则
②把最外层电子数相同的元素,按电子层数递增的顺序由上向下排成纵列叫族。
③按原子的核电荷数递增的顺序从左到右排列
1 2
3 4 5 6 7 8 9 10
11 12 13 14 15 16 17 18
02
元素周期表的结构
课堂探究
二、元素周期表的结构
重点理解
1.元素周期表中元素的排列方式:
对比学习
将电子层数相同的元素按照原子序数递增的顺序由左向右排成横行,最外层电子数相同的元素按电子层数递增的顺序由上向下排成纵列。
短周期
周期
族
课堂思考
请你思考!
观察元素周期表,思考周期序数与原子核外电子排布有何关系?
思考与讨论
观察元素周期表,针对下表中的项目进行思考,并与同学讨论,将讨论结果填写在表中。从表中你能发现周期序数与原子核外电子层数有什么关系吗?
课堂探究
二、元素周期表的结构
重点理解
对比学习
2.周期:一个横行作为1个周期,共7个周期
2
8
8
18
18
32
32
一
二
三
四
五
六
七
(镧系元素)
(锕系元素)
短周期
长周期
课堂探究
二、元素周期表的结构
重点理解
对比学习
2.周期:一个横行作为1个周期,共7个周期
周期序数 起止元素 包括元素种数 核外电子层数
1 H~He 2 1
2
3
4
5
6
7 Fr~Og 7
Li~Ne
8
2
Na~Ar
8
3
K~Kr
18
4
Rb~Xe
18
5
Cs~Rn
32
6
32
周期序数等于原子核外电子层数
短周期
长周期
课堂探究
二、元素周期表的结构
重点理解
对比学习
3.族:一列作为1个族(第8、9、10三列统称为第Ⅷ族),共16个族
长、短周期共同组成,用“A”表示
VIII族
0 族
A:主族
ⅠA , ⅡA , ⅢA , ⅣA ,ⅤA , ⅥA , ⅦA
ⅠB , ⅡB , ⅢB , ⅣB ,ⅤB , ⅥB , ⅦB, VIII族
仅由长周期组成,用“B”表示
B:副族
表示时既无“A”也无“B”
课堂探究
二、元素周期表的结构
重点理解
,
对比学习
3.族:一列作为1个族(第8、9、10三列统称为第Ⅷ族),共16个族
族 主族 0族 副族
构成周期
列序
族序数
族序数与原子结构关系 ————————————
常见族的别称
由长周期元素和短周期元素共同构成
仅由长周期元素构成
1,2,13~17
18
3~7,11,12
8,9,10
Ⅷ
ⅢB,ⅣB,ⅤB,ⅥB,ⅦB,ⅠB,ⅡB
ⅠA,ⅡA,ⅢA,ⅣA,ⅤA,ⅥA,ⅦA
0
主族序数=原子最外层电子数
第ⅠA族(除氢):碱金属元素;第ⅦA族:卤族元素;0族:稀有气体元素
典例精讲
【例1】已知氮元素、铝元素和锗元素的原子结构示意图,它们分别位于周期表的第几周期第几主族
氮元素:
铝元素:
锗元素:
第 2 周期 第 ⅤA 族
第 3 周期 第 ⅢA 族
第 4 周期 第 ⅣA 族
典例精讲
【例2】不看元素周期表,结合以上学习,你能不能写出0族元素原子序数?第ⅠA族,相邻元素原子序数差值为?哪一族元素种类最多?
2
8
8
18
18
32
32
短周期
长周期
2
8
8
18
18
32
2
10
18
36
54
86
118
课堂探究
二、元素周期表的结构
对比学习
重点理解
4.元素周期表中每一个格都标有元素的基本信息
图片中H的质量数为什么有3 个呢?
1 H
氢
1.008
原子序数
相对原子质量
元素名称
元素符号
1 H
氢
1.008
1
2
3
质量数
03
核素 同位素
课堂思考
请你思考!
下列图片中的微粒是同一种元素吗?为什么?
氯化铁
溶液
氕
e-
p+
氘
e-
p+
n
氚
e-
p+
n
n
元素是具有相同质子数(核电荷数)的一类原子的总称
都是氢元素
1 H
氢
1.008
质量数
1
2
3
课堂探究
三、核素 同位素
重点理解
对比学习
1.核素:
X
Z
A
具有一定数目质子和一定数目中子的一种原子就是一核素
每种原子就是一核素
2.同位素:即同一元素的不同核素互称为同位素
质子数相同而中子数不同的同一元素的不同原子互称为同位素
课堂探究
三、核素 同位素
重点理解
对比学习
2.同位素:
氢元素的原子核 原子名称
质子数
(Z) 中子数
(N)
1 0
1 1
1 2
氕
氘
氚
统称:
氢元素
单称:核素
互称:
同位素
H
1
1
或D
H
2
1
或T
H
3
1
课堂探究
三、核素 同位素
重点理解
3.同位素的特点
对比学习
同位素
氢元素
①两同:质子数相同、元素相同; ②两不同:中子数不同、原子不同。
③位置:在周期表里占据同一位置。 ④结构:质子数相同,中子数不同。
⑤性质:化学性质几乎完全相同,物理性质略有差异。
⑥存在:天然存在的同位素,相互之间保持一定的比率。
天然存在的元素里,不论是游离态还是化合态,各同位素原子所占原子的百分比一般是不变的。
课堂思考
请你思考!
你还知道哪些元素有同位素吗?
自然界中存在三种碳的同位素:12C、13C、14C,前两者比较稳定,而14C属低能量的放射性元素。
碳元素
C
12
6
C
13
6
C
14
6
相对质量的标准
考古断代
课堂探究
二、原子结构
重点理解
4.常见的同位素
对比学习
氧元素
O
16
8
O
17
8
O
18
8
铀元素
U
234
92
U
235
92
U
238
92
氢元素
能源、农业、医疗、考古等方面都有重要应用。
典例精讲
【例3】现有下列基本粒子:1H、2H、3H、1H+、234U、235U、238U、40K、40Ca、Cl2、14N、14C。请回答下列问题:
(1)它们分属____种元素,属于氢元素的核素有____种,属于铀元素的核素有____种,互为同位素的原子分别为____________、_______________。
(2)质量数相等的粒子有________、__________、________。(可不填满,也可补充)
7
3
3
1H、2H、3H
234U、235U、238U
1H、1H+
40K、40Ca
14N、14C
典例精讲
【例4】已知某主族元素的原子结构示意图如下,判断其位于第几周期?第几族?
常见题型
1.原子结构定元素位置
短周期主族元素
电子层数=周期序数
最外层电子数=主族序数
典例精讲
【例6】
常见题型
2.零族定位
(1)第17号元素位于第________周期________族。
(2)56号元素位于第________周期________族。
(3)114号元素位于第________周期________族。
根据0族元素原子序数判断周期数
根据差值确定族序数
典例精讲
【例7】下列各图为元素周期表的一部分,表中的数字为原子序数,其中M为37的是( )
常见题型
3.十字定位
定周期
同族上下两元素原子序数差
C
课堂小结
1、元素周期表:将电子层数相同的元素按照原子序数递增的顺序由左向右排成横行,再把不同横行中最外层电子数相同的元素,按电子层数递增的顺序由上向下排成纵列。
周期表分为7个周期(短周期和长周期),16个族
课堂小结
元素周期表
核素
元素
周期表
核素
结构
判断元素在周期表中的位置:周期、族
发展历程及编排原则
同位素:概念、特点、用途
核素的概念
元素的定义
周期:每一横行叫一周期,共7各周期
族:共18列,16个族
随堂演练
1.元素周期表揭示了化学元素间的内在联系,下列有关元素周期表的说法不正确的是( )
A.俄国化学家门捷列夫编制了第一张元素周期表
B.周期表中最外层电子数相同的元素都排列在同一列中
C.周期表中一共有18列,但只有16个族
D.随着人们的认识发展,周期表也在不断地发展变化着
B
2.假设x是第ⅡB族中某元素的原子序数,那么原子序数为x+1的元素位于( )
A.第ⅠB族 B.第ⅢB族
C.第ⅢA族 D.第ⅡA族
C
随堂演练
3.已知X、Y、Z三种主族元素在元素周期表中的位置如图所示。
设X的原子序数为a,则下列说法不正确的是( )
A.Y的原子序数可能为a-17
B.Y与Z的原子序数之和可能为2a
C.Z的原子序数可能为a+31
D.X、Y、Z可能均为短周期元素
D
Y
X
Z
第一节 原子结构与元素周期表
第四章 物质结构 元素周期律
素养目标
宏观辨识与微观探析:
宏观上认识元素周期表的基本结构七行18列,分为七个周期,16个族,从微观上理解同主族元素原子核外电子排布的相似性和递变规律,初步理解结构决定性质,性质反映结构的基本规律。
证据推理与模型认知:
建立同主族、同周期元素原子结构变化的微观模型,理解根据该模型进行元素性质推理的科学思想。
科学探究与创新意识:
通过“科学史话”及“化学与职业”栏目,培养严谨求实的科学态度,增强努力学好化学知识为社会服务的责任感和使命感。
教学目标
本节重点
元素周期表的结构,核素、同位素的概念。
本节难点
元素周期表的结构。
1.了解核素、同位素的含义,认识同位素在生产、生活中的应用。
2.了解元素周期表的形成过程,并能运用归纳、概括等方法对信息进行加工,体验科学探究的过程,进一步学习科学探究的方法。
3.通知道周期和族的概念,会描述元素周期表的结构,知道元素在周期表中的位置与原子结构的关系,初步学会推导元素在周期表中的位置的基本方法。
新课导入
你知道吗?
门捷列夫怎样绘制了他的第一张元素周期律图表?
新课导入
你知道吗?
门捷列夫的元素周期表是什么样的?
1869 年2月,门捷列夫发表了他的第一张元素周期律图表,初步实现了元素的系统化和科学分类。该表包括了当时已发现的63 种元素,并大胆预言了3 种未知元素的存在,指出按照原子量排列起来的元素,在性质上呈现出明显的周期性。
门捷列夫第一张元素周期表
门捷列夫第二张元素周期表
元素周期表编排原则
元素周期表的结构
核素 同位素
课堂思考
你知道吗?
门捷列夫制出了第一张元素周期表,他是根据什么排列的元素呢?
Ti = 50 Zr= 90 = 100
V = 51 Nb=94 Ta= 182
Cr = 52 Mo=96 W= 186
Mn= 55 Rh=104.4 Pt= 197.4
Fe = 56 Ru=104.4 Ir= 198
Ni=Co = 59 Pd=106.6 Os= 199
H=1 Cu= 63.4 Ag=108 Hg= 200
Be= 9.4 Mg= 24 Zn= 65.2 Cd=112
B= 11 Al= 27.4 = 68 U=116 Au= 197
C= 12 Si= 28 = 70 Sn=118
N= 14 P= 31 As= 75 Sb=122 Bi= 210
O= 16 S= 32 Se= 79.4 Te= 128
F= 19 Cl= 35.5 Br = 80 I= 127
Li= Na= 23 K= 39 Rb= 85.4 Cs= 133 Tl= 204
Ca= 40 Sr= 87.6 Ba= 137 Pb= 207
= 45 Ce= 92
Er= 56 La= 94
Yt= 60 Di= 95
In= 75.6 Th=118
相对原子质量
01
元素周期表编排原则
一、元素周期表编排原则
课堂探究
了解认识
对比学习
1.门捷列夫绘制的第一张元素周期表是按照元素的相对原子质量来排列的,随着科学家对原子结构认识的不断深入,元素周期表中元素的排列依据也由相对原子质量改为核电荷数。
2.原子序数:按照元素在周期表中的顺序给元素编号
原子序数=质子数=核电荷数=核外电子数
元素的性质取决于原子核外电子的排布——用原子结构示意图表示
课堂思考
请你观察!
按照元素周期表顺序,1-18号元素原子结构示意图,
观察原子结构有什么特点
1 2
3 4 5 6 7 8 9 10
11 12 13 14 15 16 17 18
课堂探究
重点理解
一、元素周期表编排原则
对比学习
3.元素周期表编排原则
①将电子层数相同的元素按照原子序数递增的顺序由左向右排成横行叫周期。
1 2
3 4 5 6 7 8 9 10
11 12 13 14 15 16 17 18
课堂探究
重点理解
一、元素周期表编排原则
对比学习
3.元素周期表编排原则
②把最外层电子数相同的元素,按电子层数递增的顺序由上向下排成纵列叫族。
③按原子的核电荷数递增的顺序从左到右排列
1 2
3 4 5 6 7 8 9 10
11 12 13 14 15 16 17 18
02
元素周期表的结构
课堂探究
二、元素周期表的结构
重点理解
1.元素周期表中元素的排列方式:
对比学习
将电子层数相同的元素按照原子序数递增的顺序由左向右排成横行,最外层电子数相同的元素按电子层数递增的顺序由上向下排成纵列。
短周期
周期
族
课堂思考
请你思考!
观察元素周期表,思考周期序数与原子核外电子排布有何关系?
思考与讨论
观察元素周期表,针对下表中的项目进行思考,并与同学讨论,将讨论结果填写在表中。从表中你能发现周期序数与原子核外电子层数有什么关系吗?
课堂探究
二、元素周期表的结构
重点理解
对比学习
2.周期:一个横行作为1个周期,共7个周期
2
8
8
18
18
32
32
一
二
三
四
五
六
七
(镧系元素)
(锕系元素)
短周期
长周期
课堂探究
二、元素周期表的结构
重点理解
对比学习
2.周期:一个横行作为1个周期,共7个周期
周期序数 起止元素 包括元素种数 核外电子层数
1 H~He 2 1
2
3
4
5
6
7 Fr~Og 7
Li~Ne
8
2
Na~Ar
8
3
K~Kr
18
4
Rb~Xe
18
5
Cs~Rn
32
6
32
周期序数等于原子核外电子层数
短周期
长周期
课堂探究
二、元素周期表的结构
重点理解
对比学习
3.族:一列作为1个族(第8、9、10三列统称为第Ⅷ族),共16个族
长、短周期共同组成,用“A”表示
VIII族
0 族
A:主族
ⅠA , ⅡA , ⅢA , ⅣA ,ⅤA , ⅥA , ⅦA
ⅠB , ⅡB , ⅢB , ⅣB ,ⅤB , ⅥB , ⅦB, VIII族
仅由长周期组成,用“B”表示
B:副族
表示时既无“A”也无“B”
课堂探究
二、元素周期表的结构
重点理解
,
对比学习
3.族:一列作为1个族(第8、9、10三列统称为第Ⅷ族),共16个族
族 主族 0族 副族
构成周期
列序
族序数
族序数与原子结构关系 ————————————
常见族的别称
由长周期元素和短周期元素共同构成
仅由长周期元素构成
1,2,13~17
18
3~7,11,12
8,9,10
Ⅷ
ⅢB,ⅣB,ⅤB,ⅥB,ⅦB,ⅠB,ⅡB
ⅠA,ⅡA,ⅢA,ⅣA,ⅤA,ⅥA,ⅦA
0
主族序数=原子最外层电子数
第ⅠA族(除氢):碱金属元素;第ⅦA族:卤族元素;0族:稀有气体元素
典例精讲
【例1】已知氮元素、铝元素和锗元素的原子结构示意图,它们分别位于周期表的第几周期第几主族
氮元素:
铝元素:
锗元素:
第 2 周期 第 ⅤA 族
第 3 周期 第 ⅢA 族
第 4 周期 第 ⅣA 族
典例精讲
【例2】不看元素周期表,结合以上学习,你能不能写出0族元素原子序数?第ⅠA族,相邻元素原子序数差值为?哪一族元素种类最多?
2
8
8
18
18
32
32
短周期
长周期
2
8
8
18
18
32
2
10
18
36
54
86
118
课堂探究
二、元素周期表的结构
对比学习
重点理解
4.元素周期表中每一个格都标有元素的基本信息
图片中H的质量数为什么有3 个呢?
1 H
氢
1.008
原子序数
相对原子质量
元素名称
元素符号
1 H
氢
1.008
1
2
3
质量数
03
核素 同位素
课堂思考
请你思考!
下列图片中的微粒是同一种元素吗?为什么?
氯化铁
溶液
氕
e-
p+
氘
e-
p+
n
氚
e-
p+
n
n
元素是具有相同质子数(核电荷数)的一类原子的总称
都是氢元素
1 H
氢
1.008
质量数
1
2
3
课堂探究
三、核素 同位素
重点理解
对比学习
1.核素:
X
Z
A
具有一定数目质子和一定数目中子的一种原子就是一核素
每种原子就是一核素
2.同位素:即同一元素的不同核素互称为同位素
质子数相同而中子数不同的同一元素的不同原子互称为同位素
课堂探究
三、核素 同位素
重点理解
对比学习
2.同位素:
氢元素的原子核 原子名称
质子数
(Z) 中子数
(N)
1 0
1 1
1 2
氕
氘
氚
统称:
氢元素
单称:核素
互称:
同位素
H
1
1
或D
H
2
1
或T
H
3
1
课堂探究
三、核素 同位素
重点理解
3.同位素的特点
对比学习
同位素
氢元素
①两同:质子数相同、元素相同; ②两不同:中子数不同、原子不同。
③位置:在周期表里占据同一位置。 ④结构:质子数相同,中子数不同。
⑤性质:化学性质几乎完全相同,物理性质略有差异。
⑥存在:天然存在的同位素,相互之间保持一定的比率。
天然存在的元素里,不论是游离态还是化合态,各同位素原子所占原子的百分比一般是不变的。
课堂思考
请你思考!
你还知道哪些元素有同位素吗?
自然界中存在三种碳的同位素:12C、13C、14C,前两者比较稳定,而14C属低能量的放射性元素。
碳元素
C
12
6
C
13
6
C
14
6
相对质量的标准
考古断代
课堂探究
二、原子结构
重点理解
4.常见的同位素
对比学习
氧元素
O
16
8
O
17
8
O
18
8
铀元素
U
234
92
U
235
92
U
238
92
氢元素
能源、农业、医疗、考古等方面都有重要应用。
典例精讲
【例3】现有下列基本粒子:1H、2H、3H、1H+、234U、235U、238U、40K、40Ca、Cl2、14N、14C。请回答下列问题:
(1)它们分属____种元素,属于氢元素的核素有____种,属于铀元素的核素有____种,互为同位素的原子分别为____________、_______________。
(2)质量数相等的粒子有________、__________、________。(可不填满,也可补充)
7
3
3
1H、2H、3H
234U、235U、238U
1H、1H+
40K、40Ca
14N、14C
典例精讲
【例4】已知某主族元素的原子结构示意图如下,判断其位于第几周期?第几族?
常见题型
1.原子结构定元素位置
短周期主族元素
电子层数=周期序数
最外层电子数=主族序数
典例精讲
【例6】
常见题型
2.零族定位
(1)第17号元素位于第________周期________族。
(2)56号元素位于第________周期________族。
(3)114号元素位于第________周期________族。
根据0族元素原子序数判断周期数
根据差值确定族序数
典例精讲
【例7】下列各图为元素周期表的一部分,表中的数字为原子序数,其中M为37的是( )
常见题型
3.十字定位
定周期
同族上下两元素原子序数差
C
课堂小结
1、元素周期表:将电子层数相同的元素按照原子序数递增的顺序由左向右排成横行,再把不同横行中最外层电子数相同的元素,按电子层数递增的顺序由上向下排成纵列。
周期表分为7个周期(短周期和长周期),16个族
课堂小结
元素周期表
核素
元素
周期表
核素
结构
判断元素在周期表中的位置:周期、族
发展历程及编排原则
同位素:概念、特点、用途
核素的概念
元素的定义
周期:每一横行叫一周期,共7各周期
族:共18列,16个族
随堂演练
1.元素周期表揭示了化学元素间的内在联系,下列有关元素周期表的说法不正确的是( )
A.俄国化学家门捷列夫编制了第一张元素周期表
B.周期表中最外层电子数相同的元素都排列在同一列中
C.周期表中一共有18列,但只有16个族
D.随着人们的认识发展,周期表也在不断地发展变化着
B
2.假设x是第ⅡB族中某元素的原子序数,那么原子序数为x+1的元素位于( )
A.第ⅠB族 B.第ⅢB族
C.第ⅢA族 D.第ⅡA族
C
随堂演练
3.已知X、Y、Z三种主族元素在元素周期表中的位置如图所示。
设X的原子序数为a,则下列说法不正确的是( )
A.Y的原子序数可能为a-17
B.Y与Z的原子序数之和可能为2a
C.Z的原子序数可能为a+31
D.X、Y、Z可能均为短周期元素
D
Y
X
Z
