人教版高中化学必修第一册第四章物质结构元素周期律4.1.3原子结构与元素的性质课件(30页ppt)
文档属性
| 名称 | 人教版高中化学必修第一册第四章物质结构元素周期律4.1.3原子结构与元素的性质课件(30页ppt) |

|
|
| 格式 | ppt | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-13 00:00:00 | ||
图片预览









文档简介
(共30张PPT)
第四章 物质结构 元素周期律
第一节 原子结构与元素周期表
第3课时 原子结构与元素的性质
一般金属元素最外层电子数≤4,具有金属性;
非金属元素最外层电子数≥4,具有非金属性。
金属性:金属元素的原子所具有的失去电子的能力;
非金属性:非金属元素的原子所具有的得到电子的能力。
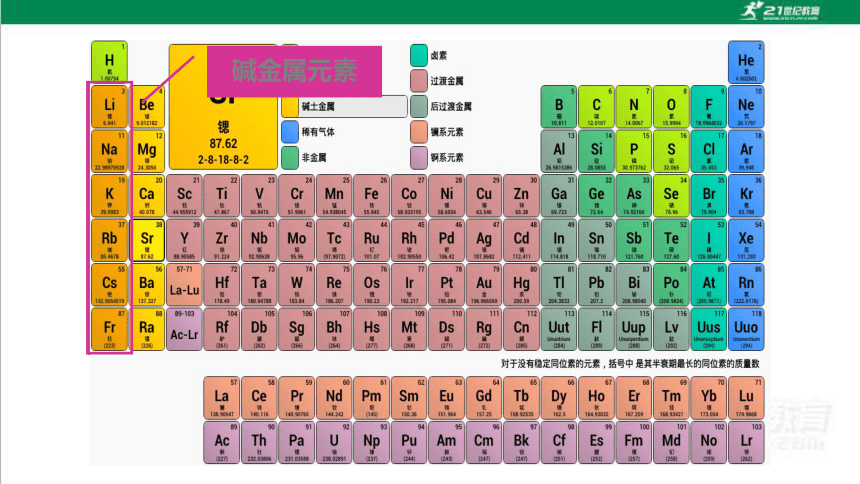
碱金属元素
碱金属元素
一、碱金属元素
碱金属是一类化学性质非常活泼的金属,在自然界中都以化合态存在。
思考与讨论:
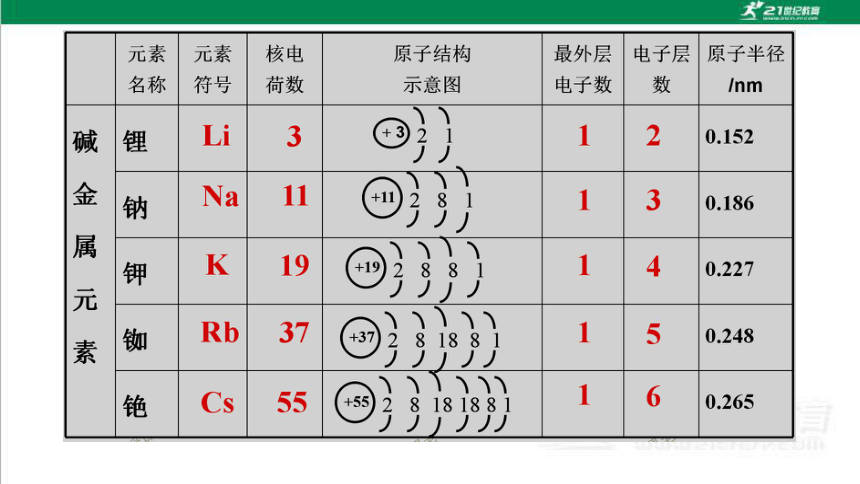
我们把第ⅠA族(除了氢)中的元素称为碱金属元素,为什么要把这些元素编在一个族呢?根据表中原子结构示意图(课本P93),完成表格,并思考和讨论下列问题。
思考与讨论:
(1)在周期表中,从上到下碱金属元素原子的核电荷数、原子半径的变化有什么特点?
(2)观察碱金属元素的原子结构示意图,它们的原子核外电子排布有什么特点?从哪一点能够推断出碱金属元素的化学性质具有相似性。
(3)请总结碱金属元素原子结构的相同点及递变性规律。
从上到下核电荷数逐渐增大,原子半径逐渐增大
最外层电子数相同,都为1,并且电子层数逐渐增大
最外层电子数相同
碱金属元素原子结构的相同点及递变性规律:
(1)相同点:
(2)递变性规律:
易失1个电子,具有还原性
失电子能力逐渐增强
金属性逐渐增强
还原性逐渐增强
思考:碱金属元素原子结构的相同点和递变性会对其性质产生哪些影响?
碱金属元素原子的最外层都有 个电子,在反应中都易 电子,生成 价的离子,表现出 ,在自然界中都以 存在。
【探究】碱金属化学性质的比较
【问题和预测】
(1)回忆第二章学过的知识,钠有哪些化学性质?
(2)结合锂、钠和钾的原子结构特点,请你预测锂、钾可能具有哪些与钠相似的化学性质?
1
失去1个
+1
化合态
还原性
钠可以和O2、H2O发生反应
都能与O2和H2O反应
【分析和结论】
(1)通过实验、观察,讨论并总结钠、钾有哪些相似的化学性质,与你最初根据原子结构特点进行的预测是否一致?
(2)从实验现象比较钾、钠与水反应的难易程度。由此,你能推断出锂与水反应的难易程度吗?
(3)通过比较碱金属与水反应的难易程度,你能发现与它们的原子结构有什么关系吗?由此,你能推断出碱金属元素化学性质的相似性和递变规律吗?
锂与水反应没有钠、钾与水反应剧烈
钠 钾
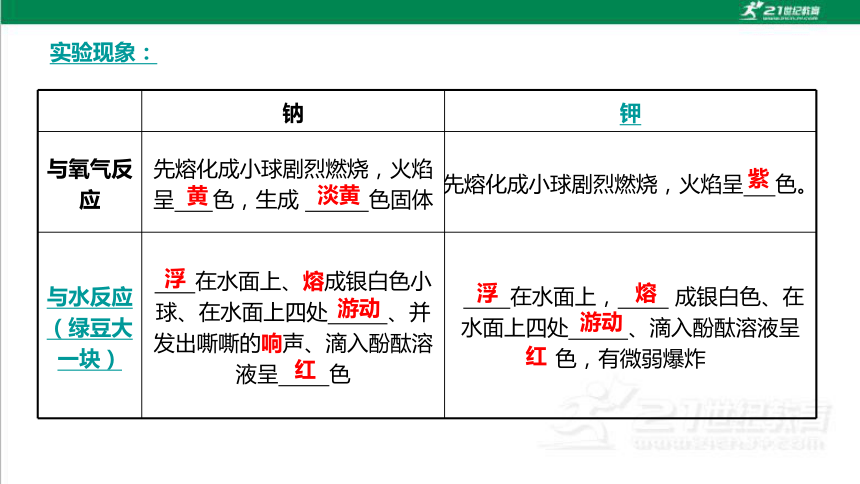
与氧气反应 先熔化成小球剧烈燃烧,火焰呈 色,生成 色固体 先熔化成小球剧烈燃烧,火焰呈 色。
与水反应(绿豆大一块) 在水面上、熔成银白色小球、在水面上四处 、并发出嘶嘶的响声、滴入酚酞溶液呈 色 在水面上, 成银白色、在水面上四处 、滴入酚酞溶液呈 色,有微弱爆炸
黄
淡黄
紫
浮
浮
熔
游动
游动
红
红
实验现象:
1. 碱金属的原子结构与化学性质的关系
(1)碱金属元素的化学性质相似
碱金属元素的原子最外层电子数相同,都是1个电子,它们的化学性质相似,都能与氧气等非金属单质以及水反应。
只有一种氧化物Li2O
氧化物有Na2O和Na2O2
(2)碱金属元素的化学性质具有递变性
随着核电荷数的增加,碱金属元素原子的电子层数逐渐增多,原子半径逐渐增大,原子核对最外层电子的引力逐渐减弱,原子失去最外层电子的能力逐渐增强。即从锂到铯,金属性逐渐增强。
2. 碱金属单质物理性质的相似性和规律性
Li
Na
K
Rb
Cs
碱金属单质 颜色和状态 密度(g.cm3) 熔点(℃) 沸点(℃)
Li 银白色,柔软 0.534 180.5 1347
Na 银白色,柔软 0.97 97.81 882.9
K 银白色,柔软 0.86 63.65 774
Rb 银白色,柔软 1.532 38.89 688
Cs 略带金属光泽,柔软 1.879 28.40 678.4
碱金属单质的主要物理性质
密度增大
熔点降低
沸点降低
比较柔软,有延展性;密度都比较小,熔点也都比较低,导热性和导电性都很好,如液态钠可用作核反应堆的传热介质。
保存在煤油中
保存在石蜡中
课堂练习:
1. 下列金属与水反应最剧烈的是( )
A.Li B.K C.Rb D.Cs
2. 下列对碱金属性质的叙述中,正确的是( )
A.都是银白色的柔软金属,密度都比较小
B.单质在空气中燃烧生成的都是过氧化物
C.碱金属单质都能与水反应生成碱和氢气
D.单质的熔、沸点随着原子序数的增加而升高
D
C
3. 碱金属钫(Fr)具有放射性,它是碱金属元素中最重的元素,下列预言错误的是( )
A.在碱金属中它具有最大的原子半径
B.它的氢氧化物化学式为FrOH,是一种极强的碱
C.钫在空气中燃烧时,只生成Fr2O
D.它能跟水反应生成相应的碱和氢气,由于反应剧烈而发生爆炸
C
卤族元素
二、卤族元素
卤族元素(简称卤素)是典型的非金属元素,它们在自然界都以化合态存在。
分析书本96页的表4-3,总结卤素单质的物理性质规律。
F2
Cl2
Br2
I2
卤素单质 颜色(常态) 密度 熔点(℃) 沸点(℃)
F2 淡黄绿色(气体) 1.69g/L(15℃) -219.6 -188.1
Cl2 黄绿色(气体) 3.214g/L(0℃) -101 -34.6
Br2 深红棕色(液体) 3.119g/cm3(20℃) -7.2 58.78
I2 紫黑色(固体) 4.93g/cm3 113.5 184.4
密度增大
熔沸点升高
卤素单质的颜色逐渐加深,状态由气态逐渐过渡到固态;密度逐渐增大,熔、沸点逐渐升高。
卤族单质的主要物理性质
注意:
①溴是常温常压下唯一的液态非金属单质。
②卤素单质都有毒,溴有很强的的腐蚀性,液溴易挥发,保存时要加一些水进行“水封”,碘可升华,淀粉溶液遇碘变蓝。
1. 卤素原子结构的相同点及递变性规律
(1)相同点:
(2)递变性规律:
F Cl Br I
① 从上往下,原子核电荷数逐渐增大 ;
② 从上往下,电子层数逐渐增大 ;
③ 从上往下,原子半径逐渐增大 。
易得1个电子,具有氧化性
得电子能力逐渐减弱
非金属性逐渐减弱
氧化性逐渐减弱
2. 卤素单质化学性质的相似性和递变性
(1)卤素单质与H2的反应
【思考与讨论】
(1)根据卤素单质与氢气的反应事实,讨论随着原子核电荷数的增多,卤素单质与氢气反应的规律性变化。
(2)根据卤素单质与H2的反应事实,讨论随着原子核电荷数的增多,卤素单质与H2反应的规律性变化。
从表中信息可知,从F2到I2:
①与氢气反应的难易程度:
②生成的氢化物的稳定性:
③卤素的非金属性强弱:
逐渐减弱
由易到难
逐渐减弱
氢化物的稳定性:HF HCl HBr HI
(2)卤素单质间的置换反应
【实验4-1】
分别向盛有4mLKBr溶液和4mLKI溶液的两支试管中加入1mL氯水,振荡,观察溶液的颜色变化,并与氯水的颜色进行比较。写出反应的化学方程式。
向盛有4mLKI溶液的试管中加入1mL溴水,振荡,观察溶液的颜色变化,并与溴水的颜色进行比较。写出反应的化学方程式。
实验操作 实验现象 化学方程式 结论
振荡静置后,溶液由无色变为 色 氧化性:_________
还原性:
_________
振荡静置后,溶液由无色变为 色
振荡静置后,溶液由无色变为 色
橙黄
褐
Cl2>Br2>I2
Cl-
褐
注意:因为F2能与H2O发生反应(2F2 + 2H2O = 4HF + O2),所以F2不能从其他卤化物的盐溶液中置换出卤素单质。
2. 卤素单质化学性质的相似性和递变性
(1)相似性(X表示卤素元素,不考虑放射性元素):原子都容易得到一个电子,卤素单质化学性质活泼,能与氢气、活泼金属和水反应。
与H2反应:
与H2O反应:
(2)递变性
随着核电荷数的增加,电子层数逐渐增多,原子半径逐渐增大,原子核对最外层电子的引力逐渐减弱,原子得到最外层电子的能力逐渐减弱。即从氟到碘,非金属性逐渐减弱。
课堂练习:
1. 下列关于卤族元素由上到下性质递变的叙述,正确的是( )
①单质的氧化性增强 ②单质的颜色加深 ③气态氢化物的稳定性增强
④单质的沸点升高 ⑤阴离子的还原性增强
A. ①②③ B. ②③④
C. ②④⑤ D. ④⑤
C
2. 砹是现知原子序数最大的卤族元素,根据卤素性质的递变规律 ,下列对砹及其化合物的叙述,正确的是( )
A. 与H2化合的能力:At2>I2
B. 砹在常温下为白色固体
C. 砹原子的最外电子层上有7个电子
D. 砹能从NaCl溶液中置换出氯单质
C
3. 下列各组物质性质的比较中,正确的是( )
A.还原性:HF>HCl>HBr>HI
B.稳定性:HFC.与水反应由易到难:Cl2>Br2>I2>F2
D.氧化性:F2>Cl2>Br2>I2
D
第四章 物质结构 元素周期律
第一节 原子结构与元素周期表
第3课时 原子结构与元素的性质
一般金属元素最外层电子数≤4,具有金属性;
非金属元素最外层电子数≥4,具有非金属性。
金属性:金属元素的原子所具有的失去电子的能力;
非金属性:非金属元素的原子所具有的得到电子的能力。
碱金属元素
碱金属元素
一、碱金属元素
碱金属是一类化学性质非常活泼的金属,在自然界中都以化合态存在。
思考与讨论:
我们把第ⅠA族(除了氢)中的元素称为碱金属元素,为什么要把这些元素编在一个族呢?根据表中原子结构示意图(课本P93),完成表格,并思考和讨论下列问题。
思考与讨论:
(1)在周期表中,从上到下碱金属元素原子的核电荷数、原子半径的变化有什么特点?
(2)观察碱金属元素的原子结构示意图,它们的原子核外电子排布有什么特点?从哪一点能够推断出碱金属元素的化学性质具有相似性。
(3)请总结碱金属元素原子结构的相同点及递变性规律。
从上到下核电荷数逐渐增大,原子半径逐渐增大
最外层电子数相同,都为1,并且电子层数逐渐增大
最外层电子数相同
碱金属元素原子结构的相同点及递变性规律:
(1)相同点:
(2)递变性规律:
易失1个电子,具有还原性
失电子能力逐渐增强
金属性逐渐增强
还原性逐渐增强
思考:碱金属元素原子结构的相同点和递变性会对其性质产生哪些影响?
碱金属元素原子的最外层都有 个电子,在反应中都易 电子,生成 价的离子,表现出 ,在自然界中都以 存在。
【探究】碱金属化学性质的比较
【问题和预测】
(1)回忆第二章学过的知识,钠有哪些化学性质?
(2)结合锂、钠和钾的原子结构特点,请你预测锂、钾可能具有哪些与钠相似的化学性质?
1
失去1个
+1
化合态
还原性
钠可以和O2、H2O发生反应
都能与O2和H2O反应
【分析和结论】
(1)通过实验、观察,讨论并总结钠、钾有哪些相似的化学性质,与你最初根据原子结构特点进行的预测是否一致?
(2)从实验现象比较钾、钠与水反应的难易程度。由此,你能推断出锂与水反应的难易程度吗?
(3)通过比较碱金属与水反应的难易程度,你能发现与它们的原子结构有什么关系吗?由此,你能推断出碱金属元素化学性质的相似性和递变规律吗?
锂与水反应没有钠、钾与水反应剧烈
钠 钾
与氧气反应 先熔化成小球剧烈燃烧,火焰呈 色,生成 色固体 先熔化成小球剧烈燃烧,火焰呈 色。
与水反应(绿豆大一块) 在水面上、熔成银白色小球、在水面上四处 、并发出嘶嘶的响声、滴入酚酞溶液呈 色 在水面上, 成银白色、在水面上四处 、滴入酚酞溶液呈 色,有微弱爆炸
黄
淡黄
紫
浮
浮
熔
游动
游动
红
红
实验现象:
1. 碱金属的原子结构与化学性质的关系
(1)碱金属元素的化学性质相似
碱金属元素的原子最外层电子数相同,都是1个电子,它们的化学性质相似,都能与氧气等非金属单质以及水反应。
只有一种氧化物Li2O
氧化物有Na2O和Na2O2
(2)碱金属元素的化学性质具有递变性
随着核电荷数的增加,碱金属元素原子的电子层数逐渐增多,原子半径逐渐增大,原子核对最外层电子的引力逐渐减弱,原子失去最外层电子的能力逐渐增强。即从锂到铯,金属性逐渐增强。
2. 碱金属单质物理性质的相似性和规律性
Li
Na
K
Rb
Cs
碱金属单质 颜色和状态 密度(g.cm3) 熔点(℃) 沸点(℃)
Li 银白色,柔软 0.534 180.5 1347
Na 银白色,柔软 0.97 97.81 882.9
K 银白色,柔软 0.86 63.65 774
Rb 银白色,柔软 1.532 38.89 688
Cs 略带金属光泽,柔软 1.879 28.40 678.4
碱金属单质的主要物理性质
密度增大
熔点降低
沸点降低
比较柔软,有延展性;密度都比较小,熔点也都比较低,导热性和导电性都很好,如液态钠可用作核反应堆的传热介质。
保存在煤油中
保存在石蜡中
课堂练习:
1. 下列金属与水反应最剧烈的是( )
A.Li B.K C.Rb D.Cs
2. 下列对碱金属性质的叙述中,正确的是( )
A.都是银白色的柔软金属,密度都比较小
B.单质在空气中燃烧生成的都是过氧化物
C.碱金属单质都能与水反应生成碱和氢气
D.单质的熔、沸点随着原子序数的增加而升高
D
C
3. 碱金属钫(Fr)具有放射性,它是碱金属元素中最重的元素,下列预言错误的是( )
A.在碱金属中它具有最大的原子半径
B.它的氢氧化物化学式为FrOH,是一种极强的碱
C.钫在空气中燃烧时,只生成Fr2O
D.它能跟水反应生成相应的碱和氢气,由于反应剧烈而发生爆炸
C
卤族元素
二、卤族元素
卤族元素(简称卤素)是典型的非金属元素,它们在自然界都以化合态存在。
分析书本96页的表4-3,总结卤素单质的物理性质规律。
F2
Cl2
Br2
I2
卤素单质 颜色(常态) 密度 熔点(℃) 沸点(℃)
F2 淡黄绿色(气体) 1.69g/L(15℃) -219.6 -188.1
Cl2 黄绿色(气体) 3.214g/L(0℃) -101 -34.6
Br2 深红棕色(液体) 3.119g/cm3(20℃) -7.2 58.78
I2 紫黑色(固体) 4.93g/cm3 113.5 184.4
密度增大
熔沸点升高
卤素单质的颜色逐渐加深,状态由气态逐渐过渡到固态;密度逐渐增大,熔、沸点逐渐升高。
卤族单质的主要物理性质
注意:
①溴是常温常压下唯一的液态非金属单质。
②卤素单质都有毒,溴有很强的的腐蚀性,液溴易挥发,保存时要加一些水进行“水封”,碘可升华,淀粉溶液遇碘变蓝。
1. 卤素原子结构的相同点及递变性规律
(1)相同点:
(2)递变性规律:
F Cl Br I
① 从上往下,原子核电荷数逐渐增大 ;
② 从上往下,电子层数逐渐增大 ;
③ 从上往下,原子半径逐渐增大 。
易得1个电子,具有氧化性
得电子能力逐渐减弱
非金属性逐渐减弱
氧化性逐渐减弱
2. 卤素单质化学性质的相似性和递变性
(1)卤素单质与H2的反应
【思考与讨论】
(1)根据卤素单质与氢气的反应事实,讨论随着原子核电荷数的增多,卤素单质与氢气反应的规律性变化。
(2)根据卤素单质与H2的反应事实,讨论随着原子核电荷数的增多,卤素单质与H2反应的规律性变化。
从表中信息可知,从F2到I2:
①与氢气反应的难易程度:
②生成的氢化物的稳定性:
③卤素的非金属性强弱:
逐渐减弱
由易到难
逐渐减弱
氢化物的稳定性:HF HCl HBr HI
(2)卤素单质间的置换反应
【实验4-1】
分别向盛有4mLKBr溶液和4mLKI溶液的两支试管中加入1mL氯水,振荡,观察溶液的颜色变化,并与氯水的颜色进行比较。写出反应的化学方程式。
向盛有4mLKI溶液的试管中加入1mL溴水,振荡,观察溶液的颜色变化,并与溴水的颜色进行比较。写出反应的化学方程式。
实验操作 实验现象 化学方程式 结论
振荡静置后,溶液由无色变为 色 氧化性:_________
还原性:
_________
振荡静置后,溶液由无色变为 色
振荡静置后,溶液由无色变为 色
橙黄
褐
Cl2>Br2>I2
Cl-
褐
注意:因为F2能与H2O发生反应(2F2 + 2H2O = 4HF + O2),所以F2不能从其他卤化物的盐溶液中置换出卤素单质。
2. 卤素单质化学性质的相似性和递变性
(1)相似性(X表示卤素元素,不考虑放射性元素):原子都容易得到一个电子,卤素单质化学性质活泼,能与氢气、活泼金属和水反应。
与H2反应:
与H2O反应:
(2)递变性
随着核电荷数的增加,电子层数逐渐增多,原子半径逐渐增大,原子核对最外层电子的引力逐渐减弱,原子得到最外层电子的能力逐渐减弱。即从氟到碘,非金属性逐渐减弱。
课堂练习:
1. 下列关于卤族元素由上到下性质递变的叙述,正确的是( )
①单质的氧化性增强 ②单质的颜色加深 ③气态氢化物的稳定性增强
④单质的沸点升高 ⑤阴离子的还原性增强
A. ①②③ B. ②③④
C. ②④⑤ D. ④⑤
C
2. 砹是现知原子序数最大的卤族元素,根据卤素性质的递变规律 ,下列对砹及其化合物的叙述,正确的是( )
A. 与H2化合的能力:At2>I2
B. 砹在常温下为白色固体
C. 砹原子的最外电子层上有7个电子
D. 砹能从NaCl溶液中置换出氯单质
C
3. 下列各组物质性质的比较中,正确的是( )
A.还原性:HF>HCl>HBr>HI
B.稳定性:HF
D.氧化性:F2>Cl2>Br2>I2
D
