山东省泰安市新泰市2024-2025学年八年级下学期7月期末考试化学试卷(含答案)
文档属性
| 名称 | 山东省泰安市新泰市2024-2025学年八年级下学期7月期末考试化学试卷(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-12 00:00:00 | ||
图片预览


文档简介
山东省泰安市新泰市2024-2025学年八年级下学期7月期末考试化学试题
一、选择题
1.2025年6月5日世界环境日我国的主题为“美丽中国我先行”,倡导绿色发展、低碳生活、保护自然的生态文明理念。下列做法符合此理念的是
A.工业污水直接浇灌稻田 B.研发汽车尾气净化系统
C.加高工厂烟囱排放废气 D.废弃塑料垃圾露天焚烧
2.非遗,源于生活、世代相传,是中华文化的根脉,是民族智慧的结晶,下列传统非遗项目制作和展示过程中,主要发生物理变化的是
A.绍兴黄酒酿制 B.景德镇手工烧瓷
C.浏阳花炮燃放 D.陕北民间剪纸
3.新版《生活饮用水卫生标准》中的水质检测修订了镉、铅等的限量。这里的镉、铅指的是
A.原子 B.元素 C.分子 D.单质
4.下列实验操作正确的是
A.称量固体 B.取用固体
C.读取液体体积 D.加热液体
5.要学会从化学的视角认识世界,对下列实例和解释都正确的是
选项 事实 解释
A 金刚石和石墨的性质存在着明显差异 碳原子结构不同
B 水蒸发为水蒸气,所占气体变大 水分子体积变大
C 一氧化碳和二氧化碳化学性质不同 构成这两种物质的原子的结构不同
D 古代用墨汁书写的字画保存很长时间而不变色 在常温下,单质碳的化学性质不活泼
A.A B.B C.C D.D
6.下列关于空气的说法中,不正确的是
A.氧气可以供给呼吸,支持燃烧,钢铁冶炼,金属焊接
B.氮气是制造氮肥的重要原料
C.空气中稀有气体化学性质稳定,不能与其他任何物质发生化学反应
D.目前计入空气质量评价的主要污染物为、可吸入颗粒物、细颗粒物等
7.2025年1月10日全球首列碳纤维地铁列车“碳星快轨”在青岛地铁1号线开启运营之旅,其车体、转向架构架等主承载结构均采用碳纤维复合材料制造,实现了车辆性能的升级。碳纤维的主要成分是由碳原子直接构成的物质。下列关于碳纤维的说法正确的是
A.碳纤维是一种新型化合物 B.碳纤维与金刚石的物理性质完全相同
C.碳纤维在氧气中充分燃烧生成二氧化碳 D.碳纤维中碳原子的最外层电子数为6
8.下列关于沼气、煤、石油的说法正确的是
A.煤的液化、煤的焦化、煤的气化都属于物理变化
B.石油的分馏和煤的干馏都是化学变化
C.沼气的主要成分是甲烷
D.石油是一种由沸点不同的化合物组成的混合物,不加热就可以直接燃烧
9.我国科学家屠呦呦因发现青蒿素(化学式为C15H22O5)荣获诺贝尔医学奖,下列有关青蒿素的叙述正确的是
A.从质量上看:青蒿素中碳、氧元素的质量比为9:4
B.从宏观上看:青蒿素分子是由碳、氢、氧三种元素组成
C.从微观上看:青蒿素中含有15个碳原子、22个氢原子和5个氧原子
D.从变化上看:青蒿素在氧气中完全燃烧生成一氧化碳和水
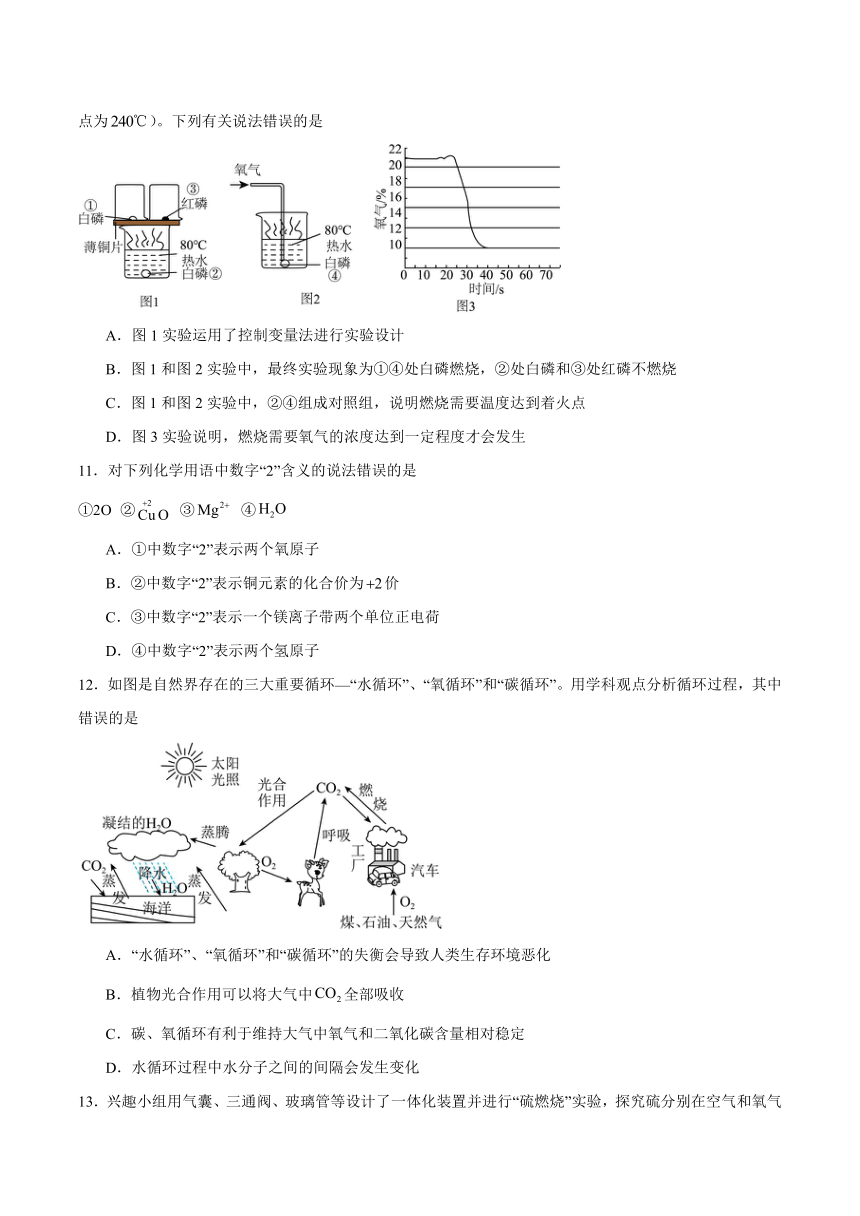
10.化学兴趣小组的同学根据课本实验探究燃烧的条件。图1、图2为实验装置图,图3是兴趣小组的同学利用氧气传感器测量木条在密闭容器中燃烧时,氧气浓度的变化情况(白磷的着火点为40℃,红磷的着火点为)。下列有关说法错误的是
A.图1实验运用了控制变量法进行实验设计
B.图1和图2实验中,最终实验现象为①④处白磷燃烧,②处白磷和③处红磷不燃烧
C.图1和图2实验中,②④组成对照组,说明燃烧需要温度达到着火点
D.图3实验说明,燃烧需要氧气的浓度达到一定程度才会发生
11.对下列化学用语中数字“2”含义的说法错误的是
①2O ② ③ ④
A.①中数字“2”表示两个氧原子
B.②中数字“2”表示铜元素的化合价为价
C.③中数字“2”表示一个镁离子带两个单位正电荷
D.④中数字“2”表示两个氢原子
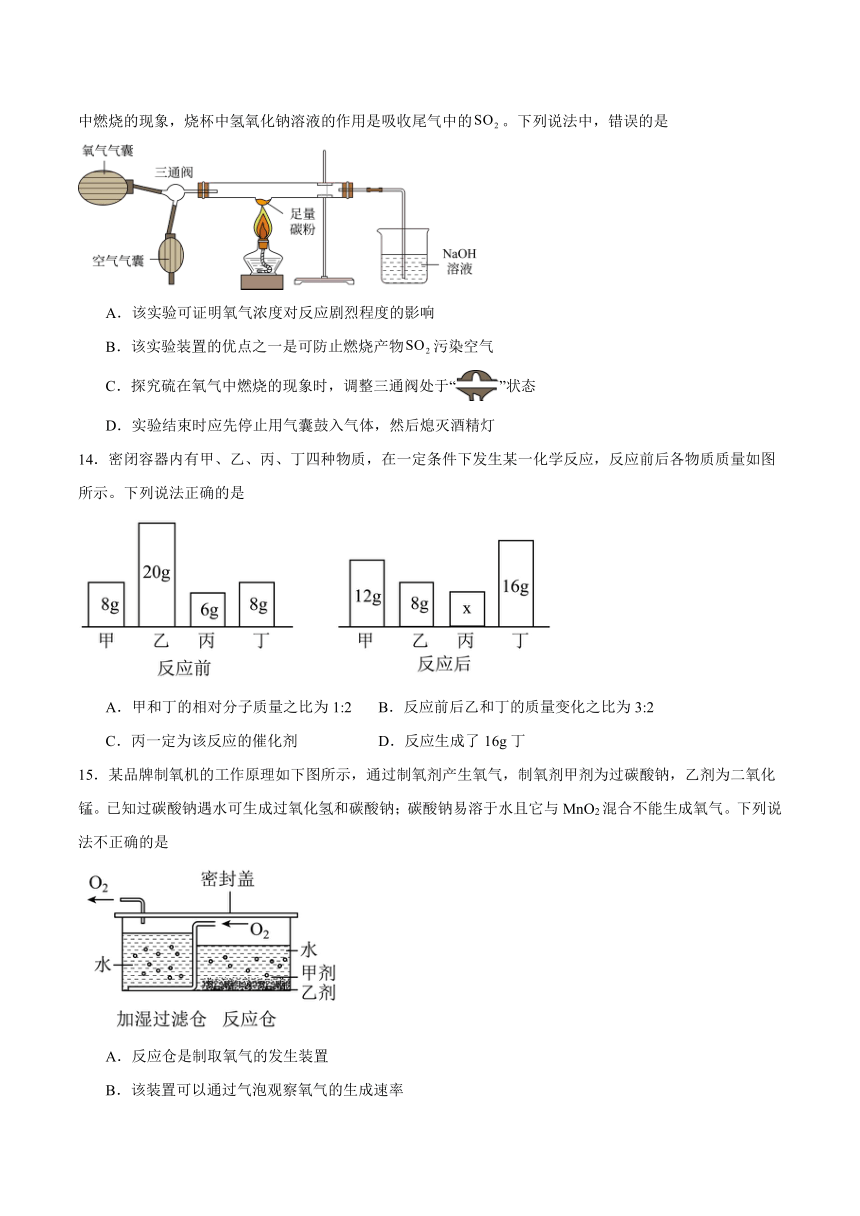
12.如图是自然界存在的三大重要循环—“水循环”、“氧循环”和“碳循环”。用学科观点分析循环过程,其中错误的是
A.“水循环”、“氧循环”和“碳循环”的失衡会导致人类生存环境恶化
B.植物光合作用可以将大气中全部吸收
C.碳、氧循环有利于维持大气中氧气和二氧化碳含量相对稳定
D.水循环过程中水分子之间的间隔会发生变化
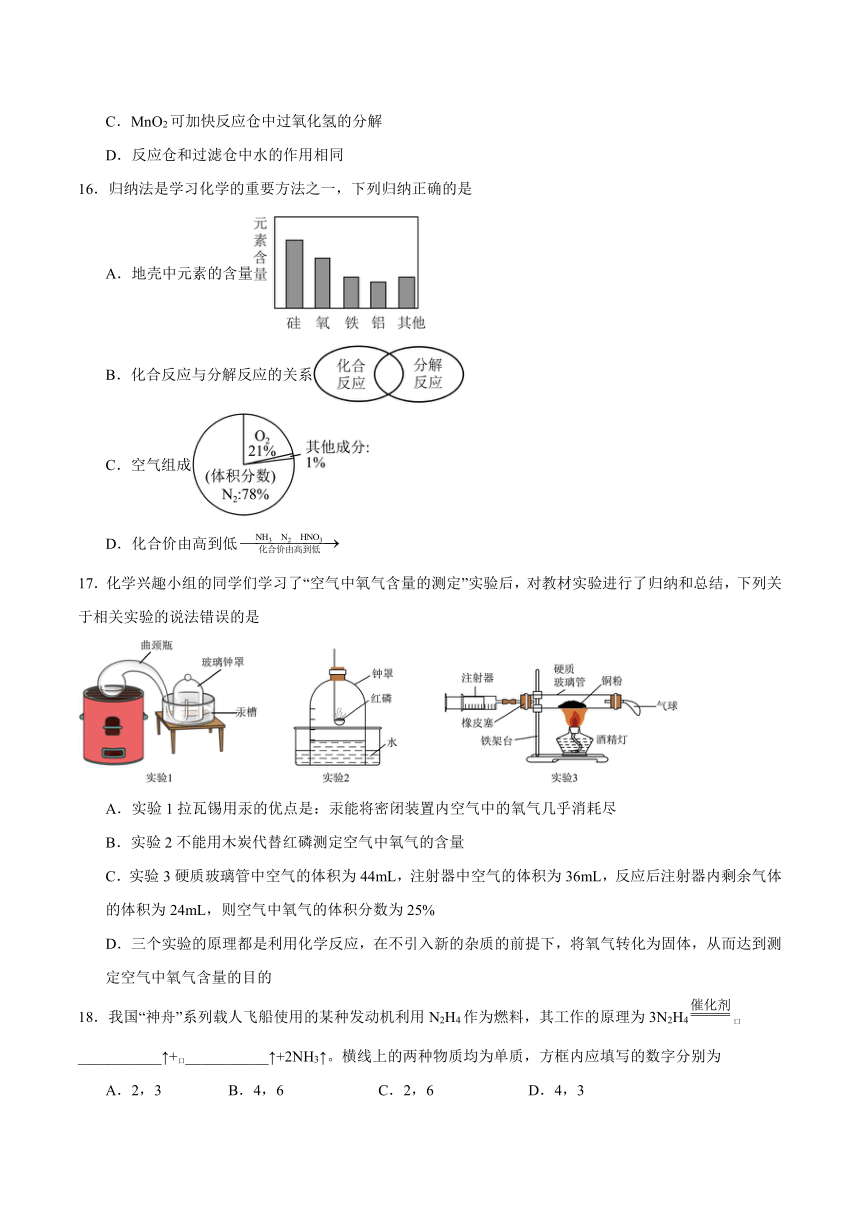
13.兴趣小组用气囊、三通阀、玻璃管等设计了一体化装置并进行“硫燃烧”实验,探究硫分别在空气和氧气中燃烧的现象,烧杯中氢氧化钠溶液的作用是吸收尾气中的。下列说法中,错误的是
A.该实验可证明氧气浓度对反应剧烈程度的影响
B.该实验装置的优点之一是可防止燃烧产物污染空气
C.探究硫在氧气中燃烧的现象时,调整三通阀处于“”状态
D.实验结束时应先停止用气囊鼓入气体,然后熄灭酒精灯
14.密闭容器内有甲、乙、丙、丁四种物质,在一定条件下发生某一化学反应,反应前后各物质质量如图所示。下列说法正确的是
A.甲和丁的相对分子质量之比为1:2 B.反应前后乙和丁的质量变化之比为3:2
C.丙一定为该反应的催化剂 D.反应生成了16g丁
15.某品牌制氧机的工作原理如下图所示,通过制氧剂产生氧气,制氧剂甲剂为过碳酸钠,乙剂为二氧化锰。已知过碳酸钠遇水可生成过氧化氢和碳酸钠;碳酸钠易溶于水且它与MnO2混合不能生成氧气。下列说法不正确的是
A.反应仓是制取氧气的发生装置
B.该装置可以通过气泡观察氧气的生成速率
C.MnO2可加快反应仓中过氧化氢的分解
D.反应仓和过滤仓中水的作用相同
16.归纳法是学习化学的重要方法之一,下列归纳正确的是
A.地壳中元素的含量
B.化合反应与分解反应的关系
C.空气组成
D.化合价由高到低
17.化学兴趣小组的同学们学习了“空气中氧气含量的测定”实验后,对教材实验进行了归纳和总结,下列关于相关实验的说法错误的是
A.实验1拉瓦锡用汞的优点是:汞能将密闭装置内空气中的氧气几乎消耗尽
B.实验2不能用木炭代替红磷测定空气中氧气的含量
C.实验3硬质玻璃管中空气的体积为44mL,注射器中空气的体积为36mL,反应后注射器内剩余气体的体积为24mL,则空气中氧气的体积分数为25%
D.三个实验的原理都是利用化学反应,在不引入新的杂质的前提下,将氧气转化为固体,从而达到测定空气中氧气含量的目的
18.我国“神舟”系列载人飞船使用的某种发动机利用N2H4作为燃料,其工作的原理为3N2H4口___________↑+口___________↑+2NH3↑。横线上的两种物质均为单质,方框内应填写的数字分别为
A.2,3 B.4,6 C.2,6 D.4,3
19.如图所示的四个图象,能正确反映对应变化关系的是
A.水的电解
B.木炭在密闭的容器内燃烧
C.加热一定量的高锰酸钾制氧气
D.铁丝在纯氧中燃烧
20.实验小组的同学按照如图1所示装置进行木炭还原氧化铜的实验,实验时,试管中固体的质量随加热时间的变化如图2所示,下列分析不正确的是
A.试管①中黑色固体逐渐变红,试管②中澄清石灰水变浑浊
B.该实验说明碳具有还原性
C.试管①中发生的化学反应为:
D.N点对应的固体物质有三种
二、填空与简答
21.从微观结构、宏观组成和符号表示等视角系统的认识物质是化学特有的思维方式。请根据所学知识结合下面的图片回答问题:
(1)图1中,b和c分别代表两种不同的物质类别,均属于纯净物,b是由一种元素组成的纯净物,则图中a、b处应分别填写 、 。
(2)下图中能够表示图1中c的是_______。
A. B. C. D.
(3)掌握分类的方法对于化学学习非常重要。下列物质中属于混合物的是 。
①高锰酸钾 ②氦气 ③稀盐酸 ④水 ⑤冰水混合物 ⑥氯化钠 ⑦空气 ⑧氢气 ⑨石油
(4)下列物质属于氧化物的是_______。
A. B. C. D.
(5)请用适当的化学用语填空。
①保持氧气化学性质的最小微粒 ;
②三个硝酸根离子 ;
③标出氯化铁中铁元素的化合价 ;
④干冰 。
22.请回答下列问题:
(1)北京冬奥会使用人工造雪技术,水通过造雪机变成雪的过程发生改变的是_______。
A.分子种类 B.分子间隔 C.分子数目 D.分子大小
(2)城市用的自来水取自于自然界,其净化过程如图1所示。操作a中玻璃棒的作用是 ;操作c主要发生的是化学变化,该过程为 。
(3)电解水时(如图2),产生氧气的一端连接的应是电源的 (填“正”或“负”)极,该反应化学方程式 。
(4)氢气被称为清洁能源,常用作航空燃料,根据图3的微观示意图写出相关反应的化学方程式 。
(5)节约用水是每个公民的义务,我们应该提倡以下方式中的_______(填字母序号)。
A.用淘米水、洗菜水浇花冲厕所
B.不间断地放水洗衣服
C.洗手后及时关上水龙头
23.元素周期表是学习和研究化学的重要工具。图1是核电荷数为1~18的元素原子结构示意图等信息,图2是溴原子的结构示意图,请结合图示内容回答下列问题:
(1)元素周期表同一周期从左往右,原子最外层电子排布规律是: ;
(2)图1中与图2溴元素化学性质相似的有 (写元素符号,任填一个);
(3)由图2可知,溴元素位于元素周期表中第 周期;
(4)13号铝元素的原子,在化学变化中容易 电子(填“得到”或“失去”),形成 离子(填“阳”或“阴”)。
(5)溴是海水中重要的非金属元素。地球上90%的溴元素以的形式存在于海水中,所以人们称溴为“海洋元素”。写出镁元素和溴元素组成的化合物的化学式 。
三、实验题
24.化学兴趣小组同学用下图装置制取气体。
(1)仪器①的名称是 。
(2)实验室使用高锰酸钾制取氧气,发生装置A试管口放一团棉花的原因是 ,收集装置选择 (填序号)。
(3)实验室制取二氧化碳的反应原理是 (用化学方程式表示),选择的发生装置是 (填序号)。
(4)将装置C和D连接,用于收集并测定生成二氧化碳的体积,产生的二氧化碳应从 (填“a”或“b”)端通入,装置C中植物油的作用是 。
(5)图2实验为证明二氧化碳和水发生反应,首先滴入Ⅰ处水,然后滴入H处稀盐酸,对比的实验现象为 。
25.某化学兴趣小组设计如下实验装置(A中加热装置已省略)验证质量守恒定律。
(1)装置A中将铜粉平铺于锥形瓶的底部,把上端系有小气球的玻璃导管插入单孔橡胶塞中,用橡胶塞塞紧锥形瓶口。将装置放在电子天平上称量,记录所称的质量。再将锥形瓶置于陶土网上,用酒精灯加热,反应一段时间后停止加热,冷却至室温后再次称量,观察到其间气球的变化是 ,记录所称的质量,则 (选填“>”“<”或“=”);
(2)利用装置B验证质量守恒定律时的现象为 ;
(3)利用装置C无法验证质量守恒定律,原因是 ;
(4)利用装置D验证质量守恒定律,反应前天平平衡,然后将烧杯倾斜,过氧化氢溶液与二氧化锰充分反应后再称量,观察天平指针向 (填“左”或“右”)偏转;
(5)小明受到装置A的启发,将装置D进行改进,如图E所示。称量反应前后质量,发现反应后总质量变小。若整个操作过程无差错,则造成上述实验结果的可能原因是 ;
(6)由质量守恒定律可知,化学反应前后,一定不变的是 (填序号)。
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质种类
四、计算题
26.菠萝具有芳香气味,是因为菠萝中含有丁酸乙酯(化学式,相对分子质量为116)。请计算:
(1)丁酸乙酯中,氧元素的质量分数是 (精确到1%).
(2)34.8g丁酸乙酯中含有 g碳元素。
27.某兴趣小组设计图1实验测定鱼骨中的碳酸钙含量,并将测得的数据绘制成图2。
提示:①醋酸和碳酸钙反应的化学方程式为CaCO3+2HAc=CaAc2+H2O+CO2↑。
②鱼骨中其他成分与食醋反应生成的气体可忽略不计。
(1)充分反应后产生二氧化碳气体的质量为 g。
(2)根据图中的数据计算鱼骨中碳酸钙的质量分数(写出计算过程)。
参考答案
1.B
2.D
3.B
4.D
5.D
6.C
7.C
8.C
9.A
10.C
11.D
12.B
13.D
14.B
15.D
16.C
17.C
18.A
19.C
20.C
21.(1) 分子 单质
(2)D
(3)③⑦⑨
(4)AD
(5)
22.(1)B
(2) 引流 杀菌消毒
(3) 正
(4).
(5)AC
23.(1)依次递增
(2)Cl/F
(3)四/4
(4) 失去 阳
(5)MgBr2
24.(1)铁架台
(2) 防止加热时试管内粉末状物质进入导管 E/F
(3) B
(4) a 防止二氧化碳溶于水,且与水反应
(5)①处纸花变红,②处纸花不变色
25.(1) 先膨胀后变瘪 =
(2)白色粉末逐渐溶解,有气泡产生,天平依然平衡
(3)酒精和水不发生化学变化
(4)右
(5)气球膨胀产生浮力
(6)①②⑤
26.(1)28%
(2)21.6
27.(1)0.11
(2)解:设鱼骨中碳酸钙的质量分数为x
x=1.25%
答:鱼骨中碳酸钙的质量分数为1.25%。
一、选择题
1.2025年6月5日世界环境日我国的主题为“美丽中国我先行”,倡导绿色发展、低碳生活、保护自然的生态文明理念。下列做法符合此理念的是
A.工业污水直接浇灌稻田 B.研发汽车尾气净化系统
C.加高工厂烟囱排放废气 D.废弃塑料垃圾露天焚烧
2.非遗,源于生活、世代相传,是中华文化的根脉,是民族智慧的结晶,下列传统非遗项目制作和展示过程中,主要发生物理变化的是
A.绍兴黄酒酿制 B.景德镇手工烧瓷
C.浏阳花炮燃放 D.陕北民间剪纸
3.新版《生活饮用水卫生标准》中的水质检测修订了镉、铅等的限量。这里的镉、铅指的是
A.原子 B.元素 C.分子 D.单质
4.下列实验操作正确的是
A.称量固体 B.取用固体
C.读取液体体积 D.加热液体
5.要学会从化学的视角认识世界,对下列实例和解释都正确的是
选项 事实 解释
A 金刚石和石墨的性质存在着明显差异 碳原子结构不同
B 水蒸发为水蒸气,所占气体变大 水分子体积变大
C 一氧化碳和二氧化碳化学性质不同 构成这两种物质的原子的结构不同
D 古代用墨汁书写的字画保存很长时间而不变色 在常温下,单质碳的化学性质不活泼
A.A B.B C.C D.D
6.下列关于空气的说法中,不正确的是
A.氧气可以供给呼吸,支持燃烧,钢铁冶炼,金属焊接
B.氮气是制造氮肥的重要原料
C.空气中稀有气体化学性质稳定,不能与其他任何物质发生化学反应
D.目前计入空气质量评价的主要污染物为、可吸入颗粒物、细颗粒物等
7.2025年1月10日全球首列碳纤维地铁列车“碳星快轨”在青岛地铁1号线开启运营之旅,其车体、转向架构架等主承载结构均采用碳纤维复合材料制造,实现了车辆性能的升级。碳纤维的主要成分是由碳原子直接构成的物质。下列关于碳纤维的说法正确的是
A.碳纤维是一种新型化合物 B.碳纤维与金刚石的物理性质完全相同
C.碳纤维在氧气中充分燃烧生成二氧化碳 D.碳纤维中碳原子的最外层电子数为6
8.下列关于沼气、煤、石油的说法正确的是
A.煤的液化、煤的焦化、煤的气化都属于物理变化
B.石油的分馏和煤的干馏都是化学变化
C.沼气的主要成分是甲烷
D.石油是一种由沸点不同的化合物组成的混合物,不加热就可以直接燃烧
9.我国科学家屠呦呦因发现青蒿素(化学式为C15H22O5)荣获诺贝尔医学奖,下列有关青蒿素的叙述正确的是
A.从质量上看:青蒿素中碳、氧元素的质量比为9:4
B.从宏观上看:青蒿素分子是由碳、氢、氧三种元素组成
C.从微观上看:青蒿素中含有15个碳原子、22个氢原子和5个氧原子
D.从变化上看:青蒿素在氧气中完全燃烧生成一氧化碳和水
10.化学兴趣小组的同学根据课本实验探究燃烧的条件。图1、图2为实验装置图,图3是兴趣小组的同学利用氧气传感器测量木条在密闭容器中燃烧时,氧气浓度的变化情况(白磷的着火点为40℃,红磷的着火点为)。下列有关说法错误的是
A.图1实验运用了控制变量法进行实验设计
B.图1和图2实验中,最终实验现象为①④处白磷燃烧,②处白磷和③处红磷不燃烧
C.图1和图2实验中,②④组成对照组,说明燃烧需要温度达到着火点
D.图3实验说明,燃烧需要氧气的浓度达到一定程度才会发生
11.对下列化学用语中数字“2”含义的说法错误的是
①2O ② ③ ④
A.①中数字“2”表示两个氧原子
B.②中数字“2”表示铜元素的化合价为价
C.③中数字“2”表示一个镁离子带两个单位正电荷
D.④中数字“2”表示两个氢原子
12.如图是自然界存在的三大重要循环—“水循环”、“氧循环”和“碳循环”。用学科观点分析循环过程,其中错误的是
A.“水循环”、“氧循环”和“碳循环”的失衡会导致人类生存环境恶化
B.植物光合作用可以将大气中全部吸收
C.碳、氧循环有利于维持大气中氧气和二氧化碳含量相对稳定
D.水循环过程中水分子之间的间隔会发生变化
13.兴趣小组用气囊、三通阀、玻璃管等设计了一体化装置并进行“硫燃烧”实验,探究硫分别在空气和氧气中燃烧的现象,烧杯中氢氧化钠溶液的作用是吸收尾气中的。下列说法中,错误的是
A.该实验可证明氧气浓度对反应剧烈程度的影响
B.该实验装置的优点之一是可防止燃烧产物污染空气
C.探究硫在氧气中燃烧的现象时,调整三通阀处于“”状态
D.实验结束时应先停止用气囊鼓入气体,然后熄灭酒精灯
14.密闭容器内有甲、乙、丙、丁四种物质,在一定条件下发生某一化学反应,反应前后各物质质量如图所示。下列说法正确的是
A.甲和丁的相对分子质量之比为1:2 B.反应前后乙和丁的质量变化之比为3:2
C.丙一定为该反应的催化剂 D.反应生成了16g丁
15.某品牌制氧机的工作原理如下图所示,通过制氧剂产生氧气,制氧剂甲剂为过碳酸钠,乙剂为二氧化锰。已知过碳酸钠遇水可生成过氧化氢和碳酸钠;碳酸钠易溶于水且它与MnO2混合不能生成氧气。下列说法不正确的是
A.反应仓是制取氧气的发生装置
B.该装置可以通过气泡观察氧气的生成速率
C.MnO2可加快反应仓中过氧化氢的分解
D.反应仓和过滤仓中水的作用相同
16.归纳法是学习化学的重要方法之一,下列归纳正确的是
A.地壳中元素的含量
B.化合反应与分解反应的关系
C.空气组成
D.化合价由高到低
17.化学兴趣小组的同学们学习了“空气中氧气含量的测定”实验后,对教材实验进行了归纳和总结,下列关于相关实验的说法错误的是
A.实验1拉瓦锡用汞的优点是:汞能将密闭装置内空气中的氧气几乎消耗尽
B.实验2不能用木炭代替红磷测定空气中氧气的含量
C.实验3硬质玻璃管中空气的体积为44mL,注射器中空气的体积为36mL,反应后注射器内剩余气体的体积为24mL,则空气中氧气的体积分数为25%
D.三个实验的原理都是利用化学反应,在不引入新的杂质的前提下,将氧气转化为固体,从而达到测定空气中氧气含量的目的
18.我国“神舟”系列载人飞船使用的某种发动机利用N2H4作为燃料,其工作的原理为3N2H4口___________↑+口___________↑+2NH3↑。横线上的两种物质均为单质,方框内应填写的数字分别为
A.2,3 B.4,6 C.2,6 D.4,3
19.如图所示的四个图象,能正确反映对应变化关系的是
A.水的电解
B.木炭在密闭的容器内燃烧
C.加热一定量的高锰酸钾制氧气
D.铁丝在纯氧中燃烧
20.实验小组的同学按照如图1所示装置进行木炭还原氧化铜的实验,实验时,试管中固体的质量随加热时间的变化如图2所示,下列分析不正确的是
A.试管①中黑色固体逐渐变红,试管②中澄清石灰水变浑浊
B.该实验说明碳具有还原性
C.试管①中发生的化学反应为:
D.N点对应的固体物质有三种
二、填空与简答
21.从微观结构、宏观组成和符号表示等视角系统的认识物质是化学特有的思维方式。请根据所学知识结合下面的图片回答问题:
(1)图1中,b和c分别代表两种不同的物质类别,均属于纯净物,b是由一种元素组成的纯净物,则图中a、b处应分别填写 、 。
(2)下图中能够表示图1中c的是_______。
A. B. C. D.
(3)掌握分类的方法对于化学学习非常重要。下列物质中属于混合物的是 。
①高锰酸钾 ②氦气 ③稀盐酸 ④水 ⑤冰水混合物 ⑥氯化钠 ⑦空气 ⑧氢气 ⑨石油
(4)下列物质属于氧化物的是_______。
A. B. C. D.
(5)请用适当的化学用语填空。
①保持氧气化学性质的最小微粒 ;
②三个硝酸根离子 ;
③标出氯化铁中铁元素的化合价 ;
④干冰 。
22.请回答下列问题:
(1)北京冬奥会使用人工造雪技术,水通过造雪机变成雪的过程发生改变的是_______。
A.分子种类 B.分子间隔 C.分子数目 D.分子大小
(2)城市用的自来水取自于自然界,其净化过程如图1所示。操作a中玻璃棒的作用是 ;操作c主要发生的是化学变化,该过程为 。
(3)电解水时(如图2),产生氧气的一端连接的应是电源的 (填“正”或“负”)极,该反应化学方程式 。
(4)氢气被称为清洁能源,常用作航空燃料,根据图3的微观示意图写出相关反应的化学方程式 。
(5)节约用水是每个公民的义务,我们应该提倡以下方式中的_______(填字母序号)。
A.用淘米水、洗菜水浇花冲厕所
B.不间断地放水洗衣服
C.洗手后及时关上水龙头
23.元素周期表是学习和研究化学的重要工具。图1是核电荷数为1~18的元素原子结构示意图等信息,图2是溴原子的结构示意图,请结合图示内容回答下列问题:
(1)元素周期表同一周期从左往右,原子最外层电子排布规律是: ;
(2)图1中与图2溴元素化学性质相似的有 (写元素符号,任填一个);
(3)由图2可知,溴元素位于元素周期表中第 周期;
(4)13号铝元素的原子,在化学变化中容易 电子(填“得到”或“失去”),形成 离子(填“阳”或“阴”)。
(5)溴是海水中重要的非金属元素。地球上90%的溴元素以的形式存在于海水中,所以人们称溴为“海洋元素”。写出镁元素和溴元素组成的化合物的化学式 。
三、实验题
24.化学兴趣小组同学用下图装置制取气体。
(1)仪器①的名称是 。
(2)实验室使用高锰酸钾制取氧气,发生装置A试管口放一团棉花的原因是 ,收集装置选择 (填序号)。
(3)实验室制取二氧化碳的反应原理是 (用化学方程式表示),选择的发生装置是 (填序号)。
(4)将装置C和D连接,用于收集并测定生成二氧化碳的体积,产生的二氧化碳应从 (填“a”或“b”)端通入,装置C中植物油的作用是 。
(5)图2实验为证明二氧化碳和水发生反应,首先滴入Ⅰ处水,然后滴入H处稀盐酸,对比的实验现象为 。
25.某化学兴趣小组设计如下实验装置(A中加热装置已省略)验证质量守恒定律。
(1)装置A中将铜粉平铺于锥形瓶的底部,把上端系有小气球的玻璃导管插入单孔橡胶塞中,用橡胶塞塞紧锥形瓶口。将装置放在电子天平上称量,记录所称的质量。再将锥形瓶置于陶土网上,用酒精灯加热,反应一段时间后停止加热,冷却至室温后再次称量,观察到其间气球的变化是 ,记录所称的质量,则 (选填“>”“<”或“=”);
(2)利用装置B验证质量守恒定律时的现象为 ;
(3)利用装置C无法验证质量守恒定律,原因是 ;
(4)利用装置D验证质量守恒定律,反应前天平平衡,然后将烧杯倾斜,过氧化氢溶液与二氧化锰充分反应后再称量,观察天平指针向 (填“左”或“右”)偏转;
(5)小明受到装置A的启发,将装置D进行改进,如图E所示。称量反应前后质量,发现反应后总质量变小。若整个操作过程无差错,则造成上述实验结果的可能原因是 ;
(6)由质量守恒定律可知,化学反应前后,一定不变的是 (填序号)。
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质种类
四、计算题
26.菠萝具有芳香气味,是因为菠萝中含有丁酸乙酯(化学式,相对分子质量为116)。请计算:
(1)丁酸乙酯中,氧元素的质量分数是 (精确到1%).
(2)34.8g丁酸乙酯中含有 g碳元素。
27.某兴趣小组设计图1实验测定鱼骨中的碳酸钙含量,并将测得的数据绘制成图2。
提示:①醋酸和碳酸钙反应的化学方程式为CaCO3+2HAc=CaAc2+H2O+CO2↑。
②鱼骨中其他成分与食醋反应生成的气体可忽略不计。
(1)充分反应后产生二氧化碳气体的质量为 g。
(2)根据图中的数据计算鱼骨中碳酸钙的质量分数(写出计算过程)。
参考答案
1.B
2.D
3.B
4.D
5.D
6.C
7.C
8.C
9.A
10.C
11.D
12.B
13.D
14.B
15.D
16.C
17.C
18.A
19.C
20.C
21.(1) 分子 单质
(2)D
(3)③⑦⑨
(4)AD
(5)
22.(1)B
(2) 引流 杀菌消毒
(3) 正
(4).
(5)AC
23.(1)依次递增
(2)Cl/F
(3)四/4
(4) 失去 阳
(5)MgBr2
24.(1)铁架台
(2) 防止加热时试管内粉末状物质进入导管 E/F
(3) B
(4) a 防止二氧化碳溶于水,且与水反应
(5)①处纸花变红,②处纸花不变色
25.(1) 先膨胀后变瘪 =
(2)白色粉末逐渐溶解,有气泡产生,天平依然平衡
(3)酒精和水不发生化学变化
(4)右
(5)气球膨胀产生浮力
(6)①②⑤
26.(1)28%
(2)21.6
27.(1)0.11
(2)解:设鱼骨中碳酸钙的质量分数为x
x=1.25%
答:鱼骨中碳酸钙的质量分数为1.25%。
同课章节目录
