2.3《醛和酮 糖类和核酸舌尖上的有机物——糖类》教学课件(32页ppt)-鲁科版高中化学(2019)选择性必修三
文档属性
| 名称 | 2.3《醛和酮 糖类和核酸舌尖上的有机物——糖类》教学课件(32页ppt)-鲁科版高中化学(2019)选择性必修三 |

|
|
| 格式 | pptx | ||
| 文件大小 | 21.2MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-14 00:00:00 | ||
图片预览










文档简介
(共32张PPT)
舌尖上的有机物
——糖类
新课导入
学习目标
本节重点
葡萄糖的结构与性质
本节难点
糖类结构探析
1.认识糖类的分子结构,从官能团角度探析糖类的性质,掌握葡萄糖、蔗糖和淀粉的特征反应;
2.通过模型搭建,理解葡萄糖由链式结构转化为氧环式的过程;
3.能够设计实验确定淀粉水解产物及水解程度,能够规范地进行实验操作;
4.联系实际应用,体会糖类在生活中的意义。
1.组成:
糖类是由C、H、O三种元素组成。这一类物质化学组成大多符合Cn(H2O)m的通式,因此糖类也被称为碳水化合物。
糖类的组成及分类
不是所有的糖类都有甜味,如淀粉、纤维素;有甜味的不一定是糖。木糖醇和糖精
【思考1】组成符合Cn(H2O)m通式的有机物是否一定属于糖类?糖类组成一定符合符合Cn(H2O)m通式嘛?
【思考2】糖类一定有甜味嘛,有甜味的一定是糖嘛?
符合Cn(H2O)m不一定是糖,如:乙酸分子式为C2H4O2 也符合C2(H2O)2。糖类组成不一定都符合Cn(H2O)m ,如:脱氧核糖C5H10O4。
葡萄糖 果糖
C6H12O6
蔗糖 麦芽糖 乳糖
C12H22O11
淀粉 纤维素
(C6H10O5)n
单糖
不能水解
二糖
水解成两分子单糖
多糖
水解成多分子单糖
2.分类
依据:能否水解和水解产物的多少进行分类
它们的结构和性质如何?
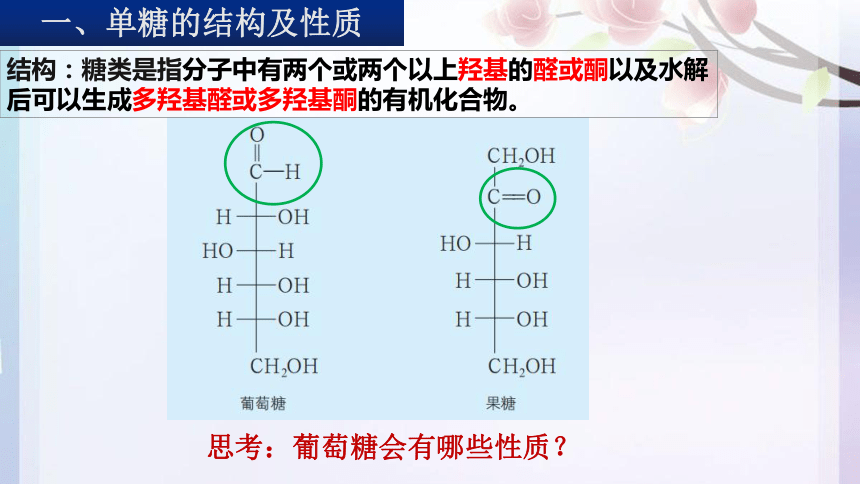
一、单糖的结构及性质
结构:糖类是指分子中有两个或两个以上羟基的醛或酮以及水解后可以生成多羟基醛或多羟基酮的有机化合物。
思考:葡萄糖会有哪些性质?
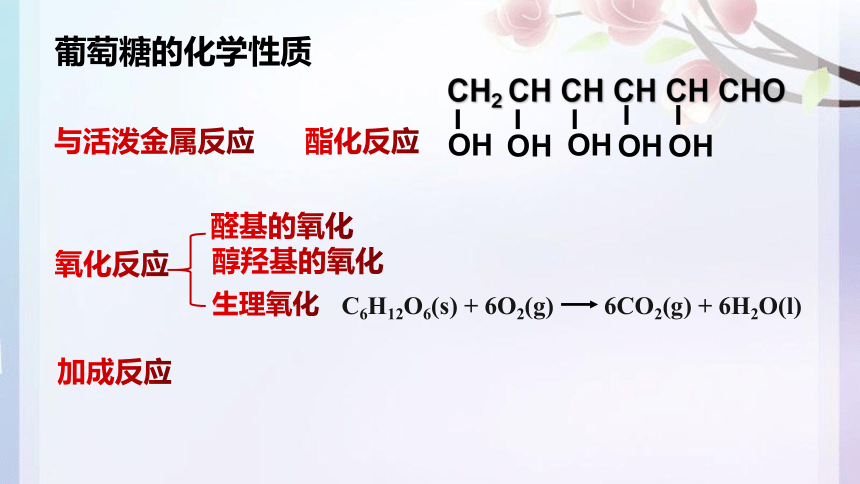
与活泼金属反应
CH2 CH CH CH CH CHO
OH
OH
OH
OH
OH
葡萄糖的化学性质
酯化反应
生理氧化
C6H12O6(s) + 6O2(g) 6CO2(g) + 6H2O(l)
氧化反应
醛基的氧化
醇羟基的氧化
加成反应
操作注意事项:
1.试管中装液不超过1/3;试管夹夹在试管的中上部(距管口约 1/3~1/4 处)
2.先均匀加热试管整体(移动试管),再集中加热液体部位,避免局部过热。
3.试管与桌面成 45°角,管口勿对人(朝向无人的方向)
1.新制氢氧化铜悬浊液
2.银氨溶液
检验醛基:
过量
加热煮沸
水浴加热
加热过程不能触碰试管
特征反应 (醛基)
①与新制Cu(OH)2悬浊液反应
实验操作
实验现象
实验结论
4-5滴 5%CuSO4
2mL 10%NaOH
试管
含NaOH的Cu(OH)2悬浊液
加入2ml10%葡萄糖溶液加热煮沸
?
试管内产生砖红色沉淀Cu2O
葡萄糖具有还原性,被新制Cu(OH)2悬浊液氧化
实验操作
实验现象
实验结论
最终试管内部产生光亮的银镜
银氨溶液中Ag+被还原成Ag,葡萄糖具有还原性
试管
2mL 2%AgNO3
边振荡边滴加2%的稀氨水至沉淀恰好溶解
水浴加热
1mL 10%葡萄糖溶液
?
葡萄糖可以用于制镜工业
思考:果糖是非还原糖,为什么生物课上老师讲,果糖也可以用斐林试剂(新制氢氧化铜悬浊液)检验呢?
阅读实验卡中的资料卡片2
可用什么试剂区分葡萄糖和果糖溶液?
溴水
酮式→烯醇式→醛式
葡萄糖的氧环式结构
葡萄糖分子中的羟基和醛基相互作用形成氧环式结构。葡萄糖分子由链式结构转化为氧环式 结构的过程可表示为:
加成反应
5
5
蔗糖
二、双糖——麦芽糖和蔗糖
麦芽糖
-O-CH-OH结构
分子式:C12H22011
如何验证蔗糖和麦芽糖是否属于还原糖?
二、双糖——麦芽糖和蔗糖
实验内容 实验现象 结论
(1)在一支洁净的试管中配制约2 mL氢氧化铜悬浊液,加入 1 mL 10%蔗糖溶液,振荡,然后加热煮沸。观察实验现象。
(2)在一支洁净的试管中配制约2 mL氢氧化铜悬浊液,加入 1 mL 10%麦芽糖溶液,振荡,然后加热煮沸。观察实验现象。
麦芽糖分子含有醛基,属于还原糖;
蔗糖分子不含醛基,不是还原糖。
《实验探究》:如何验证蔗糖在稀硫酸存在且加热的条件下是否发生了水解反应?
实验操作:向试管中加入1ml蔗糖溶液,加入2-3滴稀硫酸,加热几分钟。
催化剂
【思考】为了验证蔗糖水解生成了葡萄糖,可以在其水解液中直接滴加银氨溶液或者新制的氢氧化铜进行检验吗?
蔗糖
水解液
稀硫酸
NaOH溶液
调至碱性
新制氢氧
化铜悬浊液
使用PH试纸规范操作:撕、放、蘸、点、比
蔗糖和麦芽糖
蔗糖 麦芽糖
分子式
分子结构
化学性质
鉴别方法 C12H22O11
C12H22O11
分子中无醛基
分子中有醛基
互为同分异构体
水解生成葡萄糖和果糖
水解生成葡萄糖
非还原性糖、与银氨溶液或新制Cu(OH)2悬浊液不反应
还原性糖、与银氨溶液或新制Cu(OH)2悬浊液反应
向其溶液中分别加入银氨溶液,水浴加热,能发生银镜反应的是麦芽糖,不能发生银镜反应的是蔗糖(也可用新制氢氧化铜悬浊液来鉴别)
2024年浙江高考真题改编:
判断正误:
麦芽糖与稀硫酸共热后加氢氧化钠溶液调至碱性,再加入氢氧化铜并加热,可判断麦芽糖是否水解 ; ( )
【高考链接】
木糖醇
甜味剂
淀粉和纤维素是最重要的多糖,它们都是由大量葡萄糖单元相互连接组成的,属于天然有机高分子。淀粉和纤维素分子式可以表示为(C6H10O5)n
三、多糖——淀粉和纤维素
淀粉的特征反应:遇碘单质变蓝,可以利用该性质检验淀粉或碘单质
在葡萄糖的水溶液中,存在着链式结构与两种氧环式结构(α-D-葡萄糖和 β-D-葡萄糖)的平衡。
α-D-葡萄糖分子中,1 号和 2 号碳原子上的羟基在环的同一侧;β-D-葡萄糖分子中,1 号 和 2 号碳原子上的羟基在环的两侧。
α-葡萄糖分子间脱水聚合形成淀粉分子
β-葡萄糖分子间脱水聚合形成纤维素分子
淀粉的水解:
思考:淀粉在酸的作用下水解程度如何判断?
酸或酶
(C6H10O5)n+nH2O
nC6H12O6
淀粉
葡萄糖
【实验探究】淀粉水解程度的判断?
现象 B
碘水
淀粉
溶液
水解液
中和液
现象 A
稀硫酸
微热
NaOH溶液
新制氢氧化铜
加热
现象A 现象B 结论
① 未出现砖红色沉淀 溶液变成蓝色 淀粉尚未水解
② 出现砖红色沉淀 溶液变成蓝色 淀粉部分水解
③ 出现砖红色沉淀 溶液不变蓝色 淀粉完全水解
三种情况:淀粉未水解、部分水解、完全水解
淀粉的用途:
淀粉是食物的一种重要成分,也是重要的工业原料。
(1)以淀粉或淀粉水解生成的葡萄糖等为原料---发酵
燃料乙醇、白酒、食醋、味精, 以及氨基酸、抗生素等药物
可用于生产食品添加剂、表面活性剂和可降解塑料等
(2)淀粉酯化
【资料卡片3】
探究纤维素的化学性质
纤维素的化学性质:
化学性质与淀粉类似,在酸或酶的作用下水解,最终生成葡萄糖。
酸或酶
(C6H10O5)n+nH2O
nC6H12O6
纤维素在人体内不能水解,因为人体内没有纤维素酶,因此不能作为人类的能量来源。但适当摄入粗纤维食品,可以刺激肠道蠕动,助消化。
(3).酯化反应
纤维素醋酸酯,俗称醋酸纤维
浓硫酸
3n HOOCCH3
纤维素的用途:
制造纤维素乙酸酯(醋酸纤维):不易燃烧,可用于生产塑料、过滤膜、胶片等
制造纤维素硝酸酯(硝酸纤维):极易燃烧。可用于生产火药、塑料和涂料等。
淀粉 纤维素
分子式
关系 化学性质
存在
用途
(C6H10O5)n
(C6H10O5)n
均为天然高分子化合物
不互为同分异构体(n不同,纤维素一般较大)
①无还原性
②能水解生成葡萄糖
③遇碘单质变蓝(检验淀粉)
①无还原性
②能水解生成葡萄糖(较困难)
植物细胞壁的主要成分
植物种子或块根里
制备葡萄糖和酒精,人体的能源之一
纺织、造纸、制纤维素硝酸酯、纤维素乙酸酯等
【归纳提升3】
课堂小结结构识层面:性质方法生产生活化学问题联系生产生活实际糖类学反应速还原糖和非还原糖水解:条件、产物检验链式结构氧环式结构酮式→烯醇式异构
舌尖上的有机物
——糖类
新课导入
学习目标
本节重点
葡萄糖的结构与性质
本节难点
糖类结构探析
1.认识糖类的分子结构,从官能团角度探析糖类的性质,掌握葡萄糖、蔗糖和淀粉的特征反应;
2.通过模型搭建,理解葡萄糖由链式结构转化为氧环式的过程;
3.能够设计实验确定淀粉水解产物及水解程度,能够规范地进行实验操作;
4.联系实际应用,体会糖类在生活中的意义。
1.组成:
糖类是由C、H、O三种元素组成。这一类物质化学组成大多符合Cn(H2O)m的通式,因此糖类也被称为碳水化合物。
糖类的组成及分类
不是所有的糖类都有甜味,如淀粉、纤维素;有甜味的不一定是糖。木糖醇和糖精
【思考1】组成符合Cn(H2O)m通式的有机物是否一定属于糖类?糖类组成一定符合符合Cn(H2O)m通式嘛?
【思考2】糖类一定有甜味嘛,有甜味的一定是糖嘛?
符合Cn(H2O)m不一定是糖,如:乙酸分子式为C2H4O2 也符合C2(H2O)2。糖类组成不一定都符合Cn(H2O)m ,如:脱氧核糖C5H10O4。
葡萄糖 果糖
C6H12O6
蔗糖 麦芽糖 乳糖
C12H22O11
淀粉 纤维素
(C6H10O5)n
单糖
不能水解
二糖
水解成两分子单糖
多糖
水解成多分子单糖
2.分类
依据:能否水解和水解产物的多少进行分类
它们的结构和性质如何?
一、单糖的结构及性质
结构:糖类是指分子中有两个或两个以上羟基的醛或酮以及水解后可以生成多羟基醛或多羟基酮的有机化合物。
思考:葡萄糖会有哪些性质?
与活泼金属反应
CH2 CH CH CH CH CHO
OH
OH
OH
OH
OH
葡萄糖的化学性质
酯化反应
生理氧化
C6H12O6(s) + 6O2(g) 6CO2(g) + 6H2O(l)
氧化反应
醛基的氧化
醇羟基的氧化
加成反应
操作注意事项:
1.试管中装液不超过1/3;试管夹夹在试管的中上部(距管口约 1/3~1/4 处)
2.先均匀加热试管整体(移动试管),再集中加热液体部位,避免局部过热。
3.试管与桌面成 45°角,管口勿对人(朝向无人的方向)
1.新制氢氧化铜悬浊液
2.银氨溶液
检验醛基:
过量
加热煮沸
水浴加热
加热过程不能触碰试管
特征反应 (醛基)
①与新制Cu(OH)2悬浊液反应
实验操作
实验现象
实验结论
4-5滴 5%CuSO4
2mL 10%NaOH
试管
含NaOH的Cu(OH)2悬浊液
加入2ml10%葡萄糖溶液加热煮沸
?
试管内产生砖红色沉淀Cu2O
葡萄糖具有还原性,被新制Cu(OH)2悬浊液氧化
实验操作
实验现象
实验结论
最终试管内部产生光亮的银镜
银氨溶液中Ag+被还原成Ag,葡萄糖具有还原性
试管
2mL 2%AgNO3
边振荡边滴加2%的稀氨水至沉淀恰好溶解
水浴加热
1mL 10%葡萄糖溶液
?
葡萄糖可以用于制镜工业
思考:果糖是非还原糖,为什么生物课上老师讲,果糖也可以用斐林试剂(新制氢氧化铜悬浊液)检验呢?
阅读实验卡中的资料卡片2
可用什么试剂区分葡萄糖和果糖溶液?
溴水
酮式→烯醇式→醛式
葡萄糖的氧环式结构
葡萄糖分子中的羟基和醛基相互作用形成氧环式结构。葡萄糖分子由链式结构转化为氧环式 结构的过程可表示为:
加成反应
5
5
蔗糖
二、双糖——麦芽糖和蔗糖
麦芽糖
-O-CH-OH结构
分子式:C12H22011
如何验证蔗糖和麦芽糖是否属于还原糖?
二、双糖——麦芽糖和蔗糖
实验内容 实验现象 结论
(1)在一支洁净的试管中配制约2 mL氢氧化铜悬浊液,加入 1 mL 10%蔗糖溶液,振荡,然后加热煮沸。观察实验现象。
(2)在一支洁净的试管中配制约2 mL氢氧化铜悬浊液,加入 1 mL 10%麦芽糖溶液,振荡,然后加热煮沸。观察实验现象。
麦芽糖分子含有醛基,属于还原糖;
蔗糖分子不含醛基,不是还原糖。
《实验探究》:如何验证蔗糖在稀硫酸存在且加热的条件下是否发生了水解反应?
实验操作:向试管中加入1ml蔗糖溶液,加入2-3滴稀硫酸,加热几分钟。
催化剂
【思考】为了验证蔗糖水解生成了葡萄糖,可以在其水解液中直接滴加银氨溶液或者新制的氢氧化铜进行检验吗?
蔗糖
水解液
稀硫酸
NaOH溶液
调至碱性
新制氢氧
化铜悬浊液
使用PH试纸规范操作:撕、放、蘸、点、比
蔗糖和麦芽糖
蔗糖 麦芽糖
分子式
分子结构
化学性质
鉴别方法 C12H22O11
C12H22O11
分子中无醛基
分子中有醛基
互为同分异构体
水解生成葡萄糖和果糖
水解生成葡萄糖
非还原性糖、与银氨溶液或新制Cu(OH)2悬浊液不反应
还原性糖、与银氨溶液或新制Cu(OH)2悬浊液反应
向其溶液中分别加入银氨溶液,水浴加热,能发生银镜反应的是麦芽糖,不能发生银镜反应的是蔗糖(也可用新制氢氧化铜悬浊液来鉴别)
2024年浙江高考真题改编:
判断正误:
麦芽糖与稀硫酸共热后加氢氧化钠溶液调至碱性,再加入氢氧化铜并加热,可判断麦芽糖是否水解 ; ( )
【高考链接】
木糖醇
甜味剂
淀粉和纤维素是最重要的多糖,它们都是由大量葡萄糖单元相互连接组成的,属于天然有机高分子。淀粉和纤维素分子式可以表示为(C6H10O5)n
三、多糖——淀粉和纤维素
淀粉的特征反应:遇碘单质变蓝,可以利用该性质检验淀粉或碘单质
在葡萄糖的水溶液中,存在着链式结构与两种氧环式结构(α-D-葡萄糖和 β-D-葡萄糖)的平衡。
α-D-葡萄糖分子中,1 号和 2 号碳原子上的羟基在环的同一侧;β-D-葡萄糖分子中,1 号 和 2 号碳原子上的羟基在环的两侧。
α-葡萄糖分子间脱水聚合形成淀粉分子
β-葡萄糖分子间脱水聚合形成纤维素分子
淀粉的水解:
思考:淀粉在酸的作用下水解程度如何判断?
酸或酶
(C6H10O5)n+nH2O
nC6H12O6
淀粉
葡萄糖
【实验探究】淀粉水解程度的判断?
现象 B
碘水
淀粉
溶液
水解液
中和液
现象 A
稀硫酸
微热
NaOH溶液
新制氢氧化铜
加热
现象A 现象B 结论
① 未出现砖红色沉淀 溶液变成蓝色 淀粉尚未水解
② 出现砖红色沉淀 溶液变成蓝色 淀粉部分水解
③ 出现砖红色沉淀 溶液不变蓝色 淀粉完全水解
三种情况:淀粉未水解、部分水解、完全水解
淀粉的用途:
淀粉是食物的一种重要成分,也是重要的工业原料。
(1)以淀粉或淀粉水解生成的葡萄糖等为原料---发酵
燃料乙醇、白酒、食醋、味精, 以及氨基酸、抗生素等药物
可用于生产食品添加剂、表面活性剂和可降解塑料等
(2)淀粉酯化
【资料卡片3】
探究纤维素的化学性质
纤维素的化学性质:
化学性质与淀粉类似,在酸或酶的作用下水解,最终生成葡萄糖。
酸或酶
(C6H10O5)n+nH2O
nC6H12O6
纤维素在人体内不能水解,因为人体内没有纤维素酶,因此不能作为人类的能量来源。但适当摄入粗纤维食品,可以刺激肠道蠕动,助消化。
(3).酯化反应
纤维素醋酸酯,俗称醋酸纤维
浓硫酸
3n HOOCCH3
纤维素的用途:
制造纤维素乙酸酯(醋酸纤维):不易燃烧,可用于生产塑料、过滤膜、胶片等
制造纤维素硝酸酯(硝酸纤维):极易燃烧。可用于生产火药、塑料和涂料等。
淀粉 纤维素
分子式
关系 化学性质
存在
用途
(C6H10O5)n
(C6H10O5)n
均为天然高分子化合物
不互为同分异构体(n不同,纤维素一般较大)
①无还原性
②能水解生成葡萄糖
③遇碘单质变蓝(检验淀粉)
①无还原性
②能水解生成葡萄糖(较困难)
植物细胞壁的主要成分
植物种子或块根里
制备葡萄糖和酒精,人体的能源之一
纺织、造纸、制纤维素硝酸酯、纤维素乙酸酯等
【归纳提升3】
课堂小结结构识层面:性质方法生产生活化学问题联系生产生活实际糖类学反应速还原糖和非还原糖水解:条件、产物检验链式结构氧环式结构酮式→烯醇式异构
