2025年上海市中考化学复习重点题练习试卷(无答案)
文档属性
| 名称 | 2025年上海市中考化学复习重点题练习试卷(无答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 110.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-14 00:00:00 | ||
图片预览



文档简介
2025年上海市中考化学复习重点题练习试卷
一、单选题:本大题共14小题,共14分。
1.化学用语是学习化学的工具,下列表示两个氧离子的是( )
A. O2 B. 2O C. D. 2O2-
2.类比推理在化学学习和科学研究中有重要意义,下列说法正确的是( )
A. 单质中只含有一种元素,所以只含有一种元素的物质一定是单质
B. 点燃氢气前要检验其纯度,所以点燃可燃性气体前一定要验纯
C. 阴离子是带负电的粒子,所以带负电的粒子一定是阴离子
D. 氧化物中一定含有氧元素,所以含有氧元素的化合物一定是氧化物
3.下列关于金属的说法中正确的是( )
A. 金属材料在常温下都是固体 B. 人类最早大量使用的金属是铁
C. 金属的性质是决定金属用途的唯一因素 D. 生铁和不锈钢都是铁的合金
4.下列各组物质俗称、化学式及名称正确的是( )
A. 石灰石、CaCO3、碳酸钙 B. 乙醇、C2H3OH、酒精
C. 火碱、NaOH、氢氧化钠 D. 天然气、CH4、甲烷
5.下列有关空气的说法正确的是( )
A. 洁净的空气属于纯净物 B. 空气是由空气分子构成的
C. 空气中二氧化碳是空气污染物 D. 空气中氮气可用作保护气
6.如图为氮元素的部分化合价、物质类别二维图。下列说法错误的是( )
A. a点物质在空气中体积分数最高 B. b点物质属于大气污染物
C. c点物质的名称为硝酸 D. d点物质可能是KNO3
7.某同学测出身边一些物质的pH如下表。有关分析正确的是( )
物质 柠檬汁 西瓜汁 茶水 鸡蛋清
pH 2.6 5.8 7.5 9.0
A. 仅鸡蛋清呈碱性 B. 西瓜汁比柠檬汁酸性强
C. 茶水中滴入酚酞,溶液变红 D. 胃酸过多的人应多饮西瓜汁
8.习近平总书记在党的二十大报告中指出:“推动绿色发展,促进人与自然和谐共生”。下列措施与此理念不相符的是( )
A. 合理使用农药和化肥 B. 就地焚烧植物秸秆
C. 废旧金属回收利用 D. 工业废水达标后再排放
9.在一个密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如图所示。下列说法正确的是( )
A. x=14 B. 乙一定是催化剂
C. 该反应属于化合反应 D. 反应中丙和丁的质量之比是14:11
10.科学家发现了纯碳新材料“碳纳米泡沫”,泡沫由许多团簇组成,每个团簇含有约4000个碳原子.“碳纳米泡沫”是目前世上最轻的物质之一,密度为2mg/cm3.有铁磁性,是热和电的不良导体.下列说法不正确的是( )
A. “碳纳米泡沫”由碳元素组成 B. “碳纳米泡沫”能被磁铁吸引
C. “碳纳米泡沫”和金刚石的性质相同 D. “碳纳米泡沫”能浮在水面上
11.下列物质可以发生反应,但必须加入指示剂才能证明反应发生的是( )
A. 碳酸钠溶液和石灰水 B. 大理石和稀盐酸
C. 氢氧化钠溶液和二氧化碳 D. 氢氧化钠溶液和稀盐酸
12.阿奇霉素(C38H72N2O12)主要用于滑疗呼吸道等疾病,在酸性环境下很稳定。下列对阿奇霉素的描述正确的是( )
A. 属于氧化物 B. 能与酸反应
C. 它可以溶于水 D. 氢、氧元素的质量比为72:12
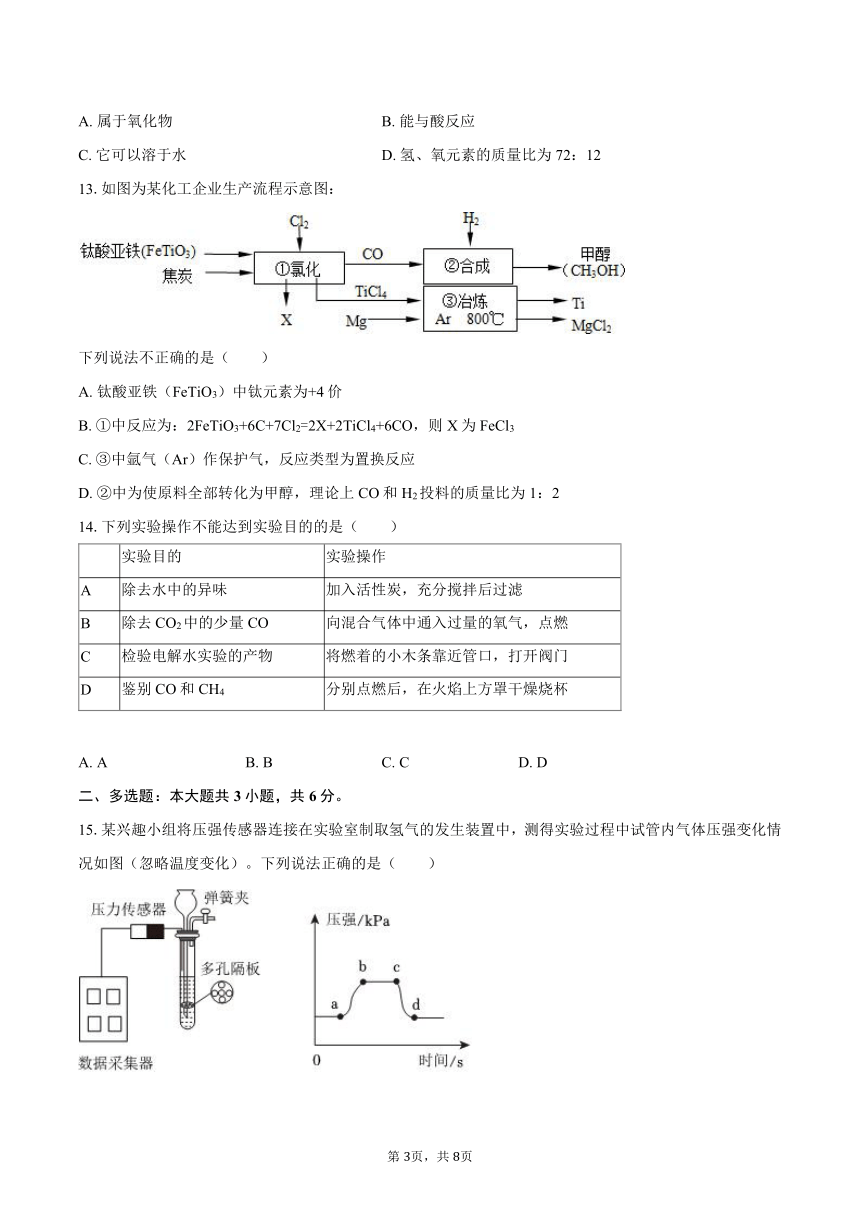
13.如图为某化工企业生产流程示意图:
下列说法不正确的是( )
A. 钛酸亚铁(FeTiO3)中钛元素为+4价
B. ①中反应为:2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO,则X为FeCl3
C. ③中氩气(Ar)作保护气,反应类型为置换反应
D. ②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为1:2
14.下列实验操作不能达到实验目的的是( )
实验目的 实验操作
A 除去水中的异味 加入活性炭,充分搅拌后过滤
B 除去CO2中的少量CO 向混合气体中通入过量的氧气,点燃
C 检验电解水实验的产物 将燃着的小木条靠近管口,打开阀门
D 鉴别CO和CH4 分别点燃后,在火焰上方罩干燥烧杯
A. A B. B C. C D. D
二、多选题:本大题共3小题,共6分。
15.某兴趣小组将压强传感器连接在实验室制取氢气的发生装置中,测得实验过程中试管内气体压强变化情况如图(忽略温度变化)。下列说法正确的是( )
A. ab段试管液面逐渐上升
B. bc段锌粒与稀硫酸脱离接触
C. c点的对应操作为关闭弹簧夹
D. 该发生装置不能用于控制过氧化氢和二氧化锰粉末混合制氧气的发生和停止
16.在密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,在不同时刻测得各物质的质量(单位为g)如表所示。下列说法正确的是( )
甲 乙 丙 丁
反应前 20 64 6 10
反应中 a 48 c 19
反应后 4 b 50 46
A. 丙和丁为生成物
B. b=0
C. 甲和丙的质量变化量之比为4:11
D. 若乙和丙的相对分子质量为32和44,则乙和丙的化学计量系数之比为1:1
17.关于酸和碱下列推理正确的是( )
A. 酸能使紫色石蕊试液变红,CO2也能使紫色石蕊试液变红,所以CO2是酸
B. 锌和铜均是金属,锌与稀硫酸反应生成氢气,则铜也能与稀硫酸反应生成氢气
C. 碱性溶液能使酚酞试液变红,滴入酚酞试液后变红的溶液一定呈碱性
D. 碱中都含有氢氧根离子,所以碱中一定含有氢、氧元素
三、填空题:本大题共2小题,共12分。
18.家庭厨房中蕴含大量化学知识。
(1)做凉拌皮蛋时,放入适量的食醋,主要目的是除去皮蛋中含有的 ______ (填“酸”或“碱”)性物质。
(2)厨房中用铁锅作炊具,是利用铁的 ______ 性,而铁锅容易生锈,结合生活实际,写出一种防止铁锅生锈的方法 ______ 。
(3)家用燃料天然气的主要成分是甲烷,甲烷完全燃烧的化学方程式是 ______ 。
(4)洗菠菜时发现叶片发黄,则需要在菠菜成长过程中施加 ______ (填“氮”“磷”或“钾”)肥。
(5)餐具上的油污可以用加入洗涤剂的水洗掉,这是利用了洗涤剂的 ______ 作用。
19.如表是氯化钠和氯化钾的部分溶解度数据,回答下列问题。
温度℃ 0 10 20 30 40 50 60
溶解度/g 氯化钠 35.7 35.8 36.0 36.3 36.6 37.0 37.3
氯化钾 27.6 31.0 34.0 37.0 40.0 42.6 45.5
(1)0℃时,氯化钠的溶解度是 ______ ;
(2)分析表中数据可知,溶解度受温度影响较大的物质是 ______ ;
(3)某同学用氯化钾进行了如图所示实验(实验过程中水分损失忽略不计)。
①A~D烧杯中溶液为饱和状态的有 ______ (填字母序号)。
②D中析出晶体的质量是 ______ g。
(4)溶质质量分数为10%的氯化钠溶液对葡萄球菌具有明显的抑制效果。如图为配制氯化钠杀菌液的过程,结合图表信息,有关分析中正确的是 ______ (填字母序号)。
A.图1中搅拌可增大氯化钠的溶解度
B.图2中溶液的溶质质量分数为10%
C.从氯化钠溶液中得到氯化钠适宜用蒸发结晶
四、流程题:本大题共1小题,共10分。
20.二氧化锰因应用广泛而备受关注。某研究小组用废旧电池炭包制备纯MnO2,制备流程如图所示。
已知:焙烧MnCO3制取MnO2的化学方程式为2MnCO3+O22CO2+2MnO2。
请回答下列问题:
(1)加入Na2CO3溶液后发生反应的基本反应类型为 ______ ;过滤Ⅱ后洗涤滤渣,证明滤渣已洗净的方法是 ______ 。
(2)试根据化学方程式求46.0gMnCO3通过焙烧最多制得的MnO2的质量是多少?(请写出计算过程)
(3)焙烧MnCO3的过程中,固体产物的质量和成分随温度的变化如图所示,则焙烧MnCO3制取MnO2应该控制反应温度不高于 ______ ℃;若把焙烧46.0gMnCO3温度控制在900℃,充分反应后的固体产物质量为 ______ g。
五、实验题:本大题共1小题,共8分。
21.水是一种重要的资源,为人类生活提供了便利。
(1)如图所示的三个实验,A中水发生了 ______ (填“物理”或“化学”)变化;C中活性炭的作用是吸附色素和异味,具有 ______ 性。属于 ______ (填“物理”或“化学”)性质。
(2)如图所示是电解水的实验,实验时试管1和2中产生气体的体积比约为 ______ ,1中产生的气体是 ______ (填化学式)。
写出电解水的化学方程式 ______ 。
(3)ClO2是新一代饮用水的消毒剂,可以用来代替Cl2进行自来水的消毒,制取ClO2的反应过程示意图如图,请回答:
(其中:表示钠原子,表示氯原子,表示氧原子)
该反应的化学方程式是 ______ 。
(4)为了保持江河湖泊的秀丽,某同学向市政府提出了保护江河的几条建议,其中不合理的是 ______ (填序号)。
①向江河中放养鱼苗,保持生态平衡
②少用或不用含磷洗衣粉
③禁止向河道内倾倒垃圾
④禁止使用化肥和农药,防止水质污染
第1页,共1页
一、单选题:本大题共14小题,共14分。
1.化学用语是学习化学的工具,下列表示两个氧离子的是( )
A. O2 B. 2O C. D. 2O2-
2.类比推理在化学学习和科学研究中有重要意义,下列说法正确的是( )
A. 单质中只含有一种元素,所以只含有一种元素的物质一定是单质
B. 点燃氢气前要检验其纯度,所以点燃可燃性气体前一定要验纯
C. 阴离子是带负电的粒子,所以带负电的粒子一定是阴离子
D. 氧化物中一定含有氧元素,所以含有氧元素的化合物一定是氧化物
3.下列关于金属的说法中正确的是( )
A. 金属材料在常温下都是固体 B. 人类最早大量使用的金属是铁
C. 金属的性质是决定金属用途的唯一因素 D. 生铁和不锈钢都是铁的合金
4.下列各组物质俗称、化学式及名称正确的是( )
A. 石灰石、CaCO3、碳酸钙 B. 乙醇、C2H3OH、酒精
C. 火碱、NaOH、氢氧化钠 D. 天然气、CH4、甲烷
5.下列有关空气的说法正确的是( )
A. 洁净的空气属于纯净物 B. 空气是由空气分子构成的
C. 空气中二氧化碳是空气污染物 D. 空气中氮气可用作保护气
6.如图为氮元素的部分化合价、物质类别二维图。下列说法错误的是( )
A. a点物质在空气中体积分数最高 B. b点物质属于大气污染物
C. c点物质的名称为硝酸 D. d点物质可能是KNO3
7.某同学测出身边一些物质的pH如下表。有关分析正确的是( )
物质 柠檬汁 西瓜汁 茶水 鸡蛋清
pH 2.6 5.8 7.5 9.0
A. 仅鸡蛋清呈碱性 B. 西瓜汁比柠檬汁酸性强
C. 茶水中滴入酚酞,溶液变红 D. 胃酸过多的人应多饮西瓜汁
8.习近平总书记在党的二十大报告中指出:“推动绿色发展,促进人与自然和谐共生”。下列措施与此理念不相符的是( )
A. 合理使用农药和化肥 B. 就地焚烧植物秸秆
C. 废旧金属回收利用 D. 工业废水达标后再排放
9.在一个密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如图所示。下列说法正确的是( )
A. x=14 B. 乙一定是催化剂
C. 该反应属于化合反应 D. 反应中丙和丁的质量之比是14:11
10.科学家发现了纯碳新材料“碳纳米泡沫”,泡沫由许多团簇组成,每个团簇含有约4000个碳原子.“碳纳米泡沫”是目前世上最轻的物质之一,密度为2mg/cm3.有铁磁性,是热和电的不良导体.下列说法不正确的是( )
A. “碳纳米泡沫”由碳元素组成 B. “碳纳米泡沫”能被磁铁吸引
C. “碳纳米泡沫”和金刚石的性质相同 D. “碳纳米泡沫”能浮在水面上
11.下列物质可以发生反应,但必须加入指示剂才能证明反应发生的是( )
A. 碳酸钠溶液和石灰水 B. 大理石和稀盐酸
C. 氢氧化钠溶液和二氧化碳 D. 氢氧化钠溶液和稀盐酸
12.阿奇霉素(C38H72N2O12)主要用于滑疗呼吸道等疾病,在酸性环境下很稳定。下列对阿奇霉素的描述正确的是( )
A. 属于氧化物 B. 能与酸反应
C. 它可以溶于水 D. 氢、氧元素的质量比为72:12
13.如图为某化工企业生产流程示意图:
下列说法不正确的是( )
A. 钛酸亚铁(FeTiO3)中钛元素为+4价
B. ①中反应为:2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO,则X为FeCl3
C. ③中氩气(Ar)作保护气,反应类型为置换反应
D. ②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为1:2
14.下列实验操作不能达到实验目的的是( )
实验目的 实验操作
A 除去水中的异味 加入活性炭,充分搅拌后过滤
B 除去CO2中的少量CO 向混合气体中通入过量的氧气,点燃
C 检验电解水实验的产物 将燃着的小木条靠近管口,打开阀门
D 鉴别CO和CH4 分别点燃后,在火焰上方罩干燥烧杯
A. A B. B C. C D. D
二、多选题:本大题共3小题,共6分。
15.某兴趣小组将压强传感器连接在实验室制取氢气的发生装置中,测得实验过程中试管内气体压强变化情况如图(忽略温度变化)。下列说法正确的是( )
A. ab段试管液面逐渐上升
B. bc段锌粒与稀硫酸脱离接触
C. c点的对应操作为关闭弹簧夹
D. 该发生装置不能用于控制过氧化氢和二氧化锰粉末混合制氧气的发生和停止
16.在密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,在不同时刻测得各物质的质量(单位为g)如表所示。下列说法正确的是( )
甲 乙 丙 丁
反应前 20 64 6 10
反应中 a 48 c 19
反应后 4 b 50 46
A. 丙和丁为生成物
B. b=0
C. 甲和丙的质量变化量之比为4:11
D. 若乙和丙的相对分子质量为32和44,则乙和丙的化学计量系数之比为1:1
17.关于酸和碱下列推理正确的是( )
A. 酸能使紫色石蕊试液变红,CO2也能使紫色石蕊试液变红,所以CO2是酸
B. 锌和铜均是金属,锌与稀硫酸反应生成氢气,则铜也能与稀硫酸反应生成氢气
C. 碱性溶液能使酚酞试液变红,滴入酚酞试液后变红的溶液一定呈碱性
D. 碱中都含有氢氧根离子,所以碱中一定含有氢、氧元素
三、填空题:本大题共2小题,共12分。
18.家庭厨房中蕴含大量化学知识。
(1)做凉拌皮蛋时,放入适量的食醋,主要目的是除去皮蛋中含有的 ______ (填“酸”或“碱”)性物质。
(2)厨房中用铁锅作炊具,是利用铁的 ______ 性,而铁锅容易生锈,结合生活实际,写出一种防止铁锅生锈的方法 ______ 。
(3)家用燃料天然气的主要成分是甲烷,甲烷完全燃烧的化学方程式是 ______ 。
(4)洗菠菜时发现叶片发黄,则需要在菠菜成长过程中施加 ______ (填“氮”“磷”或“钾”)肥。
(5)餐具上的油污可以用加入洗涤剂的水洗掉,这是利用了洗涤剂的 ______ 作用。
19.如表是氯化钠和氯化钾的部分溶解度数据,回答下列问题。
温度℃ 0 10 20 30 40 50 60
溶解度/g 氯化钠 35.7 35.8 36.0 36.3 36.6 37.0 37.3
氯化钾 27.6 31.0 34.0 37.0 40.0 42.6 45.5
(1)0℃时,氯化钠的溶解度是 ______ ;
(2)分析表中数据可知,溶解度受温度影响较大的物质是 ______ ;
(3)某同学用氯化钾进行了如图所示实验(实验过程中水分损失忽略不计)。
①A~D烧杯中溶液为饱和状态的有 ______ (填字母序号)。
②D中析出晶体的质量是 ______ g。
(4)溶质质量分数为10%的氯化钠溶液对葡萄球菌具有明显的抑制效果。如图为配制氯化钠杀菌液的过程,结合图表信息,有关分析中正确的是 ______ (填字母序号)。
A.图1中搅拌可增大氯化钠的溶解度
B.图2中溶液的溶质质量分数为10%
C.从氯化钠溶液中得到氯化钠适宜用蒸发结晶
四、流程题:本大题共1小题,共10分。
20.二氧化锰因应用广泛而备受关注。某研究小组用废旧电池炭包制备纯MnO2,制备流程如图所示。
已知:焙烧MnCO3制取MnO2的化学方程式为2MnCO3+O22CO2+2MnO2。
请回答下列问题:
(1)加入Na2CO3溶液后发生反应的基本反应类型为 ______ ;过滤Ⅱ后洗涤滤渣,证明滤渣已洗净的方法是 ______ 。
(2)试根据化学方程式求46.0gMnCO3通过焙烧最多制得的MnO2的质量是多少?(请写出计算过程)
(3)焙烧MnCO3的过程中,固体产物的质量和成分随温度的变化如图所示,则焙烧MnCO3制取MnO2应该控制反应温度不高于 ______ ℃;若把焙烧46.0gMnCO3温度控制在900℃,充分反应后的固体产物质量为 ______ g。
五、实验题:本大题共1小题,共8分。
21.水是一种重要的资源,为人类生活提供了便利。
(1)如图所示的三个实验,A中水发生了 ______ (填“物理”或“化学”)变化;C中活性炭的作用是吸附色素和异味,具有 ______ 性。属于 ______ (填“物理”或“化学”)性质。
(2)如图所示是电解水的实验,实验时试管1和2中产生气体的体积比约为 ______ ,1中产生的气体是 ______ (填化学式)。
写出电解水的化学方程式 ______ 。
(3)ClO2是新一代饮用水的消毒剂,可以用来代替Cl2进行自来水的消毒,制取ClO2的反应过程示意图如图,请回答:
(其中:表示钠原子,表示氯原子,表示氧原子)
该反应的化学方程式是 ______ 。
(4)为了保持江河湖泊的秀丽,某同学向市政府提出了保护江河的几条建议,其中不合理的是 ______ (填序号)。
①向江河中放养鱼苗,保持生态平衡
②少用或不用含磷洗衣粉
③禁止向河道内倾倒垃圾
④禁止使用化肥和农药,防止水质污染
第1页,共1页
同课章节目录
