2025年黑龙江省哈尔滨市虹桥中学中考化学二模试卷(含答案)
文档属性
| 名称 | 2025年黑龙江省哈尔滨市虹桥中学中考化学二模试卷(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-14 00:00:00 | ||
图片预览

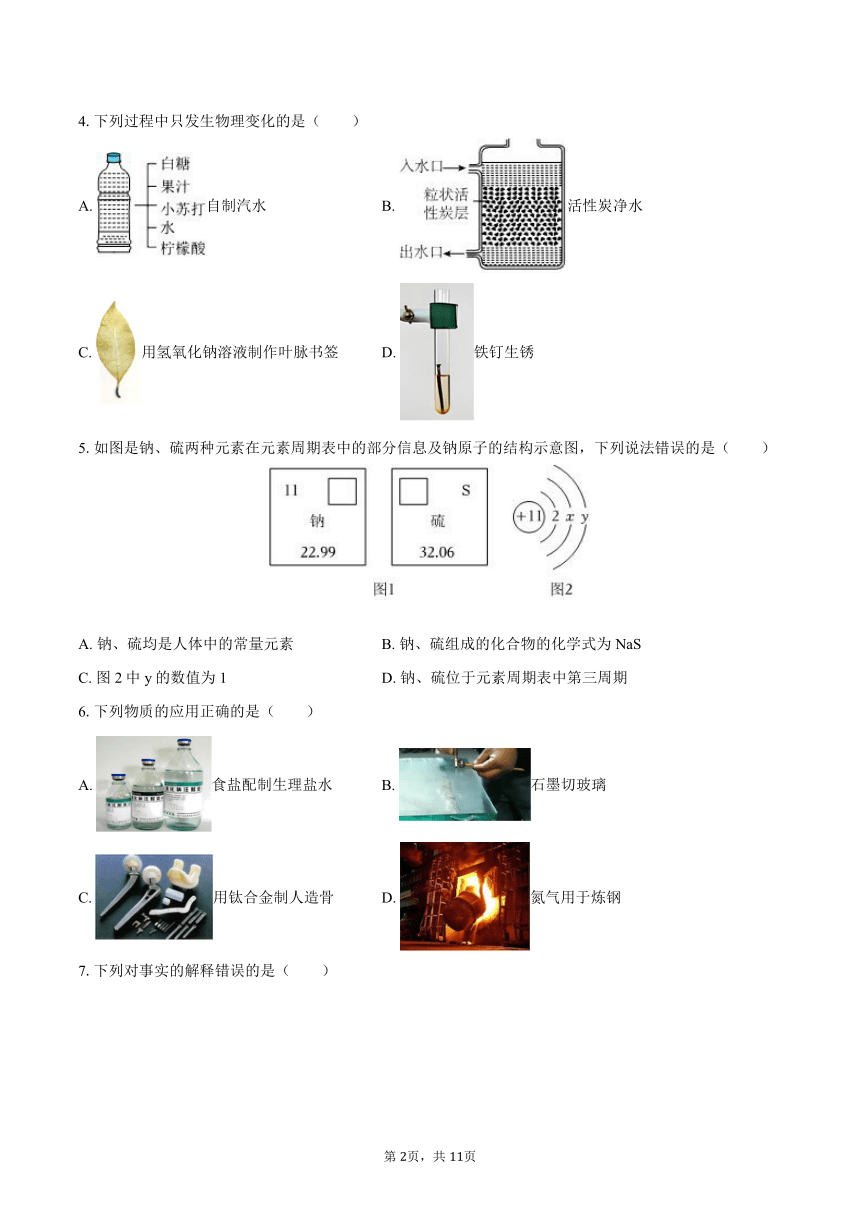



文档简介
2025年黑龙江省哈尔滨市虹桥中学中考化学二模试卷
一、单选题:本大题共13小题,共26分。
1.6月5日是世界环境日,2025年中国环境日主题是《美丽中国我先行》,下列做法不符合这一主题的是( )
A. 植树造林促进“碳中和”
B. 生活污水随意排放
C. 汽车使用乙醇汽油作燃料
D. 大力推广太阳能发电
2.下列实验操作错误的是( )
A. 滴管的使用 B. 检查装置气密性
C. 稀释浓硫酸 D. 蒸发食盐水
3.“关爱生命,拥抱健康”是永恒的主题。下列有关叙述正确的是( )
A. 为预防缺铁性贫血,在食品中大量添加铁元素
B. 用甲醛水溶液浸泡海产品以防腐
C. 在制作面包时添加适量的发酵粉,可使面包松软可口
D. 缺乏维生素C,会引起夜盲症
4.下列过程中只发生物理变化的是( )
A. 自制汽水 B. 活性炭净水
C. 用氢氧化钠溶液制作叶脉书签 D. 铁钉生锈
5.如图是钠、硫两种元素在元素周期表中的部分信息及钠原子的结构示意图,下列说法错误的是( )
A. 钠、硫均是人体中的常量元素 B. 钠、硫组成的化合物的化学式为NaS
C. 图2中y的数值为1 D. 钠、硫位于元素周期表中第三周期
6.下列物质的应用正确的是( )
A. 食盐配制生理盐水 B. 石墨切玻璃
C. 用钛合金制人造骨 D. 氮气用于炼钢
7.下列对事实的解释错误的是( )
选项 事实 解释
A 一氧化碳是一种有毒气体 一氧化碳分子是保持一氧化碳毒性的最小粒子
B 钠原子和钠离子的化学性质不同 两种粒子的最外层电子数不同
C 在溶液中进行化学反应较快 在溶液中参加反应的分子或离子直接接触
D 硝酸钾溶于水“消失了” 分子在不断运动
A. A B. B C. C D. D
8.下列有关叙述及对应的化学方程式、所属基本反应类型都正确的是( )
A. 硫在氧气中燃烧 化合反应
B. 氢气还原氧化铜 氧化反应
C. 实验室制氢气 Zn+HCl=ZnCl2+H2 置换反应
D. 苛性钠处理硫酸厂废水 2NaOH+H2SO4=Na2SO4+2H2O 中和反应
9.推理是化学学习的一种常用思维方法。下列推理正确的是( )
A. 分子能构成物质,所以物质都是由分子构成的
B. 酸能使石蕊溶液变红,将二氧化碳通入石蕊溶液,石蕊溶液变红,则二氧化碳是酸
C. 合金中一定含有金属元素,氧化铝中含有金属元素,则氧化铝是一种合金
D. 碱的溶液显碱性,显碱性的溶液不一定是碱溶液
10.区分下列各组物质的两种方法都正确的是( )
选项 A B C D
区分的物质 木炭和氧化铜 亚硝酸钠和氯化钠 聚乙烯和聚氯乙烯 空气和呼出气体
方法一 取样,空气中灼烧,观察现象 加水溶解,滴加酚酞溶液,观察现象 加热观察是否熔化 滴加相同滴数澄清石灰水,观察现象
方法二 加稀盐酸,观察溶液颜色 品尝 点燃闻气味 带火星木条
A. A B. B C. C D. D
11.科学家用新型催化剂将二氧化碳高效转化为甲醇,其反应的微观示意图如图。下列说法正确的是( )
A. 甲醇中氧元素质量分数为37.5% B. 该反应生成甲醇和水的分子个数比为1:1
C. 利用此反应,可减少酸雨的产生 D. 甲醇属于氧化物
12.除去下列物质中的少量杂质,所选用的试剂和操作方法都正确的是( )
选项 物质 杂质 试剂 除杂操作方法
A CaCl2溶液 HCl 生石灰 加入过量生石灰,过滤
B CO2 CO CuO 将气体通入氧化铜
C NaOH Ba(OH)2 稀硫酸 加入稀硫酸至沉淀恰好不再产生,过滤,蒸发结晶
D NaNO3溶液 AgNO3 碳酸钠溶液 加入适量碳酸钠溶液,过滤
A. A B. B C. C D. D
13.下列图像能正确表示对应关系的是( )
A. A——加水稀释浓盐酸
B. B——一定温度下,向一定量的饱和石灰水中加入生石灰
C. C——等质量的木炭和氧气充分反应
D. D——等质量的镁与足量溶质质量分数相同的稀盐酸反应
二、填空题:本大题共3小题,共24分。
14.龙的传人游龙江,冰城雪国赏风光,哈尔滨里寻梦幻,索菲亚钟声悠扬。请回答下列问题。
(1)大列巴面包是哈尔滨非常著名的一种传统美食,深受大家的喜爱,其富含的营养素为______(除水外)。
(2)随着时间的推移,索菲亚教堂经历多次修缮与重建,在重建中使用的钢筋属于______(选填“金属”或“合成”)材料。
(3)亚冬会期间,可用纯电动汽车为运动员服务。此种汽车行驶时的能量转化为:______能→电能→机械能。
15.如图1是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,回答下列各小题。
(1)20℃时甲的溶解度______乙的溶解度(选填“>”或“=”或“<”)。
(2)10℃时,将25g甲加入到盛有50g水的烧杯中,充分溶解后,所得溶液是______(选填“饱和”或“不饱和”)溶液。
(3)若固体乙中混有少量甲,为得到较纯净的固体乙,可采用______(选填“蒸发溶剂”或“冷却热饱和溶液”)的方法。
(4)40℃时a点所对应两种溶液的溶质质量分数:甲______乙(选填“>”或“=”或“<”)。
(5)小虹将甲、乙固体各30g分别加入100g水中后,进行了如图2所示的实验。则m的取值范围是______。
16.基于“宏观—微观—符号”视角认识物质及变化是化学学科特有的思维方式,请结合图示完成下列问题。
(1)图1中,符号“Cu”可以表示多种信息,如铜元素、铜这种物质,还可以表示______;
(2)图2为新型燃料氨气(NH3)燃烧反应的微观示意图,化学反应前后,未发生改变的粒子是______(填符号),据图写出该反应的化学方程式______;
(3)CuSO4溶液与NaOH溶液反应过程中,溶液中自由移动的离子数目______(选填“逐渐增多”、“逐渐减少”或“保持不变”),当两种物质恰好完全反应时,所得溶液中阴阳离子个数比为______。
三、推断题:本大题共1小题,共10分。
17.图中A~I是初中常见化学物质。A、B、C、D均为单质,其中A是一种紫红色固体,E、F为氧化物,I用来改良酸性土壤;图中“—”表示两端的物质间能发生化学反应:“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。
(1)写出物质A、H的化学式:A______ H______;
(2)B转化到D时,溶液由无色变为______色;
(3)E转化到C的反应方程式为______;
(4)1个F粒子的质子数是______。
四、流程题:本大题共1小题,共8分。
18.小虹同学想从含少量铜粉的银、锌混合金属粉末(随意编号为A、B、C)中分离出贵金属,并获得一种盐晶体,设计了如图流程,回答下列相关问题:
(1)根据以上流程判断,A、B、C的金属活动性由强到弱顺序为______(用A、B、C表示)。
(2)流程中加入足量AgNO3溶液,发生反应的化学方程式为______。
(3)流程中加入足量稀硫酸目的是______。
五、简答题:本大题共1小题,共8分。
19.分类、类比和迁移是学习和研究化学常用的方法。
(1)小桥同学配制一定溶质质量分数的氯化钠溶液,以下操作可能导致配制的溶液溶质质量分数发生变化,请从导致所配制溶液溶质质量分数“偏大”或“偏小”或“不变”角度,对以下操作进行分类。
A.称量氯化钠固体时,左码右物且游码已向右移动
B.用量筒量取蒸馏水时俯视读数
C.烧杯内原来有水
D.配制完溶液后装入试剂瓶时有部分溶液洒在瓶外
你所选择的操作是 ______;分类依据为 ______。
(2)石灰岩的主要成分是碳酸钙,当遇到溶有二氧化碳的水时,会反应生成溶解性较大的碳酸氢钙:CaCO3+CO2+H2O=Ca(HCO3)2。Ba(OH)2和Ca(OH)2、BaCO3和CaCO3的化学性质相似。把二氧化碳通入到Ba(OH)2溶液中的反应的图像如图。请回答下列问题:若通入CO2的质量为0—ag时,溶液中参加反应的离子是 ______(填离子符号),图像m—n之间发生反应的化学方程式为 ______。
六、实验题:本大题共1小题,共10分。
20.实验室现有大理石、稀盐酸、高锰酸钾、30%过氧化氢溶液、二氧化锰、蒸馏水,火柴、升降台、药匙、镊子、棉花及以下仪器,请回答下列问题:
Ⅰ.制取氧气
(1)从上述试剂中选择一种固体制取氧气,发生反应的化学方程式为______,制取氧气时,除上述所给仪器外,还需要补充______(填仪器名称)。
(2)在水面下收集完氧气后,盖好玻璃片,此时集气瓶中的气压______(选填“大于”或“小于”或“等于”)外界大气压。
(3)实验室一般用10%的过氧化氢溶液,而不用30%的过氧化氢溶液来制取氧气,其原因是______。
Ⅱ.制取二氧化碳
(4)利用上述仪器及试剂可以制取二氧化碳,应选择的试剂是______和稀盐酸。
(5)若利用装置J检验二氧化碳,则其中盛放的试剂为______,气体应从______(选填“a”或“b”)端通入装置J中。
七、探究题:本大题共1小题,共10分。
21.通过酸、碱、盐的学习我们已经知道,根据盐的组成里所含阴阳离子的特点,可将盐分类并称为某盐。例如,组成里含有碳酸根离子的盐称为碳酸盐,含有钾离子的盐称为钾盐,含有铵根离子的盐称为铵盐,等等。
(1)根据以上信息,请试着写出一种既属于钾盐又属于硝酸盐的一种盐的化学式______,它属于______(选填“钾”或“氮”或“复合”)肥。
(2)若想检验某种物质是否为碳酸盐,通常选用的试剂为______(填字母)。
A.稀盐酸
B.氯化钡溶液
C.澄清石灰水
HQ小组同学取某难溶性固体样品利用上述所选试剂进行如图1实验(已知试管A中金属离子为Ca2+)
【提出问题】试管A中废液的溶质是什么物质?
【猜想与假设】
小虹:溶质只有CaCl2
小桥:溶质有CaCl2、HCl
(3)经过讨论,同学们一致认为只需要检验溶液中是否存在______(填离子符号),即可证明哪个猜想正确。
【设计实验】
取试管A中所有废液于烧杯C中,一次性加入过量碳酸钠溶液如图2,反应后绘制烧杯C中物质总质量随时间的变化趋势如图3。
【讨论与交流】
(4)在加入过量碳酸钠溶液后观察到的现象是______,烧杯C中物质总质量减少时发生反应的化学方程式为______。在烧杯C物质总质量不变的过程中,溶液中______(填符号)粒子个数不变。
【拓展应用】
(5)将试管A和烧杯C中固体洗涤、干燥,测定所得固体质量相等,则上述检验实验中所取样品的纯度为______。
八、计算题:本大题共1小题,共10分。
22.为了测定某赤铁矿样品(杂质不溶于水,也不与其他物质发生反应)中氧化铁的含量,HQ兴趣小组进行了如下实验:
(1)上述实验过程中发生反应的化学方程式为______;
(2)此赤铁矿样品中氧化铁的含量为______;
(3)若用36.5%的浓盐酸配制上述实验所用稀盐酸,需加水的质量为______;
(4)向溶液A中加入93g水,得到只含一种溶质的溶液,此溶液中溶质质量分数为______;
(5)现用250t此种赤铁矿炼制生铁,炼制过程铁元素的损失率为10%,则最终可炼得含铁90%的生铁样品的质量为______t;
(6)为测定氧化铜和氧化铁的混合物中氧元素的质量分数,取16g此混合物,加入150g的稀硫酸,恰好反应后,向所得溶液中滴加质量分数为10%的氢氧化钠溶液至200g时,沉淀质量不再增加。则原混合物中氧元素的质量分数为______。
1.【答案】B
2.【答案】C
3.【答案】C
4.【答案】B
5.【答案】B
6.【答案】C
7.【答案】D
8.【答案】A
9.【答案】D
10.【答案】A
11.【答案】B
12.【答案】D
13.【答案】D
14.【答案】糖类
金属
化学
15.【答案】=;
饱和;
冷却热饱和溶液;
<;
2<m≤40
16.【答案】1个铜原子;
N、H、O;;
逐渐减少;2:1
17.【答案】Cu;CaCO3;
浅绿;
2H2O2H2↑+O2↑;
22
18.【答案】A>B>C
Cu+2AgNO3=Cu(NO3)2+2Ag
除去Zn(将Zn转化为ZnSO4)
19.【答案】AC;导致溶质质量分数偏小;
Ba2+、OH-;BaCO3+H2O+CO2=Ba(HCO3)2
20.【答案】;试管
大于
反应速率太快,不利于收集气体
大理石
澄清石灰水;a
21.【答案】KNO3;复合;
AC;
H+;
溶液中先产生气泡再产生白色沉淀;Na2CO3+2HCl=2NaCl+H2O+CO2↑;Na+、Cl-、H2O;
50%
22.【答案】Fe2O3+6HCl=2FeCl3+3H2O;
80%;
80g;
20%;
140;
25%
第1页,共1页
一、单选题:本大题共13小题,共26分。
1.6月5日是世界环境日,2025年中国环境日主题是《美丽中国我先行》,下列做法不符合这一主题的是( )
A. 植树造林促进“碳中和”
B. 生活污水随意排放
C. 汽车使用乙醇汽油作燃料
D. 大力推广太阳能发电
2.下列实验操作错误的是( )
A. 滴管的使用 B. 检查装置气密性
C. 稀释浓硫酸 D. 蒸发食盐水
3.“关爱生命,拥抱健康”是永恒的主题。下列有关叙述正确的是( )
A. 为预防缺铁性贫血,在食品中大量添加铁元素
B. 用甲醛水溶液浸泡海产品以防腐
C. 在制作面包时添加适量的发酵粉,可使面包松软可口
D. 缺乏维生素C,会引起夜盲症
4.下列过程中只发生物理变化的是( )
A. 自制汽水 B. 活性炭净水
C. 用氢氧化钠溶液制作叶脉书签 D. 铁钉生锈
5.如图是钠、硫两种元素在元素周期表中的部分信息及钠原子的结构示意图,下列说法错误的是( )
A. 钠、硫均是人体中的常量元素 B. 钠、硫组成的化合物的化学式为NaS
C. 图2中y的数值为1 D. 钠、硫位于元素周期表中第三周期
6.下列物质的应用正确的是( )
A. 食盐配制生理盐水 B. 石墨切玻璃
C. 用钛合金制人造骨 D. 氮气用于炼钢
7.下列对事实的解释错误的是( )
选项 事实 解释
A 一氧化碳是一种有毒气体 一氧化碳分子是保持一氧化碳毒性的最小粒子
B 钠原子和钠离子的化学性质不同 两种粒子的最外层电子数不同
C 在溶液中进行化学反应较快 在溶液中参加反应的分子或离子直接接触
D 硝酸钾溶于水“消失了” 分子在不断运动
A. A B. B C. C D. D
8.下列有关叙述及对应的化学方程式、所属基本反应类型都正确的是( )
A. 硫在氧气中燃烧 化合反应
B. 氢气还原氧化铜 氧化反应
C. 实验室制氢气 Zn+HCl=ZnCl2+H2 置换反应
D. 苛性钠处理硫酸厂废水 2NaOH+H2SO4=Na2SO4+2H2O 中和反应
9.推理是化学学习的一种常用思维方法。下列推理正确的是( )
A. 分子能构成物质,所以物质都是由分子构成的
B. 酸能使石蕊溶液变红,将二氧化碳通入石蕊溶液,石蕊溶液变红,则二氧化碳是酸
C. 合金中一定含有金属元素,氧化铝中含有金属元素,则氧化铝是一种合金
D. 碱的溶液显碱性,显碱性的溶液不一定是碱溶液
10.区分下列各组物质的两种方法都正确的是( )
选项 A B C D
区分的物质 木炭和氧化铜 亚硝酸钠和氯化钠 聚乙烯和聚氯乙烯 空气和呼出气体
方法一 取样,空气中灼烧,观察现象 加水溶解,滴加酚酞溶液,观察现象 加热观察是否熔化 滴加相同滴数澄清石灰水,观察现象
方法二 加稀盐酸,观察溶液颜色 品尝 点燃闻气味 带火星木条
A. A B. B C. C D. D
11.科学家用新型催化剂将二氧化碳高效转化为甲醇,其反应的微观示意图如图。下列说法正确的是( )
A. 甲醇中氧元素质量分数为37.5% B. 该反应生成甲醇和水的分子个数比为1:1
C. 利用此反应,可减少酸雨的产生 D. 甲醇属于氧化物
12.除去下列物质中的少量杂质,所选用的试剂和操作方法都正确的是( )
选项 物质 杂质 试剂 除杂操作方法
A CaCl2溶液 HCl 生石灰 加入过量生石灰,过滤
B CO2 CO CuO 将气体通入氧化铜
C NaOH Ba(OH)2 稀硫酸 加入稀硫酸至沉淀恰好不再产生,过滤,蒸发结晶
D NaNO3溶液 AgNO3 碳酸钠溶液 加入适量碳酸钠溶液,过滤
A. A B. B C. C D. D
13.下列图像能正确表示对应关系的是( )
A. A——加水稀释浓盐酸
B. B——一定温度下,向一定量的饱和石灰水中加入生石灰
C. C——等质量的木炭和氧气充分反应
D. D——等质量的镁与足量溶质质量分数相同的稀盐酸反应
二、填空题:本大题共3小题,共24分。
14.龙的传人游龙江,冰城雪国赏风光,哈尔滨里寻梦幻,索菲亚钟声悠扬。请回答下列问题。
(1)大列巴面包是哈尔滨非常著名的一种传统美食,深受大家的喜爱,其富含的营养素为______(除水外)。
(2)随着时间的推移,索菲亚教堂经历多次修缮与重建,在重建中使用的钢筋属于______(选填“金属”或“合成”)材料。
(3)亚冬会期间,可用纯电动汽车为运动员服务。此种汽车行驶时的能量转化为:______能→电能→机械能。
15.如图1是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,回答下列各小题。
(1)20℃时甲的溶解度______乙的溶解度(选填“>”或“=”或“<”)。
(2)10℃时,将25g甲加入到盛有50g水的烧杯中,充分溶解后,所得溶液是______(选填“饱和”或“不饱和”)溶液。
(3)若固体乙中混有少量甲,为得到较纯净的固体乙,可采用______(选填“蒸发溶剂”或“冷却热饱和溶液”)的方法。
(4)40℃时a点所对应两种溶液的溶质质量分数:甲______乙(选填“>”或“=”或“<”)。
(5)小虹将甲、乙固体各30g分别加入100g水中后,进行了如图2所示的实验。则m的取值范围是______。
16.基于“宏观—微观—符号”视角认识物质及变化是化学学科特有的思维方式,请结合图示完成下列问题。
(1)图1中,符号“Cu”可以表示多种信息,如铜元素、铜这种物质,还可以表示______;
(2)图2为新型燃料氨气(NH3)燃烧反应的微观示意图,化学反应前后,未发生改变的粒子是______(填符号),据图写出该反应的化学方程式______;
(3)CuSO4溶液与NaOH溶液反应过程中,溶液中自由移动的离子数目______(选填“逐渐增多”、“逐渐减少”或“保持不变”),当两种物质恰好完全反应时,所得溶液中阴阳离子个数比为______。
三、推断题:本大题共1小题,共10分。
17.图中A~I是初中常见化学物质。A、B、C、D均为单质,其中A是一种紫红色固体,E、F为氧化物,I用来改良酸性土壤;图中“—”表示两端的物质间能发生化学反应:“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。
(1)写出物质A、H的化学式:A______ H______;
(2)B转化到D时,溶液由无色变为______色;
(3)E转化到C的反应方程式为______;
(4)1个F粒子的质子数是______。
四、流程题:本大题共1小题,共8分。
18.小虹同学想从含少量铜粉的银、锌混合金属粉末(随意编号为A、B、C)中分离出贵金属,并获得一种盐晶体,设计了如图流程,回答下列相关问题:
(1)根据以上流程判断,A、B、C的金属活动性由强到弱顺序为______(用A、B、C表示)。
(2)流程中加入足量AgNO3溶液,发生反应的化学方程式为______。
(3)流程中加入足量稀硫酸目的是______。
五、简答题:本大题共1小题,共8分。
19.分类、类比和迁移是学习和研究化学常用的方法。
(1)小桥同学配制一定溶质质量分数的氯化钠溶液,以下操作可能导致配制的溶液溶质质量分数发生变化,请从导致所配制溶液溶质质量分数“偏大”或“偏小”或“不变”角度,对以下操作进行分类。
A.称量氯化钠固体时,左码右物且游码已向右移动
B.用量筒量取蒸馏水时俯视读数
C.烧杯内原来有水
D.配制完溶液后装入试剂瓶时有部分溶液洒在瓶外
你所选择的操作是 ______;分类依据为 ______。
(2)石灰岩的主要成分是碳酸钙,当遇到溶有二氧化碳的水时,会反应生成溶解性较大的碳酸氢钙:CaCO3+CO2+H2O=Ca(HCO3)2。Ba(OH)2和Ca(OH)2、BaCO3和CaCO3的化学性质相似。把二氧化碳通入到Ba(OH)2溶液中的反应的图像如图。请回答下列问题:若通入CO2的质量为0—ag时,溶液中参加反应的离子是 ______(填离子符号),图像m—n之间发生反应的化学方程式为 ______。
六、实验题:本大题共1小题,共10分。
20.实验室现有大理石、稀盐酸、高锰酸钾、30%过氧化氢溶液、二氧化锰、蒸馏水,火柴、升降台、药匙、镊子、棉花及以下仪器,请回答下列问题:
Ⅰ.制取氧气
(1)从上述试剂中选择一种固体制取氧气,发生反应的化学方程式为______,制取氧气时,除上述所给仪器外,还需要补充______(填仪器名称)。
(2)在水面下收集完氧气后,盖好玻璃片,此时集气瓶中的气压______(选填“大于”或“小于”或“等于”)外界大气压。
(3)实验室一般用10%的过氧化氢溶液,而不用30%的过氧化氢溶液来制取氧气,其原因是______。
Ⅱ.制取二氧化碳
(4)利用上述仪器及试剂可以制取二氧化碳,应选择的试剂是______和稀盐酸。
(5)若利用装置J检验二氧化碳,则其中盛放的试剂为______,气体应从______(选填“a”或“b”)端通入装置J中。
七、探究题:本大题共1小题,共10分。
21.通过酸、碱、盐的学习我们已经知道,根据盐的组成里所含阴阳离子的特点,可将盐分类并称为某盐。例如,组成里含有碳酸根离子的盐称为碳酸盐,含有钾离子的盐称为钾盐,含有铵根离子的盐称为铵盐,等等。
(1)根据以上信息,请试着写出一种既属于钾盐又属于硝酸盐的一种盐的化学式______,它属于______(选填“钾”或“氮”或“复合”)肥。
(2)若想检验某种物质是否为碳酸盐,通常选用的试剂为______(填字母)。
A.稀盐酸
B.氯化钡溶液
C.澄清石灰水
HQ小组同学取某难溶性固体样品利用上述所选试剂进行如图1实验(已知试管A中金属离子为Ca2+)
【提出问题】试管A中废液的溶质是什么物质?
【猜想与假设】
小虹:溶质只有CaCl2
小桥:溶质有CaCl2、HCl
(3)经过讨论,同学们一致认为只需要检验溶液中是否存在______(填离子符号),即可证明哪个猜想正确。
【设计实验】
取试管A中所有废液于烧杯C中,一次性加入过量碳酸钠溶液如图2,反应后绘制烧杯C中物质总质量随时间的变化趋势如图3。
【讨论与交流】
(4)在加入过量碳酸钠溶液后观察到的现象是______,烧杯C中物质总质量减少时发生反应的化学方程式为______。在烧杯C物质总质量不变的过程中,溶液中______(填符号)粒子个数不变。
【拓展应用】
(5)将试管A和烧杯C中固体洗涤、干燥,测定所得固体质量相等,则上述检验实验中所取样品的纯度为______。
八、计算题:本大题共1小题,共10分。
22.为了测定某赤铁矿样品(杂质不溶于水,也不与其他物质发生反应)中氧化铁的含量,HQ兴趣小组进行了如下实验:
(1)上述实验过程中发生反应的化学方程式为______;
(2)此赤铁矿样品中氧化铁的含量为______;
(3)若用36.5%的浓盐酸配制上述实验所用稀盐酸,需加水的质量为______;
(4)向溶液A中加入93g水,得到只含一种溶质的溶液,此溶液中溶质质量分数为______;
(5)现用250t此种赤铁矿炼制生铁,炼制过程铁元素的损失率为10%,则最终可炼得含铁90%的生铁样品的质量为______t;
(6)为测定氧化铜和氧化铁的混合物中氧元素的质量分数,取16g此混合物,加入150g的稀硫酸,恰好反应后,向所得溶液中滴加质量分数为10%的氢氧化钠溶液至200g时,沉淀质量不再增加。则原混合物中氧元素的质量分数为______。
1.【答案】B
2.【答案】C
3.【答案】C
4.【答案】B
5.【答案】B
6.【答案】C
7.【答案】D
8.【答案】A
9.【答案】D
10.【答案】A
11.【答案】B
12.【答案】D
13.【答案】D
14.【答案】糖类
金属
化学
15.【答案】=;
饱和;
冷却热饱和溶液;
<;
2<m≤40
16.【答案】1个铜原子;
N、H、O;;
逐渐减少;2:1
17.【答案】Cu;CaCO3;
浅绿;
2H2O2H2↑+O2↑;
22
18.【答案】A>B>C
Cu+2AgNO3=Cu(NO3)2+2Ag
除去Zn(将Zn转化为ZnSO4)
19.【答案】AC;导致溶质质量分数偏小;
Ba2+、OH-;BaCO3+H2O+CO2=Ba(HCO3)2
20.【答案】;试管
大于
反应速率太快,不利于收集气体
大理石
澄清石灰水;a
21.【答案】KNO3;复合;
AC;
H+;
溶液中先产生气泡再产生白色沉淀;Na2CO3+2HCl=2NaCl+H2O+CO2↑;Na+、Cl-、H2O;
50%
22.【答案】Fe2O3+6HCl=2FeCl3+3H2O;
80%;
80g;
20%;
140;
25%
第1页,共1页
同课章节目录
