2025年广东省汕头市澄海实验高级中学附中中考化学二模试卷(含答案)
文档属性
| 名称 | 2025年广东省汕头市澄海实验高级中学附中中考化学二模试卷(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 219.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-16 00:00:00 | ||
图片预览

文档简介
2025年广东省汕头市澄海实验高级中学附中中考化学二模试卷
一、单选题:本大题共15小题,共39分。
1.部分成语中蕴含着化学知识。下列成语涉及化学变化的是( )
A. 焚林而猎 B. 大浪淘沙 C. 五彩缤纷 D. 水乳交融
我国力争在2060年前实现“碳中和”。利用高效催化剂将二氧化碳聚合成性能与聚乙烯相似的塑料,解决了二氧化碳造成的环境问题。请完成各小题。
2.塑料属于( )
A. 复合材料 B. 合成材料 C. 金属材料 D. 无机非金属材料
3.下列对节能减排的建议可行的是( )
A. 生活垃圾集中焚烧 B. 大力推广燃油汽车 C. 推广使用光伏发电 D. 禁止使用化石燃料
4.下列不属于CO2吸收或转化途径的是( )
A. 光合作用 B. 加高烟囱 C. 聚合成塑料 D. 通入氢氧化钠溶液
5.2022年5月12日是第14个全国防灾减灾日。下列标志与加油站无关的是( )
A. B.
C. D.
6.下列是列车地面上残留的饮料,其中酸性最强的是( )
A. 葡萄汁(3.5~4.5) B. 鲜牛奶(6.3~6.6)
C. 苹果汁(2.9~3.3) D. 苏打水(8.5~9.5)
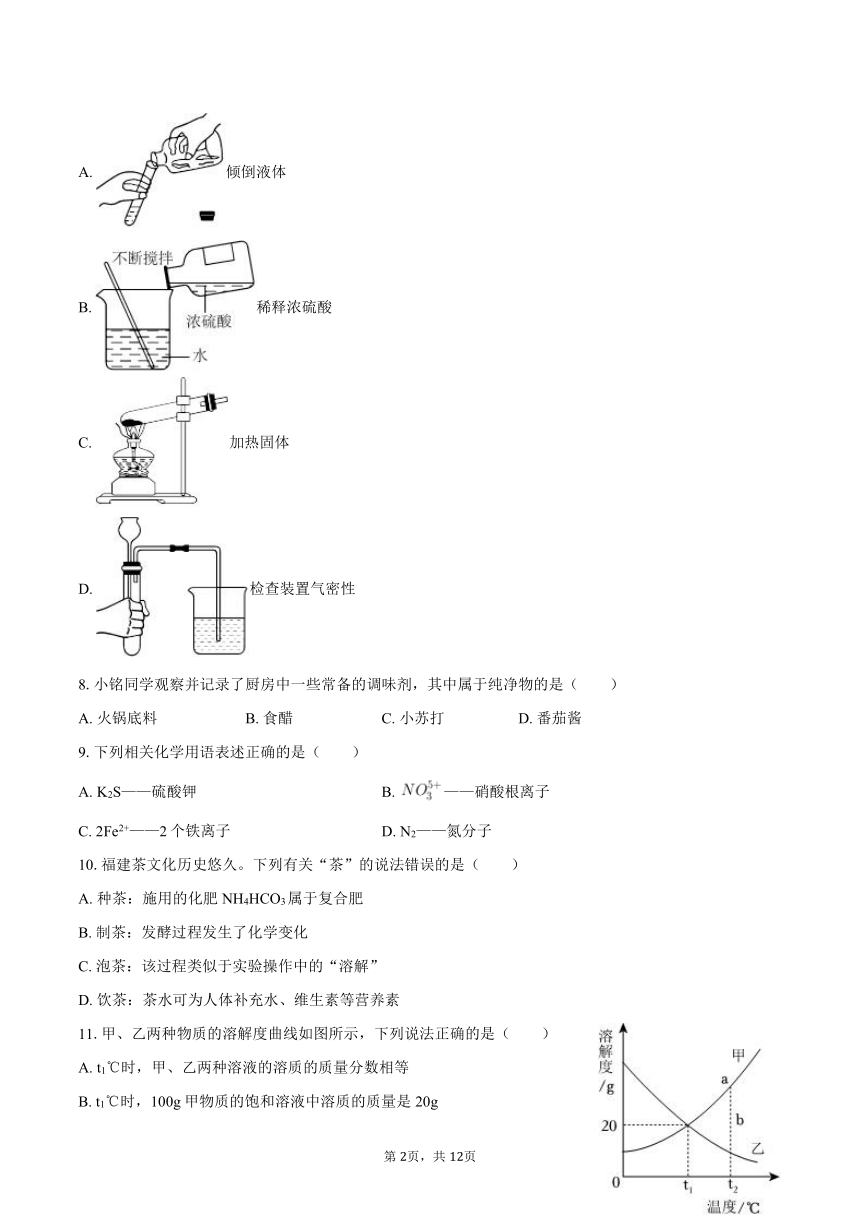
7.规范的操作是实验成功的保证。下列实验操作正确的是( )
A. 倾倒液体
B. 稀释浓硫酸
C. 加热固体
D. 检查装置气密性
8.小铭同学观察并记录了厨房中一些常备的调味剂,其中属于纯净物的是( )
A. 火锅底料 B. 食醋 C. 小苏打 D. 番茄酱
9.下列相关化学用语表述正确的是( )
A. K2S——硫酸钾 B. ——硝酸根离子
C. 2Fe2+——2个铁离子 D. N2——氮分子
10.福建茶文化历史悠久。下列有关“茶”的说法错误的是( )
A. 种茶:施用的化肥NH4HCO3属于复合肥
B. 制茶:发酵过程发生了化学变化
C. 泡茶:该过程类似于实验操作中的“溶解”
D. 饮茶:茶水可为人体补充水、维生素等营养素
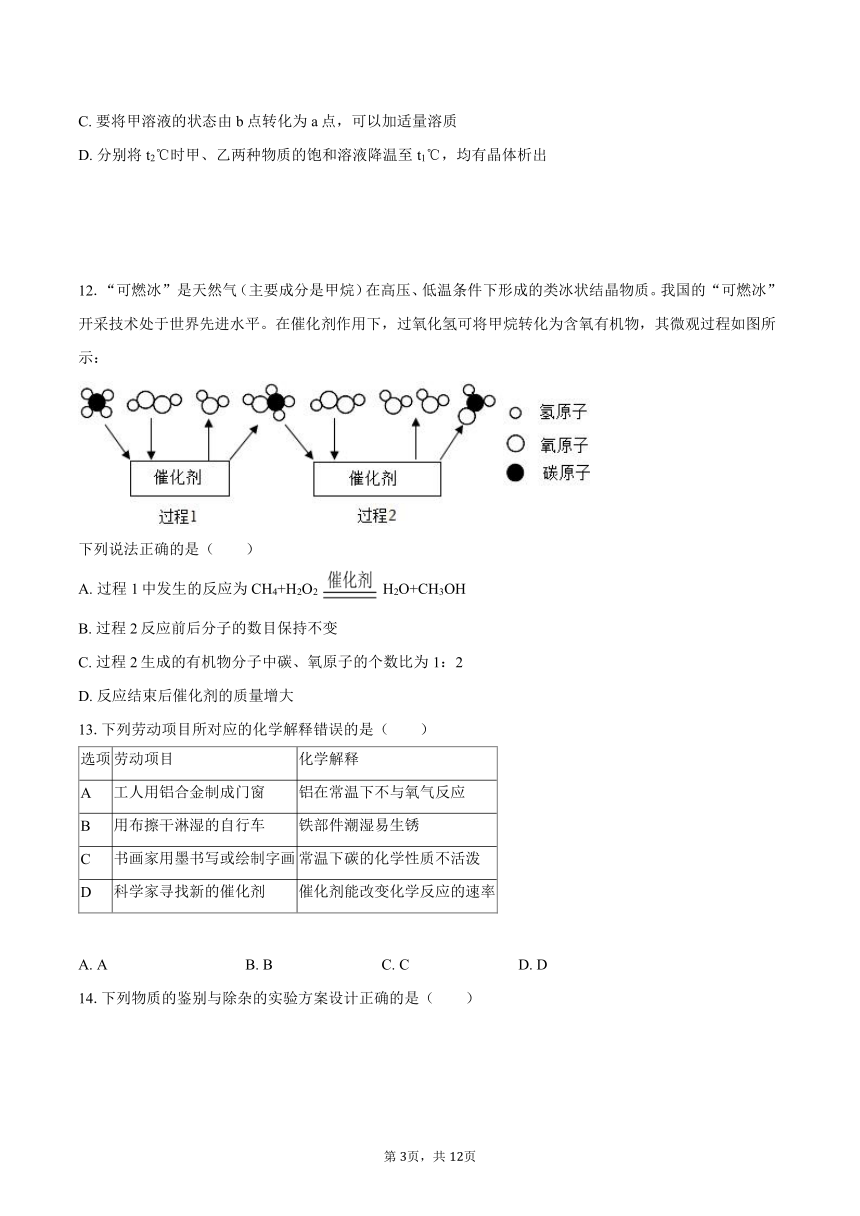
11.甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
A. t1℃时,甲、乙两种溶液的溶质的质量分数相等
B. t1℃时,100g甲物质的饱和溶液中溶质的质量是20g
C. 要将甲溶液的状态由b点转化为a点,可以加适量溶质
D. 分别将t2℃时甲、乙两种物质的饱和溶液降温至t1℃,均有晶体析出
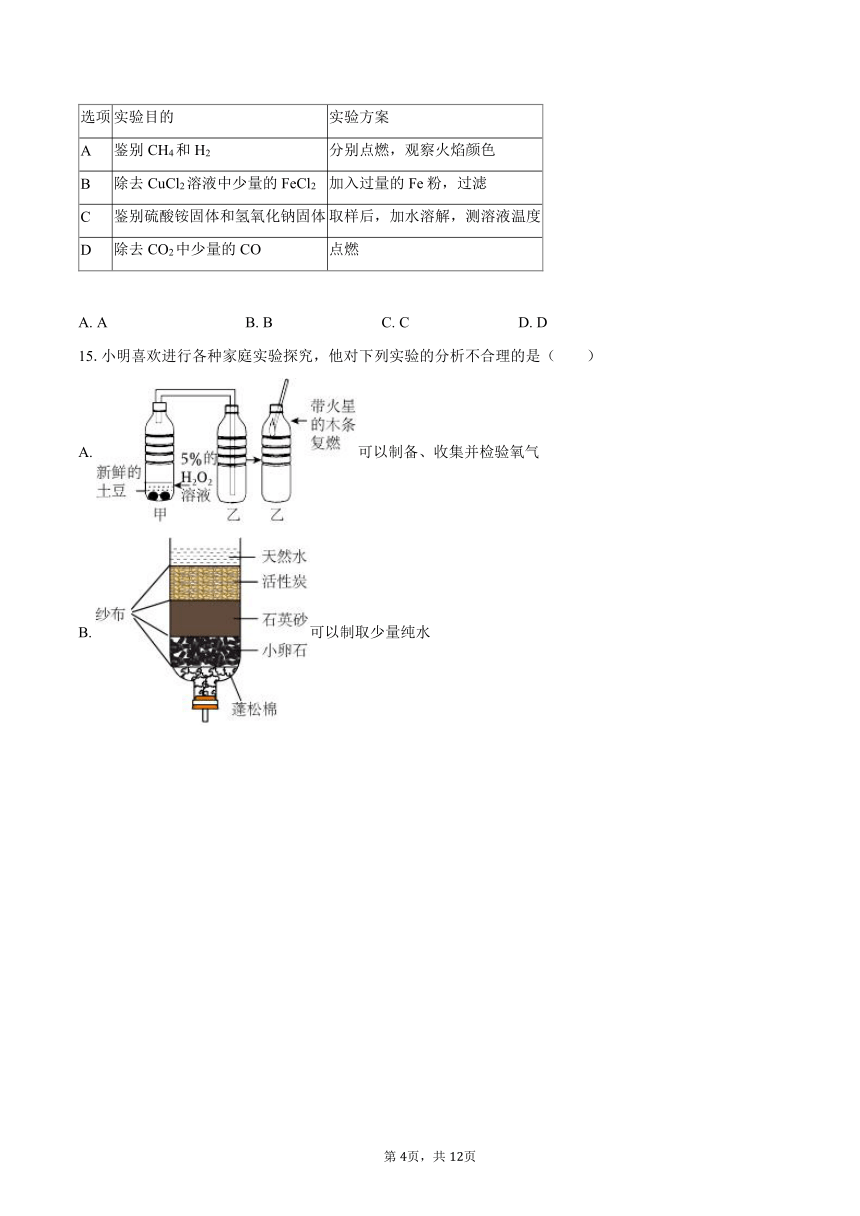
12.“可燃冰”是天然气(主要成分是甲烷)在高压、低温条件下形成的类冰状结晶物质。我国的“可燃冰”开采技术处于世界先进水平。在催化剂作用下,过氧化氢可将甲烷转化为含氧有机物,其微观过程如图所示:
下列说法正确的是( )
A. 过程1中发生的反应为CH4+H2O2H2O+CH3OH
B. 过程2反应前后分子的数目保持不变
C. 过程2生成的有机物分子中碳、氧原子的个数比为1:2
D. 反应结束后催化剂的质量增大
13.下列劳动项目所对应的化学解释错误的是( )
选项 劳动项目 化学解释
A 工人用铝合金制成门窗 铝在常温下不与氧气反应
B 用布擦干淋湿的自行车 铁部件潮湿易生锈
C 书画家用墨书写或绘制字画 常温下碳的化学性质不活泼
D 科学家寻找新的催化剂 催化剂能改变化学反应的速率
A. A B. B C. C D. D
14.下列物质的鉴别与除杂的实验方案设计正确的是( )
选项 实验目的 实验方案
A 鉴别CH4和H2 分别点燃,观察火焰颜色
B 除去CuCl2溶液中少量的FeCl2 加入过量的Fe粉,过滤
C 鉴别硫酸铵固体和氢氧化钠固体 取样后,加水溶解,测溶液温度
D 除去CO2中少量的CO 点燃
A. A B. B C. C D. D
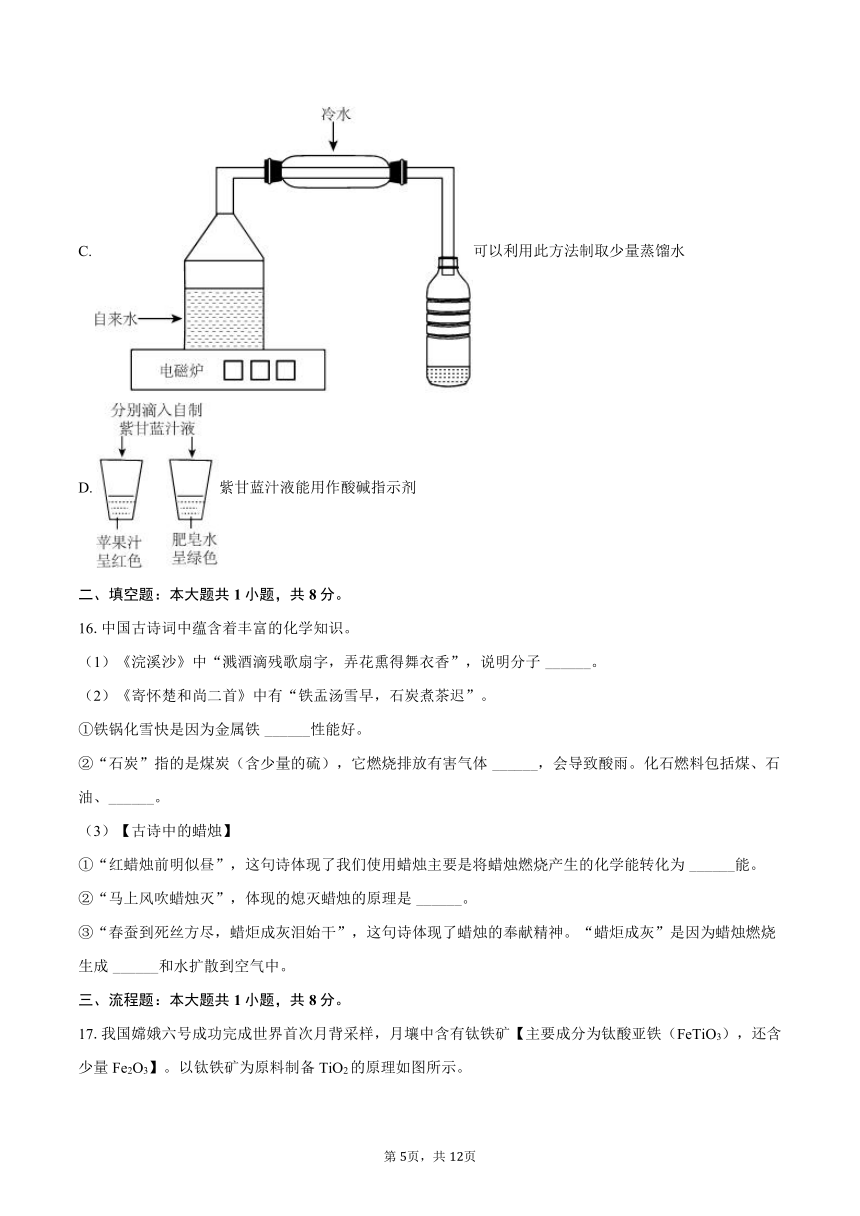
15.小明喜欢进行各种家庭实验探究,他对下列实验的分析不合理的是( )
A. 可以制备、收集并检验氧气
B. 可以制取少量纯水
C. 可以利用此方法制取少量蒸馏水
D. 紫甘蓝汁液能用作酸碱指示剂
二、填空题:本大题共1小题,共8分。
16.中国古诗词中蕴含着丰富的化学知识。
(1)《浣溪沙》中“溅酒滴残歌扇字,弄花熏得舞衣香”,说明分子 ______。
(2)《寄怀楚和尚二首》中有“铁盂汤雪早,石炭煮茶迟”。
①铁锅化雪快是因为金属铁 ______性能好。
②“石炭”指的是煤炭(含少量的硫),它燃烧排放有害气体 ______,会导致酸雨。化石燃料包括煤、石油、______。
(3)【古诗中的蜡烛】
①“红蜡烛前明似昼”,这句诗体现了我们使用蜡烛主要是将蜡烛燃烧产生的化学能转化为 ______能。
②“马上风吹蜡烛灭”,体现的熄灭蜡烛的原理是 ______。
③“春蚕到死丝方尽,蜡炬成灰泪始干”,这句诗体现了蜡烛的奉献精神。“蜡炬成灰”是因为蜡烛燃烧生成 ______和水扩散到空气中。
三、流程题:本大题共1小题,共8分。
17.我国嫦娥六号成功完成世界首次月背采样,月壤中含有钛铁矿【主要成分为钛酸亚铁(FeTiO3),还含少量Fe2O3】。以钛铁矿为原料制备TiO2的原理如图所示。
已知:相关金属离子开始生成氢氧化物沉淀的pH如表。
氢氧化物 Ti(OH)4 Fe(OH)3 Fe(OH)2
开始沉淀时的pH 0.5 1.5 7.6
(1)FeTiO3中Ti元素化合价为 ______。
(2)用研磨机进行预处理的目的是 ______。
(3)经过水解槽后得到滤液和Ti(OH)4固体的操作为 ______。
(4)酸浸槽中的主要反应为FeTiO3+2H2SO4=TiOSO4+FeSO4+2X,X的化学式为 ______,发生的另一个反应的化学方程式为 ______。
(5)为了得到纯净的Ti(OH)4固体,调节水解槽中的pH时,应始终保持pH小于 ______。滤液中主要含有的金属离子为 ______。
(6)煅烧炉中发生化学反应类型为 ______(填基本反应类型)。
四、科普短文题:本大题共1小题,共8分。
18.阅读下面科普短文,回答问题。
纳米海绵是一种新型环保清洁产品,具有网状多孔的结构,有良好的吸油能力、循环利用以及环境友好等特性,清洁过程中可以吸附物体表面污渍,可用于清洁茶垢、油垢等,还可用于解决海上石油泄漏造成的污染。科学家测定了纳米海绵对不同油品的吸收能力(吸油质量比越高,其吸油能力越强),结果如图1所示。吸油能力的差异性取决于油品自身的密度。油品密度越大,纳米海绵的吸油能力越强。
纳米海绵还具有良好的循环利用性。通过挤压,可将纳米海绵吸附的油品挤出,经洗涤干燥后再次使用,两种吸油材料对泵油的循环吸收测试结果如图2所示。
依据上文,回答下列问题。
(1)纳米海绵的清洁过程属于 ______(填“物理”或“化学”)变化,纳米海绵可以吸附物体表面污渍的原因是 ______。
(2)纳米海绵是以三聚氰胺和甲醛(HCHO)为原料制得的高分子物质,甲醛属于 ______(填“有机物”或“无机物”)。
(3)由图1可知,与黑芝麻油比较,柴油的吸油质量比更 ______(填“高”或“低”),因此纳米海绵对柴油的吸收能力比对黑芝麻油的 ______(填“强”或“弱”),吸油能力的差异性取决于 ______。
(4)图2是纳米海绵和细菌纤维素循环吸油能力的对比,可得到的结论是:在其它相同条件下,循环使用次数1~8之间时,随循环使用次数的增加,纳米海绵吸油能力变化不明显,细菌纤维素的吸油能力变 ______(填“好”或“差”)。
(5)下列说法正确的是 ______(多选,填字母)。
A.纳米海绵不可重复使用
B.纳米海绵可用于清洁茶垢、油垢等
C.纳米海绵可用于解决海上石油泄漏造成的污染
D.纳米海绵对环己烷吸收能力最强
五、实验题:本大题共1小题,共10分。
19.Ⅰ、实验室气体制取及性质验证:
(1)仪器a的名称是 ______。
(2)实验室用A装置利用高锰酸钾制氧气的化学方程式为 ______。
(3)用B装置制取气体时向长颈漏斗中加入液体时,液面应该在 ______处。
(4)CO2在不同溶剂中的溶解能力如下表所示,若某同学想利用F装置收集一瓶纯净的CO2,集气瓶中的液体应选择 ______,收集CO2气体时气体从 ______口通入。
物质种类 水 酒精 饱和NaHCO3溶液
每毫升液体中溶解CO2的体积 1mL 3.6mL 几乎不溶
Ⅱ、跨学科实践活动
(5)某同学将上图1装置置于阳光下暴晒一段时间后,观察到红墨水 ______移,证明大气中二氧化碳含量上升会加剧 ______。
(6)CO2能促进植物的 ______,植物对二氧化碳的利用率白天大于夜间,兴趣小组同学设计了图2装置用于增加蔬菜大棚中二氧化碳的浓度。该装置放置在 ______更利于二氧化碳的利用。
六、探究题:本大题共1小题,共10分。
20.化学实践小组对古代制盐的原理、盐湖多彩的成因及盐湖水的成分产生了浓厚的兴趣,他们在老师的指导下展开了项目式学习活动。
任务一:分析古代制盐的原理
【查阅资料】我国古代劳动人民在春秋战国时期就开始使用“垦畦浇晒法”制盐。
【分析交流】
(1)古代劳动人民利用盐湖水“晒”盐的原理是______。
任务二:了解盐湖多彩的成因
【查阅资料】气温上升和藻类是盐湖出现多彩的最主要原因。气温上升时,水分蒸发,湖水中各成分浓度不同导致湖水变色;同时盐湖中生长着一种嗜盐绿色微藻,正常情况下使湖水呈绿色。
【小组交流】
(2)同学们联想所学知识,想到了某些盐的溶液具有美丽的颜色,如______溶液呈蓝色。
任务三:探究盐湖水的成分
【查阅资料】①盐湖水中含有大量的NaCl、Na2SO4和MgSO4等物质;②Ag2SO4为微溶于水的白色固体。
现提供一瓶已静置澄清的盐湖水用于其成分的探究。
【进行实验】
(3)同学们设计了以下实验方案:
实验操作 实验现象 实验结论
①取少量盐湖水于试管中,加入足量稀硝酸和过量Ba(NO3)2溶液,静置 ______ 盐湖水中含有
②取步骤①的上层清液于试管中,滴加几滴 ______ 溶液 产生白色沉淀 盐湖水中含有Cl-
【反思评价】
(4)步骤①中加入Ba(NO3)2溶液“过量”的目的是______;若将步骤①中的Ba(NO3)2溶液换成BaCl2溶液,步骤②中______(填“能”或“不能”)得出相应结论,理由是______。
(5)步骤②中发生反应的化学方程式为______。
【成果分享】
(6)在人类获取盐和使用盐的历史上,始终伴随着知识的发展和技术的进步,同学们将所学所获做成板报进行宣传,请你与他们共同完成。
最美盐湖
自然美 科技美 劳动美
夏季的多彩盐湖是气温上升和藻类等共同作用的结果 古代劳动人民发明了“垦畦浇晒法”制盐 利用盐湖可以造福人类,如 ______ (写一条)
七、计算题:本大题共1小题,共10分。
21.石膏的主要成分是CaSO4 2H2O(相对分子质量为172),可用于水泥缓凝剂、建筑制品、模型制作、医用食品添加剂等,受热会发生分解。现加热42.8g石膏样品,固体质量随温度的变化如下图(杂质不参与反应且不含钙元素)。回答下列问题:
(1)石膏开始分解时的温度为 ______℃。
(2)42.8g该石膏样品中含有结晶水 ______g。
(3)根据反应,计算42.8g该石膏样品中含有CaSO4 2H2O的质量。(写出计算过程)
(4)1350~1500℃时,CaSO4继续分解生成氧化钙、二氧化硫和一种气体单质,该气体单质是 ______。最终剩余的19.6g固体中含有CaO的质量为 ______g。
1.【答案】A
2~4.【答案】B 、C 、B
5.【答案】D
6.【答案】C
7.【答案】B
8.【答案】C
9.【答案】D
10.【答案】A
11.【答案】C
12.【答案】A
13.【答案】A
14.【答案】C
15.【答案】B
16.【答案】在不断运动;
①导热;
②二氧化硫;天然气;
①光;
②降低温度至着火点以下;
③二氧化碳
17.【答案】+4;
增大反应物之间的接触面积,使反应更充分;
过滤;
H2O;Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
1.5;Fe2+、Fe3+或亚铁离子、铁离子;
分解反应
18.【答案】物理;纳米海绵具有网状多孔的结构;
有机物;
高;强;油品自身的密度;
差;
BC
19.【答案】水槽;
;
m;
饱和NaHCO3溶液;c;
左;温室效应;
光合作用;高处
20.【答案】蒸发结晶;
CuSO4(答案不唯一);
产生白色沉淀;硝酸银;
检验并除尽;不能;氯化钡BaCl2引入了氯离子,对氯离子的检验产生了干扰;
AgNO3+NaCl=AgCl↓+NaNO3;
利用盐湖可以提取NaCl制成食盐供人食用,从而造福人类(答案不唯一)
21.【答案】70;
7.2;
34.4g;
氧气;11.2
第1页,共1页
一、单选题:本大题共15小题,共39分。
1.部分成语中蕴含着化学知识。下列成语涉及化学变化的是( )
A. 焚林而猎 B. 大浪淘沙 C. 五彩缤纷 D. 水乳交融
我国力争在2060年前实现“碳中和”。利用高效催化剂将二氧化碳聚合成性能与聚乙烯相似的塑料,解决了二氧化碳造成的环境问题。请完成各小题。
2.塑料属于( )
A. 复合材料 B. 合成材料 C. 金属材料 D. 无机非金属材料
3.下列对节能减排的建议可行的是( )
A. 生活垃圾集中焚烧 B. 大力推广燃油汽车 C. 推广使用光伏发电 D. 禁止使用化石燃料
4.下列不属于CO2吸收或转化途径的是( )
A. 光合作用 B. 加高烟囱 C. 聚合成塑料 D. 通入氢氧化钠溶液
5.2022年5月12日是第14个全国防灾减灾日。下列标志与加油站无关的是( )
A. B.
C. D.
6.下列是列车地面上残留的饮料,其中酸性最强的是( )
A. 葡萄汁(3.5~4.5) B. 鲜牛奶(6.3~6.6)
C. 苹果汁(2.9~3.3) D. 苏打水(8.5~9.5)
7.规范的操作是实验成功的保证。下列实验操作正确的是( )
A. 倾倒液体
B. 稀释浓硫酸
C. 加热固体
D. 检查装置气密性
8.小铭同学观察并记录了厨房中一些常备的调味剂,其中属于纯净物的是( )
A. 火锅底料 B. 食醋 C. 小苏打 D. 番茄酱
9.下列相关化学用语表述正确的是( )
A. K2S——硫酸钾 B. ——硝酸根离子
C. 2Fe2+——2个铁离子 D. N2——氮分子
10.福建茶文化历史悠久。下列有关“茶”的说法错误的是( )
A. 种茶:施用的化肥NH4HCO3属于复合肥
B. 制茶:发酵过程发生了化学变化
C. 泡茶:该过程类似于实验操作中的“溶解”
D. 饮茶:茶水可为人体补充水、维生素等营养素
11.甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
A. t1℃时,甲、乙两种溶液的溶质的质量分数相等
B. t1℃时,100g甲物质的饱和溶液中溶质的质量是20g
C. 要将甲溶液的状态由b点转化为a点,可以加适量溶质
D. 分别将t2℃时甲、乙两种物质的饱和溶液降温至t1℃,均有晶体析出
12.“可燃冰”是天然气(主要成分是甲烷)在高压、低温条件下形成的类冰状结晶物质。我国的“可燃冰”开采技术处于世界先进水平。在催化剂作用下,过氧化氢可将甲烷转化为含氧有机物,其微观过程如图所示:
下列说法正确的是( )
A. 过程1中发生的反应为CH4+H2O2H2O+CH3OH
B. 过程2反应前后分子的数目保持不变
C. 过程2生成的有机物分子中碳、氧原子的个数比为1:2
D. 反应结束后催化剂的质量增大
13.下列劳动项目所对应的化学解释错误的是( )
选项 劳动项目 化学解释
A 工人用铝合金制成门窗 铝在常温下不与氧气反应
B 用布擦干淋湿的自行车 铁部件潮湿易生锈
C 书画家用墨书写或绘制字画 常温下碳的化学性质不活泼
D 科学家寻找新的催化剂 催化剂能改变化学反应的速率
A. A B. B C. C D. D
14.下列物质的鉴别与除杂的实验方案设计正确的是( )
选项 实验目的 实验方案
A 鉴别CH4和H2 分别点燃,观察火焰颜色
B 除去CuCl2溶液中少量的FeCl2 加入过量的Fe粉,过滤
C 鉴别硫酸铵固体和氢氧化钠固体 取样后,加水溶解,测溶液温度
D 除去CO2中少量的CO 点燃
A. A B. B C. C D. D
15.小明喜欢进行各种家庭实验探究,他对下列实验的分析不合理的是( )
A. 可以制备、收集并检验氧气
B. 可以制取少量纯水
C. 可以利用此方法制取少量蒸馏水
D. 紫甘蓝汁液能用作酸碱指示剂
二、填空题:本大题共1小题,共8分。
16.中国古诗词中蕴含着丰富的化学知识。
(1)《浣溪沙》中“溅酒滴残歌扇字,弄花熏得舞衣香”,说明分子 ______。
(2)《寄怀楚和尚二首》中有“铁盂汤雪早,石炭煮茶迟”。
①铁锅化雪快是因为金属铁 ______性能好。
②“石炭”指的是煤炭(含少量的硫),它燃烧排放有害气体 ______,会导致酸雨。化石燃料包括煤、石油、______。
(3)【古诗中的蜡烛】
①“红蜡烛前明似昼”,这句诗体现了我们使用蜡烛主要是将蜡烛燃烧产生的化学能转化为 ______能。
②“马上风吹蜡烛灭”,体现的熄灭蜡烛的原理是 ______。
③“春蚕到死丝方尽,蜡炬成灰泪始干”,这句诗体现了蜡烛的奉献精神。“蜡炬成灰”是因为蜡烛燃烧生成 ______和水扩散到空气中。
三、流程题:本大题共1小题,共8分。
17.我国嫦娥六号成功完成世界首次月背采样,月壤中含有钛铁矿【主要成分为钛酸亚铁(FeTiO3),还含少量Fe2O3】。以钛铁矿为原料制备TiO2的原理如图所示。
已知:相关金属离子开始生成氢氧化物沉淀的pH如表。
氢氧化物 Ti(OH)4 Fe(OH)3 Fe(OH)2
开始沉淀时的pH 0.5 1.5 7.6
(1)FeTiO3中Ti元素化合价为 ______。
(2)用研磨机进行预处理的目的是 ______。
(3)经过水解槽后得到滤液和Ti(OH)4固体的操作为 ______。
(4)酸浸槽中的主要反应为FeTiO3+2H2SO4=TiOSO4+FeSO4+2X,X的化学式为 ______,发生的另一个反应的化学方程式为 ______。
(5)为了得到纯净的Ti(OH)4固体,调节水解槽中的pH时,应始终保持pH小于 ______。滤液中主要含有的金属离子为 ______。
(6)煅烧炉中发生化学反应类型为 ______(填基本反应类型)。
四、科普短文题:本大题共1小题,共8分。
18.阅读下面科普短文,回答问题。
纳米海绵是一种新型环保清洁产品,具有网状多孔的结构,有良好的吸油能力、循环利用以及环境友好等特性,清洁过程中可以吸附物体表面污渍,可用于清洁茶垢、油垢等,还可用于解决海上石油泄漏造成的污染。科学家测定了纳米海绵对不同油品的吸收能力(吸油质量比越高,其吸油能力越强),结果如图1所示。吸油能力的差异性取决于油品自身的密度。油品密度越大,纳米海绵的吸油能力越强。
纳米海绵还具有良好的循环利用性。通过挤压,可将纳米海绵吸附的油品挤出,经洗涤干燥后再次使用,两种吸油材料对泵油的循环吸收测试结果如图2所示。
依据上文,回答下列问题。
(1)纳米海绵的清洁过程属于 ______(填“物理”或“化学”)变化,纳米海绵可以吸附物体表面污渍的原因是 ______。
(2)纳米海绵是以三聚氰胺和甲醛(HCHO)为原料制得的高分子物质,甲醛属于 ______(填“有机物”或“无机物”)。
(3)由图1可知,与黑芝麻油比较,柴油的吸油质量比更 ______(填“高”或“低”),因此纳米海绵对柴油的吸收能力比对黑芝麻油的 ______(填“强”或“弱”),吸油能力的差异性取决于 ______。
(4)图2是纳米海绵和细菌纤维素循环吸油能力的对比,可得到的结论是:在其它相同条件下,循环使用次数1~8之间时,随循环使用次数的增加,纳米海绵吸油能力变化不明显,细菌纤维素的吸油能力变 ______(填“好”或“差”)。
(5)下列说法正确的是 ______(多选,填字母)。
A.纳米海绵不可重复使用
B.纳米海绵可用于清洁茶垢、油垢等
C.纳米海绵可用于解决海上石油泄漏造成的污染
D.纳米海绵对环己烷吸收能力最强
五、实验题:本大题共1小题,共10分。
19.Ⅰ、实验室气体制取及性质验证:
(1)仪器a的名称是 ______。
(2)实验室用A装置利用高锰酸钾制氧气的化学方程式为 ______。
(3)用B装置制取气体时向长颈漏斗中加入液体时,液面应该在 ______处。
(4)CO2在不同溶剂中的溶解能力如下表所示,若某同学想利用F装置收集一瓶纯净的CO2,集气瓶中的液体应选择 ______,收集CO2气体时气体从 ______口通入。
物质种类 水 酒精 饱和NaHCO3溶液
每毫升液体中溶解CO2的体积 1mL 3.6mL 几乎不溶
Ⅱ、跨学科实践活动
(5)某同学将上图1装置置于阳光下暴晒一段时间后,观察到红墨水 ______移,证明大气中二氧化碳含量上升会加剧 ______。
(6)CO2能促进植物的 ______,植物对二氧化碳的利用率白天大于夜间,兴趣小组同学设计了图2装置用于增加蔬菜大棚中二氧化碳的浓度。该装置放置在 ______更利于二氧化碳的利用。
六、探究题:本大题共1小题,共10分。
20.化学实践小组对古代制盐的原理、盐湖多彩的成因及盐湖水的成分产生了浓厚的兴趣,他们在老师的指导下展开了项目式学习活动。
任务一:分析古代制盐的原理
【查阅资料】我国古代劳动人民在春秋战国时期就开始使用“垦畦浇晒法”制盐。
【分析交流】
(1)古代劳动人民利用盐湖水“晒”盐的原理是______。
任务二:了解盐湖多彩的成因
【查阅资料】气温上升和藻类是盐湖出现多彩的最主要原因。气温上升时,水分蒸发,湖水中各成分浓度不同导致湖水变色;同时盐湖中生长着一种嗜盐绿色微藻,正常情况下使湖水呈绿色。
【小组交流】
(2)同学们联想所学知识,想到了某些盐的溶液具有美丽的颜色,如______溶液呈蓝色。
任务三:探究盐湖水的成分
【查阅资料】①盐湖水中含有大量的NaCl、Na2SO4和MgSO4等物质;②Ag2SO4为微溶于水的白色固体。
现提供一瓶已静置澄清的盐湖水用于其成分的探究。
【进行实验】
(3)同学们设计了以下实验方案:
实验操作 实验现象 实验结论
①取少量盐湖水于试管中,加入足量稀硝酸和过量Ba(NO3)2溶液,静置 ______ 盐湖水中含有
②取步骤①的上层清液于试管中,滴加几滴 ______ 溶液 产生白色沉淀 盐湖水中含有Cl-
【反思评价】
(4)步骤①中加入Ba(NO3)2溶液“过量”的目的是______;若将步骤①中的Ba(NO3)2溶液换成BaCl2溶液,步骤②中______(填“能”或“不能”)得出相应结论,理由是______。
(5)步骤②中发生反应的化学方程式为______。
【成果分享】
(6)在人类获取盐和使用盐的历史上,始终伴随着知识的发展和技术的进步,同学们将所学所获做成板报进行宣传,请你与他们共同完成。
最美盐湖
自然美 科技美 劳动美
夏季的多彩盐湖是气温上升和藻类等共同作用的结果 古代劳动人民发明了“垦畦浇晒法”制盐 利用盐湖可以造福人类,如 ______ (写一条)
七、计算题:本大题共1小题,共10分。
21.石膏的主要成分是CaSO4 2H2O(相对分子质量为172),可用于水泥缓凝剂、建筑制品、模型制作、医用食品添加剂等,受热会发生分解。现加热42.8g石膏样品,固体质量随温度的变化如下图(杂质不参与反应且不含钙元素)。回答下列问题:
(1)石膏开始分解时的温度为 ______℃。
(2)42.8g该石膏样品中含有结晶水 ______g。
(3)根据反应,计算42.8g该石膏样品中含有CaSO4 2H2O的质量。(写出计算过程)
(4)1350~1500℃时,CaSO4继续分解生成氧化钙、二氧化硫和一种气体单质,该气体单质是 ______。最终剩余的19.6g固体中含有CaO的质量为 ______g。
1.【答案】A
2~4.【答案】B 、C 、B
5.【答案】D
6.【答案】C
7.【答案】B
8.【答案】C
9.【答案】D
10.【答案】A
11.【答案】C
12.【答案】A
13.【答案】A
14.【答案】C
15.【答案】B
16.【答案】在不断运动;
①导热;
②二氧化硫;天然气;
①光;
②降低温度至着火点以下;
③二氧化碳
17.【答案】+4;
增大反应物之间的接触面积,使反应更充分;
过滤;
H2O;Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
1.5;Fe2+、Fe3+或亚铁离子、铁离子;
分解反应
18.【答案】物理;纳米海绵具有网状多孔的结构;
有机物;
高;强;油品自身的密度;
差;
BC
19.【答案】水槽;
;
m;
饱和NaHCO3溶液;c;
左;温室效应;
光合作用;高处
20.【答案】蒸发结晶;
CuSO4(答案不唯一);
产生白色沉淀;硝酸银;
检验并除尽;不能;氯化钡BaCl2引入了氯离子,对氯离子的检验产生了干扰;
AgNO3+NaCl=AgCl↓+NaNO3;
利用盐湖可以提取NaCl制成食盐供人食用,从而造福人类(答案不唯一)
21.【答案】70;
7.2;
34.4g;
氧气;11.2
第1页,共1页
同课章节目录
