拉分题型4 有机合成中的机理分析、物质推断 (含答案)高中化学苏教版(2019)选择性必修3 综合复习(含解析)
文档属性
| 名称 | 拉分题型4 有机合成中的机理分析、物质推断 (含答案)高中化学苏教版(2019)选择性必修3 综合复习(含解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-17 00:00:00 | ||
图片预览



文档简介
eq \o(\s\up7(),\s\do5( 拉分题型4 有机合成中的机理分析、物质推断))
循环转化机理图的分析
需先由题给情境信息,找出催化剂、反应物、生成物、中间体:
一“剂”指催化剂 催化剂在机理图中多数是以完整的循环出现的,以催化剂粒子为主题的多个物种一定在机理图中的主线上
三“物”指反应物、生成物、中间物种(或中间体) 反应物 通过一个箭头进入整个历程的物质是反应物
生成物 通过一个箭头最终脱离整个历程的物质一般多是产物
中间体 通过一个箭头脱离整个历程,但又生成生成物的是中间体,通过2个箭头进入整个历程的中间物质也是中间体,中间体有时在反应历程中用“[ ]”标出
1. (2023泰州期末)化合物Z是X和Br2反应的主产物,反应机理如下:
下列说法错误的是( )
A. X中所有碳原子共平面
B. X→Y过程中,X和Br2断开的都是σ键
C. Z存在顺反异构体
D. Z与足量H2加成后的产物分子中有2个手性碳原子
笔记:
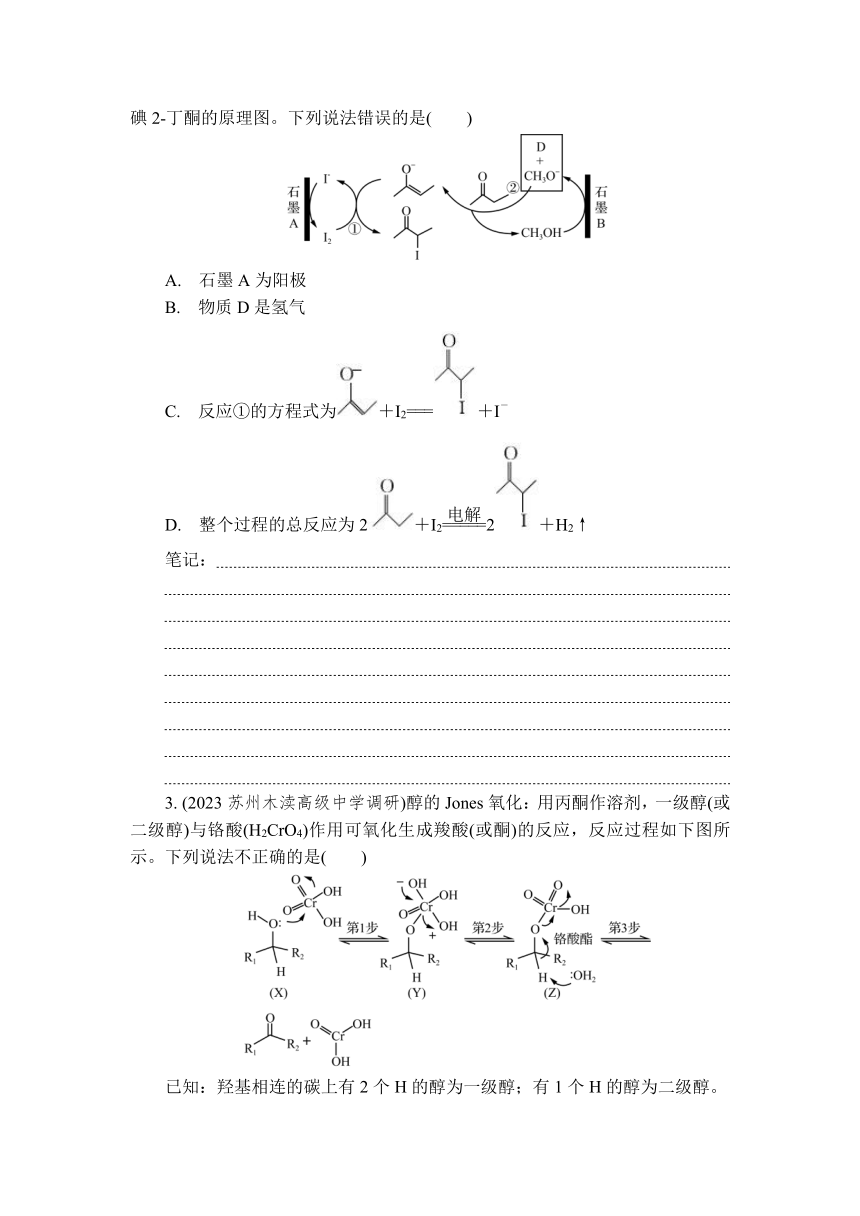
2. (2023南通如东月考)有机电合成是用电化学的方法进行有机合成的技术。如图是在KI-CH3OK-CH3OH体系中,以石墨为电极电解 2-丁酮制备中间体-3-碘2-丁酮的原理图。下列说法错误的是( )
A. 石墨A为阳极
B. 物质D是氢气
C. 反应①的方程式为+I2===+I-
D. 整个过程的总反应为2+I22+H2↑
笔记:
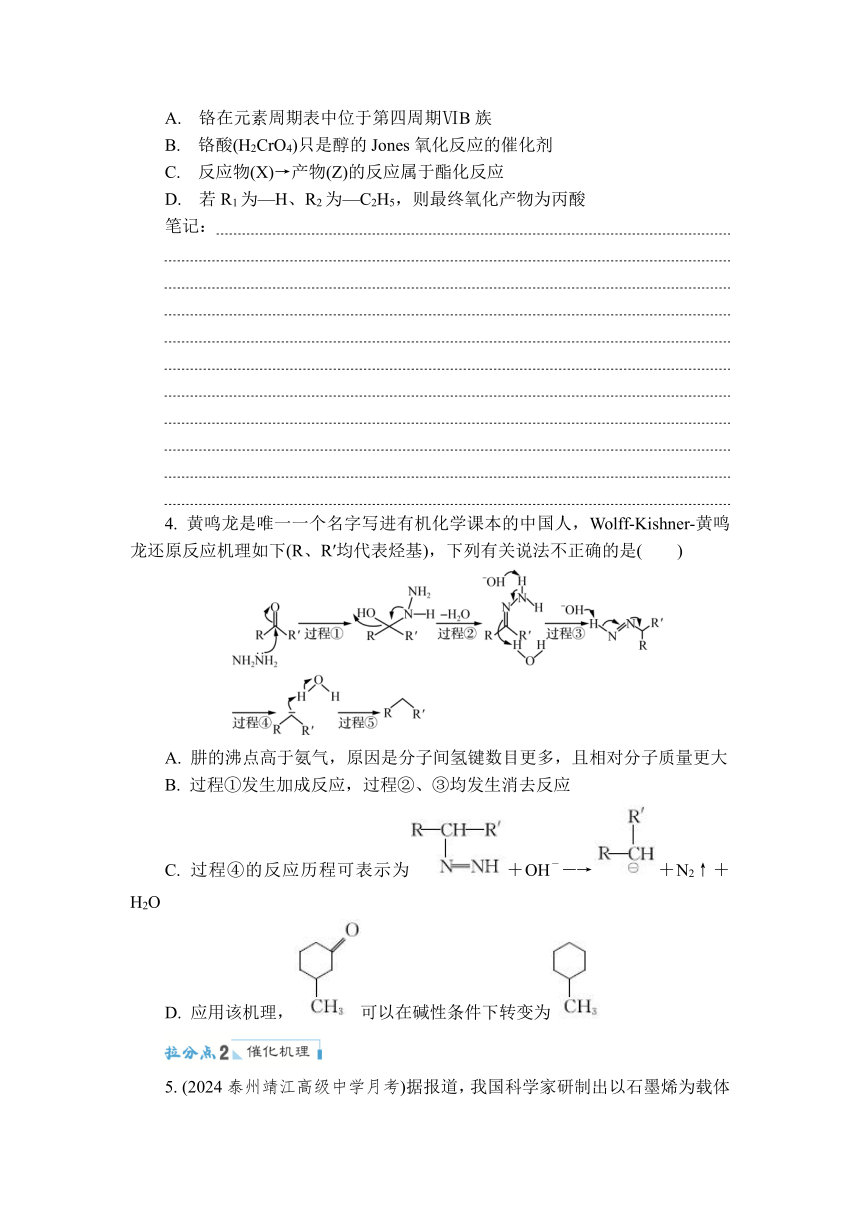
3. (2023苏州木渎高级中学调研)醇的Jones氧化:用丙酮作溶剂,一级醇(或二级醇)与铬酸(H2CrO4)作用可氧化生成羧酸(或酮)的反应,反应过程如下图所示。下列说法不正确的是( )
已知:羟基相连的碳上有2个H的醇为一级醇;有1个H的醇为二级醇。
A. 铬在元素周期表中位于第四周期ⅥB族
B. 铬酸(H2CrO4)只是醇的Jones氧化反应的催化剂
C. 反应物(X)→产物(Z)的反应属于酯化反应
D. 若R1为—H、R2为—C2H5,则最终氧化产物为丙酸
笔记:
4. 黄鸣龙是唯一一个名字写进有机化学课本的中国人,Wolff Kishner 黄鸣龙还原反应机理如下(R、R′均代表烃基),下列有关说法不正确的是( )
A. 肼的沸点高于氨气,原因是分子间氢键数目更多,且相对分子质量更大
B. 过程①发生加成反应,过程②、③均发生消去反应
C. 过程④的反应历程可表示为+OH-―→+N2↑+H2O
D. 应用该机理,可以在碱性条件下转变为
5. (2024泰州靖江高级中学月考)据报道,我国科学家研制出以石墨烯为载体的催化剂,在25 ℃下用H2O2直接将CH4转化为含氧有机物,其主要原理如图所示。下列说法正确的是( )
A. H2O2是非极性分子
B. 图中表示CH4,该模型也可以表示CCl4
C. 步骤ii涉及极性键与非极性键的断裂与生成
D. 步骤i到iv的总反应为CH4+2H2O2HCHO+3H2O
笔记:
6. (2023苏锡常镇调研一)在Pt Pd合金表面上甲醇与水蒸气重整反应的机理如图丙所示(“*”表示此微粒吸附在催化剂表面,M为反应过程中的中间产物)。
根据元素电负性的变化规律,推导M的结构简式并描述步骤2的反应机理:____________________________________________________________________________________________________________________________________________。
笔记:
7. 某科学家在常温下用S In催化剂电催化还原CO2制甲酸的机理如图甲所示,反应历程如图乙所示,其中吸附在催化剂表面的原子用“*”标注。
甲
乙
笔记:
根据图甲、乙,描述反应过程:_________________________________________
______________________________________________________________________,
写出电催化二氧化碳转化为甲酸的总的半反应式:_______________________
__________________。
笔记:
8. (2023南京、盐城二模)CO2用于制备苯乙烯有助于实现“碳中和”。在催化剂X作用下,CO2参与反应的机理如图所示(α、β表示乙苯分子中C或H原子的位置;A、B为催化剂的活性位点,其中A位点带部分正电荷,B1、B2位点带部分负电荷)。根据元素电负性的变化规律,图示的反应机理中步骤Ⅰ和步骤Ⅱ可描述为________________________________________________________________
____________________________________________________________________________________________________________________________________________。
笔记:
9. (2023盐城三模)电催化酯交换法合成碳酸二甲酯的机理如下:
已知: 代表微粒带负电荷。
I 在反应过程中的机理可描述为______________________________________
____________________________________________________________________________________________________________________________________________。
笔记:
10. 在催化剂作用下,由HCOOH释氢可以制得H2,其可能的反应机理如图所示。研究发现,其他条件不变时,以HCOOK溶液代替HCOOH催化释氢效果更佳。下列说法正确的是( )
A. HCOOH催化释氢过程中,有极性键和非极性键的断裂
B. HCOOD代替HCOOH催化释氢,生成CO2、H2、HD及D2
C. HCOOK溶液代替HCOOH时发生反应,生成CO2和H2
D. 其他条件不变时,以HCOOK溶液代替HCOOH能提高释放氢气的速率
笔记:
11. (2024苏州期中)在Fe+催化下,C2H6与N2O制备乙醛的反应机理如图所示,下列说法正确的是( )
A. 增加Fe+的量,C2H6的平衡转化率增大
B. 过程①~⑥中铁元素化合价均发生变化
C. X为C2H5OH,是反应的产物之一
D. 每消耗1 mol N2O可制备0.5 mol乙醛
笔记:
12. 利用有机分子模拟生物体内“醛缩酶”催化Diels Alder反应取得重要进展,荣获2021年诺贝尔化学奖。某Diels Alder反应催化机理如下,下列说法错误的是( )
A. 总反应为加成反应 B. Ⅰ和Ⅴ互为同系物
C. Ⅵ是反应的催化剂 D. 化合物X为H2O
13. (1) 化合物G可用于药用多肽的结构修饰,其人工合成路线如下:
F的分子式为C12H17NO2,其结构简式为________________________________。
笔记:
(2) F是一种天然产物,具有抗肿瘤等活性,其人工合成路线如图所示。
E→F中有一种分子式为C15H14O4的副产物生成,该副产物的结构简式为____________________。
(3) 化合物F是合成某种抗肿瘤药物的重要中间体,其合成路线如下:
B的结构简式为____________________。
笔记:
14. (2023南通二模)化合物G是一种重要的药物中间体,其人工合成路线如下:
B→C中经历BXYC的过程,写出中间体Y的结构简式:____________________。
拉分题型4 有机合成中的机理分析、物质推断
拉分点1 简单的反应机理
1. B X中苯环是平面结构,三键中原子共直线,所以所有碳原子共平面,A正确;X→Y过程中,X中碳碳三键变为Y中的碳碳双键,断开的是π键,B错误;Z中双键的不饱和碳分别连有不同的原子或基团,存在顺反异构体,C正确;Z与足量H2加成后的产物分子中有2个手性碳原子,D正确。
2. D 图中石墨A中I-→I2,I元素的化合价升高,发生氧化反应,A为阳极;石墨B中CH3OH→CH3O-+D,其中C、O元素的化合价不变,而B为阴极,则H元素的化合价应该降低,则D为H2。石墨A中I元素的化合价升高,发生氧化反应,A为阳极,A正确;B为阴极,则H元素的化合价降低,D为H2,B正确;反应①的方程式为+I2===+I-,C正确;参加反应的为I-、CH3OH、2-丁酮(),化学方程式为+I-+CH3OH+CH3O-+H2↑,D错误。
3. B 铬元素是24号元素,价电子排布为3d54s1,在元素周期表中的位置为第四周期ⅥB族,A正确;铬酸参加整个反应,铬元素化合价降低,则铬酸(H2CrO4)是整个反应的氧化剂,B错误;酯化反应是醇跟羧酸或含氧无机酸生成酯和水的反应,反应物(X)是醇与铬酸反应生成产物(Z),为铬酸酯,则该反应属于酯化反应,C正确;若R1为—H、R2为—C2H5,羟基相连的碳上有2个H为一级醇,与铬酸(H2CrO4)作用可氧化生成羧酸,则该氧化反应最终生成C2H5COOH,为丙酸,D正确。
4. B 肼和氨气都是分子晶体,肼分子中含有两个氨基,相对分子质量大于氨气,分子间形成的氢键数目多于氨气,所以肼分子的分子间作用力强于氨气,沸点高于氨气,A正确;过程③发生的反应为,反应中分子的不饱和度不变,不可能发生消去反应,B错误;由质量守恒定律可知,过程④发生的反应为+OH-―→+N2↑+H2O,C正确;该反应的总反应为碱性条件下与肼反应生成R—CH2—R′、氮气和水,则碱性条件下与肼反应能转化为,D正确。
拉分点2 催化机理
5. D H2O2是含有非极性键的极性分子,A错误;图中表示CH4,该模型不能表示CCl4,Cl的原子半径大于C原子的,B错误;从反应的原理图来看,步骤ii为*CH3+*H+H2O2―→CH3OH+H2O,涉及极性键的断裂与生成,涉及非极性键的断裂,不涉及非极性键的生成,C错误;一个甲烷分子和一个过氧化氢分子反应生成一个甲醇分子和一个水分子,故其总反应的化学方程式为CH4+H2O2CH3OH+H2O,D正确。
6. M的结构简式为,吸附在催化剂表面的H2O 断裂为H 和OH,H原子与甲醛分子中的氧原子结合,OH与碳原子结合,生成的(通过氧原子)吸附在催化剂表面
7. H2O在催化剂表面活性位点S2-的催化作用下,得到电子转化为OH-和被吸附的H*,同时CO2被带微量正电性In吸附后与H*结合,得到被吸附的HCOO*,HCOO*再与H*结合转化为被吸附的HCOOH*,最后脱附生成HCOOH
CO2+2H2O+2e-HCOOH+2OH-
8. 乙苯α-H带部分正电荷,被带部分负电荷的B1位点吸引,随后解离出H+并吸附在B1位点上;(B1位点上的)H+与B2位点上CO2中带部分负电荷的O作用生成,带部分正电荷的C吸附在带部分负电荷的B2位点上
9. O的电负性大于C,在碳酸1,2丙二酯的分子中,酯基碳原子带有部分正电荷,受到体系中I 进攻,碳氧双键断裂,酯基氧所带的负电荷离去,恢复碳氧双键; CH3O 进攻酯基中的碳原子,I 离去,恢复碳氧双键
拉分点3 循环催化
10. D HCOOH催化释氢过程中,涉及N—H键的断裂和形成、O—H键的断裂以及H—H键的形成,有极性键的断裂,有极性键和非极性键的生成,A错误;HCOOD代替HCOOH催化释氢,除生成CO2外,还有HD,没有D2,B错误;HCOOK溶液代替HCOOH时发生反应,生成的KOH能吸收CO2转变成HCO,C错误;其他条件不变时,以HCOOK溶液代替HCOOH反应,HCOO-浓度高,有利于第一步快速进行,能提高释放氢气的速率和纯度,D正确。
11. C 由图可知,Fe+是反应的催化剂,主反应为乙烷与一氧化二氮反应生成乙醛、氮气和水,副反应为乙烷与一氧化二氮反应生成乙醇和氮气。Fe+是反应的催化剂,催化剂能增大反应速率,但化学平衡不移动,则增加Fe+的量,乙烷的转化率不变,A错误;反应③、④中,铁元素化合价没有发生变化,B错误;乙烷与一氧化二氮制备乙醛时,会发生副反应生成乙醇,所以X为反应的产物之一的乙醇,C正确;乙烷与一氧化二氮制备乙醛时,会发生副反应生成乙醇,由得失电子数目守恒可知,消耗1 mol N2O时,反应生成乙醛的物质的量小于0.5 mol,D错误。
12. B 由催化机理可知,总反应为,该反应为加成反应,A正确;结构相似、分子组成上相差若干个CH2原子团的有机物互为同系物,和结构不相似、分子组成上也不是相差若干个CH2原子团,两者不互为同系物,B错误;由催化机理可知,反应消耗了Ⅵ又生成了Ⅵ,Ⅵ是反应的催化剂,C正确;Ⅰ+Ⅵ―→X+Ⅱ,由Ⅰ、Ⅵ、Ⅱ的结构简式可知,X为H2O,D正确。
拉分点4 有机推断
13. (1)
(2)
(3)
14. 解析:B→C中经历BXYC的过程,结合C的结构分析,说明通过加成反应,醛基中的碳氧双键和氨基之间进行加成反应连成环,即生成,再消去形成双键,生成,再加成形成C。
循环转化机理图的分析
需先由题给情境信息,找出催化剂、反应物、生成物、中间体:
一“剂”指催化剂 催化剂在机理图中多数是以完整的循环出现的,以催化剂粒子为主题的多个物种一定在机理图中的主线上
三“物”指反应物、生成物、中间物种(或中间体) 反应物 通过一个箭头进入整个历程的物质是反应物
生成物 通过一个箭头最终脱离整个历程的物质一般多是产物
中间体 通过一个箭头脱离整个历程,但又生成生成物的是中间体,通过2个箭头进入整个历程的中间物质也是中间体,中间体有时在反应历程中用“[ ]”标出
1. (2023泰州期末)化合物Z是X和Br2反应的主产物,反应机理如下:
下列说法错误的是( )
A. X中所有碳原子共平面
B. X→Y过程中,X和Br2断开的都是σ键
C. Z存在顺反异构体
D. Z与足量H2加成后的产物分子中有2个手性碳原子
笔记:
2. (2023南通如东月考)有机电合成是用电化学的方法进行有机合成的技术。如图是在KI-CH3OK-CH3OH体系中,以石墨为电极电解 2-丁酮制备中间体-3-碘2-丁酮的原理图。下列说法错误的是( )
A. 石墨A为阳极
B. 物质D是氢气
C. 反应①的方程式为+I2===+I-
D. 整个过程的总反应为2+I22+H2↑
笔记:
3. (2023苏州木渎高级中学调研)醇的Jones氧化:用丙酮作溶剂,一级醇(或二级醇)与铬酸(H2CrO4)作用可氧化生成羧酸(或酮)的反应,反应过程如下图所示。下列说法不正确的是( )
已知:羟基相连的碳上有2个H的醇为一级醇;有1个H的醇为二级醇。
A. 铬在元素周期表中位于第四周期ⅥB族
B. 铬酸(H2CrO4)只是醇的Jones氧化反应的催化剂
C. 反应物(X)→产物(Z)的反应属于酯化反应
D. 若R1为—H、R2为—C2H5,则最终氧化产物为丙酸
笔记:
4. 黄鸣龙是唯一一个名字写进有机化学课本的中国人,Wolff Kishner 黄鸣龙还原反应机理如下(R、R′均代表烃基),下列有关说法不正确的是( )
A. 肼的沸点高于氨气,原因是分子间氢键数目更多,且相对分子质量更大
B. 过程①发生加成反应,过程②、③均发生消去反应
C. 过程④的反应历程可表示为+OH-―→+N2↑+H2O
D. 应用该机理,可以在碱性条件下转变为
5. (2024泰州靖江高级中学月考)据报道,我国科学家研制出以石墨烯为载体的催化剂,在25 ℃下用H2O2直接将CH4转化为含氧有机物,其主要原理如图所示。下列说法正确的是( )
A. H2O2是非极性分子
B. 图中表示CH4,该模型也可以表示CCl4
C. 步骤ii涉及极性键与非极性键的断裂与生成
D. 步骤i到iv的总反应为CH4+2H2O2HCHO+3H2O
笔记:
6. (2023苏锡常镇调研一)在Pt Pd合金表面上甲醇与水蒸气重整反应的机理如图丙所示(“*”表示此微粒吸附在催化剂表面,M为反应过程中的中间产物)。
根据元素电负性的变化规律,推导M的结构简式并描述步骤2的反应机理:____________________________________________________________________________________________________________________________________________。
笔记:
7. 某科学家在常温下用S In催化剂电催化还原CO2制甲酸的机理如图甲所示,反应历程如图乙所示,其中吸附在催化剂表面的原子用“*”标注。
甲
乙
笔记:
根据图甲、乙,描述反应过程:_________________________________________
______________________________________________________________________,
写出电催化二氧化碳转化为甲酸的总的半反应式:_______________________
__________________。
笔记:
8. (2023南京、盐城二模)CO2用于制备苯乙烯有助于实现“碳中和”。在催化剂X作用下,CO2参与反应的机理如图所示(α、β表示乙苯分子中C或H原子的位置;A、B为催化剂的活性位点,其中A位点带部分正电荷,B1、B2位点带部分负电荷)。根据元素电负性的变化规律,图示的反应机理中步骤Ⅰ和步骤Ⅱ可描述为________________________________________________________________
____________________________________________________________________________________________________________________________________________。
笔记:
9. (2023盐城三模)电催化酯交换法合成碳酸二甲酯的机理如下:
已知: 代表微粒带负电荷。
I 在反应过程中的机理可描述为______________________________________
____________________________________________________________________________________________________________________________________________。
笔记:
10. 在催化剂作用下,由HCOOH释氢可以制得H2,其可能的反应机理如图所示。研究发现,其他条件不变时,以HCOOK溶液代替HCOOH催化释氢效果更佳。下列说法正确的是( )
A. HCOOH催化释氢过程中,有极性键和非极性键的断裂
B. HCOOD代替HCOOH催化释氢,生成CO2、H2、HD及D2
C. HCOOK溶液代替HCOOH时发生反应,生成CO2和H2
D. 其他条件不变时,以HCOOK溶液代替HCOOH能提高释放氢气的速率
笔记:
11. (2024苏州期中)在Fe+催化下,C2H6与N2O制备乙醛的反应机理如图所示,下列说法正确的是( )
A. 增加Fe+的量,C2H6的平衡转化率增大
B. 过程①~⑥中铁元素化合价均发生变化
C. X为C2H5OH,是反应的产物之一
D. 每消耗1 mol N2O可制备0.5 mol乙醛
笔记:
12. 利用有机分子模拟生物体内“醛缩酶”催化Diels Alder反应取得重要进展,荣获2021年诺贝尔化学奖。某Diels Alder反应催化机理如下,下列说法错误的是( )
A. 总反应为加成反应 B. Ⅰ和Ⅴ互为同系物
C. Ⅵ是反应的催化剂 D. 化合物X为H2O
13. (1) 化合物G可用于药用多肽的结构修饰,其人工合成路线如下:
F的分子式为C12H17NO2,其结构简式为________________________________。
笔记:
(2) F是一种天然产物,具有抗肿瘤等活性,其人工合成路线如图所示。
E→F中有一种分子式为C15H14O4的副产物生成,该副产物的结构简式为____________________。
(3) 化合物F是合成某种抗肿瘤药物的重要中间体,其合成路线如下:
B的结构简式为____________________。
笔记:
14. (2023南通二模)化合物G是一种重要的药物中间体,其人工合成路线如下:
B→C中经历BXYC的过程,写出中间体Y的结构简式:____________________。
拉分题型4 有机合成中的机理分析、物质推断
拉分点1 简单的反应机理
1. B X中苯环是平面结构,三键中原子共直线,所以所有碳原子共平面,A正确;X→Y过程中,X中碳碳三键变为Y中的碳碳双键,断开的是π键,B错误;Z中双键的不饱和碳分别连有不同的原子或基团,存在顺反异构体,C正确;Z与足量H2加成后的产物分子中有2个手性碳原子,D正确。
2. D 图中石墨A中I-→I2,I元素的化合价升高,发生氧化反应,A为阳极;石墨B中CH3OH→CH3O-+D,其中C、O元素的化合价不变,而B为阴极,则H元素的化合价应该降低,则D为H2。石墨A中I元素的化合价升高,发生氧化反应,A为阳极,A正确;B为阴极,则H元素的化合价降低,D为H2,B正确;反应①的方程式为+I2===+I-,C正确;参加反应的为I-、CH3OH、2-丁酮(),化学方程式为+I-+CH3OH+CH3O-+H2↑,D错误。
3. B 铬元素是24号元素,价电子排布为3d54s1,在元素周期表中的位置为第四周期ⅥB族,A正确;铬酸参加整个反应,铬元素化合价降低,则铬酸(H2CrO4)是整个反应的氧化剂,B错误;酯化反应是醇跟羧酸或含氧无机酸生成酯和水的反应,反应物(X)是醇与铬酸反应生成产物(Z),为铬酸酯,则该反应属于酯化反应,C正确;若R1为—H、R2为—C2H5,羟基相连的碳上有2个H为一级醇,与铬酸(H2CrO4)作用可氧化生成羧酸,则该氧化反应最终生成C2H5COOH,为丙酸,D正确。
4. B 肼和氨气都是分子晶体,肼分子中含有两个氨基,相对分子质量大于氨气,分子间形成的氢键数目多于氨气,所以肼分子的分子间作用力强于氨气,沸点高于氨气,A正确;过程③发生的反应为,反应中分子的不饱和度不变,不可能发生消去反应,B错误;由质量守恒定律可知,过程④发生的反应为+OH-―→+N2↑+H2O,C正确;该反应的总反应为碱性条件下与肼反应生成R—CH2—R′、氮气和水,则碱性条件下与肼反应能转化为,D正确。
拉分点2 催化机理
5. D H2O2是含有非极性键的极性分子,A错误;图中表示CH4,该模型不能表示CCl4,Cl的原子半径大于C原子的,B错误;从反应的原理图来看,步骤ii为*CH3+*H+H2O2―→CH3OH+H2O,涉及极性键的断裂与生成,涉及非极性键的断裂,不涉及非极性键的生成,C错误;一个甲烷分子和一个过氧化氢分子反应生成一个甲醇分子和一个水分子,故其总反应的化学方程式为CH4+H2O2CH3OH+H2O,D正确。
6. M的结构简式为,吸附在催化剂表面的H2O 断裂为H 和OH,H原子与甲醛分子中的氧原子结合,OH与碳原子结合,生成的(通过氧原子)吸附在催化剂表面
7. H2O在催化剂表面活性位点S2-的催化作用下,得到电子转化为OH-和被吸附的H*,同时CO2被带微量正电性In吸附后与H*结合,得到被吸附的HCOO*,HCOO*再与H*结合转化为被吸附的HCOOH*,最后脱附生成HCOOH
CO2+2H2O+2e-HCOOH+2OH-
8. 乙苯α-H带部分正电荷,被带部分负电荷的B1位点吸引,随后解离出H+并吸附在B1位点上;(B1位点上的)H+与B2位点上CO2中带部分负电荷的O作用生成,带部分正电荷的C吸附在带部分负电荷的B2位点上
9. O的电负性大于C,在碳酸1,2丙二酯的分子中,酯基碳原子带有部分正电荷,受到体系中I 进攻,碳氧双键断裂,酯基氧所带的负电荷离去,恢复碳氧双键; CH3O 进攻酯基中的碳原子,I 离去,恢复碳氧双键
拉分点3 循环催化
10. D HCOOH催化释氢过程中,涉及N—H键的断裂和形成、O—H键的断裂以及H—H键的形成,有极性键的断裂,有极性键和非极性键的生成,A错误;HCOOD代替HCOOH催化释氢,除生成CO2外,还有HD,没有D2,B错误;HCOOK溶液代替HCOOH时发生反应,生成的KOH能吸收CO2转变成HCO,C错误;其他条件不变时,以HCOOK溶液代替HCOOH反应,HCOO-浓度高,有利于第一步快速进行,能提高释放氢气的速率和纯度,D正确。
11. C 由图可知,Fe+是反应的催化剂,主反应为乙烷与一氧化二氮反应生成乙醛、氮气和水,副反应为乙烷与一氧化二氮反应生成乙醇和氮气。Fe+是反应的催化剂,催化剂能增大反应速率,但化学平衡不移动,则增加Fe+的量,乙烷的转化率不变,A错误;反应③、④中,铁元素化合价没有发生变化,B错误;乙烷与一氧化二氮制备乙醛时,会发生副反应生成乙醇,所以X为反应的产物之一的乙醇,C正确;乙烷与一氧化二氮制备乙醛时,会发生副反应生成乙醇,由得失电子数目守恒可知,消耗1 mol N2O时,反应生成乙醛的物质的量小于0.5 mol,D错误。
12. B 由催化机理可知,总反应为,该反应为加成反应,A正确;结构相似、分子组成上相差若干个CH2原子团的有机物互为同系物,和结构不相似、分子组成上也不是相差若干个CH2原子团,两者不互为同系物,B错误;由催化机理可知,反应消耗了Ⅵ又生成了Ⅵ,Ⅵ是反应的催化剂,C正确;Ⅰ+Ⅵ―→X+Ⅱ,由Ⅰ、Ⅵ、Ⅱ的结构简式可知,X为H2O,D正确。
拉分点4 有机推断
13. (1)
(2)
(3)
14. 解析:B→C中经历BXYC的过程,结合C的结构分析,说明通过加成反应,醛基中的碳氧双键和氨基之间进行加成反应连成环,即生成,再消去形成双键,生成,再加成形成C。
