鲁科版高中化学必修一第一章第二节研究物质的方法和程序第二课时导学案
文档属性
| 名称 | 鲁科版高中化学必修一第一章第二节研究物质的方法和程序第二课时导学案 |

|
|
| 格式 | docx | ||
| 文件大小 | 467.7KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-19 00:00:00 | ||
图片预览


文档简介
研究物质的方法和程序第二课时导学案
【课标分析】
1.了解研究物质性质的基本程序。
2.能列举、描述、辨识氯气的重要物理性质、化学性质及实验现象。
3.能说明氯水的重要性质及其应用。
4.能说明次氯酸的性质。
【教学目标】
1. 宏观辨识与微观探析
通过运用观察法来观察氯气,了解氯气的主要物理性质。
2. 变化观念与平衡思想
通过学习氯气的化学性质,能够利用氯气的化学性质去解释生活中的一些常见生活用品的原理。(漂白粉、84消毒液等)
3. 证据推理与模型认知
学生在上节课初步学会四种研究物质性质的基本方法,在本节课的学习中通过这四种方法去建立研究物质的性质的基本程序的认知结构,以氯气为例,系统性的学习一种物质的物理性质和化学性质。
4. 科学探究与创新意识
通过实验探究活动,引导学生按照研究物质的基本程序来研究氯气的性质,体验怎样科学、合理地运用观察方法。
5. 科学态度与社会责任
通过对氯气的性质的探究,激发学生学习化学的兴趣,乐于探究物质变化的奥秘。
【评价目标】
1.学生能了解研究物质性质的基本程序。
2.能掌握氯气的重要物理性质、化学性质及实验现象。
3.能说明氯水的重要性质及其应用。
4.能说明次氯酸的性质并能掌握84消毒液 漂白粉的制备及消毒漂白原理。
【教学重难点】
1. 教学重点:
(1)氯气的物理性质和化学性质。
(2)运用研究物质性质的程序去研究物质的性质。
2. 教学难点:
(1)含氯化合物(漂白粉)的制取、漂白原理和失效原因。
(2)液氯、氯水成分的区分。
【教法与学法】
教学方法---引导探究法
学习方法---分组实验、合作学习
【教学准备】
电脑多媒体课件、实验视频、实验用品(氯气、氢气、铁丝、铜丝、紫色石蕊试液、硝酸银溶液、集气瓶、坩埚钳、火柴、试管、水槽、铁架台等)等。
【教学过程】
[复习回顾] 复习金属钠的性质,研究物质性质的基本方法有哪些?
[学生回答]:
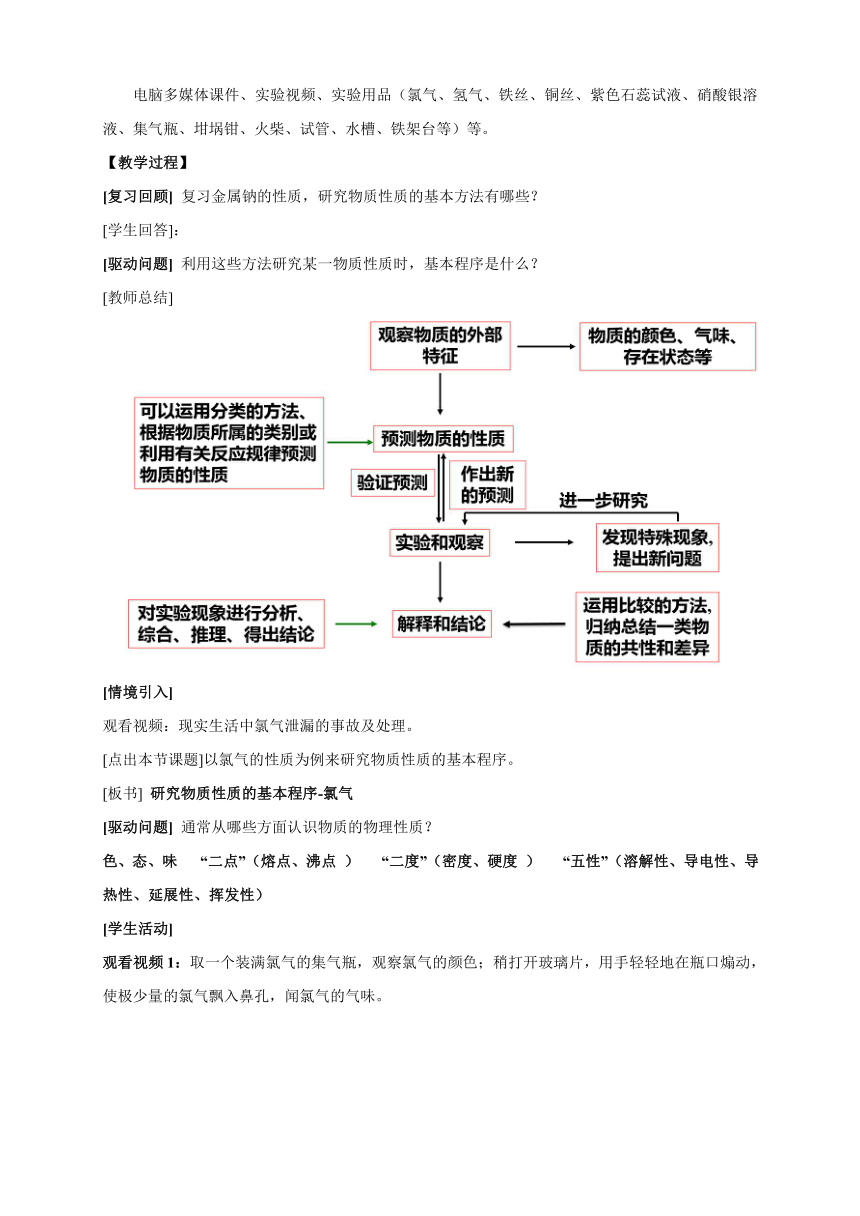
[驱动问题] 利用这些方法研究某一物质性质时,基本程序是什么?
[教师总结]
[情境引入]
观看视频:现实生活中氯气泄漏的事故及处理。
[点出本节课题]以氯气的性质为例来研究物质性质的基本程序。
[板书] 研究物质性质的基本程序-氯气
[驱动问题] 通常从哪些方面认识物质的物理性质?
色、态、味 “二点”(熔点、沸点 ) “二度”(密度、硬度 ) “五性”(溶解性、导电性、导热性、延展性、挥发性)
[学生活动]
观看视频1:取一个装满氯气的集气瓶,观察氯气的颜色;稍打开玻璃片,用手轻轻地在瓶口煽动,使极少量的氯气飘入鼻孔,闻氯气的气味。
观看视频2:取一个装满氯气的试管,将其倒扣在水槽中,静置一段时间后观察现象。
[驱动问题]
请同学们总结氯气物理性质?
氯气的物理性质
①通过直接观察能够认识气体物质的颜色、状态;嗅闻气体气味的正确操作方法是用手在集气瓶口轻轻扇动,仅使极少量气体飘进鼻孔。
②观察实验并填表:
颜色 气味 密度 水溶性 毒性 氯水颜色
色 强烈 气味 比空气___ 溶于水 _____ 色
[板书]一、氯气的物理性质
黄绿色,有毒,刺激性气味 密度比空气大 能溶于水 氯水为浅黄绿色
[驱动问题] 1、氯气是一种非金属单质,预测跟哪个学过的物质性质类似?它可能具有哪些化学性质?
2、可以通过哪些实验来验证你的预测?
[提醒] 通常可以通过物质的类别来认识一类物质的化学性质。氧气是一种非金属单质。根据氧气的化学性质,预测氯气的化学性质。还要从化合价来预测物质的化学性质。
[学生活动] 谈论回顾O2 的化学性质?
[学生回答] 1 、O2 -------(非金属单质)
与Fe、Al、Cu、Na等金属反应;
3Fe + 2O2 Fe3O4
2Cu + O2 2CuO
2Na+ O2Na2O2
与非金属单质反应:如H2、S、P等。
2H2 + O2 2H2O
2、预测氯气的化学性质:
[驱动问题] 氯气是否也有上面的性质?
Fe + Cl2
Cu + Cl2
Na+ Cl2
H2 + Cl2
[学生活动] 观看以下实验视频 分组讨论总结氯气化学性质
实验视频1:取一块绿豆大小的金属钠,用滤纸吸干表面的煤油,切去表层,放在石棉网上,用酒精灯微热。待金属钠融化成球状时,将盛有氯气的集气瓶迅速倒扣在钠球上方,观察现象。
实验现象:熔化的钠球在氯气中剧烈燃烧,产生白色的烟。
2Na+Cl22NaCl
实验视频2:用坩埚钳夹住一束铁丝,灼烧后立刻放入充满氯气的集气瓶中,观察发生的现象。然后把少量的水注入集气瓶里,用玻璃片盖住瓶口,振荡,观察溶液的颜色。
实验现象:铁丝在氯气中剧烈燃烧,产生棕红色的烟,得到黄色溶液。
2Fe+3Cl22FeCl3
实验视频3:用坩埚钳夹住一束铜丝,灼烧后立刻放入充满氯气的集气瓶中,观察发生的现象,然后把少量的水注入集气瓶里,用玻璃片盖住瓶口,振荡,观察溶液的颜色。
实验现象:铜丝在氯气中剧烈燃烧,产生棕黄色的烟,得到绿色溶液。
Cu+Cl2CuCl2
实验视频4:在空气中点燃氢气(点燃前要“验纯”),然后把导管伸入盛有氯气的集气瓶中,观察氢气在氯气中燃烧的现象。
实验现象:纯净的氢气在氯气中安静燃烧,产生苍白色火焰。集气瓶瓶口上方产生白雾。
H2+Cl22HCl
[驱动问题] 请归纳总结氯气的化学性质
[学生回答] (1)氯气和氧气相似,是一种非常活泼的非金属单质,容易与多数金属单质和H2、P等某些非金属单质发生反应,生成相应的氯化物。
①变价金属与Cl2反应生成高价氯化物。
②H2和Cl2在强光照射下会发生爆炸生成HCl,工业上利用氢气在氯气中燃烧的方法制取HCl。
(2)燃烧是一切发光放热的剧烈反应,燃烧过程中不一定有氧气参加反应。
[板书] 二、氯气的化学性质
与金属单质反应:
2Na+Cl22NaCl
2Fe+3Cl22FeCl3
Cu+Cl2CuCl2
(2)与非金属单质反应: H2+Cl22HCl
[问题驱动]
1、在研究氯气的溶解性实验中,将氯气放置一段时间后发现氯水的颜色变浅。这说明什么氯气具有什么性质呢?
2、氯气能和水发生反应吗?
3、如果氯气能与水发生反应,生成物是什么?
干燥的氯气依次通过干燥的红色布条、湿润的红色布条观察现象。
[学生活动] 观看视频,分组讨论以上问题
实验现象:干燥的有色布条不褪色,而湿润的有色布条褪色。
氯水中加入的试剂 实验现象 起作用的微粒 化学方程式或解释
AgNO3溶液 产生 沉淀 ____
红纸条 使湿润的红纸条_____ _____ 次氯酸具有_______
石蕊溶液 先变 后_____ ________ 酸性使石蕊变 ,次氯酸使之_____
[学生回答] 实验结论:
(1) 氯气不仅能溶于水,还会与水发生化学反应,反应的化学方程式:
Cl2 + H2O = HCl + HClO
(2) 干燥的Cl2不具有漂白性。
(3) HClO具有漂白性,它遇到有色物质时,能破坏其中的有机色质,使有色物质褪色,并能杀灭细菌,因此次氯酸具有漂白作用和消毒作用。
[板书] (3) 与水的反应: Cl2 + H2O = HCl + HClO
[驱动问题] 采用实验、观察、比较、分类方法研究HClO和氯水的性质
氯水与液氯的区别
液氯 新制氯水(三分子四离子) 久置氯水
成分 Cl2 Cl2、HClO、H2O、 H+、Cl-、ClO-、OH- H+、Cl-、 H2O、OH-
分类 纯净物 混合物 混合物
颜色 黄绿色 浅黄绿色 无色
性质 氧化性 酸性、氧化性、漂白性 酸性
次氯酸的性质
1. 漂白性:它遇到有色物质时,能破坏其中的有机色质,使有色物质褪色。
2. 不稳定性:HClO不稳定,见光会分解: 2HClO=2HCl + O2 ↑
3. 弱酸性:其酸性比碳酸还弱。
4. 强氧化性。
[驱动问题] 为什么氯气的实验最后用NaOH溶液处理?
[学生回答] Cl2 + 2NaOH === NaCl + NaClO + H2O
注意:实验室常用 NaOH 溶液等碱液吸收或除去多余的 Cl2 ,防止其污染环境。
[学生活动] 阅读材料讨论回答: 84消毒液、漂白粉的制备原理?其主要成分、有效成分是什么?
[学生回答]
Cl2 + 2NaOH === NaCl + NaClO + H2O (制84消毒液)
84消毒液的主要成分:NaCl 、 NaClO
漂白粉的有效成分: NaClO
2Cl2 + 2Ca(OH) 2 === CaCl2 + Ca(ClO)2 + 2H2O(制漂白粉)
漂白粉的主要成分: CaCl2 、 Ca(ClO)2
漂白粉的有效成分: Ca(ClO)2
工业上制取漂白粉用石灰乳,而不是石灰水。
【板书】(4) 与碱的反应:Cl2 + 2NaOH === NaCl + NaClO + H2O
2Cl2 + 2Ca(OH) 2 === CaCl2 + Ca(ClO)2 + 2H2O
[学习评价]
1.可以用氯气灌洞的方法来消灭田鼠,这是利用了氯气的( )
A.密度比空气大 B.易液化 C.能溶于水 D.有毒
2.用氯气跟单质化合不能制取的物质是( )
A.KCl B.FeCl2 C.FeCl3 D.CuCl2
3.某学生用氯气消毒过的自来水配制下列物质的溶液,不会产生明显药品变质的是( )
A.石蕊 B.AgNO3 C.NaOH D.AlCl3
4.下列化学反应的实验现象结论描述错误的是( )
A.钠在空气中燃烧发出黄色火焰,生成氧化钠
B.铜粉在氯气中燃烧生成棕色的烟
C.铁在氯气中燃烧产生红棕色烟
D.氢气在氯气中燃烧产生淡蓝色火焰
5.将适量的物质分别加到干燥的红色布条上,不能使其褪色的是( )
A.新制的氯水 B.氯化钙溶液
C.液氯 D.次氯酸溶液
6.把石蕊试液滴加到新制的氯水中,出现的现象是( )
A.溶液变红色 B.溶液变蓝色
C.溶液变紫色 D.溶液颜色先变红,后立即消失
答案:1.AD 2.B 3.D 4.AD 5.BC 6.D
[归纳提升]
【课标分析】
1.了解研究物质性质的基本程序。
2.能列举、描述、辨识氯气的重要物理性质、化学性质及实验现象。
3.能说明氯水的重要性质及其应用。
4.能说明次氯酸的性质。
【教学目标】
1. 宏观辨识与微观探析
通过运用观察法来观察氯气,了解氯气的主要物理性质。
2. 变化观念与平衡思想
通过学习氯气的化学性质,能够利用氯气的化学性质去解释生活中的一些常见生活用品的原理。(漂白粉、84消毒液等)
3. 证据推理与模型认知
学生在上节课初步学会四种研究物质性质的基本方法,在本节课的学习中通过这四种方法去建立研究物质的性质的基本程序的认知结构,以氯气为例,系统性的学习一种物质的物理性质和化学性质。
4. 科学探究与创新意识
通过实验探究活动,引导学生按照研究物质的基本程序来研究氯气的性质,体验怎样科学、合理地运用观察方法。
5. 科学态度与社会责任
通过对氯气的性质的探究,激发学生学习化学的兴趣,乐于探究物质变化的奥秘。
【评价目标】
1.学生能了解研究物质性质的基本程序。
2.能掌握氯气的重要物理性质、化学性质及实验现象。
3.能说明氯水的重要性质及其应用。
4.能说明次氯酸的性质并能掌握84消毒液 漂白粉的制备及消毒漂白原理。
【教学重难点】
1. 教学重点:
(1)氯气的物理性质和化学性质。
(2)运用研究物质性质的程序去研究物质的性质。
2. 教学难点:
(1)含氯化合物(漂白粉)的制取、漂白原理和失效原因。
(2)液氯、氯水成分的区分。
【教法与学法】
教学方法---引导探究法
学习方法---分组实验、合作学习
【教学准备】
电脑多媒体课件、实验视频、实验用品(氯气、氢气、铁丝、铜丝、紫色石蕊试液、硝酸银溶液、集气瓶、坩埚钳、火柴、试管、水槽、铁架台等)等。
【教学过程】
[复习回顾] 复习金属钠的性质,研究物质性质的基本方法有哪些?
[学生回答]:
[驱动问题] 利用这些方法研究某一物质性质时,基本程序是什么?
[教师总结]
[情境引入]
观看视频:现实生活中氯气泄漏的事故及处理。
[点出本节课题]以氯气的性质为例来研究物质性质的基本程序。
[板书] 研究物质性质的基本程序-氯气
[驱动问题] 通常从哪些方面认识物质的物理性质?
色、态、味 “二点”(熔点、沸点 ) “二度”(密度、硬度 ) “五性”(溶解性、导电性、导热性、延展性、挥发性)
[学生活动]
观看视频1:取一个装满氯气的集气瓶,观察氯气的颜色;稍打开玻璃片,用手轻轻地在瓶口煽动,使极少量的氯气飘入鼻孔,闻氯气的气味。
观看视频2:取一个装满氯气的试管,将其倒扣在水槽中,静置一段时间后观察现象。
[驱动问题]
请同学们总结氯气物理性质?
氯气的物理性质
①通过直接观察能够认识气体物质的颜色、状态;嗅闻气体气味的正确操作方法是用手在集气瓶口轻轻扇动,仅使极少量气体飘进鼻孔。
②观察实验并填表:
颜色 气味 密度 水溶性 毒性 氯水颜色
色 强烈 气味 比空气___ 溶于水 _____ 色
[板书]一、氯气的物理性质
黄绿色,有毒,刺激性气味 密度比空气大 能溶于水 氯水为浅黄绿色
[驱动问题] 1、氯气是一种非金属单质,预测跟哪个学过的物质性质类似?它可能具有哪些化学性质?
2、可以通过哪些实验来验证你的预测?
[提醒] 通常可以通过物质的类别来认识一类物质的化学性质。氧气是一种非金属单质。根据氧气的化学性质,预测氯气的化学性质。还要从化合价来预测物质的化学性质。
[学生活动] 谈论回顾O2 的化学性质?
[学生回答] 1 、O2 -------(非金属单质)
与Fe、Al、Cu、Na等金属反应;
3Fe + 2O2 Fe3O4
2Cu + O2 2CuO
2Na+ O2Na2O2
与非金属单质反应:如H2、S、P等。
2H2 + O2 2H2O
2、预测氯气的化学性质:
[驱动问题] 氯气是否也有上面的性质?
Fe + Cl2
Cu + Cl2
Na+ Cl2
H2 + Cl2
[学生活动] 观看以下实验视频 分组讨论总结氯气化学性质
实验视频1:取一块绿豆大小的金属钠,用滤纸吸干表面的煤油,切去表层,放在石棉网上,用酒精灯微热。待金属钠融化成球状时,将盛有氯气的集气瓶迅速倒扣在钠球上方,观察现象。
实验现象:熔化的钠球在氯气中剧烈燃烧,产生白色的烟。
2Na+Cl22NaCl
实验视频2:用坩埚钳夹住一束铁丝,灼烧后立刻放入充满氯气的集气瓶中,观察发生的现象。然后把少量的水注入集气瓶里,用玻璃片盖住瓶口,振荡,观察溶液的颜色。
实验现象:铁丝在氯气中剧烈燃烧,产生棕红色的烟,得到黄色溶液。
2Fe+3Cl22FeCl3
实验视频3:用坩埚钳夹住一束铜丝,灼烧后立刻放入充满氯气的集气瓶中,观察发生的现象,然后把少量的水注入集气瓶里,用玻璃片盖住瓶口,振荡,观察溶液的颜色。
实验现象:铜丝在氯气中剧烈燃烧,产生棕黄色的烟,得到绿色溶液。
Cu+Cl2CuCl2
实验视频4:在空气中点燃氢气(点燃前要“验纯”),然后把导管伸入盛有氯气的集气瓶中,观察氢气在氯气中燃烧的现象。
实验现象:纯净的氢气在氯气中安静燃烧,产生苍白色火焰。集气瓶瓶口上方产生白雾。
H2+Cl22HCl
[驱动问题] 请归纳总结氯气的化学性质
[学生回答] (1)氯气和氧气相似,是一种非常活泼的非金属单质,容易与多数金属单质和H2、P等某些非金属单质发生反应,生成相应的氯化物。
①变价金属与Cl2反应生成高价氯化物。
②H2和Cl2在强光照射下会发生爆炸生成HCl,工业上利用氢气在氯气中燃烧的方法制取HCl。
(2)燃烧是一切发光放热的剧烈反应,燃烧过程中不一定有氧气参加反应。
[板书] 二、氯气的化学性质
与金属单质反应:
2Na+Cl22NaCl
2Fe+3Cl22FeCl3
Cu+Cl2CuCl2
(2)与非金属单质反应: H2+Cl22HCl
[问题驱动]
1、在研究氯气的溶解性实验中,将氯气放置一段时间后发现氯水的颜色变浅。这说明什么氯气具有什么性质呢?
2、氯气能和水发生反应吗?
3、如果氯气能与水发生反应,生成物是什么?
干燥的氯气依次通过干燥的红色布条、湿润的红色布条观察现象。
[学生活动] 观看视频,分组讨论以上问题
实验现象:干燥的有色布条不褪色,而湿润的有色布条褪色。
氯水中加入的试剂 实验现象 起作用的微粒 化学方程式或解释
AgNO3溶液 产生 沉淀 ____
红纸条 使湿润的红纸条_____ _____ 次氯酸具有_______
石蕊溶液 先变 后_____ ________ 酸性使石蕊变 ,次氯酸使之_____
[学生回答] 实验结论:
(1) 氯气不仅能溶于水,还会与水发生化学反应,反应的化学方程式:
Cl2 + H2O = HCl + HClO
(2) 干燥的Cl2不具有漂白性。
(3) HClO具有漂白性,它遇到有色物质时,能破坏其中的有机色质,使有色物质褪色,并能杀灭细菌,因此次氯酸具有漂白作用和消毒作用。
[板书] (3) 与水的反应: Cl2 + H2O = HCl + HClO
[驱动问题] 采用实验、观察、比较、分类方法研究HClO和氯水的性质
氯水与液氯的区别
液氯 新制氯水(三分子四离子) 久置氯水
成分 Cl2 Cl2、HClO、H2O、 H+、Cl-、ClO-、OH- H+、Cl-、 H2O、OH-
分类 纯净物 混合物 混合物
颜色 黄绿色 浅黄绿色 无色
性质 氧化性 酸性、氧化性、漂白性 酸性
次氯酸的性质
1. 漂白性:它遇到有色物质时,能破坏其中的有机色质,使有色物质褪色。
2. 不稳定性:HClO不稳定,见光会分解: 2HClO=2HCl + O2 ↑
3. 弱酸性:其酸性比碳酸还弱。
4. 强氧化性。
[驱动问题] 为什么氯气的实验最后用NaOH溶液处理?
[学生回答] Cl2 + 2NaOH === NaCl + NaClO + H2O
注意:实验室常用 NaOH 溶液等碱液吸收或除去多余的 Cl2 ,防止其污染环境。
[学生活动] 阅读材料讨论回答: 84消毒液、漂白粉的制备原理?其主要成分、有效成分是什么?
[学生回答]
Cl2 + 2NaOH === NaCl + NaClO + H2O (制84消毒液)
84消毒液的主要成分:NaCl 、 NaClO
漂白粉的有效成分: NaClO
2Cl2 + 2Ca(OH) 2 === CaCl2 + Ca(ClO)2 + 2H2O(制漂白粉)
漂白粉的主要成分: CaCl2 、 Ca(ClO)2
漂白粉的有效成分: Ca(ClO)2
工业上制取漂白粉用石灰乳,而不是石灰水。
【板书】(4) 与碱的反应:Cl2 + 2NaOH === NaCl + NaClO + H2O
2Cl2 + 2Ca(OH) 2 === CaCl2 + Ca(ClO)2 + 2H2O
[学习评价]
1.可以用氯气灌洞的方法来消灭田鼠,这是利用了氯气的( )
A.密度比空气大 B.易液化 C.能溶于水 D.有毒
2.用氯气跟单质化合不能制取的物质是( )
A.KCl B.FeCl2 C.FeCl3 D.CuCl2
3.某学生用氯气消毒过的自来水配制下列物质的溶液,不会产生明显药品变质的是( )
A.石蕊 B.AgNO3 C.NaOH D.AlCl3
4.下列化学反应的实验现象结论描述错误的是( )
A.钠在空气中燃烧发出黄色火焰,生成氧化钠
B.铜粉在氯气中燃烧生成棕色的烟
C.铁在氯气中燃烧产生红棕色烟
D.氢气在氯气中燃烧产生淡蓝色火焰
5.将适量的物质分别加到干燥的红色布条上,不能使其褪色的是( )
A.新制的氯水 B.氯化钙溶液
C.液氯 D.次氯酸溶液
6.把石蕊试液滴加到新制的氯水中,出现的现象是( )
A.溶液变红色 B.溶液变蓝色
C.溶液变紫色 D.溶液颜色先变红,后立即消失
答案:1.AD 2.B 3.D 4.AD 5.BC 6.D
[归纳提升]
