江苏省天一中学2024-2025学年高一下学期期末考试化学试卷(含答案)
文档属性
| 名称 | 江苏省天一中学2024-2025学年高一下学期期末考试化学试卷(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 693.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-19 19:11:08 | ||
图片预览




文档简介
江苏省天一中学 2024—2025 学年第二学期期末考试
高一化学学科
本试卷总分 100 分,考试时间 75 分钟。
可能用到的相对原子质量:
H1 C12 N14 O16 Cl 35.5 I 127 Na23 Mg24 Al 27 Fe 56 Cu 64
第Ⅰ卷 选择题
一、选择题:(本题包括 13 小题,每小题 3 分,共计 39 分。每小题只有一个选项符合题意)。
我国饮食注重营养均衡,讲究“色香味形”。下列说法不正确的是 A.烹饪糖醋排骨加醋和酒发生了酯化反应,生成了独特香味的酯
B.芳香烃带有独特的芳香气味,可以油炸食物以增香
C.凉拌黄瓜加醋使其具有可口酸味,食醋中含有极性分子
D.端午时节用棕叶将糯米包裹成形,糯米中的淀粉可在淀粉酶作用下水解
关于物质的分离、提纯,下列说法错误的是
蒸馏法分离 CH Cl 和 CCl B.过滤法分离 1,2-二溴乙烷和溴水溶液
C.萃取和柱色谱法从青蒿中提取分离青蒿素 D.重结晶法提纯含有少量食盐和泥沙的苯甲酸
下列化学用语或图示正确的是
A.1,3-丁二烯的键线式: B. O 分子的球棍模型: C.激发态 H 原子的轨道表示式:
D. p-pπ 键形成的轨道重叠示意图:
乙酸(CH COOH)是弱酸, 而氯乙酸(ClCH COOH)的酸性强于乙酸, 这是因为---Cl 是一种强吸引电子的基团,能使----OH 上的 H 原子活性增大,有的基团属斥电子基团,能减弱---OH 上 H 原子的活性,这种作用称“诱导效应”。下列说法正确的是
HCOOH 显酸性,H O 呈中性,是因为 HCOOH 中存在强吸引电子基团醛基
CH COOH 酸性弱于 HCOOH, 是因为 CH COOH 中存在强吸引电子的基团甲基
相同温度下,等物质的量浓度的 ClCH COOH 溶液的酸性比 FCH COOH 溶液酸性大
“诱导效应”说明有机化合物的性质仅决定于官能团的结构
利用下列装置(夹持装置略)进行实验,不能达到相应实验目的的是
用甲装置制取乙烯
用乙装置制备溴苯并验证有 NBr 产生 C.用丙装置制取并收集乙酸乙酯
D.用丁装置验证乙醇的结构简式是( 3 3还是 CH CH OH
下列有关同分异构体数目(不考虑立体异构)的叙述正确的是
与互为同分异构体的芳香烃有 3 种
它与硝酸反应,可生成 4 种一硝基取代物
与两分子溴发生加成反应的产物,理论上最多有 3 种
分子式为 C7H16 的烃,分子中有 4 个甲基的同分异构体有 4 种
一定条件下,烯烃经臭氧化和还原性水解反应生成羰基化合物,该反应可表示为
化合物 Y 是合成丹参醇的中间体,其合成路线如下:下列说法正确的是
X 分子中含手性碳原子
X 转化为 Y 的过程中,8 与(CH MgBr 反应生成
Y 与 Br 以物质的量 1:1 发生加成反应时可得 3 种产物
X、Y 可用酸性 KMnO 溶液进行鉴别
化学试卷 第 2 页 共 7 页
化工原料 Z 是 X 与 HI 反应的主产物,X—→Z 的反应机理如下:
下列说法正确的是
X 分子中所有碳原子位于同一平面上 B. Y 与 Z 中碳原子杂化轨道类型相同
C. X 与 Z 分子中均含有 1 个手性碳原子 D. X 与 HI 反应有副产物 CH CH CH CH I 产生
化学品 Y 可由 X 通过加成、消去两步反应制得。下列说法不正确的是
X 能使溴水褪色,说明 X 中含碳碳双键
X→Y 有副产物生成
X、Y 都存在顺反异构体
Y 与足量 H 加成后的产物分子中只有一个手性碳原子
有机物结构决定性质。下列实验方案能达到探究目的的是
选项 探究目的 实验方案
A 苯中是否混有溴苯 向样品中滴加硝酸酸化的硝酸银溶液,观察实验现象
B 某物质是否属于醛类 向新制 Cu(OH) 悬浊液加入少量该物质的溶液,加热,观察实验现象
C 某芳香烃是否含有甲苯 向样品溶液中滴加酸性高锰酸钾溶液,观察是否褪色
D 柠檬酸的酸性是否比碳酸强 向小苏打粉末中滴入柠檬酸,观察实验现象
下列有关[Ni(NH ) ]SO 的说法正确的是
Ni 的核外电子排布式为[Ar]3d 4s B. 1m ol [Ni(NH ) ] 中 σ 键的数目为 18 mol
C.[Ni(NH ) ] ;中 H——N—H 的键角大于 NH 中的键角 D. VA 族元素单质的晶体类型相同
由硫酸铜溶液制取[Cu(NH ) ]SO ·H O 的实验如下:
步骤 1. 向盛有 4mL 0.1m ol/L 蓝色 CuSO 溶液的试管中, 滴加几滴 1m ol/L 氨水, 有蓝色沉淀生成;步骤 2.继续滴加氨水并振荡试管,沉淀溶解,得到深蓝色溶液;
步骤 3.向试管中加入 8mL95%乙醇,并用玻璃棒摩擦试管壁,有深蓝色晶体析出。下列说法错误的是
CuSO 溶液呈蓝色的原因是因溶液中含有 [ ( 2 )4]2+
步骤 2 发生反应的离子方程式为 4 3 + ( )2 = [ ( 3)4]2+ +2
步骤 3 中加入 8mL 95%乙醇是因为乙醇与水可形成分子间氢键,易溶于水
H O 与 Cu 的配位能力弱于 NH
化学试卷 第 3 页 共 7 页
第Ⅱ卷 非选择题
二、非选择题:共 4 题,共 61 分
(本题 18 分)
从结构角度分析, (C H ) N 能与 HCl 反应的原因是 ▲ 。
将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下列物质属于顺磁性物质的是 ▲ (填字母)。
A.[Cu(NH ) ] Cl B.[Cu(H O) ]SO C. Na[Al(OH) ]
Cu 与( 2 4)2生成环状结构的配离子 [ ( 2 4)2]2 ,该配离子的结构式为 ▲ (不考虑立体异构)。
CuCl 属于共价化合物,气态 CuCl 分子的相对分子质量为 199,该分子中含有配位键,则气态 CuCl 分子的结构式可能为 ▲ 。
1 ( 3)5 3 与足量的硝酸银溶液反应生成 2molAgCl,该配合物内界的化学式为 ▲ 。
苯甲醇与苯甲酸是重要的化工原料,某研究小组在实验室制备得到苯甲醇与苯甲酸钠混合溶液,已知:苯甲醇易溶于乙醚、乙醇,在水中溶解度较小。苯甲酸微溶于水。
则萃取分离苯甲醇与苯甲酸钠时,合适的萃取剂是 ▲ ,其理由是 ▲ 。萃取分液后,所得水层用盐酸
酸化得到苯甲酸,然后过滤、重结晶得到苯甲酸。
配合物 [ ( 3)5 ] 2和 [ ( 3)6] 3的配位数之比为 ▲ 。区别这两种配合物的实验方案为 ▲ 。
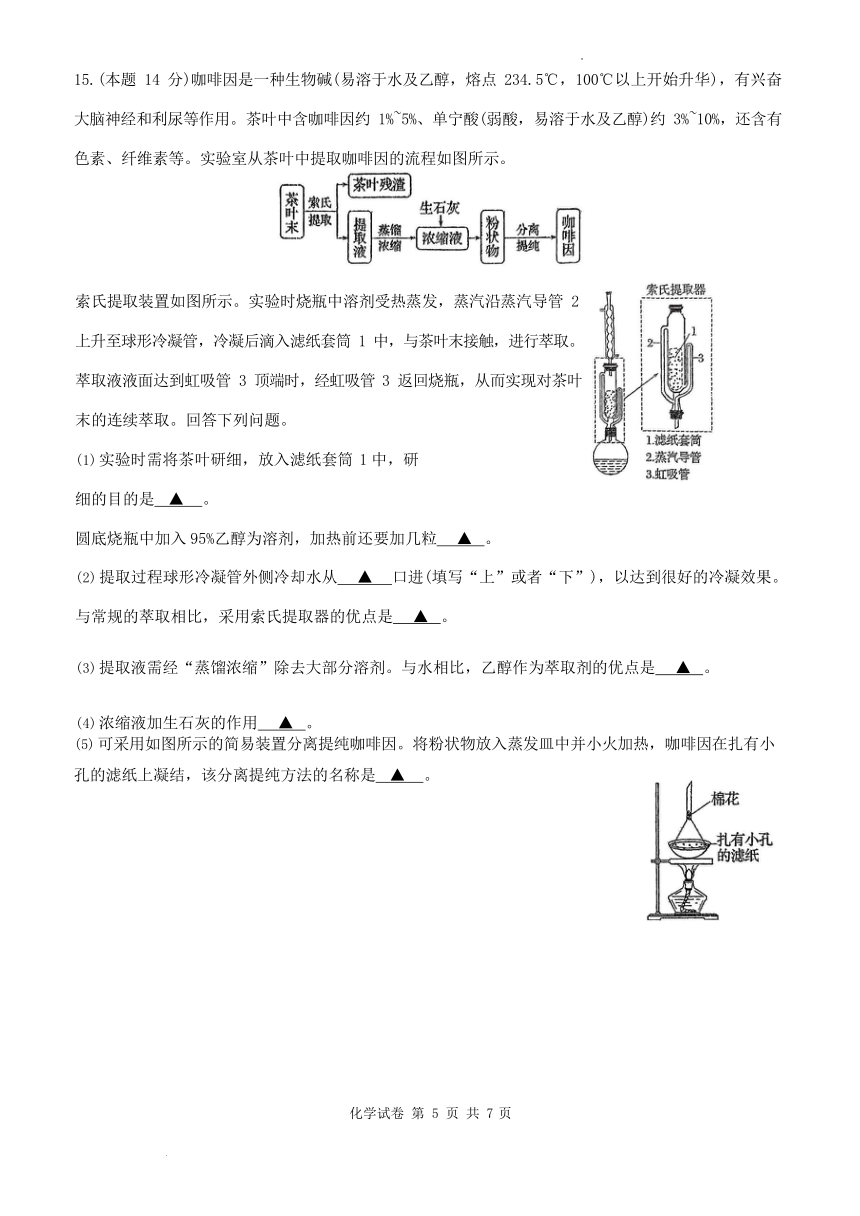
15.(本题 14 分)咖啡因是一种生物碱(易溶于水及乙醇,熔点 234.5℃,100℃以上开始升华),有兴奋大脑神经和利尿等作用。茶叶中含咖啡因约 1%~5%、单宁酸(弱酸,易溶于水及乙醇)约 3%~10%,还含有色素、纤维素等。实验室从茶叶中提取咖啡因的流程如图所示。
索氏提取装置如图所示。实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管 2上升至球形冷凝管,冷凝后滴入滤纸套筒 1 中,与茶叶末接触,进行萃取。萃取液液面达到虹吸管 3 顶端时,经虹吸管 3 返回烧瓶,从而实现对茶叶末的连续萃取。回答下列问题。
实验时需将茶叶研细,放入滤纸套筒 1 中,研细的目的是 ▲ 。
圆底烧瓶中加入 95%乙醇为溶剂,加热前还要加几粒 ▲ 。
提取过程球形冷凝管外侧冷却水从 ▲ 口进(填写“上”或者“下”),以达到很好的冷凝效果。
与常规的萃取相比,采用索氏提取器的优点是 ▲ 。
提取液需经“蒸馏浓缩”除去大部分溶剂。与水相比,乙醇作为萃取剂的优点是 ▲ 。
浓缩液加生石灰的作用 ▲ 。
可采用如图所示的简易装置分离提纯咖啡因。将粉状物放入蒸发皿中并小火加热,咖啡因在扎有小孔的滤纸上凝结,该分离提纯方法的名称是 ▲ 。
16. (本题 12 分)
乙炔是重要的化工原料,一种药物中间体 G 合成路线如图所示:
物质 F 所含的官能团名称 ▲ 。
物质 D 的结构简式为 ▲ 。
D 与 F 反应时会生成副产物 X,X 与 G 互为同分异构体,X 的结构简式为 ▲ 。
C 到 D 的反应类型为 ▲ 。
反应 A→B 机理示例如下图所示。
①请按示例在下图中标出反应 A→E 过程中 CO2 分子中一个 C 原子和一个 O 原子所带电荷,并用箭头表示反应连接方式(原子所带负电荷用δ 标注,原子所带正电荷用δ 标注,箭头由带负电荷原子指向带正电荷原子) ▲ 。
②已知:
① R M gC l
② H 2O
;下列流程中产物 Y 的结构简式为 ▲ 。
17.(本题 17 分)由芳香烃 X 合成一种功能高分子 H 的过程如图(部分产物、合成路线、反应条件略去)。
其中 A 是一氯代物,H 的链节组成为C7 H5 NO。
已知:I.芳香烃 X 用质谱仪测出的质谱图如图所示:
II.
III.
G 的系统命名名称是 ▲ 。
A 生成 B 的化学方程式是 ▲ 。
反应⑤的离子方程式是 ▲ ,该反应产物中碳原子的杂化类型是 ▲ 。
Y 与 X 同系物,相对分子质量多 42,苯环只有一个支链,能够使酸性高锰酸钾褪色,同时含有一个手性碳,请写出 Y 的结构简式 ▲ 。
设计以 X 和乙醛为原料,合成肉桂醛( )的合成路线 ▲ (其他无机试剂任选)。 (合成路线可表示为:A 反 应试 剂 BLL 反 应 试剂 目标产物)
反应条件 反应条件
江苏省天一中学 2024—2025 学年第二学期期末考试
一、选择题:(本题包括 13 小题,每小题 3 分,共计 39 分。每小题只有一个选项符合题意)。
B B A A B D B C D A D C C
二、非选择题:共 4 题,共 61 分
(1)增加固液接触面积,提取充分 沸石 (2)下 使用溶剂少,可连续萃取(萃取效率高) (3)
乙醇沸点低,易浓缩 (4)单宁酸 水 (5)升华
(1)碳碳三键、酯基
还原反应
(1)2-硝基苯甲酸 氧化反应
(2)
+3NaOH △ CH COONa+
2H2O
(3)
+2 Ag NH + +2OH- △
+2Ag +NH+ +3NH +H O
sp2
(5) Cl2
H2O/Δ NaOH
C u/Δ
2
NaOH/Δ CH3CHO
高一化学学科
本试卷总分 100 分,考试时间 75 分钟。
可能用到的相对原子质量:
H1 C12 N14 O16 Cl 35.5 I 127 Na23 Mg24 Al 27 Fe 56 Cu 64
第Ⅰ卷 选择题
一、选择题:(本题包括 13 小题,每小题 3 分,共计 39 分。每小题只有一个选项符合题意)。
我国饮食注重营养均衡,讲究“色香味形”。下列说法不正确的是 A.烹饪糖醋排骨加醋和酒发生了酯化反应,生成了独特香味的酯
B.芳香烃带有独特的芳香气味,可以油炸食物以增香
C.凉拌黄瓜加醋使其具有可口酸味,食醋中含有极性分子
D.端午时节用棕叶将糯米包裹成形,糯米中的淀粉可在淀粉酶作用下水解
关于物质的分离、提纯,下列说法错误的是
蒸馏法分离 CH Cl 和 CCl B.过滤法分离 1,2-二溴乙烷和溴水溶液
C.萃取和柱色谱法从青蒿中提取分离青蒿素 D.重结晶法提纯含有少量食盐和泥沙的苯甲酸
下列化学用语或图示正确的是
A.1,3-丁二烯的键线式: B. O 分子的球棍模型: C.激发态 H 原子的轨道表示式:
D. p-pπ 键形成的轨道重叠示意图:
乙酸(CH COOH)是弱酸, 而氯乙酸(ClCH COOH)的酸性强于乙酸, 这是因为---Cl 是一种强吸引电子的基团,能使----OH 上的 H 原子活性增大,有的基团属斥电子基团,能减弱---OH 上 H 原子的活性,这种作用称“诱导效应”。下列说法正确的是
HCOOH 显酸性,H O 呈中性,是因为 HCOOH 中存在强吸引电子基团醛基
CH COOH 酸性弱于 HCOOH, 是因为 CH COOH 中存在强吸引电子的基团甲基
相同温度下,等物质的量浓度的 ClCH COOH 溶液的酸性比 FCH COOH 溶液酸性大
“诱导效应”说明有机化合物的性质仅决定于官能团的结构
利用下列装置(夹持装置略)进行实验,不能达到相应实验目的的是
用甲装置制取乙烯
用乙装置制备溴苯并验证有 NBr 产生 C.用丙装置制取并收集乙酸乙酯
D.用丁装置验证乙醇的结构简式是( 3 3还是 CH CH OH
下列有关同分异构体数目(不考虑立体异构)的叙述正确的是
与互为同分异构体的芳香烃有 3 种
它与硝酸反应,可生成 4 种一硝基取代物
与两分子溴发生加成反应的产物,理论上最多有 3 种
分子式为 C7H16 的烃,分子中有 4 个甲基的同分异构体有 4 种
一定条件下,烯烃经臭氧化和还原性水解反应生成羰基化合物,该反应可表示为
化合物 Y 是合成丹参醇的中间体,其合成路线如下:下列说法正确的是
X 分子中含手性碳原子
X 转化为 Y 的过程中,8 与(CH MgBr 反应生成
Y 与 Br 以物质的量 1:1 发生加成反应时可得 3 种产物
X、Y 可用酸性 KMnO 溶液进行鉴别
化学试卷 第 2 页 共 7 页
化工原料 Z 是 X 与 HI 反应的主产物,X—→Z 的反应机理如下:
下列说法正确的是
X 分子中所有碳原子位于同一平面上 B. Y 与 Z 中碳原子杂化轨道类型相同
C. X 与 Z 分子中均含有 1 个手性碳原子 D. X 与 HI 反应有副产物 CH CH CH CH I 产生
化学品 Y 可由 X 通过加成、消去两步反应制得。下列说法不正确的是
X 能使溴水褪色,说明 X 中含碳碳双键
X→Y 有副产物生成
X、Y 都存在顺反异构体
Y 与足量 H 加成后的产物分子中只有一个手性碳原子
有机物结构决定性质。下列实验方案能达到探究目的的是
选项 探究目的 实验方案
A 苯中是否混有溴苯 向样品中滴加硝酸酸化的硝酸银溶液,观察实验现象
B 某物质是否属于醛类 向新制 Cu(OH) 悬浊液加入少量该物质的溶液,加热,观察实验现象
C 某芳香烃是否含有甲苯 向样品溶液中滴加酸性高锰酸钾溶液,观察是否褪色
D 柠檬酸的酸性是否比碳酸强 向小苏打粉末中滴入柠檬酸,观察实验现象
下列有关[Ni(NH ) ]SO 的说法正确的是
Ni 的核外电子排布式为[Ar]3d 4s B. 1m ol [Ni(NH ) ] 中 σ 键的数目为 18 mol
C.[Ni(NH ) ] ;中 H——N—H 的键角大于 NH 中的键角 D. VA 族元素单质的晶体类型相同
由硫酸铜溶液制取[Cu(NH ) ]SO ·H O 的实验如下:
步骤 1. 向盛有 4mL 0.1m ol/L 蓝色 CuSO 溶液的试管中, 滴加几滴 1m ol/L 氨水, 有蓝色沉淀生成;步骤 2.继续滴加氨水并振荡试管,沉淀溶解,得到深蓝色溶液;
步骤 3.向试管中加入 8mL95%乙醇,并用玻璃棒摩擦试管壁,有深蓝色晶体析出。下列说法错误的是
CuSO 溶液呈蓝色的原因是因溶液中含有 [ ( 2 )4]2+
步骤 2 发生反应的离子方程式为 4 3 + ( )2 = [ ( 3)4]2+ +2
步骤 3 中加入 8mL 95%乙醇是因为乙醇与水可形成分子间氢键,易溶于水
H O 与 Cu 的配位能力弱于 NH
化学试卷 第 3 页 共 7 页
第Ⅱ卷 非选择题
二、非选择题:共 4 题,共 61 分
(本题 18 分)
从结构角度分析, (C H ) N 能与 HCl 反应的原因是 ▲ 。
将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下列物质属于顺磁性物质的是 ▲ (填字母)。
A.[Cu(NH ) ] Cl B.[Cu(H O) ]SO C. Na[Al(OH) ]
Cu 与( 2 4)2生成环状结构的配离子 [ ( 2 4)2]2 ,该配离子的结构式为 ▲ (不考虑立体异构)。
CuCl 属于共价化合物,气态 CuCl 分子的相对分子质量为 199,该分子中含有配位键,则气态 CuCl 分子的结构式可能为 ▲ 。
1 ( 3)5 3 与足量的硝酸银溶液反应生成 2molAgCl,该配合物内界的化学式为 ▲ 。
苯甲醇与苯甲酸是重要的化工原料,某研究小组在实验室制备得到苯甲醇与苯甲酸钠混合溶液,已知:苯甲醇易溶于乙醚、乙醇,在水中溶解度较小。苯甲酸微溶于水。
则萃取分离苯甲醇与苯甲酸钠时,合适的萃取剂是 ▲ ,其理由是 ▲ 。萃取分液后,所得水层用盐酸
酸化得到苯甲酸,然后过滤、重结晶得到苯甲酸。
配合物 [ ( 3)5 ] 2和 [ ( 3)6] 3的配位数之比为 ▲ 。区别这两种配合物的实验方案为 ▲ 。
15.(本题 14 分)咖啡因是一种生物碱(易溶于水及乙醇,熔点 234.5℃,100℃以上开始升华),有兴奋大脑神经和利尿等作用。茶叶中含咖啡因约 1%~5%、单宁酸(弱酸,易溶于水及乙醇)约 3%~10%,还含有色素、纤维素等。实验室从茶叶中提取咖啡因的流程如图所示。
索氏提取装置如图所示。实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管 2上升至球形冷凝管,冷凝后滴入滤纸套筒 1 中,与茶叶末接触,进行萃取。萃取液液面达到虹吸管 3 顶端时,经虹吸管 3 返回烧瓶,从而实现对茶叶末的连续萃取。回答下列问题。
实验时需将茶叶研细,放入滤纸套筒 1 中,研细的目的是 ▲ 。
圆底烧瓶中加入 95%乙醇为溶剂,加热前还要加几粒 ▲ 。
提取过程球形冷凝管外侧冷却水从 ▲ 口进(填写“上”或者“下”),以达到很好的冷凝效果。
与常规的萃取相比,采用索氏提取器的优点是 ▲ 。
提取液需经“蒸馏浓缩”除去大部分溶剂。与水相比,乙醇作为萃取剂的优点是 ▲ 。
浓缩液加生石灰的作用 ▲ 。
可采用如图所示的简易装置分离提纯咖啡因。将粉状物放入蒸发皿中并小火加热,咖啡因在扎有小孔的滤纸上凝结,该分离提纯方法的名称是 ▲ 。
16. (本题 12 分)
乙炔是重要的化工原料,一种药物中间体 G 合成路线如图所示:
物质 F 所含的官能团名称 ▲ 。
物质 D 的结构简式为 ▲ 。
D 与 F 反应时会生成副产物 X,X 与 G 互为同分异构体,X 的结构简式为 ▲ 。
C 到 D 的反应类型为 ▲ 。
反应 A→B 机理示例如下图所示。
①请按示例在下图中标出反应 A→E 过程中 CO2 分子中一个 C 原子和一个 O 原子所带电荷,并用箭头表示反应连接方式(原子所带负电荷用δ 标注,原子所带正电荷用δ 标注,箭头由带负电荷原子指向带正电荷原子) ▲ 。
②已知:
① R M gC l
② H 2O
;下列流程中产物 Y 的结构简式为 ▲ 。
17.(本题 17 分)由芳香烃 X 合成一种功能高分子 H 的过程如图(部分产物、合成路线、反应条件略去)。
其中 A 是一氯代物,H 的链节组成为C7 H5 NO。
已知:I.芳香烃 X 用质谱仪测出的质谱图如图所示:
II.
III.
G 的系统命名名称是 ▲ 。
A 生成 B 的化学方程式是 ▲ 。
反应⑤的离子方程式是 ▲ ,该反应产物中碳原子的杂化类型是 ▲ 。
Y 与 X 同系物,相对分子质量多 42,苯环只有一个支链,能够使酸性高锰酸钾褪色,同时含有一个手性碳,请写出 Y 的结构简式 ▲ 。
设计以 X 和乙醛为原料,合成肉桂醛( )的合成路线 ▲ (其他无机试剂任选)。 (合成路线可表示为:A 反 应试 剂 BLL 反 应 试剂 目标产物)
反应条件 反应条件
江苏省天一中学 2024—2025 学年第二学期期末考试
一、选择题:(本题包括 13 小题,每小题 3 分,共计 39 分。每小题只有一个选项符合题意)。
B B A A B D B C D A D C C
二、非选择题:共 4 题,共 61 分
(1)增加固液接触面积,提取充分 沸石 (2)下 使用溶剂少,可连续萃取(萃取效率高) (3)
乙醇沸点低,易浓缩 (4)单宁酸 水 (5)升华
(1)碳碳三键、酯基
还原反应
(1)2-硝基苯甲酸 氧化反应
(2)
+3NaOH △ CH COONa+
2H2O
(3)
+2 Ag NH + +2OH- △
+2Ag +NH+ +3NH +H O
sp2
(5) Cl2
H2O/Δ NaOH
C u/Δ
2
NaOH/Δ CH3CHO
同课章节目录
