2024-2025学年天津二十中高二(下)期中化学试卷(含答案)
文档属性
| 名称 | 2024-2025学年天津二十中高二(下)期中化学试卷(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 219.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-20 00:00:00 | ||
图片预览

文档简介
2024-2025学年天津二十中高二(下)期中化学试卷
一、单选题:本大题共16小题,共48分。
1.下列有关化学用语表示不正确的是( )
A. 钠原子2Px电子云图: B. NH3的 VSEPR模型:
C. 乙酸甲酯的结构简式CH3OOCCH3 D. HCHO 的电子式:
2.下列有关物质结构与性质的比较正确的是( )
A. 沸点:PH3<NH3 B. 酸性:CH2ClCOOH>CH2FCOOH
C. 键角: D. 热稳定性:HCl>HF
3.下列叙述不正确的是( )
A. 第一电离能:N>O B. 酸性:CH2BrCOOH<CH2ClCOOH
C. 电负性:S>Se D. 键长:C=C>C—C
4.A、B、C、D、E为原子序数依次增大的前四周期元素。A是半径最小的元素,B的价电子层中有3个未成对电子;C与D同主族;E的最外层只有1个电子,但次外层有18个电子。五种元素形成的离子化合物可表示为[E(BA3)4(A2C)2]2+[DC4]2-。下列说法错误的是( )
A. [E(BA3)4(A2C)2]2+[DC4]2-中含有σ键数目为26
B. 呈正四面体形
C. 该化合物受热分解时首先失去的是BA3
D. A与B、C均可形成含有非极性共价键的化合物
5.下列实验装置或操作正确的是( )
A. 图1是排出碱式滴定管中的气泡操作
B. 图2装置可以测定化学反应速率
C. 图3装置可以分离二氯甲烷、三氯甲烷和四氯化碳的混合物
D. 图4装置用CCl4萃取碘水中的碘
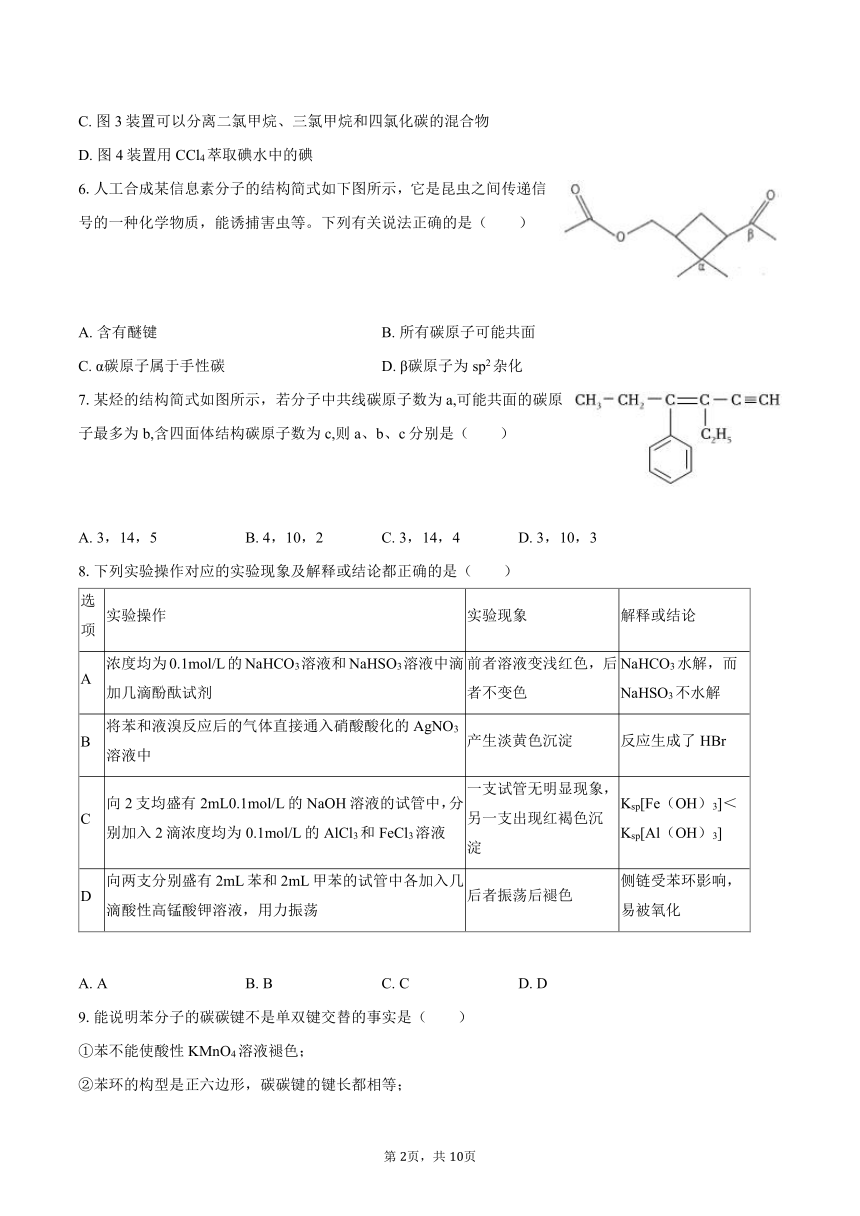
6.人工合成某信息素分子的结构简式如下图所示,它是昆虫之间传递信号的一种化学物质,能诱捕害虫等。下列有关说法正确的是( )
A. 含有醚键 B. 所有碳原子可能共面
C. α碳原子属于手性碳 D. β碳原子为sp2杂化
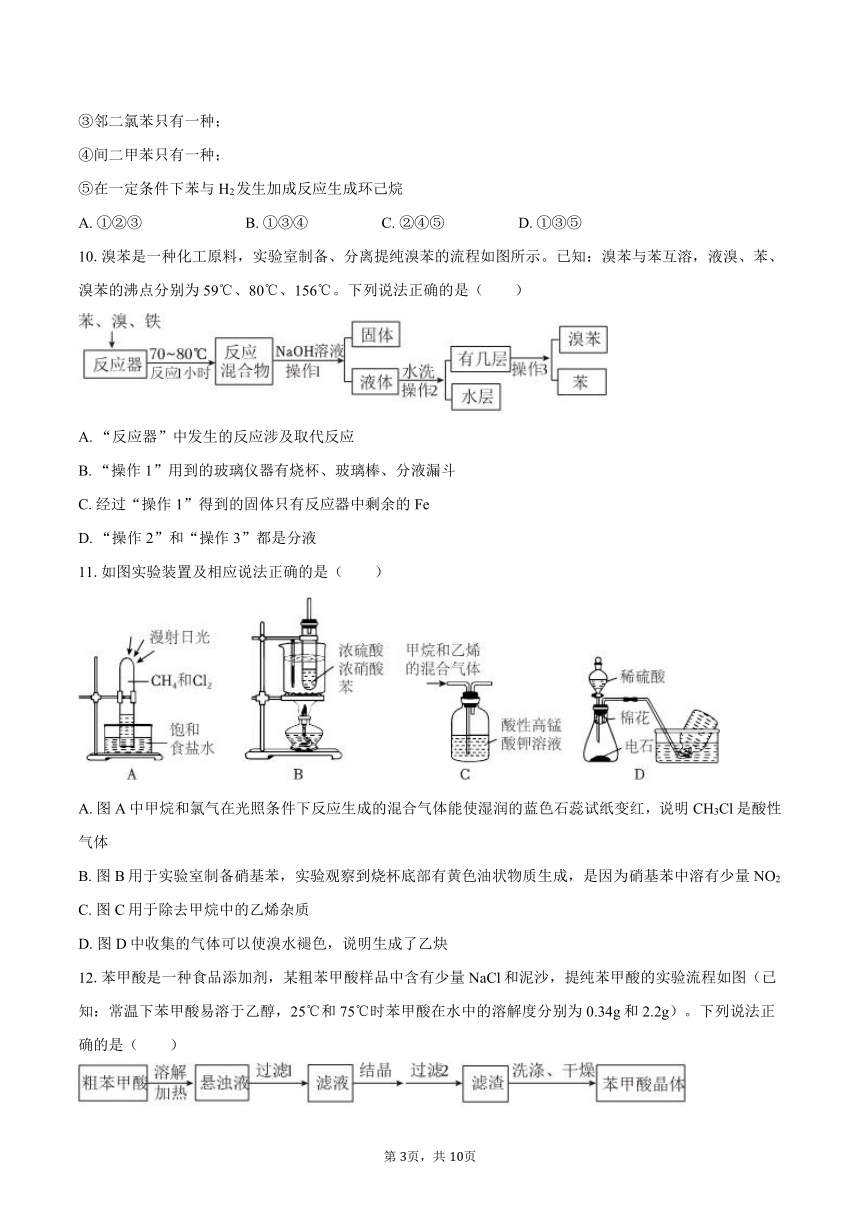
7.某烃的结构简式如图所示,若分子中共线碳原子数为a,可能共面的碳原子最多为b,含四面体结构碳原子数为c,则a、b、c分别是( )
A. 3,14,5 B. 4,10,2 C. 3,14,4 D. 3,10,3
8.下列实验操作对应的实验现象及解释或结论都正确的是( )
选项 实验操作 实验现象 解释或结论
A 浓度均为0.1mol/L的NaHCO3溶液和NaHSO3溶液中滴加几滴酚酞试剂 前者溶液变浅红色,后者不变色 NaHCO3水解,而NaHSO3不水解
B 将苯和液溴反应后的气体直接通入硝酸酸化的AgNO3溶液中 产生淡黄色沉淀 反应生成了HBr
C 向2支均盛有2mL0.1mol/L的NaOH溶液的试管中,分别加入2滴浓度均为0.1mol/L的AlCl3和FeCl3溶液 一支试管无明显现象,另一支出现红褐色沉淀 Ksp[Fe(OH)3]<Ksp[Al(OH)3]
D 向两支分别盛有2mL苯和2mL甲苯的试管中各加入几滴酸性高锰酸钾溶液,用力振荡 后者振荡后褪色 侧链受苯环影响,易被氧化
A. A B. B C. C D. D
9.能说明苯分子的碳碳键不是单双键交替的事实是( )
①苯不能使酸性KMnO4溶液褪色;
②苯环的构型是正六边形,碳碳键的键长都相等;
③邻二氯苯只有一种;
④间二甲苯只有一种;
⑤在一定条件下苯与H2发生加成反应生成环己烷
A. ①②③ B. ①③④ C. ②④⑤ D. ①③⑤
10.溴苯是一种化工原料,实验室制备、分离提纯溴苯的流程如图所示。已知:溴苯与苯互溶,液溴、苯、溴苯的沸点分别为59℃、80℃、156℃。下列说法正确的是( )
A. “反应器”中发生的反应涉及取代反应
B. “操作1”用到的玻璃仪器有烧杯、玻璃棒、分液漏斗
C. 经过“操作1”得到的固体只有反应器中剩余的Fe
D. “操作2”和“操作3”都是分液
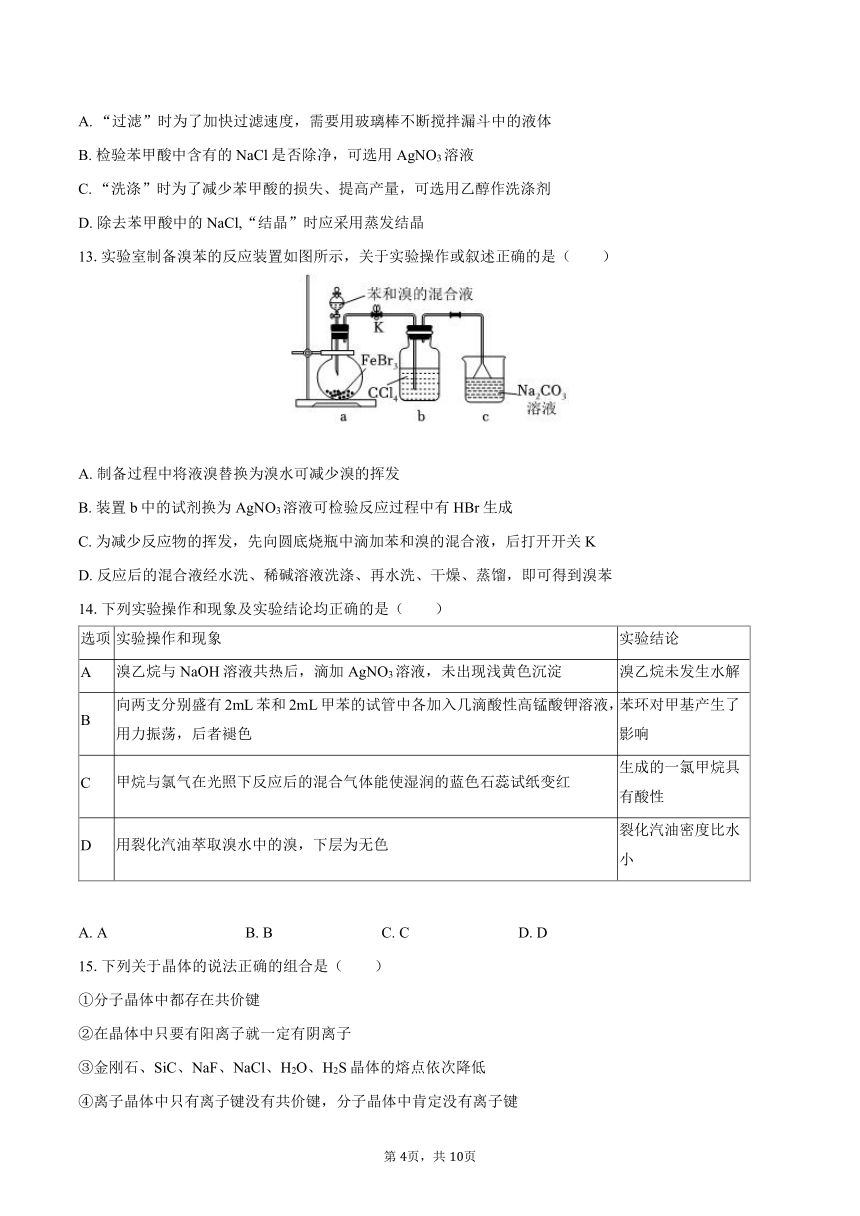
11.如图实验装置及相应说法正确的是( )
A. 图A中甲烷和氯气在光照条件下反应生成的混合气体能使湿润的蓝色石蕊试纸变红,说明CH3Cl是酸性气体
B. 图B用于实验室制备硝基苯,实验观察到烧杯底部有黄色油状物质生成,是因为硝基苯中溶有少量NO2
C. 图C用于除去甲烷中的乙烯杂质
D. 图D中收集的气体可以使溴水褪色,说明生成了乙炔
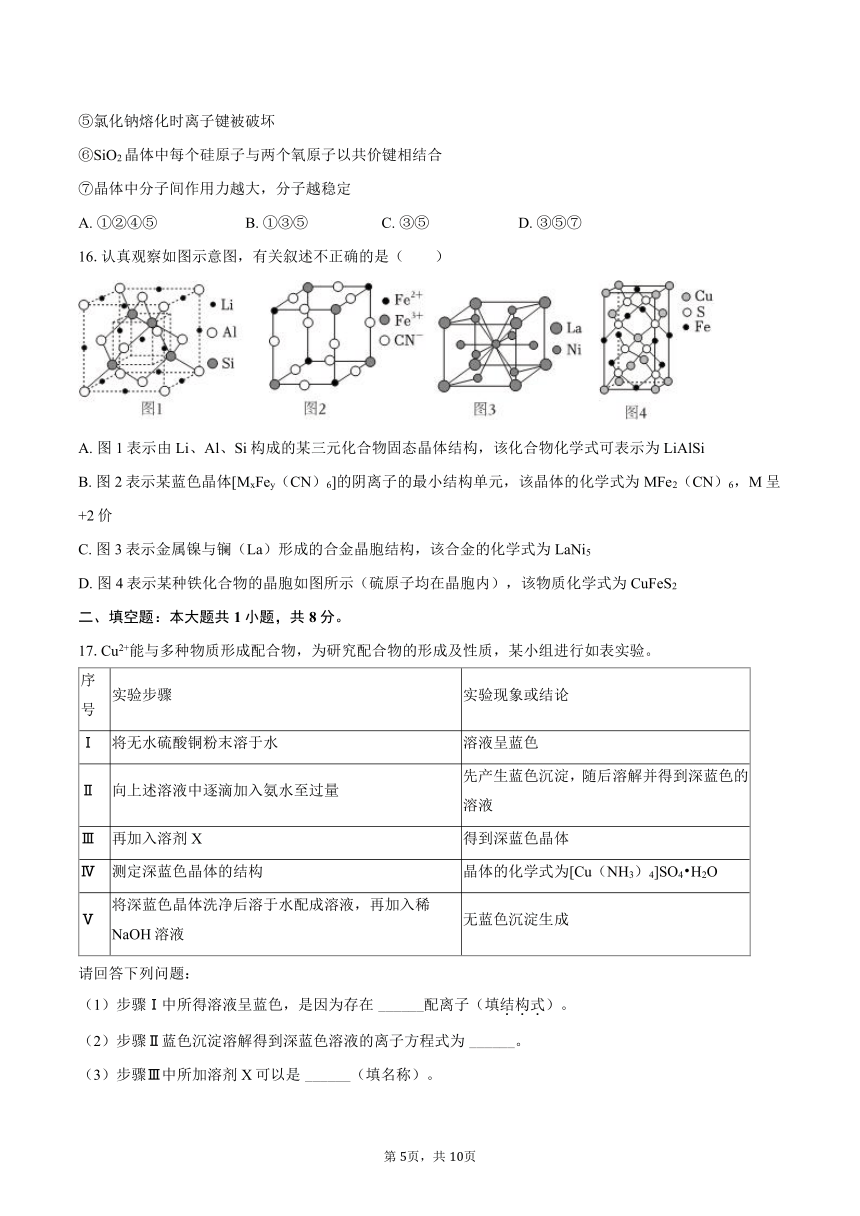
12.苯甲酸是一种食品添加剂,某粗苯甲酸样品中含有少量NaCl和泥沙,提纯苯甲酸的实验流程如图(已知:常温下苯甲酸易溶于乙醇,25℃和75℃时苯甲酸在水中的溶解度分别为0.34g和2.2g)。下列说法正确的是( )
A. “过滤”时为了加快过滤速度,需要用玻璃棒不断搅拌漏斗中的液体
B. 检验苯甲酸中含有的NaCl是否除净,可选用AgNO3溶液
C. “洗涤”时为了减少苯甲酸的损失、提高产量,可选用乙醇作洗涤剂
D. 除去苯甲酸中的NaCl,“结晶”时应采用蒸发结晶
13.实验室制备溴苯的反应装置如图所示,关于实验操作或叙述正确的是( )
A. 制备过程中将液溴替换为溴水可减少溴的挥发
B. 装置b中的试剂换为AgNO3溶液可检验反应过程中有HBr生成
C. 为减少反应物的挥发,先向圆底烧瓶中滴加苯和溴的混合液,后打开开关K
D. 反应后的混合液经水洗、稀碱溶液洗涤、再水洗、干燥、蒸馏,即可得到溴苯
14.下列实验操作和现象及实验结论均正确的是( )
选项 实验操作和现象 实验结论
A 溴乙烷与NaOH溶液共热后,滴加AgNO3溶液,未出现浅黄色沉淀 溴乙烷未发生水解
B 向两支分别盛有2mL苯和2mL甲苯的试管中各加入几滴酸性高锰酸钾溶液,用力振荡,后者褪色 苯环对甲基产生了影响
C 甲烷与氯气在光照下反应后的混合气体能使湿润的蓝色石蕊试纸变红 生成的一氯甲烷具有酸性
D 用裂化汽油萃取溴水中的溴,下层为无色 裂化汽油密度比水小
A. A B. B C. C D. D
15.下列关于晶体的说法正确的组合是( )
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低
④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤氯化钠熔化时离子键被破坏
⑥SiO2晶体中每个硅原子与两个氧原子以共价键相结合
⑦晶体中分子间作用力越大,分子越稳定
A. ①②④⑤ B. ①③⑤ C. ③⑤ D. ③⑤⑦
16.认真观察如图示意图,有关叙述不正确的是( )
A. 图1表示由Li、Al、Si构成的某三元化合物固态晶体结构,该化合物化学式可表示为LiAlSi
B. 图2表示某蓝色晶体[MxFey(CN)6]的阴离子的最小结构单元,该晶体的化学式为MFe2(CN)6,M呈+2价
C. 图3表示金属镍与镧(La)形成的合金晶胞结构,该合金的化学式为LaNi5
D. 图4表示某种铁化合物的晶胞如图所示(硫原子均在晶胞内),该物质化学式为CuFeS2
二、填空题:本大题共1小题,共8分。
17.Cu2+能与多种物质形成配合物,为研究配合物的形成及性质,某小组进行如表实验。
序号 实验步骤 实验现象或结论
Ⅰ 将无水硫酸铜粉末溶于水 溶液呈蓝色
Ⅱ 向上述溶液中逐滴加入氨水至过量 先产生蓝色沉淀,随后溶解并得到深蓝色的溶液
Ⅲ 再加入溶剂X 得到深蓝色晶体
Ⅳ 测定深蓝色晶体的结构 晶体的化学式为[Cu(NH3)4]SO4 H2O
Ⅴ 将深蓝色晶体洗净后溶于水配成溶液,再加入稀NaOH溶液 无蓝色沉淀生成
请回答下列问题:
(1)步骤Ⅰ中所得溶液呈蓝色,是因为存在 ______配离子(填结构式)。
(2)步骤Ⅱ蓝色沉淀溶解得到深蓝色溶液的离子方程式为 ______。
(3)步骤Ⅲ中所加溶剂X可以是 ______(填名称)。
(4)步骤Ⅳ中测定晶体结构的最常用仪器是 ______。
(5)该实验说明,Cu2+与NH3的结合能力 ______(填>、<或=)Cu2+与OH-的结合能力。
(6)NH3分子能与Co3+形成配合物[Co(NH3)5Cl]Cl2,该配合物中H—N—H键角 ______(填“>”“<”或“=”)NH3分子中的H—N—H键角。1mol[Co(NH3)5Cl]Cl2中含有的σ键数目为 ______NA。1mol[Co(NH3)5Cl]Cl2溶于水,加入足量AgNO3溶液,能得到 ______mol AgCl沉淀。
(7)Cu2+也能与乙二胺(H2NCH2CH2NH2)形成[Cu(H2NCH2CH2NH2)2]2+离子,结构如图,关于该配离子的说法错误的是 ______。
A.该离子的配位数是4
B.该离子的配体数是2
C.形成配离子前后,Cu的化合价不变
D.该离子中含有离子键、非极性键与极性键
三、实验题:本大题共2小题,共20分。
18.以乙炔为原料合成聚苯乙烯{}的路线如图。请根据所学知识回答下列问题:
(1)乙炔为 ______(填“极性”或“非极性”)分子。
(2)实验室制备乙炔并检验其性质的装置如图。
①盛有饱和食盐水的仪器名称为 ______;该实验开始前应先进行的操作为 ______。
②B装置中的现象为 ______。
③C装置中的现象为 ______,发生的反应类型为 ______反应。
④D装置中发生反应的化学方程式为 ______(反应中、HC≡CH→(CO2),反应中乙炔表现出的性质为 ______。
(3)写出合成路线中反应③的化学方程式:______。
(4)合成路线中,符合原子经济性的反应为 ______(填标号)。
19.某化学课外小组用如图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
(1)写出A中反应的化学方程式:______。
(2)观察到A中的现象是 ______。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是 ______。写出有关反应的化学方程式:______。
(4)C中盛放CCl4的作用是 ______。
(5)为证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入稀硝酸酸化的AgNO3溶液,若产生浅黄色沉淀,则能证明。另一种验证的方法是向试管D中加入 ______,现象是 ______。
四、简答题:本大题共1小题,共8分。
20.回答下列问题:
Ⅰ.烷烃可以发生取代反应。如图所示,用强光照射硬质玻璃管。
(1)B装置有三种功能:①混匀混合气体;②控制气流速度;③______。
(2)写出装置C中CH2Cl2与Cl2反应生成氯仿的化学方程式 ______。
(3)一段时间后,C中玻璃管内的实验现象:______、______。
(4)若1.6molCH4与Cl2在光照条件下发生取代反应,CH4全部消耗完,测得生成CH3Cl、CH2Cl2、CHCl3和CCl4的物质的量之比为1:3:5:7,则消耗的氯气的物质的量是 ______mol。
Ⅱ.从下列各组物质中,找出合适的序号填在对应的空格内:
①16O和18O
②O2和O3
③NO2和N2O4
④H2O和D2O
⑤和
⑥CH3CH2CH3和CH3C(CH3)3
⑦CH2=CHCH3和CH2=CHCH2CH3
⑧和
⑨和CH3(CH2)3CH3
⑩和
(5)互为同素异形体的是 ______(填序号,下同)。
(6)互为同分异构体的是 ______。
(7)互为同系物的是 ______。
1.【答案】D
2.【答案】A
3.【答案】D
4.【答案】C
5.【答案】D
6.【答案】D
7.【答案】C
8.【答案】D
9.【答案】A
10.【答案】A
11.【答案】B
12.【答案】B
13.【答案】D
14.【答案】B
15.【答案】C
16.【答案】B
17.【答案】;
Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-;
乙醇;
X射线衍射仪;
>;
①>;
②21;
③2;
D
18.【答案】非极性;
①分液漏斗;检验装置的气密性;
②产生黑色沉淀;
③溶液褪色;加成反应;
④CH≡CH+2KMnO4+3H2SO4=K2SO4+2MnSO4+2CO2+4H2O;还原性;
CH2=CHCl++HCl;
①②④
19.【答案】2Fe+3Br2=2FeBr3、+Br2+HBr↑;
反应液微沸,有红棕色气体充满A容器;
除去溶于溴苯中的溴;Br2+2NaOH=NaBr+NaBrO+H2O;
除去溴化氢气体中的溴蒸气;
紫色石蕊溶液;溶液变红色(其他合理答案亦可)
20.【答案】干燥甲烷和氯气;
CH2Cl2+Cl2CHCl3+HCl;
玻璃管内壁上出现黄绿色油状液滴;玻璃管内黄绿色变浅;
5;
②;
⑨⑩;
⑥⑦
第1页,共1页
一、单选题:本大题共16小题,共48分。
1.下列有关化学用语表示不正确的是( )
A. 钠原子2Px电子云图: B. NH3的 VSEPR模型:
C. 乙酸甲酯的结构简式CH3OOCCH3 D. HCHO 的电子式:
2.下列有关物质结构与性质的比较正确的是( )
A. 沸点:PH3<NH3 B. 酸性:CH2ClCOOH>CH2FCOOH
C. 键角: D. 热稳定性:HCl>HF
3.下列叙述不正确的是( )
A. 第一电离能:N>O B. 酸性:CH2BrCOOH<CH2ClCOOH
C. 电负性:S>Se D. 键长:C=C>C—C
4.A、B、C、D、E为原子序数依次增大的前四周期元素。A是半径最小的元素,B的价电子层中有3个未成对电子;C与D同主族;E的最外层只有1个电子,但次外层有18个电子。五种元素形成的离子化合物可表示为[E(BA3)4(A2C)2]2+[DC4]2-。下列说法错误的是( )
A. [E(BA3)4(A2C)2]2+[DC4]2-中含有σ键数目为26
B. 呈正四面体形
C. 该化合物受热分解时首先失去的是BA3
D. A与B、C均可形成含有非极性共价键的化合物
5.下列实验装置或操作正确的是( )
A. 图1是排出碱式滴定管中的气泡操作
B. 图2装置可以测定化学反应速率
C. 图3装置可以分离二氯甲烷、三氯甲烷和四氯化碳的混合物
D. 图4装置用CCl4萃取碘水中的碘
6.人工合成某信息素分子的结构简式如下图所示,它是昆虫之间传递信号的一种化学物质,能诱捕害虫等。下列有关说法正确的是( )
A. 含有醚键 B. 所有碳原子可能共面
C. α碳原子属于手性碳 D. β碳原子为sp2杂化
7.某烃的结构简式如图所示,若分子中共线碳原子数为a,可能共面的碳原子最多为b,含四面体结构碳原子数为c,则a、b、c分别是( )
A. 3,14,5 B. 4,10,2 C. 3,14,4 D. 3,10,3
8.下列实验操作对应的实验现象及解释或结论都正确的是( )
选项 实验操作 实验现象 解释或结论
A 浓度均为0.1mol/L的NaHCO3溶液和NaHSO3溶液中滴加几滴酚酞试剂 前者溶液变浅红色,后者不变色 NaHCO3水解,而NaHSO3不水解
B 将苯和液溴反应后的气体直接通入硝酸酸化的AgNO3溶液中 产生淡黄色沉淀 反应生成了HBr
C 向2支均盛有2mL0.1mol/L的NaOH溶液的试管中,分别加入2滴浓度均为0.1mol/L的AlCl3和FeCl3溶液 一支试管无明显现象,另一支出现红褐色沉淀 Ksp[Fe(OH)3]<Ksp[Al(OH)3]
D 向两支分别盛有2mL苯和2mL甲苯的试管中各加入几滴酸性高锰酸钾溶液,用力振荡 后者振荡后褪色 侧链受苯环影响,易被氧化
A. A B. B C. C D. D
9.能说明苯分子的碳碳键不是单双键交替的事实是( )
①苯不能使酸性KMnO4溶液褪色;
②苯环的构型是正六边形,碳碳键的键长都相等;
③邻二氯苯只有一种;
④间二甲苯只有一种;
⑤在一定条件下苯与H2发生加成反应生成环己烷
A. ①②③ B. ①③④ C. ②④⑤ D. ①③⑤
10.溴苯是一种化工原料,实验室制备、分离提纯溴苯的流程如图所示。已知:溴苯与苯互溶,液溴、苯、溴苯的沸点分别为59℃、80℃、156℃。下列说法正确的是( )
A. “反应器”中发生的反应涉及取代反应
B. “操作1”用到的玻璃仪器有烧杯、玻璃棒、分液漏斗
C. 经过“操作1”得到的固体只有反应器中剩余的Fe
D. “操作2”和“操作3”都是分液
11.如图实验装置及相应说法正确的是( )
A. 图A中甲烷和氯气在光照条件下反应生成的混合气体能使湿润的蓝色石蕊试纸变红,说明CH3Cl是酸性气体
B. 图B用于实验室制备硝基苯,实验观察到烧杯底部有黄色油状物质生成,是因为硝基苯中溶有少量NO2
C. 图C用于除去甲烷中的乙烯杂质
D. 图D中收集的气体可以使溴水褪色,说明生成了乙炔
12.苯甲酸是一种食品添加剂,某粗苯甲酸样品中含有少量NaCl和泥沙,提纯苯甲酸的实验流程如图(已知:常温下苯甲酸易溶于乙醇,25℃和75℃时苯甲酸在水中的溶解度分别为0.34g和2.2g)。下列说法正确的是( )
A. “过滤”时为了加快过滤速度,需要用玻璃棒不断搅拌漏斗中的液体
B. 检验苯甲酸中含有的NaCl是否除净,可选用AgNO3溶液
C. “洗涤”时为了减少苯甲酸的损失、提高产量,可选用乙醇作洗涤剂
D. 除去苯甲酸中的NaCl,“结晶”时应采用蒸发结晶
13.实验室制备溴苯的反应装置如图所示,关于实验操作或叙述正确的是( )
A. 制备过程中将液溴替换为溴水可减少溴的挥发
B. 装置b中的试剂换为AgNO3溶液可检验反应过程中有HBr生成
C. 为减少反应物的挥发,先向圆底烧瓶中滴加苯和溴的混合液,后打开开关K
D. 反应后的混合液经水洗、稀碱溶液洗涤、再水洗、干燥、蒸馏,即可得到溴苯
14.下列实验操作和现象及实验结论均正确的是( )
选项 实验操作和现象 实验结论
A 溴乙烷与NaOH溶液共热后,滴加AgNO3溶液,未出现浅黄色沉淀 溴乙烷未发生水解
B 向两支分别盛有2mL苯和2mL甲苯的试管中各加入几滴酸性高锰酸钾溶液,用力振荡,后者褪色 苯环对甲基产生了影响
C 甲烷与氯气在光照下反应后的混合气体能使湿润的蓝色石蕊试纸变红 生成的一氯甲烷具有酸性
D 用裂化汽油萃取溴水中的溴,下层为无色 裂化汽油密度比水小
A. A B. B C. C D. D
15.下列关于晶体的说法正确的组合是( )
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低
④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤氯化钠熔化时离子键被破坏
⑥SiO2晶体中每个硅原子与两个氧原子以共价键相结合
⑦晶体中分子间作用力越大,分子越稳定
A. ①②④⑤ B. ①③⑤ C. ③⑤ D. ③⑤⑦
16.认真观察如图示意图,有关叙述不正确的是( )
A. 图1表示由Li、Al、Si构成的某三元化合物固态晶体结构,该化合物化学式可表示为LiAlSi
B. 图2表示某蓝色晶体[MxFey(CN)6]的阴离子的最小结构单元,该晶体的化学式为MFe2(CN)6,M呈+2价
C. 图3表示金属镍与镧(La)形成的合金晶胞结构,该合金的化学式为LaNi5
D. 图4表示某种铁化合物的晶胞如图所示(硫原子均在晶胞内),该物质化学式为CuFeS2
二、填空题:本大题共1小题,共8分。
17.Cu2+能与多种物质形成配合物,为研究配合物的形成及性质,某小组进行如表实验。
序号 实验步骤 实验现象或结论
Ⅰ 将无水硫酸铜粉末溶于水 溶液呈蓝色
Ⅱ 向上述溶液中逐滴加入氨水至过量 先产生蓝色沉淀,随后溶解并得到深蓝色的溶液
Ⅲ 再加入溶剂X 得到深蓝色晶体
Ⅳ 测定深蓝色晶体的结构 晶体的化学式为[Cu(NH3)4]SO4 H2O
Ⅴ 将深蓝色晶体洗净后溶于水配成溶液,再加入稀NaOH溶液 无蓝色沉淀生成
请回答下列问题:
(1)步骤Ⅰ中所得溶液呈蓝色,是因为存在 ______配离子(填结构式)。
(2)步骤Ⅱ蓝色沉淀溶解得到深蓝色溶液的离子方程式为 ______。
(3)步骤Ⅲ中所加溶剂X可以是 ______(填名称)。
(4)步骤Ⅳ中测定晶体结构的最常用仪器是 ______。
(5)该实验说明,Cu2+与NH3的结合能力 ______(填>、<或=)Cu2+与OH-的结合能力。
(6)NH3分子能与Co3+形成配合物[Co(NH3)5Cl]Cl2,该配合物中H—N—H键角 ______(填“>”“<”或“=”)NH3分子中的H—N—H键角。1mol[Co(NH3)5Cl]Cl2中含有的σ键数目为 ______NA。1mol[Co(NH3)5Cl]Cl2溶于水,加入足量AgNO3溶液,能得到 ______mol AgCl沉淀。
(7)Cu2+也能与乙二胺(H2NCH2CH2NH2)形成[Cu(H2NCH2CH2NH2)2]2+离子,结构如图,关于该配离子的说法错误的是 ______。
A.该离子的配位数是4
B.该离子的配体数是2
C.形成配离子前后,Cu的化合价不变
D.该离子中含有离子键、非极性键与极性键
三、实验题:本大题共2小题,共20分。
18.以乙炔为原料合成聚苯乙烯{}的路线如图。请根据所学知识回答下列问题:
(1)乙炔为 ______(填“极性”或“非极性”)分子。
(2)实验室制备乙炔并检验其性质的装置如图。
①盛有饱和食盐水的仪器名称为 ______;该实验开始前应先进行的操作为 ______。
②B装置中的现象为 ______。
③C装置中的现象为 ______,发生的反应类型为 ______反应。
④D装置中发生反应的化学方程式为 ______(反应中、HC≡CH→(CO2),反应中乙炔表现出的性质为 ______。
(3)写出合成路线中反应③的化学方程式:______。
(4)合成路线中,符合原子经济性的反应为 ______(填标号)。
19.某化学课外小组用如图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
(1)写出A中反应的化学方程式:______。
(2)观察到A中的现象是 ______。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是 ______。写出有关反应的化学方程式:______。
(4)C中盛放CCl4的作用是 ______。
(5)为证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入稀硝酸酸化的AgNO3溶液,若产生浅黄色沉淀,则能证明。另一种验证的方法是向试管D中加入 ______,现象是 ______。
四、简答题:本大题共1小题,共8分。
20.回答下列问题:
Ⅰ.烷烃可以发生取代反应。如图所示,用强光照射硬质玻璃管。
(1)B装置有三种功能:①混匀混合气体;②控制气流速度;③______。
(2)写出装置C中CH2Cl2与Cl2反应生成氯仿的化学方程式 ______。
(3)一段时间后,C中玻璃管内的实验现象:______、______。
(4)若1.6molCH4与Cl2在光照条件下发生取代反应,CH4全部消耗完,测得生成CH3Cl、CH2Cl2、CHCl3和CCl4的物质的量之比为1:3:5:7,则消耗的氯气的物质的量是 ______mol。
Ⅱ.从下列各组物质中,找出合适的序号填在对应的空格内:
①16O和18O
②O2和O3
③NO2和N2O4
④H2O和D2O
⑤和
⑥CH3CH2CH3和CH3C(CH3)3
⑦CH2=CHCH3和CH2=CHCH2CH3
⑧和
⑨和CH3(CH2)3CH3
⑩和
(5)互为同素异形体的是 ______(填序号,下同)。
(6)互为同分异构体的是 ______。
(7)互为同系物的是 ______。
1.【答案】D
2.【答案】A
3.【答案】D
4.【答案】C
5.【答案】D
6.【答案】D
7.【答案】C
8.【答案】D
9.【答案】A
10.【答案】A
11.【答案】B
12.【答案】B
13.【答案】D
14.【答案】B
15.【答案】C
16.【答案】B
17.【答案】;
Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-;
乙醇;
X射线衍射仪;
>;
①>;
②21;
③2;
D
18.【答案】非极性;
①分液漏斗;检验装置的气密性;
②产生黑色沉淀;
③溶液褪色;加成反应;
④CH≡CH+2KMnO4+3H2SO4=K2SO4+2MnSO4+2CO2+4H2O;还原性;
CH2=CHCl++HCl;
①②④
19.【答案】2Fe+3Br2=2FeBr3、+Br2+HBr↑;
反应液微沸,有红棕色气体充满A容器;
除去溶于溴苯中的溴;Br2+2NaOH=NaBr+NaBrO+H2O;
除去溴化氢气体中的溴蒸气;
紫色石蕊溶液;溶液变红色(其他合理答案亦可)
20.【答案】干燥甲烷和氯气;
CH2Cl2+Cl2CHCl3+HCl;
玻璃管内壁上出现黄绿色油状液滴;玻璃管内黄绿色变浅;
5;
②;
⑨⑩;
⑥⑦
第1页,共1页
同课章节目录
