2.2 金属的化学性质
图片预览








文档简介
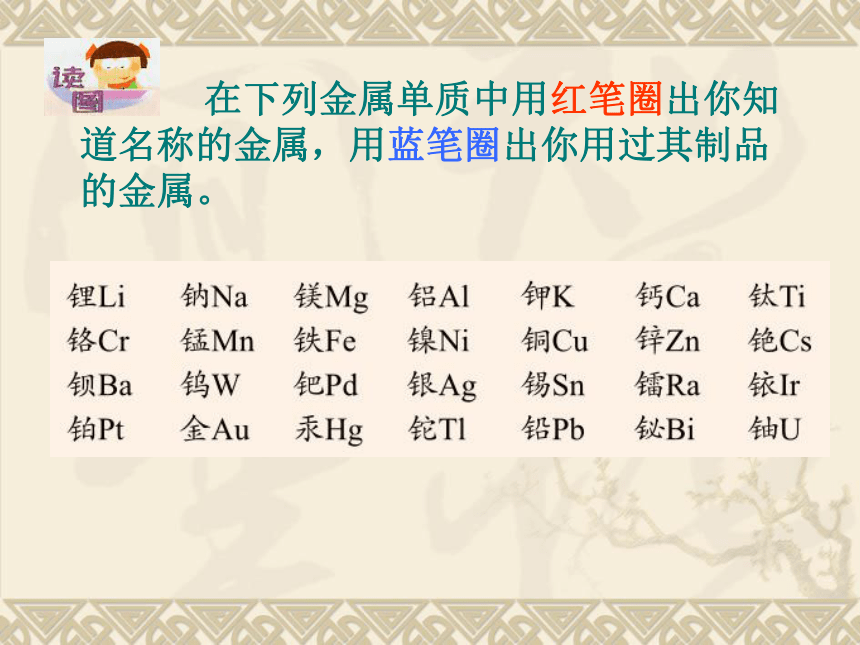
课件28张PPT。第2节 金属的化学性质 在下列金属单质中用红笔圈出你知道名称的金属,用蓝笔圈出你用过其制品的金属。钯钡铂铬水银镭锂锰镍铯铊钛了解:金属的化学性质1、将一根镁带、一根铜丝同时在酒精灯的外焰上加热,哪根金属先在空气中燃烧?________。不燃烧的那根金属冷却后表面的颜色发生了什么变化?____________。
2、将不燃烧的那根金属插入盛有盐酸的试管中,观察现象。镁逐渐变黑没有明显的现象变化金属和氧气的反应金属铁在潮湿的空气中会被氧气所氧化而生锈(铁锈的主要成分是Fe2O3)。 将铝片放入盛有稀盐酸的试管中,观察并记录现象:大量的气泡产生2Al + 6HCl = 2AlCl3 + 3H2↑是否所有的金属都能被酸腐蚀?不会的,如金、银很难被腐蚀。金属和酸的反应金属和酸的反应1、取少量镁条、锌粒、铜片分别放入盛有稀盐酸的3支试管中,观察现象:
Mg + 2HCl = MgCl2 + H2↑
Zn + 2HCl = ZnCl2 + H2↑ 镁、锌的试管中有大量的气泡产生,镁反应更剧烈;铜片则没有任何变化。2、用拇指按住盛有锌粒和稀盐酸的试管口,将燃着的火柴接近试管口,发现__________,此气体应是________。有爆鸣声氢气 根据刚才实验比较镁、锌、铜的活动性,并从大到小列出镁、锌、铜的活动性顺序。如果把氢也列入其中,应如何排列?Mg>Zn>H>Cu金属和酸的反应3、取少量镁条、锌粒、铜片分别放入盛有稀硫酸的3支试管中,观察现象:________。试验产生的气体。同1Mg + H2SO4 = MgSO4 + H2↑
Zn + H2SO4 = ZnSO4 + H2↑4、跟稀盐酸、稀硫酸不发生反应的金属是_______。铜 上述反应与前面学过的化合、分解、复分解反应有什么不同?Mg + 2HCl = MgCl2 + H2↑
Zn + 2HCl = ZnCl2 + H2↑
Mg + H2SO4 = MgSO4 + H2↑
Zn + H2SO4 = ZnSO4 + H2↑单质化合物单质化合物像这类由一种单质跟一种化合物起反应生成另一种单质和另一种化合物的反应叫做置换反应+=+金属跟盐反应1、在盛有硫酸铜溶液的试管里浸入一段洁净的(经过除油、除锈)铁丝,过一会儿取出,观察有什么变化。____________________________。铁丝的表面覆盖一层红色物质2、在盛有硫酸亚铁溶液的试管中,浸入一段洁净的铜丝,过一会儿取出,观察有什么变化。________________________。现象没有明显的变化Fe + CuSO4 = FeSO4 + Cu
Cu+ FeSO4 ≠∴金属活动性: Fe>Cu 在盛有硝酸银溶液和硫酸锌溶液的试管中,分别浸入一段洁净的铜丝,过一会儿取出,观察有什么变化。在硝酸银溶液中,铜丝表面覆盖一层银白色物质;在硫酸锌溶液中,现象没有明显变化。Cu + 2AgNO3 = Cu(NO3)2 + 2Ag
Cu + ZnSO4 ≠∴金属活动性: Zn>Cu >Ag应用:金属活动性的应用:1、一种活动性较强的金属能把另一种活动性较弱的金属从它的盐的水溶液中置换出来。
金属 + 可溶性的盐 = 金属 + 盐2、排在氢前面的金属可以把酸里的氢置换出来,排在氢后面的金属不能。
金属 + 酸 = 盐 + 氢气Al + FeSO4 =Al + H2SO4 = 用不活泼的金属制造货币,可以防止生锈、被腐蚀等。不能,因为锡能跟酸反应。
Sn + 2HCl = SnCl2 + H2↑不能,铁能跟波尔多液反应。
Fe + CuSO4 = FeSO4 + Cu湿法炼铜湿法炼铜化学反应中的电子转移问题: 你能说出金属有哪些缺点吗?易锈蚀是许多金属的共同弊端。 随着科学技术的不断进步,人类对于钢铁的需求量也在不断的增大,我国是钢铁生产大国,钢铁工人不断的制造出一些性能优良的钢材。但是,根据一些数据统计,每年由于锈蚀而浪费掉的钢铁材料仍占每年钢铁产量的1/4,因此给国家带来了较为严重的经济损失。
你知道钢铁产生锈蚀的原因是什么吗?实验:金属锈蚀的条件有哪些?如何用实验验证?(外/内 条件)2.提供的器材:带塞子的试管若干支,普通铁片若干,蒸馏水,干燥剂。1.分析各种猜测的可能性。锈蚀的条件有:空气、水3.根据所提供的器材,设计实验方案,以验证锈蚀的条件,并画出装置图A:普通铁片,水、空气
B:普通铁片,空气。(内有干燥剂)
C:普通铁片,蒸馏水。(无空气)4. 比较( B与A ,C 与A ):铁锈蚀的外部条件是:
______________________。同时具备空气和水。5、利用纯铁(D)按上述方案进行实验,纯铁生锈了吗,为什么?6. 比较( D与A ):铁锈蚀的内部条件是:
______________________。与内部结构有关讨论:根据金属锈蚀的条件,讨论金属防护的常用方法?
调查生活中常用的金属防腐蚀的措施。1、保护膜法:(外部措施)油漆、搪瓷、金属镀层、氧化膜法2、改变金属内部结构法:(内部措施)1.金属的生锈的原因:1) 与周围环境中的水和空气等物质的 作用有关 。2) 与金属内部的结构有关。金属生锈与防锈2.金属的防锈的方法:1)保护膜法:2)改变金属内部结构法:
2、将不燃烧的那根金属插入盛有盐酸的试管中,观察现象。镁逐渐变黑没有明显的现象变化金属和氧气的反应金属铁在潮湿的空气中会被氧气所氧化而生锈(铁锈的主要成分是Fe2O3)。 将铝片放入盛有稀盐酸的试管中,观察并记录现象:大量的气泡产生2Al + 6HCl = 2AlCl3 + 3H2↑是否所有的金属都能被酸腐蚀?不会的,如金、银很难被腐蚀。金属和酸的反应金属和酸的反应1、取少量镁条、锌粒、铜片分别放入盛有稀盐酸的3支试管中,观察现象:
Mg + 2HCl = MgCl2 + H2↑
Zn + 2HCl = ZnCl2 + H2↑ 镁、锌的试管中有大量的气泡产生,镁反应更剧烈;铜片则没有任何变化。2、用拇指按住盛有锌粒和稀盐酸的试管口,将燃着的火柴接近试管口,发现__________,此气体应是________。有爆鸣声氢气 根据刚才实验比较镁、锌、铜的活动性,并从大到小列出镁、锌、铜的活动性顺序。如果把氢也列入其中,应如何排列?Mg>Zn>H>Cu金属和酸的反应3、取少量镁条、锌粒、铜片分别放入盛有稀硫酸的3支试管中,观察现象:________。试验产生的气体。同1Mg + H2SO4 = MgSO4 + H2↑
Zn + H2SO4 = ZnSO4 + H2↑4、跟稀盐酸、稀硫酸不发生反应的金属是_______。铜 上述反应与前面学过的化合、分解、复分解反应有什么不同?Mg + 2HCl = MgCl2 + H2↑
Zn + 2HCl = ZnCl2 + H2↑
Mg + H2SO4 = MgSO4 + H2↑
Zn + H2SO4 = ZnSO4 + H2↑单质化合物单质化合物像这类由一种单质跟一种化合物起反应生成另一种单质和另一种化合物的反应叫做置换反应+=+金属跟盐反应1、在盛有硫酸铜溶液的试管里浸入一段洁净的(经过除油、除锈)铁丝,过一会儿取出,观察有什么变化。____________________________。铁丝的表面覆盖一层红色物质2、在盛有硫酸亚铁溶液的试管中,浸入一段洁净的铜丝,过一会儿取出,观察有什么变化。________________________。现象没有明显的变化Fe + CuSO4 = FeSO4 + Cu
Cu+ FeSO4 ≠∴金属活动性: Fe>Cu 在盛有硝酸银溶液和硫酸锌溶液的试管中,分别浸入一段洁净的铜丝,过一会儿取出,观察有什么变化。在硝酸银溶液中,铜丝表面覆盖一层银白色物质;在硫酸锌溶液中,现象没有明显变化。Cu + 2AgNO3 = Cu(NO3)2 + 2Ag
Cu + ZnSO4 ≠∴金属活动性: Zn>Cu >Ag应用:金属活动性的应用:1、一种活动性较强的金属能把另一种活动性较弱的金属从它的盐的水溶液中置换出来。
金属 + 可溶性的盐 = 金属 + 盐2、排在氢前面的金属可以把酸里的氢置换出来,排在氢后面的金属不能。
金属 + 酸 = 盐 + 氢气Al + FeSO4 =Al + H2SO4 = 用不活泼的金属制造货币,可以防止生锈、被腐蚀等。不能,因为锡能跟酸反应。
Sn + 2HCl = SnCl2 + H2↑不能,铁能跟波尔多液反应。
Fe + CuSO4 = FeSO4 + Cu湿法炼铜湿法炼铜化学反应中的电子转移问题: 你能说出金属有哪些缺点吗?易锈蚀是许多金属的共同弊端。 随着科学技术的不断进步,人类对于钢铁的需求量也在不断的增大,我国是钢铁生产大国,钢铁工人不断的制造出一些性能优良的钢材。但是,根据一些数据统计,每年由于锈蚀而浪费掉的钢铁材料仍占每年钢铁产量的1/4,因此给国家带来了较为严重的经济损失。
你知道钢铁产生锈蚀的原因是什么吗?实验:金属锈蚀的条件有哪些?如何用实验验证?(外/内 条件)2.提供的器材:带塞子的试管若干支,普通铁片若干,蒸馏水,干燥剂。1.分析各种猜测的可能性。锈蚀的条件有:空气、水3.根据所提供的器材,设计实验方案,以验证锈蚀的条件,并画出装置图A:普通铁片,水、空气
B:普通铁片,空气。(内有干燥剂)
C:普通铁片,蒸馏水。(无空气)4. 比较( B与A ,C 与A ):铁锈蚀的外部条件是:
______________________。同时具备空气和水。5、利用纯铁(D)按上述方案进行实验,纯铁生锈了吗,为什么?6. 比较( D与A ):铁锈蚀的内部条件是:
______________________。与内部结构有关讨论:根据金属锈蚀的条件,讨论金属防护的常用方法?
调查生活中常用的金属防腐蚀的措施。1、保护膜法:(外部措施)油漆、搪瓷、金属镀层、氧化膜法2、改变金属内部结构法:(内部措施)1.金属的生锈的原因:1) 与周围环境中的水和空气等物质的 作用有关 。2) 与金属内部的结构有关。金属生锈与防锈2.金属的防锈的方法:1)保护膜法:2)改变金属内部结构法:
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
