吉林省白山市五校2024-2025学年高二下学期期末联考化学试卷(含答案)
文档属性
| 名称 | 吉林省白山市五校2024-2025学年高二下学期期末联考化学试卷(含答案) | 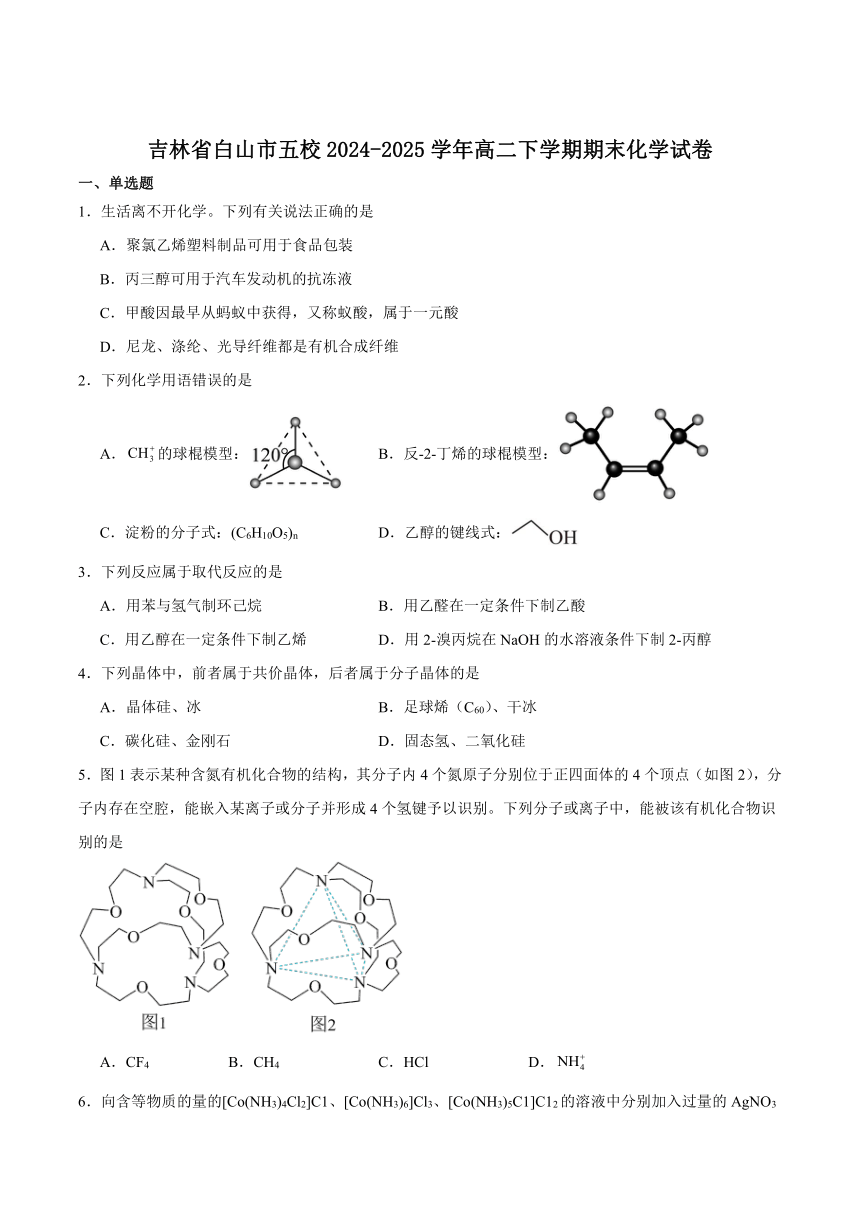 | |
| 格式 | docx | ||
| 文件大小 | 964.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-22 21:24:55 | ||
图片预览





文档简介
吉林省白山市五校2024-2025学年高二下学期期末化学试卷
一、单选题
1.生活离不开化学。下列有关说法正确的是
A.聚氯乙烯塑料制品可用于食品包装
B.丙三醇可用于汽车发动机的抗冻液
C.甲酸因最早从蚂蚁中获得,又称蚁酸,属于一元酸
D.尼龙、涤纶、光导纤维都是有机合成纤维
2.下列化学用语错误的是
A.的球棍模型: B.反-2-丁烯的球棍模型:
C.淀粉的分子式:(C6H10O5)n D.乙醇的键线式:
3.下列反应属于取代反应的是
A.用苯与氢气制环己烷 B.用乙醛在一定条件下制乙酸
C.用乙醇在一定条件下制乙烯 D.用2-溴丙烷在NaOH的水溶液条件下制2-丙醇
4.下列晶体中,前者属于共价晶体,后者属于分子晶体的是
A.晶体硅、冰 B.足球烯(C60)、干冰
C.碳化硅、金刚石 D.固态氢、二氧化硅
5.图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(如图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是
A.CF4 B.CH4 C.HCl D.
6.向含等物质的量的[Co(NH3)4Cl2]C1、[Co(NH3)6]Cl3、[Co(NH3)5C1]C12的溶液中分别加入过量的AgNO3溶液,生成AgCl沉淀的质量最多的是
A.[Co(NH3)4Cl2]C1 B.[Co(NH3)6]Cl3
C.[Co(NH3)5C1]C12 D.一样多
7.香草醛是一种食品添加剂,可用愈创木酚作原料合成。
下列试剂中能鉴别愈创木酚和香草醛的是
A.NaOH溶液 B.溶液 C.浓溴水 D.银氨溶液
8.下列关于糖类、油脂和蛋白质这三大营养物质的叙述正确的是
A.糖类、油脂、蛋白质都能发生水解反应
B.淀粉和纤维素均能在人体内水解为葡萄糖
C.皮肤、指甲上不慎沾上浓硝酸会出现黄色
D.油脂在酸性条件下能发生皂化反应,生成甘油和高级脂肪酸盐
9.近年来,食品安全事故频繁发生,人们对食品添加剂的认识逐渐加深。BHT是一种常用的食品抗氧化剂,其合成方法有如下图两种。下列说法错误的是
A.BHT在水中的溶解度大于苯酚
B.与BHT均可以使酸性KMnO4溶液褪色
C.与足量溴水反应,可消耗Br2
D.方法一发生了加成反应,方法二发生了取代反应
10.乙酰水杨酸(阿司匹林)的结构如图。下列说法中错误的是
A.乙酰水杨酸可发生酯化反应和水解反应
B.乙酰水杨酸是一种烃的含氧衍生物
C.1mol乙酰水杨酸与足量H2反应,最多消耗4molH2
D.苯环上有两个羧基,一个甲基的乙酰水杨酸的同分异构体有6种
11.物质结构决定物质性质。下列关于物质的结构或性质以及解释均正确的是
选项 结构或性质 原因解释
A 键角:NH3>PH3 NH3中N的孤电子对数比PH3中P的孤电子对数多
B 沸点:H2O>HF O—H…O的键能大于F—H…F的键能
C 硬度:碳化硅>金刚石 C—Si键能大于C—C键能
D 在水中的溶解性:O3>O2 分子极性
A.A B.B C.C D.D
12.酪氨酸学名为2-氨基-3-对羟苯基丙酸,是一种生命活动不可缺少的氨基酸,其结构如图所示。下列说法正确的是
A.酪氨酸为高分子化合物
B.酪氨酸分子中含有1个手性碳原子
C.酪氨酸既能与盐酸反应又能与NaOH溶液反应,且消耗盐酸和NaOH的物质的量之比为1:1
D.1mol酪氨酸分子与足量金属Na反应可产生22.4LH2
13.下列化学实验中的操作、现象及结论都正确的是
选项 操作 现象 结论
A 向淀粉溶液中加入稀硫酸,水浴加热后,加入新制氢氧化铜,加热 得到蓝色溶液 淀粉没有水解
B 向两份相同的蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液 均有固体析出 蛋白质均发生变性
C 向肉桂醛()中加酸性KMnO4溶液,振荡 酸性KMnO4溶液褪色 肉桂醛中仅醛基可与酸性KMnO4溶液发生反应
D 将(CH3)3CCH2Cl与NaOH的乙醇溶液加热一段时间后冷却,先加入硝酸酸化,再滴入硝酸银溶液 没有白色沉淀产生 (CH3)3CCH2Cl与NaOH的乙醇溶液不能发生反应
A.A B.B C.C D.D
14.BeO晶体晶胞的结构如图所示。原子A、B的坐标分别为(0,0,0)、(,,1),O与Be的最近距离为apm,用NA表示阿伏加德罗常数的值。下列说法错误的是
A.C原子的坐标为(,,)
B.与Be距离最近且相等的Be有4个
C.该晶体的密度为
D.晶胞内由O原子构成的正八面体空隙有4个
15.聚酰胺(PA)具有良好的力学性能,一种合成路线如下图所示。下列说法错误的是
A.Y的结构简式为
B.Z生成PA的反应类型为缩聚反应
C.该合成路线中甲醇可循环使用
D.PA可发生水解反应重新生成Z
二、解答题
16.在人类文明的历程中,许多物质发挥过重要作用,如铜、硝酸钾、青霉素、聚乙烯、二氧化硅、甲醇、含硼物质等。回答下列问题:
(1)写出的结构式,并用→表示配位键: 。肼(N2H4)分子可视为NH3分子中的一个氢原子被—NH2(氨基)取代形成的一种氮的氢化物。N2H4分子中氮原子采取 杂化。
(2)的VSEPR模型是 。已知常温常压下H2O的沸点是100℃,CH3OH中的沸点是64.7℃,导致这种差异的主要原因是 。
(3)在BF3分子中F-B-F的键角是 ;1mol丙烯腈分子()中键与π键的个数比为 。
(4)COS中所有原子最外层都满足8电子稳定结构,COS属于 (填“极性”或“非极性”)分子,沸点:COS (填“>”“=”或“<”)CO2。
17.常温下对甲基苯甲醚为无色液体,具有紫罗兰的香气,可由对甲基苯酚与甲醇在浓硫酸催化作用下制取:。反应装置(部分夹持装置已略去)如图所示。
可能用到的数据如下:
物质性质 甲醇 对甲基苯酚 对甲基苯甲醚
熔点/℃ -97 34.7 -32.1
沸点/℃ 64.7 202 177
密度/(g·cm-3) 0.79 1.03 0.969
水溶性 易溶 难溶 不溶
Ⅰ.合成反应:在图1的烧瓶中先加入几片碎瓷片,再依次加入10.8g对甲基苯酚、10mL甲醇,最后加入2mL浓硫酸,控制反应温度为60℃(水浴加热)进行反应。
Ⅱ.产物提纯:①将反应混合液冷却后加入足量饱和碳酸钠溶液,充分反应后转移至分液漏斗中,静置分液;②将有机层转移至图2烧瓶中,加热,控制温度为100℃进行蒸馏,待蒸馏结束后,向烧瓶内剩余液体中加入足量无水氯化钙,然后趁热过滤,并将所得液体再次进行蒸馏,收集177℃左右的馏分,蒸馏结束后,称量所得馏分为7.32g。
(1)仪器A的名称为 。
(2)向图1的烧瓶中加入碎瓷片的目的是 ,采用水浴加热的目的是 。
(3)产物提纯时,先控制温度为100℃进行蒸馏的目的是 。
(4)加入足量无水氯化钙的目的是 。
(5)收集到的177℃左右的馏分主要成分是 (填名称)。
(6)对甲基苯甲醚的产率为 。
18.自然界中绝大多数的物质是固体。固体有晶体和非晶体两大类,晶体的结构决定了晶体的性质。回答下列问题:
(1)NF3可由NH3和F2在Cu催化剂存在下反应直接得到:。上述化学方程式中不涉及的晶体类型有 (填字母)。
a.离子晶体 b.分子晶体 c.共价晶体 d.金属晶体
(2)冰结构中,每个水分子最多与相邻的 个水分子通过 (填分子间作用力类型)相连接。
(3)锡元素位于元素周期表的第ⅣA族。灰锡具有立方金刚石结构,晶胞如图所示。SnCl2和SnCl4是锡的常见氯化物,SnCl2可被氧化得到SnCl4。
灰锡晶胞含 个Sn原子。SnCl2的空间结构为 。
(4)磷和钼形成的某种化合物的立方晶胞如图所示,已知晶胞中Mo位于顶点和面心,而P原子位于棱边中点和体心。
以A为原点建立三维坐标系,请在图a中画出晶胞中各原子沿z轴的投影图 (用“·”代表Mo原子,用“o”代表P原子,用“▽”代表Mo原子和P原子的重合)。
(5)氮和碳组成的一种新型材料,硬度超过金刚石,其部分结构如下图所示。它的化学式为 ,它的硬度超过金刚石的主要原因是 。
(6)立方硫化锌的晶胞结构如图所示。
若该晶体的密度为,Zn2+与S2-之间的核间距为dcm,则阿伏加德罗常数的值NA为 (用含、d的代数式表示)。
19.茚(苯并环戊二烯)是从煤焦油中提取的一种芳香烃,可用于生产茚-古马隆树脂,是杀虫剂的中间体。其一种合成方法如下:
已知:Et为乙基。
回答下列问题:
(1)D的化学名称是 。
(2)I中所含的官能团名称是 ;J的结构简式为 。
(3)反应①、②、③、④、⑤中,属于加成反应的有 (填序号)。
(4)写出反应①的化学方程式: 。
(5)J的同分异构体中,满足下列条件的化合物共有 种(不考虑立体异构),其中核磁共振氢谱显示有4组峰,峰面积之比为6:2:1:1的结构简式为 (任写一种)。
①能发生银镜反应;②属于芳香族化合物。
(6)根据本题信息和已学知识,写出以为原料制备的合成路线: (无机试剂任选)。
参考答案
1.C
2.B
3.D
4.A
5.D
6.B
7.D
8.C
9.A
10.C
11.D
12.B
13.D
14.B
15.D
16.(1) sp3
(2) 平面三角形 等物质的量的水、甲醇,前者分子间形成的氢键数目比后者多(答案合理均可)
(3) 120° 6:3(或2:1)
(4) 极性 >
17.(1)(球形)冷凝管
(2) 防暴沸 使反应液受热均匀(或易于控制反应温度)
(3)蒸出混合物中的甲醇、水(答案合理均可)
(4)除去混合液中少量的水(或干燥有机相)
(5)对甲基苯甲醚
(6)60%
18.(1)c
(2) 4 氢键
(3) 8 V形
(4)
(5) C3N4 氮化碳和金刚石都是共价晶体,且N的原子半径小于C,氮碳键的键能大于碳碳键(答案合理均可)
(6)(答案合理均可)
19.(1)苯乙醇(或2-苯基乙醇)
(2) 羰基
(3)⑤
(4)
(5) 14 或
(6)
一、单选题
1.生活离不开化学。下列有关说法正确的是
A.聚氯乙烯塑料制品可用于食品包装
B.丙三醇可用于汽车发动机的抗冻液
C.甲酸因最早从蚂蚁中获得,又称蚁酸,属于一元酸
D.尼龙、涤纶、光导纤维都是有机合成纤维
2.下列化学用语错误的是
A.的球棍模型: B.反-2-丁烯的球棍模型:
C.淀粉的分子式:(C6H10O5)n D.乙醇的键线式:
3.下列反应属于取代反应的是
A.用苯与氢气制环己烷 B.用乙醛在一定条件下制乙酸
C.用乙醇在一定条件下制乙烯 D.用2-溴丙烷在NaOH的水溶液条件下制2-丙醇
4.下列晶体中,前者属于共价晶体,后者属于分子晶体的是
A.晶体硅、冰 B.足球烯(C60)、干冰
C.碳化硅、金刚石 D.固态氢、二氧化硅
5.图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(如图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是
A.CF4 B.CH4 C.HCl D.
6.向含等物质的量的[Co(NH3)4Cl2]C1、[Co(NH3)6]Cl3、[Co(NH3)5C1]C12的溶液中分别加入过量的AgNO3溶液,生成AgCl沉淀的质量最多的是
A.[Co(NH3)4Cl2]C1 B.[Co(NH3)6]Cl3
C.[Co(NH3)5C1]C12 D.一样多
7.香草醛是一种食品添加剂,可用愈创木酚作原料合成。
下列试剂中能鉴别愈创木酚和香草醛的是
A.NaOH溶液 B.溶液 C.浓溴水 D.银氨溶液
8.下列关于糖类、油脂和蛋白质这三大营养物质的叙述正确的是
A.糖类、油脂、蛋白质都能发生水解反应
B.淀粉和纤维素均能在人体内水解为葡萄糖
C.皮肤、指甲上不慎沾上浓硝酸会出现黄色
D.油脂在酸性条件下能发生皂化反应,生成甘油和高级脂肪酸盐
9.近年来,食品安全事故频繁发生,人们对食品添加剂的认识逐渐加深。BHT是一种常用的食品抗氧化剂,其合成方法有如下图两种。下列说法错误的是
A.BHT在水中的溶解度大于苯酚
B.与BHT均可以使酸性KMnO4溶液褪色
C.与足量溴水反应,可消耗Br2
D.方法一发生了加成反应,方法二发生了取代反应
10.乙酰水杨酸(阿司匹林)的结构如图。下列说法中错误的是
A.乙酰水杨酸可发生酯化反应和水解反应
B.乙酰水杨酸是一种烃的含氧衍生物
C.1mol乙酰水杨酸与足量H2反应,最多消耗4molH2
D.苯环上有两个羧基,一个甲基的乙酰水杨酸的同分异构体有6种
11.物质结构决定物质性质。下列关于物质的结构或性质以及解释均正确的是
选项 结构或性质 原因解释
A 键角:NH3>PH3 NH3中N的孤电子对数比PH3中P的孤电子对数多
B 沸点:H2O>HF O—H…O的键能大于F—H…F的键能
C 硬度:碳化硅>金刚石 C—Si键能大于C—C键能
D 在水中的溶解性:O3>O2 分子极性
A.A B.B C.C D.D
12.酪氨酸学名为2-氨基-3-对羟苯基丙酸,是一种生命活动不可缺少的氨基酸,其结构如图所示。下列说法正确的是
A.酪氨酸为高分子化合物
B.酪氨酸分子中含有1个手性碳原子
C.酪氨酸既能与盐酸反应又能与NaOH溶液反应,且消耗盐酸和NaOH的物质的量之比为1:1
D.1mol酪氨酸分子与足量金属Na反应可产生22.4LH2
13.下列化学实验中的操作、现象及结论都正确的是
选项 操作 现象 结论
A 向淀粉溶液中加入稀硫酸,水浴加热后,加入新制氢氧化铜,加热 得到蓝色溶液 淀粉没有水解
B 向两份相同的蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液 均有固体析出 蛋白质均发生变性
C 向肉桂醛()中加酸性KMnO4溶液,振荡 酸性KMnO4溶液褪色 肉桂醛中仅醛基可与酸性KMnO4溶液发生反应
D 将(CH3)3CCH2Cl与NaOH的乙醇溶液加热一段时间后冷却,先加入硝酸酸化,再滴入硝酸银溶液 没有白色沉淀产生 (CH3)3CCH2Cl与NaOH的乙醇溶液不能发生反应
A.A B.B C.C D.D
14.BeO晶体晶胞的结构如图所示。原子A、B的坐标分别为(0,0,0)、(,,1),O与Be的最近距离为apm,用NA表示阿伏加德罗常数的值。下列说法错误的是
A.C原子的坐标为(,,)
B.与Be距离最近且相等的Be有4个
C.该晶体的密度为
D.晶胞内由O原子构成的正八面体空隙有4个
15.聚酰胺(PA)具有良好的力学性能,一种合成路线如下图所示。下列说法错误的是
A.Y的结构简式为
B.Z生成PA的反应类型为缩聚反应
C.该合成路线中甲醇可循环使用
D.PA可发生水解反应重新生成Z
二、解答题
16.在人类文明的历程中,许多物质发挥过重要作用,如铜、硝酸钾、青霉素、聚乙烯、二氧化硅、甲醇、含硼物质等。回答下列问题:
(1)写出的结构式,并用→表示配位键: 。肼(N2H4)分子可视为NH3分子中的一个氢原子被—NH2(氨基)取代形成的一种氮的氢化物。N2H4分子中氮原子采取 杂化。
(2)的VSEPR模型是 。已知常温常压下H2O的沸点是100℃,CH3OH中的沸点是64.7℃,导致这种差异的主要原因是 。
(3)在BF3分子中F-B-F的键角是 ;1mol丙烯腈分子()中键与π键的个数比为 。
(4)COS中所有原子最外层都满足8电子稳定结构,COS属于 (填“极性”或“非极性”)分子,沸点:COS (填“>”“=”或“<”)CO2。
17.常温下对甲基苯甲醚为无色液体,具有紫罗兰的香气,可由对甲基苯酚与甲醇在浓硫酸催化作用下制取:。反应装置(部分夹持装置已略去)如图所示。
可能用到的数据如下:
物质性质 甲醇 对甲基苯酚 对甲基苯甲醚
熔点/℃ -97 34.7 -32.1
沸点/℃ 64.7 202 177
密度/(g·cm-3) 0.79 1.03 0.969
水溶性 易溶 难溶 不溶
Ⅰ.合成反应:在图1的烧瓶中先加入几片碎瓷片,再依次加入10.8g对甲基苯酚、10mL甲醇,最后加入2mL浓硫酸,控制反应温度为60℃(水浴加热)进行反应。
Ⅱ.产物提纯:①将反应混合液冷却后加入足量饱和碳酸钠溶液,充分反应后转移至分液漏斗中,静置分液;②将有机层转移至图2烧瓶中,加热,控制温度为100℃进行蒸馏,待蒸馏结束后,向烧瓶内剩余液体中加入足量无水氯化钙,然后趁热过滤,并将所得液体再次进行蒸馏,收集177℃左右的馏分,蒸馏结束后,称量所得馏分为7.32g。
(1)仪器A的名称为 。
(2)向图1的烧瓶中加入碎瓷片的目的是 ,采用水浴加热的目的是 。
(3)产物提纯时,先控制温度为100℃进行蒸馏的目的是 。
(4)加入足量无水氯化钙的目的是 。
(5)收集到的177℃左右的馏分主要成分是 (填名称)。
(6)对甲基苯甲醚的产率为 。
18.自然界中绝大多数的物质是固体。固体有晶体和非晶体两大类,晶体的结构决定了晶体的性质。回答下列问题:
(1)NF3可由NH3和F2在Cu催化剂存在下反应直接得到:。上述化学方程式中不涉及的晶体类型有 (填字母)。
a.离子晶体 b.分子晶体 c.共价晶体 d.金属晶体
(2)冰结构中,每个水分子最多与相邻的 个水分子通过 (填分子间作用力类型)相连接。
(3)锡元素位于元素周期表的第ⅣA族。灰锡具有立方金刚石结构,晶胞如图所示。SnCl2和SnCl4是锡的常见氯化物,SnCl2可被氧化得到SnCl4。
灰锡晶胞含 个Sn原子。SnCl2的空间结构为 。
(4)磷和钼形成的某种化合物的立方晶胞如图所示,已知晶胞中Mo位于顶点和面心,而P原子位于棱边中点和体心。
以A为原点建立三维坐标系,请在图a中画出晶胞中各原子沿z轴的投影图 (用“·”代表Mo原子,用“o”代表P原子,用“▽”代表Mo原子和P原子的重合)。
(5)氮和碳组成的一种新型材料,硬度超过金刚石,其部分结构如下图所示。它的化学式为 ,它的硬度超过金刚石的主要原因是 。
(6)立方硫化锌的晶胞结构如图所示。
若该晶体的密度为,Zn2+与S2-之间的核间距为dcm,则阿伏加德罗常数的值NA为 (用含、d的代数式表示)。
19.茚(苯并环戊二烯)是从煤焦油中提取的一种芳香烃,可用于生产茚-古马隆树脂,是杀虫剂的中间体。其一种合成方法如下:
已知:Et为乙基。
回答下列问题:
(1)D的化学名称是 。
(2)I中所含的官能团名称是 ;J的结构简式为 。
(3)反应①、②、③、④、⑤中,属于加成反应的有 (填序号)。
(4)写出反应①的化学方程式: 。
(5)J的同分异构体中,满足下列条件的化合物共有 种(不考虑立体异构),其中核磁共振氢谱显示有4组峰,峰面积之比为6:2:1:1的结构简式为 (任写一种)。
①能发生银镜反应;②属于芳香族化合物。
(6)根据本题信息和已学知识,写出以为原料制备的合成路线: (无机试剂任选)。
参考答案
1.C
2.B
3.D
4.A
5.D
6.B
7.D
8.C
9.A
10.C
11.D
12.B
13.D
14.B
15.D
16.(1) sp3
(2) 平面三角形 等物质的量的水、甲醇,前者分子间形成的氢键数目比后者多(答案合理均可)
(3) 120° 6:3(或2:1)
(4) 极性 >
17.(1)(球形)冷凝管
(2) 防暴沸 使反应液受热均匀(或易于控制反应温度)
(3)蒸出混合物中的甲醇、水(答案合理均可)
(4)除去混合液中少量的水(或干燥有机相)
(5)对甲基苯甲醚
(6)60%
18.(1)c
(2) 4 氢键
(3) 8 V形
(4)
(5) C3N4 氮化碳和金刚石都是共价晶体,且N的原子半径小于C,氮碳键的键能大于碳碳键(答案合理均可)
(6)(答案合理均可)
19.(1)苯乙醇(或2-苯基乙醇)
(2) 羰基
(3)⑤
(4)
(5) 14 或
(6)
同课章节目录
